Что такое мезенхимальная дифференцировка
Эпителиально-мезенхимальный переход (Epithelial-mesenchymal transition, EMT) — сложный процесс изменения эпителиальными клетками эпителиального фенотипа на мезенхимальный, происходящий в эмбриональном развиитии, заживлении ран, а также при патологических процессах — например, при фиброзе, а также при опухолевой прогрессии.
Существует также и обратный процесс — мезенхимально-эпителиальный переход (Mesenchymal-epithelial transition).
Среди механизмов EMT можно выделить несколько ключевых моментов:
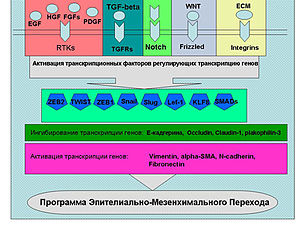
Растворимые факторы роста (на схеме), цитокины, молекулы внеклеточного матрикса активируют сигнальные пути ведущие к реализации программы ЭМП. Эти пути активируют ряд транскрипционных факторов (Snail, Twist, Slug, ZEB1, ZEB2, Lef-1 и др.), которые связываются с промоторами генов ответственных за ЭМП.
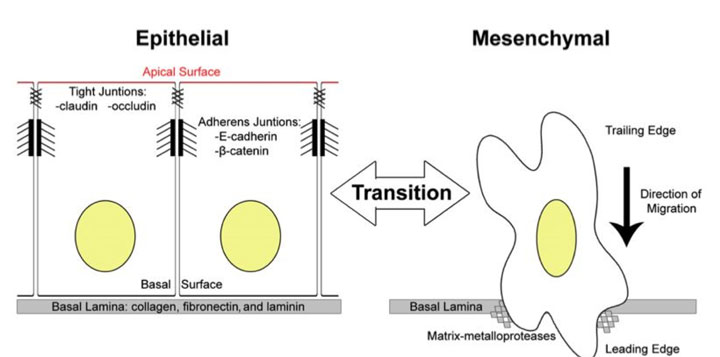
Одним из основных процессов, происходящих во время регенерации тканей является превращение эпителиальных клеток в мезенхимальные и наоборот, из мезенхимальных клеток в эпителиальные.
На рисунке выше показана разница между этими двумя основными фенотипами клеток. Важно, что нет никаких других многоклеточных тканей. Эпителиальные клетки плотно связаны друг с другом и с внеклеточным матриксом. Внеклеточный матрикс является базальной пластинкой, которая служит своего рода «колыбелью» для эпителиальных клеток. Мезенхимальные клетки расположены в 3D внеклеточной матрицы. Они биполярны, а это значит, что у них есть другое расположение цитоскелета и распределение органелл внутри них.
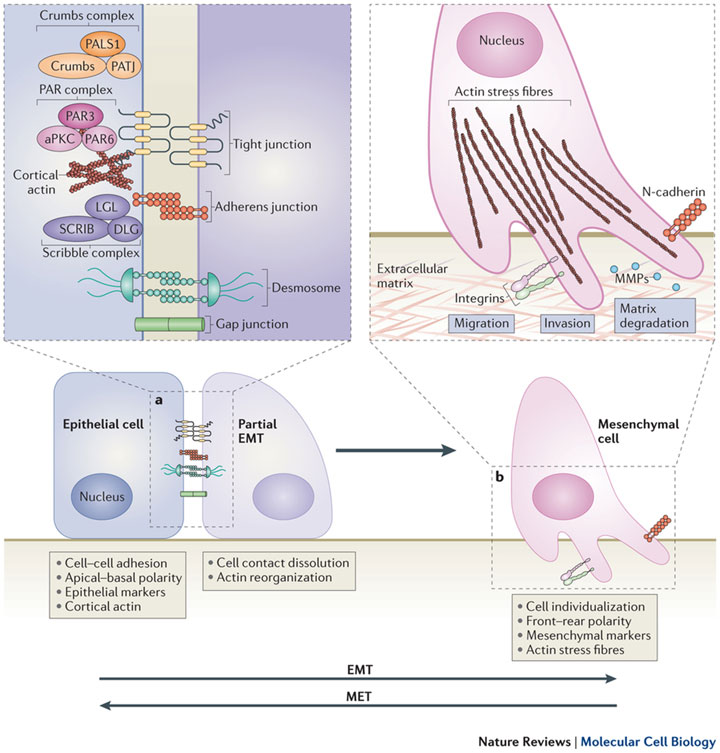
Утрата характерных черт эпителия (структуры ткани, клеточных взаимодействий, контроля специфическими факторами роста, приобретение подвижности и морфологии фибробластов) – это так называемое EMT, эпителиально-мезенхимальное превращение. ЕМТ свойственно нормальному эпителию в процессе развития, особенно раннего, например при гаструляции, когда эпителий приобретает подвижность и активно внедряется в подлежащие слои. ЕМТ имеет место при временных повреждениях ткани, при этом эпителиальные клетки теряют полярность, прекращают синтез кадхеринов, образуют виментин и фибронектин и одновременно с этим приобретают подвижность. Они прекращают синтез клеточных ядерных трансфакторов и образование антигенов, характерных для эпителиальных тканей. Эпителиальные клетки становятся типичными фибробластами. ЕМТ, по-видимому, лежит в основе инвазии и метастазирования: клетки эпителиальной опухоли становятся подвижными и приобретают способность расселяться по разным территориям организма. При этом очень существенно, что клетки претерпевают физиологическое, а не генетическое превращение, так как ЕМТ обратимо.
Метастазы, возникшие на основе ЕМТ, могут приобретать морфологию исходной опухоли, а эпителий в краевых районах раны может приобретать фибробластные свойства. Индукция ЕМТ имеет место при взаимодействии опухолей, экспрессирующих онкоген Ras и TGFр. Но так или иначе ЕМТ выглядит как заключительный этап прогрессии эпителиальной опухоли, когда опухоль теряет эпителиальные признаки (полярность клеток, специфические клеточные контакты, характерную морфологию и тканеспецифическую антигенную структуру) и одновременно приобретает черты фибробластов (экспрессию виментина, подвижность, независимость от территории роста).
Можно думать, что понимание этого процесса и факторов, в нем участвующих, создадут основу для рациональной терапии инвазии и метастазирования – главных свойств злокачественности. При этом непонятно, что будет дальше. Ведь прогрессия должна быть бесконечна, а EMT как бы завершает ее.
Источник: Nature Reviews Molecular Cell Biology 15,178–196, (2014)
Что такое мезенхимальная дифференцировка
ДЛЯ ТОГО ЧТОБЫ СКАЧАТЬ СТАТЬЮ В ФОРМАТЕ PDF ВАМ НЕОБХОДИМО АВТОРИЗОВАТЬСЯ, ЛИБО ЗАРЕГИСТРИРОВАТЬСЯ
Развивающимся направлением клеточной медицины является использование уникальных свойств прогениторных клеток, обладающих высокой биологической активностью и потенциалом дифференцировки. Мультипотентные мезенхимные стромальные клетки (ММСК) являются полипотентными клетками, обладающими рядом важных для клинического применения свойств. Применение ММСК, культивированных «ex vivo», открывает вопрос об оценке качества и безопасности культуры для клинического применения. Целью настоящего обзора являлась разработка программы культивирования и исследования значимых свойств человеческих ММСК для клинического применения. Приведена характеристика этапов оценки качества и безопасности ММСК, включая культивирование клеток «ex vivo», оценку иммунофенотипа, ростовых, иммуномодулирующих, регенеративных и прогениторных свойств, оценку генетической и микробиологической безопасности. Проведена оценка «in vitro» тестов для определения качества и безопасности ММСК. Подчёркивается, что выраженность свойств каждого отдельного образца различна и зависит от источника и условий культивирования клеток.
Остаётся открытым вопрос об оценке качества и безопасности ММСК, культивируемых для клинического применения. Очевидно, что каждый образец ММСК, который будет применён для лечения, должен быть оценен с позиции наличия у клеток необходимых в данной клинической ситуации полезных биологических свойств и безопасности для пациента.
Целью настоящего обзора литературы являлось определение основных этапов исследований индивидуальных значимых свойств образцов человеческих ММСК в процессе культивирования для клинического применения.
Источники получения ММСК
Очевидно, что эксплантация источников ММСК взрослого организма (костный мозг, жировая ткань) требуют инвазивного вмешательства, чреватого осложнениями. Неонатальные же источники ММСК могут быть получены без какого-либо значимого вмешательства в процесс родов.
Таким образом, контроль качества материала для экспансии ММСК должен включать комплекс медицинских, этических и правовых мероприятий, связанных с забором материала для экспансии, особенно связанного с инвазивными процедурами. Важен возраст донора в случае культивирования ММСК из взрослых тканей, в случае забора плацентарной ткани требуется оценка доли клеток фетального происхождения и доли материнских ММСК.
Условия культивирования ММСК
Таким образом, различные условия культивирования ММСК существенно влияют на их свойства. Следовательно, изменяя условия культивирования образцов ММСК можно добиться улучшения их клинически значимых характеристик.
Оценка «чистоты» полученной культуры ММСК
При изучении свойств ММСК было обнаружено большое количество поверхностных кластеров дифференцировки, экспрессируемых клетками. Если взять все описанные для ММСК маркеры, использующиеся для идентификации или селекции ММСК, то их число превысит несколько десятков. Данные по экспрессии поверхностных маркеров ММСК представлены в таблице.
Оценка способности ММСК к дифференцировке
Таким образом, оценка дифференцировочного потенциала ММСК проводится в двух направлениях:
1) качественное, цель которого подтвердить способность данной культуры к дифференцировке;
2) количественное, с целью оценить клиническую ценность данного конкретного образца.
Определение пролиферативного потенциала ММСК и старения клеток в культуре
Взаимодействие ММСК с другими клетками
Важнейшим свойством ММСК, которое является основой большинства случаев их клинического применения, является способность взаимодействовать с другими клетками как in vitro, так и in vivo. Взаимодействие с другими клетками реализуется как за счет непосредственных клеточных контактов, так и посредством продукции паракринных факторов. Виды взаимодействия ММСК с другими клетками организма, определяющие клинический эффект, можно подразделить на:
– взаимодействие ММСК с клетками иммунной системы (иммуномодулирующий и противовоспалительный эффект);
– взаимодействие с клетками повреждённых тканей (трофический и антиапоптотический эффект);
– стимуляция ангиогенеза (улучшение васкуляризации тканей);
– формирование стромы для гемопоэтических предшественников (обеспечение гемопоэза).
Оценка генетической стабильности ММСК
Исходя из данных литературы, можно сделать вывод, что оценка генетической стабильности ММСК является неотъемлемой частью системы контроля качества культивируемых ex vivo клеток. Однако литературные источники говорят, что большинство нарушений, выявляемых в трансформированных ММСК, проявляются на генном уровне и лишь в ходе опухолевой прогрессии начинают проявляться грубые поломки генома.
Следует добавить, что исследования генетической стабильности ММСК важны не только для реципиента ММСК, но и для донора. Вероятно, наличие генетических поломок в культуре ММСК является неблагоприятным прогностическим признаком в плане возможного возникновения онкологических заболеваний у донора в будущем.
Микробиологическая безопасность культуры ММСК
Не нуждается в комментариях то, что ММСК, полученные для клинического применения, должны быть безопасны в плане отсутствия контаминации микрофлорой. Бактериологическая безопасность образцов ММСК достигается путём соблюдения ряда правил и норм асептики и антисептики, касающихся всего процесса экспансии ММСК – от забора материала до выдачи готовой к применению культуры. Более интересным и неисследованным является вопрос о вирусологической безопасности ММСК, так как возможен перенос вирусов как вне клеток вследствие загрязнения материала, полученного от донора – носителя вируса, так и внутри самих ММСК при наличии тропизма вируса к клеткам.
Из приведённых данных следует вывод, что вирусологическое исследование образца ММСК должно включать как обследование самого донора, так и тестирование культуры ММСК на наличие в ней генома вирусов, тропных к ММСК.
Заключение
Таким образом, на основании анализа данных литературы можно привести основные этапы исследования клинически значимых свойств образцов ММСК. Контроль качества ММСК можно разделить на:
1. Общий контроль качества – безопасность полученных клеток и их общебиологических свойств, включающий:
а) оценку микробиологической безопасности:
– бактериологическое исследование среды, в которой культивировались клетки;
– серологическое исследование донорской сыворотки на антитела и антигены ВИЧ, гемотрансмиссивных гепатитов, парвовируса, цитомегаловируса, ВПГ1 и герпеса 6 типа;
– ПЦР исследование МСК с целью выявления вирусов: парвовирус, цитомегаловирус, ВПГ 1, герпес 6 типа;
б) иммунофенотипирование полученных ММСК – иммунологический минимум для подтверждения принадлежности к ММСК: определение экспрессии CD105, CD73 и CD90 в сочетании с отсутствием экспрессии CD45, CD34; CD14 или CD11b; CD79α или CD19 и HLA-DR;
в) оценка пролиферативных свойств и темпа старения ММСК в культуре – определение кумулятивного времени удвоения популяции, определение относительного количества КОЕ-Ф, МТТ-тест, качественная или количественная оценка активности ассоциированной со старением β-галактозидазы, оценка длины теломер;
г) качественная оценка способности к дифференцировке в остеогенном, хондрогенном и адипогенном направлении – с целью подтверждения принадлежности культуры к ММСК – культивирование в соответствующих дифференцировочных средах.
2. Специальный контроль качества – набор лабораторных тестов (в зависимости от поставленной конкретной клинической задачи):
а) оценка генетической стабильности включает:
– кариотипирование, выявление транслокаций и делеций участков 12, 20 и других хромосом, сравнительная геномная гибридизация (CGH);
– определение экспрессии генов p14, c-Myc, p21, p53, CDK-1, CDK-2, CDK-6, c-Myc, HGMA2, INK4A и RB;
– определение длины теломер и активности теломеразы;
б) количественная оценка способности к остеогенной и хондрогенной дифференцировке – с целью оценки активности образца ММСК в перспективе дальнейшего приживления in vivo и замещения дефектов целевых тканей. Остеогенная дифференцировка может быть определена по экспрессии генов CDC20, HIST2H2AA3, Runx2, ИЛ11, количественной оценке уровня щелочной фосфатазы, глюкозоаминогликанов. Хондрогенная дифференцировка может быть оценена по экспрессии генов агрекана Aggrecan, Sox9, Col2a1, можно дополнительно определять уровень miR-140;
в) оценка иммуномодулирующих свойств ММСК – способность подавлять в культуре пролиферацию NK клеток и Т-лимфоцитов, уровень экспрессии цитокинов TGFβ, ИЛ6, ИЛ10, ИЛ12, TNF-α, простагландина Е2, индоламин 2,3-дезоксигеназы, HGF;
г) оценка поддержки ГСК – определение уровня цитокинов SDF1, ГМ-КСФ, Г-КСФ, SCF, ИЛ6, EPO;
д) оценка паракринной функции – определение уровня цитокинов b-NGF, NT-3, NT-4, BDNF нейрорегулин-1, IGF-1, VEGF, М-КСФ, ИЛ6, ИЛ11, ИЛ15, SCF, SDF-1,sICAM-1, TGF-b, HGF, FGFIGF, имеющих помимо всего прочего нейротрофическое, ангиогенное и противоапоптотическое действие;
е) проведение HLA-типирования в случае, если клинический эффект предполагает приживление и дифференцировку аллогенных ММСК.
Указанный перечень, сформулированный нами на основе анализа значительного объема экспериментально-клинических данных, является обобщенным – для каждой конкретной ситуации, в зависимости от цели клинического применения культуры ММСК из приведенного списка должны быть выполнены отдельные, наиболее значимые пункты.