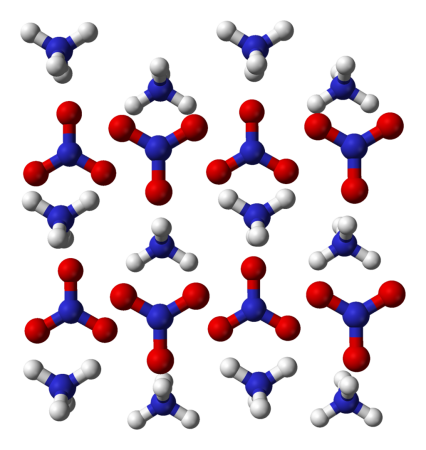
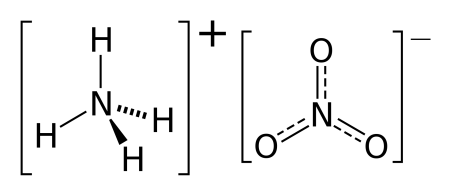Описание нитрата аммония и формула селитры, правила применения
Добиться высокой урожайности в сельском хозяйстве без удобрений весьма сложно. Активному росту растений в начале сезона способствуют азотные препараты. Благодаря использованию нитрата аммония стимулируется развитие зеленой массы. Препарат хорошо поглощает влагу, не наносит вреда почве и культурам, быстро усваивается растениями. При использовании важно соблюдать инструкции производителя.
Описание средства
Азотнокислый аммоний нельзя смешивать с опилками, соломой, торфом и другими органическими материалами, поскольку велика вероятность самовозгораний.
Какие физические свойства проявляет
При использовании любого вещества нужно учитывать его физические качества (цвет, концентрация, плотность, температура кипения).
Растворимость
В процессе растворения кристаллов происходит сильное поглощение тепла, в связи с чем замедляется растворение. Примерные цифры разложения селитры в воде, в зависимости от температуры жидкости: 0° С – 119 г/мл, 50° С – 346 г/мл, 100° С – 1024 г/мл).
Состав
Нитрат аммония состоит из нескольких элементов, пропорциональное соотношение которых может меняться. Популярное содержание: азот – 35 %, кислород – 60 %, водород – 5 %. Но иногда в удобрении доля азота может составлять 26-34 % и присутствует сера 3-14 %.
Именно азот является важным элементом питания зеленой массы растений. Вещество содействует полноценному развитию растительных культур, является участником фотосинтеза. На развитие растений отрицательно влияют как недостаток азота (снижается качество урожая, сокращается срок хранения плодов), так и избыток (замедляется развитие растений в конце сезона, что провоцирует снижение устойчивости к морозам).
Как получают вещество
Для производства нитрата аммония используют концентрированную азотную кислоту и безводный аммиак. Из концентрированного раствора выпаривают лишнюю воду, получая расплавленное вещество, в котором содержание нитрата аммония составляет 95-99 %.
Для получения удобрения расплав гранулируют в специальных аппаратах, сушат, охлаждают и покрывают особыми составами, предупреждающими склеивание/слеживания гранул.
Основные химические свойства
Правила использования в качестве удобрения
Препарат можно применять на различных видах грунта, желательно соблюдать некоторые ограничения по выбору растительных культур.
Нормы внесения для разных растений
При удобрении сельскохозяйственных растений важно принимать во внимание рекомендации производителя, чтобы избежать негативного воздействия удобрения.
| Объект обработки | Норма расхода | Особенности применения |
| Рассада томатов, перца, белокочанной капусты | 25-30г на кв. м грядок | рекомендуется гранулы при посадке рассыпать в подготовленные лунки, слегка присыпав землей |
| Корнеплоды | 5 г на кв. метр | применяют однократно через 2,5-3 недели после прорастания. Гранулы перед поливом просыпают по междурядьям и присыпают землей |
| Картофель | рабочий раствор 30-35г гранул на ведро воды | во время первого окучивания раствор льют под корень |
| Садовые деревья | 30-50 г гранул на кв. м | удобрение рассыпают в приствольном круге перед поливом |
| Ягодные кустарники | 15-20 г на куст | в начале вегетационного периода |
| Клубника | 10-15 г на кв. м | в начале вегетационного периода |
Поскольку при попадании на зелень удобрение может вызвать ожоги листвы, стеблей. Не применяют вещество при выращивании огурцов, кабачков, бахчевых культур, чтобы исключить накопление нитратов в плодах.
Подкормка озимых культур
Повторно удобрение применяют на стадии выхода растений в трубку. При определении нормы расхода препарата обращают внимание на состояние листьев и учитывают дозу первой подкормки. Как правило, используют 45-50 % общей нормы азота. В третий раз селитру применяют на стадии колошение-полный налив зерен, что способствует повышению эффекта фотосинтеза и увеличению веса зерен.
Применение против сорняков
Поскольку превышение дозировки удобрения способствует торможению роста растений, препарат можно применять для борьбы с сорными растительными культурами. Приготавливая рабочий раствор, рекомендуется в 2-2,5 раза превысить норму расхода гранул. Чтобы не навредить выращиваемым полезным растениям, грядки от сорняков обрабатывают после уборки урожая или за несколько дней до сева, посадки рассады.
Когда вносить в почву
Препарат довольно быстро усваивается растениями. В открытый грунт желательно вносить гранулы перед вспашкой, пока почва сохраняет влажность. Наибольший эффект аммониевой селитры проявляется в период с начала весны до середины лета. Именно в это время растительные культуры активно формируют зеленую массу.
Основное требование использования удобрения – подкормку вносят в подготовленные лунки и присыпают небольшим слоем грунта, чтобы предупредить ожог корневой системы. В сезон достаточно однократного применения селитры. Осенью не рекомендуется использовать подкормку, чтобы не стимулировать активный рост зеленой массы.
Техника безопасности
По степени воздействия на организм препарат относят к умеренно опасным. Однако следует строго соблюдать меры безопасности, чтобы исключить нанесение вреда здоровью:
В случае продолжительной работы желательно делать 5-10-минутные перерывы после получасовой работы в респираторе. По окончании работ рекомендуется принять душ с мылом.
Плюсы и минусы
При использовании любых химикатов для ухода за растениями важно учитывать положительные и отрицательные качества препаратов. Достоинства селитры:
Отрицательные моменты использования нитрата аммония: превышение дозировки приводит к накоплению нитратов в плодах, при попадании вещества на зеленую массу растений или открытые участки тела возможен ожог, взрывоопасность.
Как хранить
Поскольку препарат отличается высокой гигроскопичностью, для хранения гранул выделяют отдельное сухое, проветриваемое помещение. Рекомендуемый режим хранения: температура воздуха не выше 29-30° С, влажность не превышает 45-50 %.
Чтобы исключить самовозгорание вещества, запрещается в помещении складировать опилки, солому, торфяные брикеты. Также запрещается рядом располагать легко воспламеняющиеся жидкости/предметы, продукты питания, корма для животных, питьевую воду и вещи из домашнего обихода. Неиспользованное удобрение хранят в герметично закрывающейся промаркированной таре (подойдут стеклянные, пластиковые емкости).
Нитрат аммония – универсальное азотное удобрение, активно применяемое для ухода за культурами на приусадебных участках, в сельском хозяйстве и при выращивании растений в комнатных условиях. Основные нюансы использования – соблюдение норм расхода и правил безопасности.
Азотнокислый аммоний что это такое
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
Reagents. Ammonium nitrate.
Specifications
ОКП 26 2116 0020 06
Дата введения 1979-01-01
1. РАЗРАБОТАН И ВНЕСЕН Министерством химической промышленности СССР
В.П.Чуб, Л.К.Хайдукова, В.К.Окунева, В.Н.Корецкая, Т.Г.Манова, Г.В.Грязнов, З.М.Ривина, Э.П.Кравчук, М.В.Перловская
2. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета стандартов Совета Министров СССР от 28.12.77 N 3095
4. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
Обозначение НТД, на который дана ссылка
Номер пункта, подпункта
3.2.1, 3.3.1, 3.5, 3.11.1, 3.12a.1
3.3.1, 3.11.1, 3.12.1, 3.12a.1
3.2.1, 3.3.1, 3.11.1, 3.12.1, 3.15
5. Ограничение срока действия снято по протоколу Межгосударственного Совета по стандартизации, метрологии и сертификации (ИУС 5-6-93)
6. ПЕРЕИЗДАНИЕ (апрель 1997 г.) с Изменениями N 1, 2, утвержденными в июне 1988 г., феврале 1993 г. (ИУС 10-88, 8-93)
Настоящий стандарт распространяется на азотнокислый аммоний, представляющий собой кристаллический порошок, хорошо растворимый в воде и спирте; гигроскопичен, способен слеживаться.
Допускается изготовление азотнокислого аммония по ИСО 6353-3-87 (Р.44) (приложение 1) и проведение анализов по ИСО 6353-1-82 (приложение 2).
(Измененная редакция, Изм. N 2).
1. ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ
1.1. Азотнокислый аммоний должен быть изготовлен в соответствии с требованиями настоящего стандарта по технологическому регламенту, утвержденному в установленном порядке.
1.2. По физико-химическим показателям азотнокислый аммоний должен соответствовать нормам, указанным в таблице.
Химически чистый х.ч.
ОКП 26 2116
0023 03
Чистый для анализа ч.д.а.
ОКП 26 2116
0022 04
Чистый ч.
ОКП 26 2116
0021 05
1. Массовая доля азотнокислого аммония (NH NO ), %, не менее
2. Массовая доля нерастворимых в воде веществ, %, не более
3. Массовая доля остатка после прокаливания в виде сульфатов, %, не более
4. Массовая доля нитритов (NO ), %, не более
5. Массовая доля сульфатов (SO ), %, не более
6. Массовая доля фосфатов (РО ), %, не более
7. Массовая доля хлоридов (CI), %, не более
8. Массовая доля железа (Fe), %, не более
9. Массовая доля кальция (Са), %, не более
10. Массовая доля магния (Mg), %, не более
11. Массовая доля мышьяка (As), %, не более
12. Массовая доля тяжелых металлов, (Pb), %, не более
13. рН раствора препарата с массовой долей 5%
(Измененная редакция, Изм. N 1, 2).
2. ПРАВИЛА ПРИЕМКИ
2.2. Массовую долю фосфатов, магния и мышьяка изготовитель определяет в каждой 20-й партии.
(Введен дополнительно, Изм. N 1).
3. МЕТОДЫ АНАЛИЗА
При взвешивании используют лабораторные весы по ГОСТ 24104 2-го класса точности с наибольшим пределом взвешивания 200 г и 3-го класса точности с наибольшими пределами взвешивания 500 г и 1 кг.
Допускается применение других средств измерения с метрологическими характеристиками и оборудования с техническими характеристиками не хуже, а также реактивов по качеству не ниже указанных в настоящем стандарте.
3.1. Пробы отбирают по ГОСТ 3885. Масса средней пробы должна быть не менее 600 г.
3.1а, 3.1. (Измененная редакция, Изм. N 2).
3.2. Определение массовой доли азотнокислого аммония
3.2.1. Аппаратура, реактивы и растворы
Бюретка 1(2)-2-50-0,1 по НТД.
Колба Кн-2-250-34 ТХС по ГОСТ 25336.
Вода дистиллированная, не содержащая углекислоты; готовят по ГОСТ 4517.
Натрия гидроокись по ГОСТ 4328; раствор молярной концентрации (NaOH)=0,5 моль/дм (0,5 н.); готовят по ГОСТ 25794.1.
Спирт этиловый ректификованный технический по ГОСТ 18300 высшего сорта.
Фенолфталеин, спиртовой раствор с массовой долей 1%; готовят по ГОСТ 4919.1.
Формалин технический по ГОСТ 1625, раствор 1:1, нейтральный; готовят по ГОСТ 4517.
Нитрат аммония
| Нитрат аммония | |
 | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Нитрат аммония |
| Химическая формула | NH4NO3 |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдый |
| Отн. молек. масса | 80,04 а. е. м. |
| Молярная масса | 80,04 г/моль |
| Плотность | 1,725 (IV модификация) г/см³ |
| Термические свойства | |
| Температура плавления | 169,6 °C |
| Температура кипения | 235 °C |
| Температура разложения | |
| Химические свойства | |
| Растворимость в воде | 20 °C — 190 г/100 мл |
| Классификация | |
| Рег. номер CAS | 6484-52-2 |
Нитра́т аммо́ния (аммонийная (аммиачная) селитра) — химическое соединение NH4NO3, соль азотной кислоты. Впервые получена Глаубером в 1659 году.
Содержание
Физические свойства
Кристаллическое вещество белого цвета. Температура плавления 169,6 °C, при нагреве выше этой температуры начинается постепенное разложение вещества, а при температуре 210 °C происходит полное разложение. Температура кипения при повышенном давлении — 235 °C. Молекулярная масса 80,04 а. е. м.. Скорость детонации 2570 м/с.
Растворимость
| Температура, °C | Растворимость, г/100мл |
|---|---|
| 0 | 119 |
| 25 | 212 |
| 50 | 346 |
| 100 | 1024 |
При растворении происходит сильное поглощение тепла (аналогично нитрату калия), что значительно замедляет растворение. Поэтому для приготовления насыщенных растворов нитрата аммония применяется нагревание, при этом твёрдое вещество засыпается небольшими порциями.
Состав
Содержание элементов в нитрате аммония в массовых процентах:
Методы получения
Основной метод
В промышленном производстве используется безводный аммиак и концентрированная азотная кислота:
Реакция протекает бурно с выделением большого количества тепла. Проведение такого процесса в кустарных условиях крайне опасно (хотя в условиях большого разбавления водой нитрат аммония может быть легко получен). После образования раствора, обычно с концентрацией 83 %, лишняя вода выпаривается до состояния расплава, в котором содержание нитрата аммония составляет 95—99,5 % в зависимости от сорта готового продукта. Для использования в качестве удобрения расплав гранулируется в распылительных аппаратах, сушится, охлаждается и покрывается составами для предотвращения слёживания. Цвет гранул варьируется от белого до бесцветного. Нитрат аммония для применения в химии обычно обезвоживается, так как он очень гигроскопичен и процентное количество воды в нём (
Метод Габера
По способу Габера из азота и водорода синтезируется аммиак, часть которого окисляется до азотной кислоты и реагирует с аммиаком, в результате чего образуется нитрат аммония:
Нитрофосфатный метод
Этот способ также известен как способ Одда, названный так в честь норвежского города, в котором был разработан этот процесс. Он применяется непосредственно для получения азотных и азотно-фосфорных удобрений из широко доступного природного сырья. При этом протекают следующие процессы:
А также амфотерный метод.
Химические свойства
Реакции разложения
Термическое разложение нитрата аммония может происходить по-разному, в зависимости от температуры:
Кристаллические состояния нитрата аммония
Изменения кристаллического состояния нитрата аммония под воздействием температуры и давления меняют его физические свойства. Обычно различают следующие состояния:
| Система | Диапазон температур (°C) | Состояние | Изменение объёма (%) |
|---|---|---|---|
| — | > 169.6 | жидкость | |
| I | 169.6 — 125.2 | кубическая | +2.1 |
| II | 125.5 — 84.2 | тетрагональная | −1.3 |
| III | 84.2 — 32.3 | α-ромбическая | +3.6 |
| IV | 32.3 — −16.8 | β-ромбическая | −2.9 |
| V | Применение Взрывчатые веществаНаиболее широко в промышленности и горном деле применяются смеси аммиачной селитры с различными видами углеводородных горючих материалов, других взрывчатых веществ, а также многокомпонентные смеси: УдобренияБо́льшая часть нитрата аммония используется либо непосредственно как хорошее азотное удобрение, либо как полупродукт для получения прочих удобрений. Аварии и взрывыДополнительная информацияМировое производство аммиачной селитры на 1980 год составляло 14 млн т, в пересчёте на азот. Нитрат аммония | ||
| Систематическое наименование | Нитрат аммония | ||
| Хим. формула | NH4NO3 | ||
| Состояние | твёрдый | ||
| Молярная масса | 80,04 г/моль | ||
| Плотность | 1,725 (IV модификация) | ||
| Т. плав. | 169,6 °C | ||
| Т. кип. | 235 °C | ||
| Т. разл. | 210 °C | ||
| Растворимость в воде | 20 °C — 190 г/100 мл | ||
| ГОСТ | ГОСТ 14702-79 | ||
| Рег. номер CAS | 6484-52-2 | ||
| PubChem | 22985 | ||
| Рег. номер EINECS | 229-347-8 | ||
| SMILES | |||
| RTECS | BR9050000 | ||
| ChEBI | 63038 | ||
| ChemSpider | 21511 | ||
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |||
Нитрат аммония (аммонийная (аммиачная) селитра) — химическое соединение NH4NO3, соль азотной кислоты. Впервые получена Глаубером в 1659 году. Используется в качестве компонента взрывчатых веществ и как азотное удобрение.
Содержание
Физические свойства
Кристаллическое вещество белого цвета. Температура плавления 169,6 °C, при нагреве выше этой температуры начинается постепенное разложение вещества, а при температуре 210 °C происходит полное разложение. Температура кипения при пониженном давлении — 235 °C. Молекулярная масса 80,04 а. е.м. Скорость детонации 2570 м/с.
Растворимость
Растворимость в воде:
| Температура, °C | Растворимость, г/100мл |
|---|---|
| 0 | 119 |
| 10 | 150 |
| 25 | 212 |
| 50 | 346 |
| 80 | 599 |
| 100 | 1024 |
При растворении происходит сильное поглощение тепла (аналогично нитрату калия), что значительно замедляет растворение. Поэтому для приготовления насыщенных растворов нитрата аммония применяется нагревание, при этом твёрдое вещество засыпается небольшими порциями.
Также соль растворима в аммиаке, пиридине, метаноле, этаноле.
Состав
Содержание элементов в нитрате аммония в массовых процентах:
Методы получения
Основной метод
В промышленном производстве используется безводный аммиак и концентрированная азотная кислота:
Реакция протекает бурно с выделением большого количества тепла. Проведение такого процесса в кустарных условиях крайне опасно (хотя в условиях большого разбавления водой нитрат аммония может быть легко получен). После образования раствора, обычно с концентрацией 83 %, лишняя вода выпаривается до состояния расплава, в котором содержание нитрата аммония составляет 95—99,5 % в зависимости от сорта готового продукта. Для использования в качестве удобрения расплав гранулируется в распылительных аппаратах, сушится, охлаждается и покрывается составами для предотвращения слёживания. Цвет гранул варьируется от белого до бесцветного. Нитрат аммония для применения в химии обычно обезвоживается, так как он очень гигроскопичен и процентное количество воды в нём получить практически невозможно.
Метод Габера
По способу Габера из азота и водорода синтезируется аммиак, часть которого окисляется до азотной кислоты и реагирует с аммиаком, в результате чего образуется нитрат аммония:
Нитрофосфатный метод
Этот способ также известен как способ Одда, названный так в честь норвежского города, в котором был разработан этот процесс. Он применяется непосредственно для получения азотных и азотно-фосфорных удобрений из широко доступного природного сырья. При этом протекают следующие процессы:
А также амфотерный метод.
Химические свойства
Термическое разложение нитрата аммония может происходить по-разному, в зависимости от температуры:
Кристаллические состояния нитрата аммония
Изменения кристаллического состояния нитрата аммония под воздействием температуры и давления меняют его физические свойства. Обычно различают следующие состояния:
| Система | Диапазон температур (°C) | Состояние | Изменение объёма (%) | |
|---|---|---|---|---|
| — | > 169.6 | жидкость | ||
| I | 169.6 — 125.2 | кубическая | −2.13 | |
| II | 125.5 — 84.2 | тетрагональная | −1.33 | |
| III | 84.2 — 32.3 | α-ромбическая | +0.8 | |
| IV | 32.3 — −16.8 | β-ромбическая | −3.3 | |
| V | −50 — −16.8 | тетрагональная | +1.65 | |
| VI | существует при высоких давлениях | |||
| VII | 170 | |||
| VIII | существует при высоких давлениях | |||
| IX | существует при высоких давлениях |
Фазовый переход от IV к III при 32,3 °C приносит неприятности производителям удобрений, потому как изменения плотности приводят к разрушению частиц при хранении и применении. Это особенно важно в тропических странах, где нитрат аммония испытывает циклические изменения, приводящие к разрушению гранул, слёживанию, повышенному пылению и риску возникновения взрыва.
Применение
Удобрения
Бо́льшая часть нитрата аммония используется либо непосредственно как хорошее азотное удобрение, либо как полупродукт для получения прочих удобрений. Для предотвращения создания взрывчатых веществ на основе нитрата аммония в удобрения, доступные в широкой продаже, добавляют компоненты, снижающие взрывоопасность и детонационные свойства чистого нитрата аммония, такие как мел (карбонат кальция).
В Австралии, Китае, Афганистане, Ирландии и некоторых других странах свободная продажа нитрата аммония даже в виде удобрений запрещена или ограничена. После террористического акта в Оклахома-Сити ограничения на продажу и хранение нитрата аммония были введены в некоторых штатах США.
Взрывчатые вещества
Наиболее широко в промышленности и горном деле применяются смеси аммиачной селитры с различными видами углеводородных горючих материалов, других взрывчатых веществ, а также многокомпонентные смеси:
Безопасный состав
Дополнительная информация
Мировое производство аммиачной селитры на 1980 год составляло 14 млн т, в пересчёте на азот.