Натрия Гипохлорит
Химическое название
Натриевая соль хлорноватистой кислоты
Химические свойства
Гипохлорит Натрия — что это такое? Это неорганическое соединение, в составе которого находится до 95% активного хлора. Вещество имеет несколько нетривиальных, исторических названий: «лабарракова вода», «жавелевая вода». Химическая формула гипохлорита натрия: NaOCl. Молекулярная масса соединения = 74,4 грамма на моль. В связи с тем, что вещество достаточно неустойчиво в свободном состоянии, оно чаще всего применяется в форме пентагидрата или водного раствора. У раствора сильный, резкий запах хлора. Безводная форма вещества синтезируется в виде бесцветных кристаллов, которые хорошо растворяются в воде. Пентагидрат обладает желто-зеленым оттенком, кристаллы ромбической формы.
По своим химическим свойствам – это сильный окислитель. Гипохлорид легко разлагается до хлорида Na и кислорода, при нагревании подвергается диспропорционированию. В воде диссоциирует на ионы. Вещество подвергает коррозии большинство металлов.
Гипохлорит Натрия производится в огромных количествах. Около половины синтезированного вещества применяют в бытовой химии и медицине, остальное – в промышленности. Существует два метода производства средства: химический, хлорирование водного раствора натрия гидроксида (концентрированный и основной) и электролитический, используют электролизные установки для электролиза водного хлорида натрия.
Химическое соединение активно применяется в промышленности:
Вещество используют в бытовой химии, его часто можно обнаружить в составе отбеливателей, средств для дезинфекции и очистки. В медицине используют наружно или местно в качестве противовирусного, бактерицидного и противогрибкового средства; в небольших концентрациях — для обработки операционных ран, в гинекологии и акушерстве, оториноларингологии, в стоматологии (эндодонтия).
Химическое соединение может оказывать вредное воздействие на организм человека, при вдыхании оказывать удушающий и раздражающий эффект. При попадании средства в глаза вещество вызывает химический ожог, может привести к потере зрения. Средство раздражает кожу, в больших концентрациях вызывает отмирание тканей, язвы и ожоги. После приема внутрь 3-6% раствора у человека развивается ацидоз, раздражение пищевода, более высокие концентрации могут вызвать перфорацию пищеварительного тракта. Несмотря на это, при соблюдении рекомендации по использованию препаратов, воды и бытовой химии, гипохлорит считается достаточно безопасным средством. Не обладает канцерогенными, мутагенными и тератогенными средствами. Токсическая доза при внутривенном введения для человека составляет 45 мг на кг веса; пероральная – 1 грамм на кг. Также считается, что вещество не создает экологических проблем, так как в окружающей среде быстро разлагается до воды, кислорода и поваренной соли. Класс опасности для концентрированных растворов (до 20%): 1 – по химической активности; 3 – опасность для здоровья человека. Не территории Российской Федерации гипохлорит Na выпускают по ГОСТу 11086-76.
Фармакологическое действие
Дезинфицирующее, детоксицирующее, антисептическое, противомикробное.
Фармакодинамика и фармакокинетика
Натрия Гипохлорит – одно из сильнейших антибактериальных средств. Гипохлорит-ион проявляет высокую активность по отношению к множеству известных микроорганизмов, причем действует в достаточно низких концентрациях. Наивысшая активность проявляется при нейтральном рН. Образующиеся при разложении вещества частицы окисляют биополимеры в структуре вредоносных агентов, разрушают молекулы практически всех орг. субстратов. Средство проявляет активность по отношению к грамотрицательным бактериям, кишечной палочке, серрации, синегнойной палочке, грамположительным бактериям, патогенным грибам, простейшим, вирусам. Однако лекарство не действует на возбудители криптоспоридиоза и лямблиоза. Средство не обладает тератогенными, канцерогенными и мутагенными свойствами.
Показания к применению
Применяют наружно и вводят внутрь полости в концентрации 0,06%:
Раствор применяют для инъекционного введения при эндо- и экзотоксикозах, отравлениях, сепсисе, ожогах, заболеваниях печени и почек.
В виде жидкости и гелей вещество используют для дезинфекции оборудования в пищевой промышленности, при обработке поверхностей.
Противопоказания
Натрия Гипохлорит противопоказан к применению:
Побочные действия
Редко вещество вызывает:
Гипохлорит Натрия, инструкция по применению (Способ и дозировка)
Вещество используют для обработки помещения и различных поверхностей в соответствии с рекомендациями.
Лекарство применяют внутривенно, наружно и вводят в полости в форме 0,06% раствора. Следует соблюдать инструкцию по применению.
Передозировка
Нельзя превышать рекомендуемую дозировку и пренебрегать правилами использования гипохлорита Na. Средство может раздражать дыхательные пути, кожу, вызывать эрозии и перфорации ЖКТ, раздражать глаза.
Взаимодействие
Вещество не рекомендуется сочетать с прочими антисептическими средствами и мылом. Перед применением других лекарственных средств рекомендуется тщательно промыть обрабатываемый участок.
Особые указания
Раствором гипохлорита нельзя обрабатывать хирургические инструменты и материалы.
Не допускать попадания средства в глаза и дыхательные пути.
При беременности и лактации
Вещество не используют для инъекционного введения у беременных женщин.
Гипохлорит натрия. Вся польза Лабарраковой воды
Для чего нужен раствор гипохлорита натрия
Гипохлорит натрия – технический химикат для очистки зараженной воды, оборудования, стоков, кроме того, его используют для отбелки разных материалов, для окисления в фармацевтической отрасли при изготовлении витаминов. Давайте рассмотрим более полный список:
Итак, мы видим, что сфера применения препарата весьма и весьма широка. Если говорить в целом, то львиная доля всего произведенного на планете ГПХН расходуется на отбеливание (67%) и дезинфекцию (33%).
Химические характеристики гипохлорита натрия
Гипохлорит натрия ГОСТ определяет, как продукт хлорирования газом раствора едкого гидрокарбоната натрия. Несмотря на наличие массы других способов его получения, за эталон взят именно этот. В результате реакции получается химическое соединение с формулой NaOCl.
Это вещество называют натриевой солью хлорноватистой кислоты. Кристаллы крайне нестабильны и быстро разлагаются. Относительно стабильная форма получается путем образования пентагидрата.
Гипохлорит натрия и его более агрессивные родственники
Несмотря на то, что гипохлорит натрия требует достаточно осторожного обращения с ним, его рабочий раствор ведет себя спокойно и в подавляющем большинстве случаев не вызывает нареканий. Особенно если его сравнивать с активным хлором, который использовали для обеззараживания воды вплоть до начала 21 века в некоторых странах, в том числе в России, для очистительных мероприятий.
К сожалению, в нашей стране гипохлорит натрия долгое время производился в недостаточных количествах и для водоочистных сооружений поставлялся сжиженный хлор. Это вещество представляет из себя несравнимо более существенную опасность: хранение в сжиженном виде под большим давлением; убойные концентрации хлора в ближайшем воздушном пространстве при переливании, когда не любой противогаз поможет; более активные испарения из уже обработанной, обеззараженной воды, о чем свидетельствует более резкий запах.
Можно еще добавить, что хранение и транспортировка сжиженных активных газов, это не только опасно, но и затратно. Да, гипохлорит натрия требует деликатного обращения, но если его случайно пролить, то такой катастрофы, как если бы это был сжиженный хлор, не будет.
Активный хлор применяется на производственном уровне, а с таки веществом, как хлорная известь — попросту хлорка, многие знакомы на бытовом уровне и раньше использовали ее в личном хозяйстве постоянно. Применение хлорки, которая выпускается в виде нестабильного порошка, состоящего из смеси гипохлорита, хлорида и гидроксида кальция, это эффективно, но мягко говоря, не очень приятно: отмерять, растворять, затаив дыхание — не каждому под силу такие испытания. Еще не всем нравится, когда хлорка мягкими хлопьями украшает воду в бассейне.
Вот по таким простым причинам подавляющее большинство потребителей дезсредств предпочитает гипохлорит натрия. Еще с тех пор, как появились такие удобные для применения в домашнем хозяйстве и менее едкие средства, как «Белизна», «Domestos» и прочие, изготовленные на его основе.
Разновидности гипохлорит натрия
Чтобы читателю было проще увидеть разницу между марками ГПХН, мы свели их основные отличия в таблицу:
Таблица видов ГПХН
Наиболее качественным и чистым можно считать гипохлорит натрия МАРКА А. Именно здесь отмечается самое высокое содержание хлора, самая малая концентрация оснований и железа, соответственно, это дает более высокие результаты в отбелке тканей и дезинфекции. Гипохлорит натрия 25 кг в канистрах производит компания GOODHIM в соответствие со стандартом для марки А (возможна покупка гипохлорита натрия оптом).
Производство гипохлорита натрия
Мировые показатели объемов производства препарата приближаются к нескольким миллионам тонн. Потребности человечества в антисептике постоянно растут вместе с ростом населения, потребления искусственно подготовленной воды и общим развитием цивилизации на планете.
В промышленности используют такие методы получения:
Наиболее эффективным способом получения товарного ГПХН является низкосолевой процесс. В России так производит гипохлорит натрия фирма GOODHIM.
Воздействие на человека и природу
Интересно, что бактерицидное и, вообще, биоцидное действие ГПХН связано с выделением в процессе разложения таких частиц, как синглетный кислород. Это весьма напоминает борьбу некоторых наших клеток, например, гепатоцидов, с инородными микроорганизмами путем синтеза хлорноватистой кислоты.
Для человека ГПХН может нести опасность при проникновении в глаза, на участки незащищенной кожи и при вдыхании. Вдыхание вызывает жжение в глотке, резь в области глаз, кашель и эффект удушения. Поражение глаз способно привести к химическому ожогу с потерей зрения. Длительный контакт с кожей вызывает раздражение, при повышении концентрации – изъязвление и даже некроз.
Прием препарата в пищу ведет к гастропатии, раздражению внутренних поверхностей кишечника и пищевода, иногда – к ацидозу печени и перфорации ЖКТ.
Средство длительное время подвергалось всестороннему исследованию ученых разных стран мира, ведь его эффективность в разы превышала показатели риска и отвергнуть столь действенный дезинфектант было бы безрассудно! В исследованиях была убедительно показана безопасность дезинфектанта при применении по назначению и согласно инструкции. Также было установлено, что соединение не вызывает тенденции к образованию рака, мутации или неправильной беременности.
Заключение
Гипохлорит натрия – один из наиболее распространенных, эффективных и безопасных дезинфектантов и отбеливателей из всех известных человечеству. Вещество отличается доступностью для покупки, низкой ценой и солидным опытом использования. Польза Лабарраковой воды была убедительно показана в борьбе с эпидемиями, для обеззараживания воды, в отбелке целлюлозы и тканей.
Гипохлорит натрия
| Гипохлорит натрия | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Гипохлорит натрия |
| Традиционные названия | Гипохлорит натрия, лабарракова вода, жавелевая вода [К 1] |
| Химическая формула | NaOCl |
| Эмпирическая формула | NaOCl |
| Физические свойства | |
| Молярная масса | 74,443 г/моль |
| Плотность | пентагидрат: 1,574 [1] г/см³; 1,1 [2] г/см³ |
| Термические свойства | |
| Температура плавления | NaOCl · 5H2O [К 2] : 24,4 °C; NaOCl · 2,5H2O: 57,5 [3] °C |
| Температура разложения | 5%-й раствор [2] : 40 |
| Энтальпия образования (ст. усл.) | пентагидрат [К 3] : − 350,4 [3] кДж/моль |
| Химические свойства | |
| Растворимость в воде | NaOCl · 5H2O (20 °C): 53,4 [4] |
| Растворимость в в воде | NaOCl · 2,5H2O (50 °C): 129,9 [4] |
| Классификация | |
| Рег. номер CAS | 7681-52-9 |
| Регистрационный номер EC | 231-668-3 |
| RTECS | NH3486300 |
Соединение в свободном состоянии очень неустойчиво, обычно используется в виде относительно стабильного пентагидрата NaOCl · 5H2O или водного раствора, имеющего характерный резкий запах хлора и обладающего высокими коррозионными свойствами.
Содержание
История открытия
Физические свойства
Безводный гипохлорит натрия представляет собой неустойчивое бесцветное кристаллическое вещество. Элементный состав: Na (30,9 %), Cl (47,6 %), O (21,5 %).
У соединения известно три кристаллогидрата:
Плотность водного раствора гипохлорита натрия при 18 °C [11] :
| 1 % | 2 % | 4 % | 6 % | 8 % | 10 % | 14 % | |
|---|---|---|---|---|---|---|---|
| Плотность, г/л | 1005,3 | 1012,1 | 1025,8 | 1039,7 | 1053,8 | 1068,1 | 1097,7 |
| 18 % | 22 % | 26 % | 30 % | 34 % | 38 % | 40 % | |
| 1128,8 | 1161,4 | 1195,3 | 1230,7 | 1268,0 | 1308,5 | 1328,5 |
Температура замерзания водных растворов гипохлорита натрия различных концентраций [12] :[стр. 458] :
| 0,8 % | 2 % | 4 % | 6 % | 8 % | 10 % | 12 % | 15,6 % | |
|---|---|---|---|---|---|---|---|---|
| Температура замерзания, °C | −1,0 | −2,2 | −4,4 | −7,5 | −10,0 | −13,9 | −19,4 | −29,7 |
Термодинамические характеристики гипохлорита натрия в бесконечно разбавленном водном растворе [13] :
Химические свойства
Разложение и диспропорционирование
Гипохлорит натрия — неустойчивое соединение, легко разлагающееся с выделением кислорода:
При нагревании параллельно происходит реакция диспропорционирования [13] :
Гидролиз и разложение в водных растворах
Растворяясь в воде, гипохлорит натрия диссоциирует на ионы:
Так как хлорноватистая кислота (HOCl) очень слабая (pKa = 7,537 [13] ), гипохлорит-ион в водной среде подвергается гидролизу:
Именно наличие хлорноватистой кислоты в водных растворах гипохлорита натрия объясняет его сильные дезинфицирующие и отбеливающие свойства [13] (см. раздел «Физиологическое действие и воздействие на окружающую среду»).
В сильнощелочной среде (pH > 10), когда гидролиз гипохлорит-иона подавлен, разложение происходит следующим образом [15] :
При температурах выше 35 °C распад сопровождается реакцией диспропорционирования [15] :
При диапазоне pH от 5 до 10, когда концентрация хлорноватистой кислоты в растворе становится заметной, разложение идёт по следующей схеме [15] :

В кислой среде разложение HOCl ускоряется, а в очень кислой среде (pH [13] :
Если для подкисления используется соляная кислота, в результате выделяется хлор:
Пропуская через охлаждённый водный раствор гипохлорита натрия углекислый газ, можно получить раствор хлорноватистой кислоты:
Окислительные свойства
Рассмотрим основные варианты развития окислительно-восстановительного процесса и стандартные электродные потенциалы полуреакций в водной среде [17] [К 7] :
Некоторые окислительно-восстановительные реакции с участием гипохлорита натрия:
Идентификация
Среди качественных аналитических реакций на гипохлорит-ион можно отметить выпадение коричневого осадка метагидроксида при добавлении при комнатной температуре испытуемого образца к щелочному раствору соли одновалентного таллия (предел обнаружения 0,5 мкг гипохлорита):
Коррозионное воздействие
Гипохлорит натрия оказывает довольно сильное коррозионное воздействие на различные материалы, о чём свидетельствуют приведённые ниже данные [24] :
| Материал | Концентрация NaOCl, масс. % | Форма воздействия | Температура, °C | Скорость и характер коррозии | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Алюминий | — | твёрдый, влажный | 25 | > 10 мм/год | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 10; pH>7 | водный раствор | 25 | > 10 мм/год | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Медь | 2 | водный раствор | 20 | 10 мм/год | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Медные сплавы: БрА5, БрА7, Л59, Л63, Л68, Л80, ЛО68-1 | 10 | водный раствор | 20 | > 10 мм/год | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Никель | 10 | водный раствор | 20 | 0,1 | водный раствор | 25 | > 10,0 мм/год | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Сталь 12Х17, 12Х18Н10Т | 5 | водный раствор | 20 | > 10,0 мм/год | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Сталь 10Х17Н13М2Т | 7 | водный раствор | 25 | 0,1 | водный раствор | 25 | > 10,0 мм/год | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Чугун СЧ15, СЧ17 | Физиологическое действие и воздействие на окружающую среду NaOCl одно из лучших известных средств, проявляющих благодаря гипохлорит-иону сильную антибактериальную активность. Он убивает микроорганизмы очень быстро и уже в очень низких концентрациях. Высокие окислительные свойства гипохлорита натрия позволяют его успешно использовать для обезвреживания различных токсинов. В приведённой ниже таблице представлены результаты инактивации токсинов при 30-минутной экспозиции различных концентраций NaOCl («+» — токсин инактивирован; «−» — токсин остался активен) [27] :
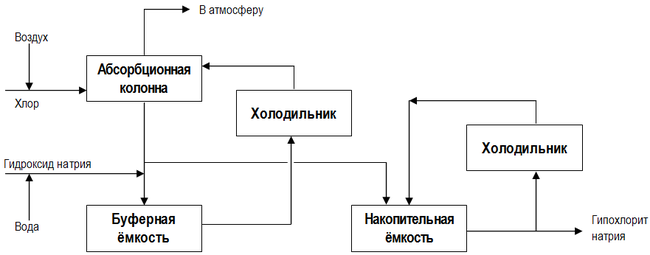
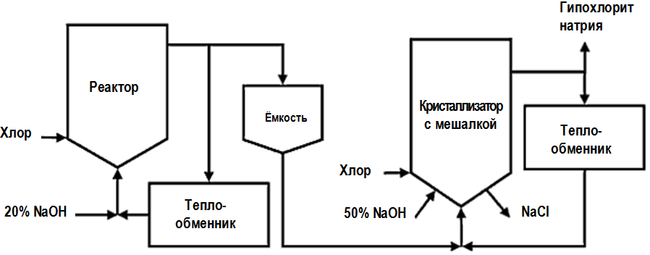
Пероральная токсичность соединения [30] : Внутривенная токсичность соединения [30] : Гипохлорит натрия не представляет угрозы с точки зрения пожароопасности. Рейтинг NFPA 704 для концентрированных растворов (10—20 %) [31] : Лабораторные методы полученияОсновным лабораторным методом получения гипохлорита натрия является пропускание газообразного хлора через охлаждённый насыщенный раствор гидроксида натрия [32] : Вместо гидроксида для синтеза можно взять карбонат натрия [33] : Водный раствор гипохлорита натрия можно получить обменной реакцией карбоната натрия с гипохлоритом кальция [34] : Промышленное производствоМировое производствоОбзор промышленных способов полученияВыдающиеся отбеливающие и дезинфекционные свойства гипохлорита натрия привели к интенсивному росту его потребления, что в свою очередь дало стимул для создания крупномасштабных промышленных производств. В современной промышленности существует два основных метода производства гипохлорита натрия: В свою очередь, способ химического хлорирования, предлагает две производственные схемы: Химический методСущность химического метода получения NaOCl не изменилась с момента его открытия Лабарраком (см. подраздел «История открытия»): Современная технологическая схема непрерывного производства гипохлорита натрия представлена на рисунке [36] :[стр. 442] : Низкосолевой процесс производства, в отличие от основной технологической схемы, представленной выше, включает в себя две стадии хлорирования, причём в кристаллизатор (см. на рисунке), где происходит концентрирование готового продукта, подаётся разбавленный раствор NaOCl из первого реактора [36] :[стр. 450] : В России товарный гипохлорит натрия производят следующие предприятия: Электрохимический метод Процесс в электролизёре за счёт химического взаимодействия образующихся продуктов: Общая схема процесса: Характеристика продукции, обращение, хранение и транспортировкаВ Российской Федерации гипохлорит натрия выпускается в соответствии с ГОСТ 11086-76 «Гипохлорит натрия. Технические условия». В соответствии с этим документом, по назначению NaOCl делится на две марки, характеристики которых представлены ниже [47] :
Растворы товарного гипохлорита натрия со временем теряют свою активность из-за разложения NaOCl, что наглядно иллюстрирует следующая таблица [12] :[стр. 469] :
ПрименениеОбзор направлений использованияВесь широкий спектр использования гипохлорита натрия можно разбить на три условные группы: Бытовое использование включает в себя: Промышленное использование включает в себя: Применение в бытовой химииКоммерческая доступность и высокая эффективность действующего вещества определяет его широкое использование различными производственными компаниями, где гипохлорит натрия или средства на его основе выпускаются под различными торговыми марками, некоторые из которых представлены в таблице:
Применение в медицинеПромышленное применениеПрименение в качестве промышленного отбеливателяГипохлорит натрия широко используется в качестве отбеливателя и пятновыводителя в текстильном производстве и промышленных прачечных и химчистках. Он может быть безопасно использован для многих видов тканей, включая хлопок, полиэстер, нейлон, ацетат, лён, вискозу и другие. Он очень эффективен для удаления следов почвы и широкого спектра пятен в том числе, кровь, кофе, трава, горчица, красное вино и т. д. [29] Применение в качестве промышленного дезинфицирующего средстваШирокое применение гипохлорита натрия в качестве промышленного дезинфицирующего средства связано, прежде всего, со следующими направлениями [49] : Промышленные дезинфицирующие и отбеливающие растворы выпускаются многими производителями под различными торговыми марками, некоторые из которых представлены в таблице:
Использование для дезинфекции водыИспользование гипохлорита натрия в качестве дезинфицирующего агента в отличие от применения хлора обладает рядом существенных достоинств: Также с технической точки зрения, для условий использования в РФ, эксперты отмечают: Производство гидразина В качестве побочной реакции наблюдается взаимодействие гидразина с хлорамином [80] : Модификацией процесса Рашига стал процесс Хофмана (англ. Hoffmann Process или англ. Urea Process ), где вместо аммиака используется мочевина [83] : Применение в промышленном органическом синтезеСильные окислительные свойства гипохлорита натрия используются в промышленном органическом синтезе для получения различных соединений, среди которых: Применение в лабораторном органическом синтезеГипохлорит натрия находит широкое применение в лабораторной органической практике прежде всего, из-за своих сильных окислительных свойств и доступности как реактива. Окислительные возможности NaOCl используются в следующих превращениях: Среди других вариантов использования отметим: Прочие направления использованияСреди прочих направлений использования гипохлорита натрия отметим: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
















 [К 12]
[К 12]