Мономорфные ядра что обозначает
хирург-онколог, маммолог, кандидат медицинских наук
Ленинградская область, Всеволожский район, пос.Кузьмоловский, Заозерная ул., 2
Врач в третьем поколении. Закончил в 1998 году с отличием Санкт-Петербургскую государственную медицинскую академию им. И.И. Мечникова, после чего сразу же поступил в клиническую ординатуру по хирургии этой же академии. Во время обучения в клинической ординатуре, которую с отличием закончил в 2000 году, получил специализацию по онкологии (1999). Начиная с 1999 года, обучение проводилось на базе Ленинградского областного онкологического диспансера (отделение общей онкологии). С 2000 по 2004 год проходил обучение в аспирантуре и в 2004 году защитил кандидатскую диссертацию на тему «Хирургическое и адъювантное лечение ранних форм рака молочной железы». Имею действительные сертификаты по хирургии (2021) и онкологии (2018), реконструктивной и пластической хирургии (2019). Являюсь лучшим маммологом Санкт-Петербурга 2016 года по версии сайта НаПоправку, лучшим маммологом Санкт-Петербурга в 2020 и 2021 годах по версии Prodoctorov.Ru
Лечу рак молочной железы по федеральным квотам в Клинической больнице Российской академии наук, принимаю и лечу пациентов в клинике онкологических решений ЛУЧ
С 2004 года являюсь главным исследователем и координатором международных клинических исследований по раку молочной железы в Ленинградском областном клиническом онкологическом диспансере, клинике онкологических решений ЛУЧ.
Имею более 10 печатных работ, в том числе в центральной зарубежной печати.
Рабочий телефон +7921 945 33 18
Мобильный телефон +7 921 945 33 18
Телефон администратора +7 981 710 40 41
Мономорфные ядра что обозначает
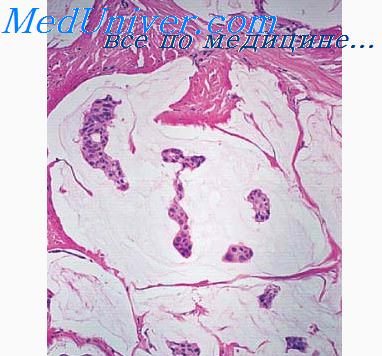
Диагностика этих доброкачественных опухолей слюнных желез представляет известные трудности. Они связаны прежде всего с тем, что по строению эти опухоли принципиально не отличаются от эпителиального компонента плеоморфных аденом. Главное, что отличает эти две опухоли,— это отсутствие так называемого мезенхимального компонента. В связи с этим необходимо исследовать максимальный объем опухолевого узла.
Клинически опухоли данной группы не отличаются от плеоморфных аденом. Так же как и последние, возникают как в больших, так и в малых слюнных железах, несколько чаще у женщин, но в возрастной группе от 50 до 70 лет.
По сравнению с плеоморфными структура мономорфных аденом характеризуется большей однородностью строения. Встречаются опухоли с преобладанием тубуляриых структур в виде железистых просветов с двухслойной выстилкой, последние могут быть заключены в трабекулярные тяжи. Выявляются аденомы преимущественно солидного строения, иногда отдельные тяжн н комплексы имеют базалоидную ориентацию периферического слоя эпителиальных клеток. В некоторых случаях переплетающиеся трабекулы создают сетевндную, решетчатую структуру, однако в отличие от аденокистозного рака гиалиноподобные включении содержат стромальные клеточные элементы и мелкие сосуды.
Во всех случаях отличительной чертой мономорфных аденом являются четкие контуры эпителиальных комплексов, их обособленность от стромы, которая при этом на отдельных участках может быть рыхлой, отечной или несколько клеточной. Преобладают клетки небольших размеров. Внутренний слой железистых структур образован клетками с более плотной, слегка эозинофильной цитоплазмой. Иногда в солидных тяжах встречаются клеточные элементы со светлой цитоплазмой, напоминающие эпидермоидные.
В мономорфных аденомах с преобладанием тубулярных структур по сравнению с плеоморфными аденомами не выявляются миоэпнтелиальные клетки. Эпителиальные элементы обнаруживают признаки плоскоэпителиальной дифференцировки, встречаются клетки с секреторными гранулами и клетки, сочетающие оба указанных признака. Специфическая секреторная функция эпителиальных клеток выражена слабо. Эпителиальные клетки тубулярных структур нмеют специализированные боковые цитоплазматнческне мембраны с пальцевидными выростами, что при наличии большого количества десмосом обеспечивает более плотное сцепление клеток.
Иногда между клеточными элементами солидно-альвеолярных комплексов возникают округлой формы скопления межклеточной основы с коллагеном без поперечной исчерченности, возможно симулирующие при светооптическом исследовании тубулярные структуры. Указанные признаки дают основание предполагать участие эпителиальных клеток (наряду с фибробластами соединительнотканных прослоек) в формировании стромы. Однако отсутствие миоэпителиальных клеток, направление и уровень функциональной дифференцировки эпителиальных клеточных элементов (преобладание эпителиальных клеток с секреторными гранулами), выраженная склонность к образованию тубулярных структур с плотным сцеплением клеток, вероятно, и обусловливают отсутствие мезенхимального компонента в мономорфной аденоме.
В последние годы как вариант других типов мономорфных аденом описывают так называемые базально-клеточные аденомы. Считают, что эта форма доброкачественных новообразований слюнных желез выделена Kleinsasser и Klein в 1967 г. Явное сходство с базалиомами кожи (мелкие мономорфные клетки и палисадообраэное их расположение по периферии комплексов) привело к выбору указанного термина. Впоследствии этим термином стали обозначать новообразования, в которых наряду с указанными признаками выявлялись солидно-альвеолярные, трабекулярно-каналикуляриые, трабекулярные, тубулярные структуры.
Более того, в базально-клеточной аденоме описывались участки трабекулярного строения из светлых клеток. Таким образом, термин «базально-клеточная аденома» потерял определенность к объединил все возможные варианты строения других типов мономорфных аденом. На основании анализа данных литературы создается впечатление нечеткости гистологических критериев и необоснованности выделения базально-клеточных аденом в отдельную группу. Об этом же свидетельствуют разноречивость сведений о частоте данных новообразований н их ультраструктуре. По-видимому, в таких случаях следует ограничиваться термином «мономорфная аденома» с указанием особенностей составляющих опухоль структур.
Известные диагностические трудности возникают при анализе строения мономорфных аденом с преобладанием базалоидных структур. Тщательное, по возможности тотальное, исследование новообразования позволяет провести дифференциальный диагноз между аденомой н аденокнстозным раком. Основными диагностическими признаками, склоняющими в пользу аденомы, является отсутствие гиалинового превращения межклеточной основы, кри-брозных структур и инфильтративного роста.
Мы — Иные. Клеточный атипизм
Отсюда мораль: всякому овощу свое время. Или если сказать попроще… Никогда не думай, что ты иная, чем могла бы не быть иначе, чем будучи иной в тех случаях, когда иначе нельзя не быть.
Льюис Кэрролл, «Алиса в стране чудес»
Злокачественная трансформация клеток опосредована генетическими нарушениями. Опухолевые клетки приобретают особый, отличный от нормальных клеток фенотип, на выявлении которого основана морфологическая верификация онкологического диагноза.
Архитектурные перестройки в опухолевой ткани отмечаются на разных уровнях организации. Глобальные изменения, такие как нарушение соотношения паренхимы и стромы, изменение величины и формы тканевых структур, представляют явление тканевого атипизма. Но помимо масштабных нарушений, при «строительстве» опухоли используются и неправильные, атипичные «кирпичи»-клетки. Характерный комплекс цитологических критериев злокачественности формирует клеточный атипизм — одно из фундаментальных понятий в онкоморфологии. Для максимальной объективизации анализа материального субстрата патологического процесса используются критериальные системы оценивания, способствующие унификации, и, следовательно, упрощению исследования. У патоморфолога складывается «образ злокачественной клетки» — некая визуальная форма, достаточно яркая для быстрой идентификации. Рассмотрим на светооптическом уровне штрихи (критерии), из которых складывается этот образ.
1. Клетка:
2. Ядро:
3. Ядрышки:
4. Хроматин:
Выраженность цито- и гистологических нарушений увеличивается с ростом степени злокачественности.
Патологическая анатомия немыслима без визуализации информации, поэтому представим процесс озлокачествления клеток на конкретном примере. В доставленном материале — фрагмент ткани мочевого пузыря. В нормальных условиях уротелиальные клетки относительно мономорфны, содержат достаточный объем цитоплазмы и овальные ядра, имеют округлые гладкие контуры, нежный хроматин, мелкие или вовсе невидимые ядрышки (рис. 1) [5].
.
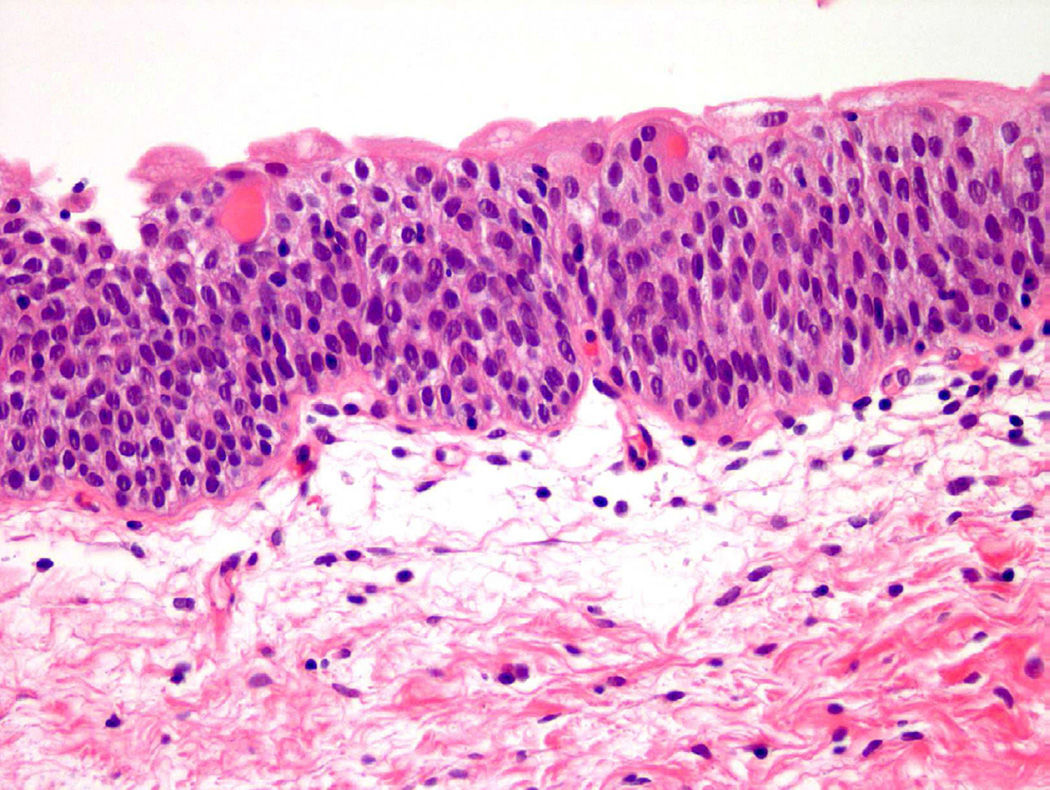
Рисунок 1 | Микроскопическая картина нормального уротелия [5]
Определимся с относительностью мономорфности клеток. Даже нормальным уротелиальным клеткам «разрешено» иметь определенные вариации в размерах. Особенно это характерно для самого поверхностного (апикального) слоя уротелия, который находится в постоянном контакте с содержимым мочевого тракта. Он представлен крупными зонтичными клетками с обильной эозинофильной цитоплазмой. Их наличие служит одним из критериев злокачественности уротелиальной карциномы. В опухолях High Grade (высокой степени злокачественности) они не определяются. Но в то же время физиологический фактор — растяжение мочевого пузыря — может привести к уплощению поверхностных зонтичных клеток до такой степени, что слой может быть трудно определить микроскопически, что дополнительно затрудняет морфологическую диагностику [6].
Несмотря на большое разнообразие морфологии нормальных уротелиальных клеток, определены специфические особенности, указывающие на атипию. Информативны не поверхностные и не дегенеративные уротелиальные клетки. Основной маркер — увеличение ядерно-цитоплазматического соотношения (более 0,5) [5]. Дополнительные критерии: гиперхромия, неравномерный, грубый хроматин, неравномерный контур ядра. Если ядерно-цитоплазматическое соотношение более 0,7 и присутствуют два дополнительных признака, необходимо заподозрить уротелиальную карциному высокой степени злокачественности (рис. 2) [6].
.
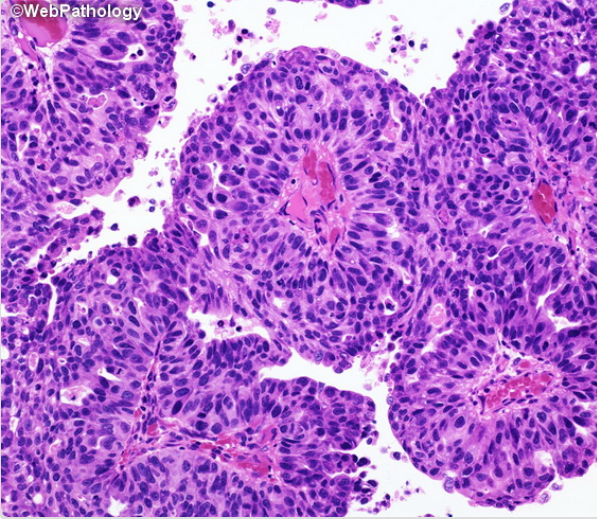
Рисунок 2 | Папиллярная уротелиальная карцинома High Grade
Выраженная тканевая и клеточная атипия. Внутри папиллярных структур опухолевые клетки расположены хаотично, с утратой полярности. Значительный полиморфизм ядер, гиперхромность, отчетливые ядрышки. Митотическая активность увеличивается, фигуры митоза отмечаются во всех слоях уротелия. Единичные очаги некроза [8].
Цитологические критерии уротелиальной карциномы высокой степени злокачественности: высокое ядерно-цитоплазматическое соотношение, неравномерный контур мембран ядер, эксцентрическая локализация ядра, крупные, полиморфные ядра, выраженные ядрышки (рис. 3.1, 3.2) [7], могут обнаруживаться признаки плоскоклеточной и железистой дифференцировки (рис. 4) [8].
.
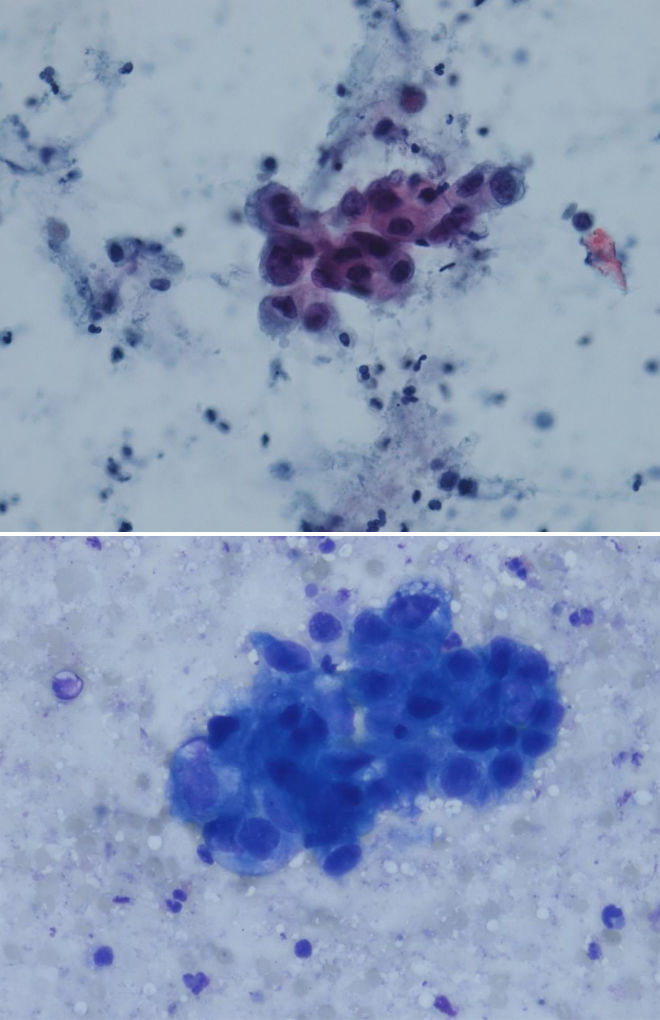
Рисунки 3.1 и 3.2 | Папиллярная уротелиальная карцинома High Grade
Крупные ядра с высоким ядерно-цитоплазматическим соотношением, грубый хроматин и нечеткие, размытые контуры ядра (окраска Papanicolaou и DiffQuik) [9].
.
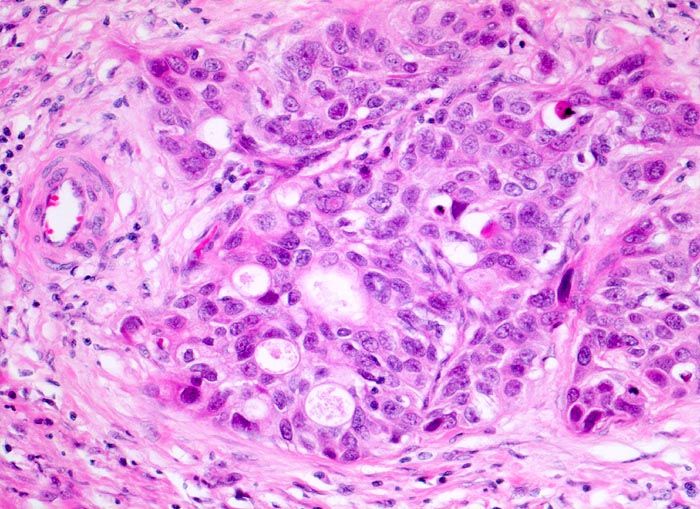
Рисунок 4 | Папиллярная уротелиальная карцинома High Grade с формированием железистых структур [10]
Фундаментальное понимание явления атипизма как отличия от нормы может рассматриваться в различных аспектах. Помимо морфологического атипизма, в опухолевой клетке наблюдается антигенный, функциональный, метаболический атипизм. Морфологию, в свою очередь, можно рассматривать на уровне электронной микроскопии, анализируя ультраструктуры клетки (патологию рибосом, митохондрий, мембранных структур, компонентов цитоскелета и т. д.). В рутинной практике большее значение имеет все же светооптический уровень исследования. Для снижения доли субъективизма в определении различных степеней «атипичности» в доставленном материале требуются как четкие критерии каждого этапа анапластических изменений, так и внедрение систем анализа изображений.
Мономорфные ядра что обозначает
Злокачественные опухоли молочной железы, как причина смертности от онкологических заболеваний среди женщин, занимают первое место как в России, так и в мире. Это также основная причина смерти среди женщин старше 40 лет. Примерно у 8% женщин (одной из 13) в течение жизни развивается злокачественная опухоль молочной железы. К сожалению, отмечается тенденция к росту заболеваемости и смертности от рака молочной железы, особенно выраженная в странах с высоким уровнем жизни. Так, в странах Северной Европы, Северной Америки и Австралии заболеваемость составляет 70-90 вновь выявленных случаев злокачественных опухолей на 100 000 населения в год (ВОЗ, 2003). Около 90% злокачественных опухолей молочной железы составляет рак, реже встречаются неэпителиальные опухоли.
Врач, устанавливающий морфологический диагноз рака, должен отдавать себе отчет в том, что этот диагноз может служить основанием к началу, как правило, тяжелого лечения (хирургического, лучевого, химиотерапевтического и проч.).






Небольшой полиморфизм может отмечаться при фиброаденоме и фиброзно-кистозной болезни, однако при этих поражениях обычно обнаруживают значительное число доброкачественных «голых» ядер, упорядоченное расположение клеток в структурах.
На малом увеличении примерно у 15% опухолевых клеток ядра выглядят сравнительно мономорфными, что особенно хорошо проявляется при высокодифференцированном раке.
Разрозненное (рыхлое) расположение клеток
Связано с нарушением межклеточных связей, поэтому клетки перестают выстраиваться в привычном для данной ткани порядке, а также отрываются от структур и располагаются разрозненно. В связи с этим отмечается:



Однако при некоторых формах рака, например при слизистом, может сохраняться плотное расположение клеток в скоплениях. Такие скопления нужно рассматривать очень внимательно, чтобы оценить характер клеток, детали которых увидеть трудно из-за наложения ядер.
Дегенеративные изменения клеток и ядер
Дегенеративные измененения приводят к разрежению структуры хроматина (вакуоли, просвет), появлению «голых» ядер разрушенных клеток. В отличие от доброкачественных процессов «голые» ядра различаются по размерам и форме, в них могут просматриваться укрупненные ядрышки. Особенно характерны для рака ядра очень крупных размеров (рис. 70, 71).
Наличие слизи или эритроцитов в аспирате не является признаком доброкачественности или злокачественности.
Нарушение ядерно-цитоплазматического соотношения
Для рака характерны разные размеры и форма опухолевых клеток. Однако некоторые классические для большинства локализаций критерии злокачественности не могут быть оценены по пун-ктатам из молочной железы. Так, например, увеличение ядерно-цитоплазменного соотношения в пунктатах молочной железы удается отметить не всегда. Ядерно-цитоплазменное соотношение в клетках протокового эпителия, как правило, сдвинуто в сторону ядер. В злокачественных опухолях нередко увеличивается размер и ядер и цитоплазмы, кроме того, цитоплазма клеток бывает нежной, клеточная мембрана недостаточно плотной, границы ее видны нечетко, оценить ядерно-цитоплазменное соотношение достаточно сложно, поэтому при установлении диагноза рака большое значение имеют изменения ядер.

Дифференциальная диагностика между внутрипротоковой папилломой и папиллярным раком иногда представляет значительные трудности, и даже инвазия в ткань молочной железы не может служить достоверным признаком рака из-за возможности псевдоинвазии.
В эпидермисе соска отмечается пролиферация атипических клеток с крупными ядрами и обильной светлой цитоплазмой, содержащей часто муцин и редко гранулы меланина (клетки Педжета). Клетки собираются в скопления в центре и в нижних слоях эпидермиса и в верхних слоях дермы. Как правило, поражены крупные протоки соска, у 30-60% больных изменения соска сочетаются с формированием узла инфильтративного протокового рака в молочной железе.
Клетки Педжета обнаруживают разрозненно или в группах в эпидермисе и предлежащих протоках. Клетки Педжета крупные, выражено ядрышко, цитоплазма обильная.

Если имеется прорастание опухолью околососковой зоны, клетки рака располагаются на фоне элементов клеточного распада («голых» ядер разрушенных клеток, в том числе полиморфных, детрита, фибрина) и воспаления (нейтрофильных лейкоцитов, лимфоидных элементов, макрофагов; могут присутствовать гигантские многоядерные гистиоциты).
При микроскопическом исследовании выявляются солидные и протокоподобные структуры различной величины, «плавающие в озерах» слизи, разделенной на отдельные сектора тонкими фиброзными перегородками. Клетки округлой формы сравнительно однотипны, митозы практически отсутствуют (рис. 101). Иногда отмечается внутриклеточная продукция муцина, а при окраске по Гримелиусу может выявляться нейро-эндокринная дифференцировка опухоли.
Прогноз благоприятный: 10-летняя выживаемость составляет 80-100%. Нередко слизистый рак комбинируется с инвазивным протоковым и дольковым раком, тогда прогноз определяется этими компонентами опухоли.




Цитологическая картина характеризуется обилием слизи в препарате. «Озера» слизи составляют фон препарата (гомогенные сине-фиолетовые или розовато-сиреневые массы при окрашивании по Романовскому.
Апокриновый рак характеризуется образованием структур, типичных для инвазивного протокового рака, но клетки имеют характерный вид с хорошо выраженной эозинофильной цитоплазмой. Ядра клеток характеризуются выраженным полиморфизмом, четко дифференцируются крупные ядрышки. Цитоплазма обильная гомогенная или слегка зернистая, содержит РАS-положительные диастазорезистентные вещества, такие же вещества имеются и в просвете структур. Митотическая активность выражена слабо или умеренно.
Гистологически различают крупноклеточный ороговевающий, веретеноклеточный, акантолитический и аденопластический варианты.
В «чистом виде» опухоль встречается редко, чаще она представляет собой участки плоскоклеточной дифференцировки в опухоли, имеющей строение протокового рака. Поэтому, если при пункции получают необильный материал, представленный элементами плоскоклеточного рака, прежде чем уверенно судить о гистогенезе опухоли, желательно повторить пункцию, чтобы исключить или установить наличие протокового рака с участками плоскоклеточной дифференцировки.

При плоскоклеточном раке обнаруживают клетки плоского типа, располагающиеся разрозненно или в небольших группах, цитоплазма обильная с признаками ороговения (плотная, блестящая, ясно-голубого, серого, синего цвета). Особенно хорошо видны признаки ороговения цитоплазмы при окрашивании мазков по Папаниколау (ярко-оранжевая плотная цитоплазма).
Ядра гиперхромные, с угловатыми границами, структура хроматина просматривается с трудом. Фон препарата составляют некротические массы, обломки ороговевшей цитоплазмы, встречаются безъядерные клетки (чешуйки). Иногда обнаруживают гигантские многоядерные клетки, появление которых считают реакцией на кератин (рис. 108, 109).
Признаки злокачественности при плоскоклеточном раке могут быть выражены нерезко. В этом случае следует проводить дифференциальный диагноз между злокачественной опухолью и фиброаденомой (в том числе листовидной) с плоскоклеточной метаплазией, а также с эпидермальной кистой. При этих поражениях также могут встречаться и клетки плоского типа и чешуйки, однако цитоплазма клеток менее плотная, ядра с ровными контурами, хроматин распределен равномерно (рис. 110).
Опухоль развивается из мезенхимальной ткани молочной железы, составляет около 1% злокачественных опухолей.
Злокачественная листовидная опухоль
Клеточная строма, состоящая из веретенообразных клеток с атипией, характерно обилие фигур митоза. Эпителий, окружающий опухоль, имеет листовидные выросты; обычно эпителиальный компонент доброкачественный. Прогноз различный, зависит от митотической активности опухоли и ядерного полиморфизма: чем они выраженнее, тем опухоль агрессивнее.
Лечение такое же, как рака, но не обязательно удаление лимфатических узлов, так как опухоль метастазирует гематогенным путем.

Обильный клеточный состав. Большая часть клеток вытянутой формы, цитоплазма вытянута по полюсам клетки. Встречаются многоядерные клетки и клетки уродливой формы (рис. 111, 112).
Метастазы в молочной железе
Вторичные опухоли встречаются редко. Первичным очагом может быть лейкоз, лимфома, меланома, рак легкого, эндометрия и др.
| Страница 1 2 3 4 5 6 7 8 9 10 | всего страниц: 10 |
Источник: И.П. Шабалова, Т.В.Джангирова, Н.Н.Волченко, К.К.Пугачев. Цитологический атлас: Диагностика заболеваний молочной железы.- М.-Тверь: ООО «Издательство «Триада», 2005
Гистологическая дифференцировка рака молочной железы
Международные названия
Содержание
Гистологическую градацию РМЖ впервые ввел R.B. Greenough из Бостона, который в 1925 г. опубликовал анализ 73 случаев РМЖ [6]. Несмотря на то что прошло много времени и опубликовано большое количество работ о применении гистологической градации РМЖ, ничего существенного не добавлено в перечень морфологических критериев, определяющих группы РМЖ, имеющих клиническое значение [8–11]. Работа R.B. Greenough актуальна и сегодня, он сформулировал прогностически значимые категории инвазивного РМЖ низкой, средней и высокой степени злокачественности.
Это деление базируется на 5 признаках:
В соответствии с градациями по Greenough типы рака высокой степени злокачественности имеют клетки и ядра неправильной формы и различного размера, без секреторной функции, клетки расположены столбцами, отмечают гиперхроматоз ядер и большое количество атипичных митозов. И наоборот, опухоли, состоящие из желез, построенных из единообразных по размеру и строению клеток без гиперхроматоза, с малым количеством митозов, следует относить к РМЖ низкой степени злокачественности. По данным R.B. Greenough, после радикальной мастэктомии пациентки с раком низкой степени злокачественности были излечены в 68%, умеренной — в 33% случаев и нулевым был результат при высокой.
Bloom и Richardson установили что 26% из 1409 исследованных случаев РМЖ имели 1-ю степень гистологической злокачественности, 45% — 2-ю, 29% — 3-ю. Результаты сравнения гистологических степеней злокачественности первичной опухоли и метастазов в аксиллярных лимфатических узлах показали, что в 82% степени совпадали. В 12% случаев степень злокачественности была выше, а в 6% — ниже в метастазе, чем в первичной опухоли. Авторы выявили, что степень гистологической злокачественности, как и статус регионарных лимфатических узлов, дает независимую прогностическую информацию [14, 15] (табл. 2).
| Степень гистологической градации | Без метастазов в лимфоузлах, % | С метастазами в лимфоузлах, % |
| 1 | 86 | 66 |
| 2 | 68 | 33 |
| 3 | 64 | 19 |
| Степень гистологической градации | Без метастазов в лимфоузлах, % | С метастазами в лимфоузлах, % |
| 1 | 61 | 51 |
| 2 | 47 | 14 |
| 3 | 42 | 9 |
| Степень гистологической градации | Без метастазов в лимфоузлах, % | С метастазами в лимфоузлах, % |
| 1 | 49 | 15 |
| 2 | 29 | 11 |
| 3 | 25 | 7 |
Важность этого показателя очевидна, однако в ряде публикаций гистологическое стадирование подвергается жесткой критике из-за трудности, возникающей при его воспроизводимости [16]. Отмечают, что процент расхождения в оценке гистологической дифференцировки иногда составляет 50–60%. Однако когда критерии оценки гистологической степени злокачественности оценивают профессионально и тщательно, совпадение результатов этой оценки составляет 90% [8, 18]. Н. F. Frierson и соавторы прорецензировали патологоанатомические заключения 7 патологоанатомов, проводивших исследование 75 случаев инвазивного протокового РМЖ. Совпадение при оценке гистологической структуры составило 71%, тубулярных структур — 81%, полиморфизма ядер — 64%, митозов — 67% [17].
С.W. Elston рекомендует проводить двойное исследование [8, 9]. Это возможно при проведении исследования двумя патологами или одним патологом дважды на разных образцах.
Модифицированная схема по Scraff — Bloom — Richardson
А. Оценка полиморфизма ядра: 1, 2, 3 балла присваивают соответственно схеме Bloom — Richardson
Суммирование баллов по этим двум показателям позволит определить градацию рака: G- 1 —2 балла, G- 2 — 3 балла, G- 3 — 4 балла, G- 4 — 5 баллов, G- 5 — 6 баллов.
C.W. Elsston с соавторами в своих исследованиях изучили прогностическое значение гистологических типов РМЖ [8, 9]. Результаты их исследований показали, что «особые типы РМЖ» составляют около 25% и большинство из них относятся к G- 1. Использование гистологического типа вместе с градациями по Bloom и Richardson помогает более точно прогнозировать поведение опухоли.
10-летняя выживаемость больных инвазивным РМЖ (Pereira Н. et al., Histopathol, 1995)