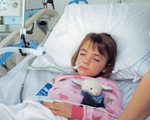
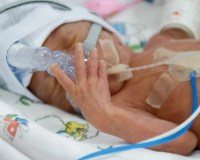
Реанимация и интенсивная терапия новорожденных с асфиксией
Общепринятого определения асфиксии новорожденного пока не существует. Наиболее информативной и объективной представляется дефиниция асфиксии, представленная Н. П. Шабаловым и соавторами (2003). Они считают асфиксией новорожденного синдром, характеризующ
Общепринятого определения асфиксии новорожденного пока не существует. Наиболее информативной и объективной представляется дефиниция асфиксии, представленная Н. П. Шабаловым и соавторами (2003). Они считают асфиксией новорожденного синдром, характеризующийся отсутствием эффективности газообмена в легких сразу после рождения, неспособность самостоятельно дышать при наличии сердцебиений и (или) других признаков живорожденности (спонтанное движение мышц, пульсация пуповины).
До середины 1980-х гг. основным критерием диагностики асфиксии была оценка по шкале Апгар, что нашло отражение в Международной классификации болезней 9-го пересмотра (1975). Однако в 1986 г. Американская академия педиатрии и Американский колледж акушеров и гинекологов на основании многочисленных катамнестических исследований пришли к заключению о том, что баллы по шкале Апгар через 1 и 5 мин после рождения слабо коррелируют как с причиной данного состояния, так и с прогнозом и сами по себе не должны рассматриваться как показатели проявления или последствия асфиксии.
В то же время при состоянии с низкой оценкой по шкале Апгар (0–3 балла), сохраняющемся в течение 15 мин, детский церебральный паралич наблюдается у 10%, а в течение 20 мин — у 60% пациентов.
Несмотря на критическое отношение к шкале Апгар и вопреки мнению о том, что она не должна рассматриваться в качестве критерия диагностики и степени тяжести асфиксии в родах (Н. П. Шабалов и соавт., 2003), целесообразо обратиться непосредственно к Международной классификации болезней 10-го пересмотра (1993).
Рубрика Р 21. Асфиксия при родах
Примечание. Эту рубрику не следует использовать при низких показателях по шкале Апгар без упоминания об асфиксии и других дыхательных расстройствах.
Р 21.0. Тяжелая асфиксия при рождении.
Пульс при рождении менее 100 уд./мин, замедляющийся или устойчивый, дыхание отсутствует или затруднено, кожа бледная, мышцы атоничны. Асфиксия с оценкой по шкале Апгар 0–3 балла через минуту после рождения. Белая асфиксия.
Р 21.1. Средняя и умеренная асфиксия при рождении.
Нормальное дыхание в течение первой минуты после рождения не установилось, но частота сердцебиений составляет 100 уд./мин или более, незначительный мышечный тонус, незначительный ответ на раздражение.
Оценка по шкале Апгар 4–7 баллов через минуту после рождения. Синяя асфиксия.
Различают также острую асфиксию, являющуюся проявлением интранатальной гипоксии, и асфиксию, развившуюся на фоне хронической внутриутробной антенатальной гипоксии.
Частота встречаемости асфиксии новорожденных, по данным различных авторов, колеблется в весьма широких пределах, что, очевидно, связано с отсутствием общепринятой дефиниции. Так, Саrter и соавторы (1993) полагают, что частота асфиксии составляет 1–1,5%. Еще в 10–15% случаев низкая оценка по шкале Апгар оказывается обусловлена кардиореспираторной депрессией. В сумме названные состояния составляют до 16,5%. Примерно такие же показатели за 2003 г. опубликованы Министерством здравоохранения и социального развития РФ. При этом летальность от асфиксии среди доношенных детей составляет 0,2%, а среди недоношенных — 1,16%.
По данным С. Г. Эзутаган (1999), частота перинатальной асфиксии у недоношенных детей составляет 30%, а у доношенных новорожденных — 20%.
Н. Н. Володин и С. О. Рогаткин (2004) сообщают, что ежегодно в мире рождаются в состоянии асфиксии 4 млн детей: 840 тыс. из них умирают, еще столько же в дальнейшем страдают от стойких нарушений функциональной деятельности центральной нервной системы.
Выделяют пять главных причин асфиксии новорожденного.
Гипоксемия, гиперкапния и связанный с ними ацидоз являются ведущими звеньями патогенеза асфиксии. Они активируют гемодинамическое перераспределение объемов крови, секрецию гормонов стрессового типа, продукцию цитокинов, молекул адгезии и факторов роста, каскадную систему плазменных протеаз. Эти же факторы после реоксигенации активируют перекисное окисление липидов клеточных мембран с образованием метаболитов арахидоновой кислоты (простагландинов и лейкотриенов) и повышением содержания клеточных метаболитов (аденозина, оксида азота, эндотелина и др.).
Напряжение кислорода в крови ниже 40 мм рт. ст. включает так называемый «ишемический рефлекс», хеморецепторный механизм которого приводит к возбуждению одновременно вазомоторного и дыхательного центров, централизации кровообращения, т. е. ишемии кожи, легких, почек, печени, желудочно-кишечного тракта, ради обеспечения жизненно важных органов (сердца, мозга, диафрагмы, надпочечников).
В процессе централизации кровообращения, кроме адреналина и норадреналина, участвуют ангиотензин II и вазопрессин.
Высокое сопротивление сосудов малого круга, поддерживаемое гипоксемией и гиперкапнией, является причиной легочной гипертензии и шунтирования крови, дыхательной недостаточности, а также перегрузки правых отделов сердца давлением, а левых отделов — объемом.
Отрицательным эффектом гипоксемии, гиперкапнии и централизации кровообращения является накопление недоокисленных продуктов и тяжелый смешанный ацидоз. Компенсаторная активация анаэробного гликолиза с накоплением лактата еще больше усиливает ацидоз. Последний крайне отрицательно влияет на системную гемодинамику, микроциркуляцию, гемореологию, водно-электролитный баланс, обменные процессы.
Нарастание гипоксии и смешанного ацидоза вызывает раскрытие прекапиллярных сфинктеров, децентрализацию кровообращения с падением артериального давления, т. е. гемодинамический коллапс, снижающий тканевую перфузию в жизненно важных органах.
В сосудах ишемизированных тканей активизируются тромбоциты, эндотелиоциты, моноциты, что приводит к активации каскада плазменных протеаз, а также освобождению клеточных ферментов, про- и антикоагулянтов, метаболитов арахидоновой кислоты, активных форм кислорода и оксида азота, которые причастны к повреждению функции органов.
Активация тромбиновой, фибринолитической, кининовой и системы комплемента ведет к эндотоксикозу продуктами протеолиза и наряду с ацидозом — к повреждению мембран клеток, митохондрий, лизосом, гематоэнцефалического барьера, повышению сосудистой проницаемости, падению сосудистого тонуса, деструкции клеток, отеку интерстициального пространства, сладж-феномену, запуску внутрисосудистого свертывания, тромбозу, блокаде микроциркуляции, дистрофическим процессам, в конечном счете — к полиорганной недостаточности.
Клинические признаки и симптомы
При асфиксии средней тяжести ребенок рождается с апноэ или с единичными гаспами, с частотой сердцебиений 90–160 уд./мин, со сниженным мышечным тонусом и рефлекторным ответом на назофарингеальный катетер, с выраженным цианозом (синяя асфиксия). Общее состояние оценивается как тяжелое или средней тяжести. В первые минуты жизни ребенок вял, быстро охлаждается. Слабо реагирует на осмотр и раздражения. Спонтанная двигательная активность низкая. Физиологические рефлексы угнетены. При аускультации сердца часто выявляют тахикардию, приглушенность тонов, акцент II тона над легочной артерией. Дыхание нередко с участием вспомогательной мускулатуры, аускультации — ослабленное, с обилием сухих и разнокалиберных влажных хрипов.
Нередко уже в первые часы жизни появляются гипервозбудимость, крупноразмашистый тремор рук, гиперстезия, спонтанный рефлекс Моро, кратковременные судороги. В то же время у некоторых пациентов нарастают клинические признаки угнетения центральной нервной системы. Динамика мышечного тонуса, физиологические рефлексы, признаки угнетения или повышенной возбудимости нервной системы весьма индивидуальны и во многом зависят от адекватности оказания помощи.
Тяжелая асфиксия характеризуется наличием при рождении признаков II или III стадии шока: дыхание отсутствует или наблюдаются неэффективные гаспы, пульс менее 100 уд./мин, кожные покровы очень бледные (белая асфиксия), мышцы атоничны, реакция на назофарингеальный катетер отсутствует, симптом «белого пятна» более 3 с, артериальная гипотония.
Общее состояние оценивается как тяжелое или крайне тяжелое.
В первые часы и дни жизни клиническая картина обусловлена полиорганной недостаточностью. Со стороны центральной нервной системы: гипоксически-ишемическая энцефалопатия, отек мозга, внутричерепные кровоизлияния, судороги.
Со стороны легких: синдром аспирации меконием, легочная гипертензия, синдром дыхательных расстройств II типа.
Со стороны сердечно-сосудистой системы: шок, гипотензия, полицитемия, гиперволемия или гиповолемия, патологическое шунтирование крови, трикуспидальная недостаточность, ишемические некрозы эндокарда/миокарда.
Со стороны выделительной системы: олигурия, острая почечная недостаточность с тромбозами сосудов почек или без них.
Со стороны желудочно-кишечного тракта: функциональная непроходимость, рвота, срыгивания, печеночные дисфункции, некротизирующий энтероколит.
Со стороны эндокринной системы: транзиторная недостаточность симпато-адреналовой системы, щитовидной железы, надпочечников.
Все это сопровождается нарушениями гомеостаза (декомпенсированный ацидоз, гипогликемия, гипокальциемия, гипоантриемия, гипомагниемия) и гемостаза (тромбоцитопения, ДВС-синдром).
Вторичный иммунодефицит, сопровождающий полиорганную недостаточность, способствует активации и генерализации внутриутробных инфекций, а также развитию госпитальных инфекций.
Диагностика и рекомендуемые клинические исследования
Критериями тяжелой асфиксии являются:
Важными критериями тяжести асфиксии являются ответ на адекватную терапию, а также течение и исход патологии в раннем неонатальном периоде, отражающие выраженность повреждения витальных функций. Следовательно, окончательно тяжесть асфиксии диагностируют не сразу после родов, а по окончании раннего неонатального периода.
Необходимый объем исследований:
В оптимальном варианте — допплерографическое определение центральной и церебральной гемодинамики.
С учетом необходимости проведения дифференциального диагноза с тяжелыми инфекционными заболеваниями показано микробиологическое, вирусологическое исследование.
Дифференциальный диагноз в первую очередь необходимо проводить со следующими состояниями:
Общие принципы лечения
Проведение реанимационных мероприятий при асфиксии новорожденных регламентируется приказом министра здравоохранения и медицинской промышленности РФ «Первичная и реанимационная помощь новорожденному в родильном зале» (1995 г.).
При оказании реанимационной помощи новорожденному необходимо строго соблюдать следующую последовательность действий:
Лекарственные средства (ЛС) при первичной реанимации назначаются при отсутствии сердцебиения и в тех случаях, когда несмотря на искусственную вентиляцию легких (ИВЛ) 100% кислородом и непрямой массаж сердца, проведенные в течение 30 с, у ребенка сохраняется брадикардия ниже 80 уд./мин.
Используются следующие ЛС: раствор адреналина гидрохлорида, препараты, восполняющие объем циркулирующей жидкости (раствор альбумина 5%, изотонический раствор натрия хлорида, раствор рингера), раствор гидрокарбоната натрия 4%.
Адреналина гидрохлорид является синтетическим аналогом адреналина надпочечников. Обладает адренопозитивным действием, оказывая стимулирующее влияние на α- и β-адренорецепторы. Инотропное кардиотоническое действие адреналина связано с воздействием на β1-адренорецепторы, локализующиеся в миокарде. Это ведет к повышению силы и частоты сердечных сокращений. Наряду с этим адреналин, воздействуя на α-адренорецепторы, повышает периферическое сосудистое сопротивление и артериальное давление крови, тем самым увеличивая коронарный кровоток и кровоснабжение миокарда.
Бронхорасширяющее действие адреналина обусловлено воздействием на β2-адренорецепторы.
Адреналин вводится новорожденным в разведении 1:10 000 в объеме 0,1–0,3 мл/кг массы тела (0,01–0,03 мг/кг) внутривенно или эндотрахеально. При введении через эндотрахеальную трубку требуется дополнительное разведение физиологическим раствором (1:1). Внутривенно адреналин вводится струйно.
В результате должно наблюдаться увеличение частоты сердечных сокращений до 100 уд./мин и выше через 30 с после введения ЛС. Если частота сердечных сокращений остается менее 100 уд./мин, следует повторить введение адреналина. При отсутствии эффекта и признаков общей кровопотери или гиповолемии необходимо ввести восполнители объема циркулирующей крови.
Показаниями к восполнению объема циркулирующей крови служат кровопотеря и гиповолемия. При этом наблюдаются следующие симптомы:
Восполнители объема циркулирующей крови (изотонический раствор натрия хлорида, раствор альбумина 5%, раствор рингера) вводятся новорожденным при первичной реанимации в вену пуповины из расчета 10 мл/кг массы тела в течение 5–10 мин.
Показания к применению гидрокарбоната натрия:
Используется 4% раствор гидрокарбоната натрия, содержащий 0,5 мэкв/мл. Назначается в дозе 2 мэкв (4 мл 4% раствора) на кг массы тела. Вводится в вену пуповины на фоне ИВЛ со скоростью не выше 1 мэкв /кг/мин.
Ожидаемый эффект: увеличение частоты сердечных сокращений до 100 и более ударов в минуту на фоне уменьшения метаболического ацидоза.
Положительный эффект от реанимационных мероприятий — в течение первых 20 мин после рождения восстанавливаются адекватное дыхание, нормальные частота сердечных сокращений и цвет кожных покровов — служит основанием к прекращению ИВЛ и непрямого массажа сердца. Однако реанимация в родильном зале является лишь первым этапом оказания помощи детям, родившимся c асфиксией.
Дальнейшее наблюдение и лечение новорожденных, перенесших асфиксию, в том числе и детей, у которых не восстановилось адекватное дыхание, наблюдаются судороги, центральный цианоз, проводится в отделении интенсивной терапии.
При внутривенном введении раствора гидрокарбоната натрия на фоне неадекватной вентиляции возможно усиление ацидоза, а избыточное введение этого ЛС ведет к гипернатриемии и риску развития внутрижелудочковых кровоизлияний.
Эффективная сердечно-легочная реанимация при асфиксии является главным фактором, улучшающим прогноз. При средней и умеренной асфиксии прогноз, как правило, благоприятный. При тяжелой асфиксии персистирующая низкая оценка по шкале Апгар (0–3 балла) на 10, 15 и 20-й минутах достаточно тесно коррелирует с неблагоприятным исходом и указывает на повышенный риск смерти (60% — у доношенных новорожденных и 50–100 % — у детей с очень малой массой тела).
Литература
А. Г. Антонов, доктор медицинских наук, профессор
НЦАГиП РАМН, Москва
Кома у ребенка
Кома у ребенка — это нарушение сознания, сопровождающееся отсутствием психической деятельности, расстройствами всех видов чувствительности и двигательных функций. Основные причины патологии в педиатрии: перинатальные повреждения ЦНС, травмы головы, нейроинфекции и эндокринные расстройства. Для диагностики комы выполняется полное неврологическое обследование ребенка, стандартные анализы крови, методики нейровизуализации для установления этиологии. Интенсивная терапия включает адекватную оксигенацию, коррекцию водно-электролитного баланса и борьбу с отеком мозга, проведение этиопатогенетического лечения.
МКБ-10
Общие сведения
Кома (от греческого «koma» ‒ глубокий сон) является симптомокомплексом тяжелых повреждений нервной системы или метаболических нарушений, а не самостоятельным заболеванием. Состояние встречается у 5% детей, поступающих в отделение реанимации и интенсивной терапии (ОРИТ). В современной педиатрии проблема расстройств сознания очень актуальна, поскольку от слаженных действий врача в первые часы развития комы зависит прогноз для жизни ребенка и восстановления его неврологических функций.
Причины
Нарушенное сознание отмечается при сотне различных патологических состояний. Специалисты называют основной причиной комы у младенцев врожденные и инфекционные поражения ЦНС, у дошкольников — отравления, у школьников — черепно-мозговые травмы. Все этиологические факторы можно разделить на несколько групп, среди которых:
Патогенез
Независимо от первичного этиологического фактора, развитие коматозного состояния идет по сходным механизмам и представлено несколькими типичными этапами. Церебральная недостаточность в основном вызвана расстройствами формирования и передачи нервных импульсов между участками головного мозга, что служит ответом на недостаточное снабжение органа кислородом и энергетическими соединениями. В нейронах нет запасов энергии, поэтому даже при кратковременных нарушениях сознание угнетается.
Постепенно нарастает гипоксия тканей, связанная с торможением дыхательного центра и отсутствием адекватной самостоятельной вентиляции легких. У ребенка происходят метаболические изменения, провоцирующие отек и набухание головного мозга и его оболочек. В это же время формируются расстройства регуляции вегетативных функций, которые усугубляют водно-электролитные нарушения и замыкают «порочный круг» патогенеза комы.
Классификация
По этиологическому фактору комы делят на цереброгенные, обусловленные поражением ЦНС, и нецереброгенные, которые возникают под действием метаболических, токсических или инфекционных факторов. По шкале Глазго патологическому состоянию соответствует оценка от 3 до 8 баллов. В практической медицине широко используется систематизация по тяжести, согласно которой выделяют 4 степени:
Симптомы комы у ребенка
Родители обнаруживают, что ребенок не реагирует на звуки и прикосновения, не открывает глаза, его руки и ноги безвольно лежат в неестественной позе. Кожные покровы могут иметь различный вид: бледные с синюшным оттенком, ярко-розовые, слишком сухие или покрытые липким потом. Иногда родители замечают стонущее или прерывистое дыхание, сопровождающееся хриплыми звуками. Лицо может быть загрязнено рвотными массами.
Специфические отличительные черты коматозного состояния зависят от особенностей повреждающего фактора. При ЧМТ зачастую видна кровь и открытая рана на голове, а произошедшие события можно установить по окружающей обстановке (падение на улице, ДТП, криминальное происшествие). При эпилептическом статусе у ребенка наблюдаются периодические судороги всего тела, выделение розовой пены изо рта, непроизвольные мочеиспускание и дефекация.
Для кетоацидотической комы типична сухость кожи и слизистых, запах ацетона из ротовой полости, редкое шумное дыхание. При гипогликемическом нарушении сознания коме предшествует период возбуждения, дрожь во всем теле, головокружение и предобморочное состояние. При наличии уремии от ребенка исходит резкий запах мочи, кожа сухая и покрыта расчесами, возможны редкие мышечные подергивания.
Осложнения
Показатель летальности при комах составляет 10-90% в зависимости от их причин и степени тяжести. Негативные последствия нарушения сознания делятся на 2 группы: непосредственно связанные с повреждением нейронов и обусловленные утратой нервной регуляции внутренних органов. Более опасна первая категория, которая включает остановку дыхания, критические расстройства гемодинамики, центральную гипертермию.
Кома, если только она не вызвана травмой, свидетельствует о нарушениях работы организма и декомпенсации основного заболевания. У 88% пациентов в течение года после эпизода нарушенного сознания случается рецидив, который нередко приводит к летальному исходу. У 25% детей с ЧМТ выявляются отдаленные последствия, поэтому в ближайшие пару лет у них повторяется состояние комы.
Диагностика
Чтобы установить степень комы, достаточно осмотра, который проводится по стандартной схеме. Врач-реаниматолог обследует кожный покров, проверяет состояние дыхательной и сердечной деятельности, изучает функции ЧМН и безусловные рефлексы. У ребенка оценивают симптомы Брудзинского и Бабинского, двигательную реакцию и мышечный тонус. Для выявления причины коматозного состояния делают расширенную диагностику, в которую включают:
Лечение комы у ребенка
На догоспитальном и госпитальном этапе обеспечивается недифференцированная терапия коматозных состояний, от своевременности и полноты которой зависит жизнь ребенка. Она направлена на стабилизацию витальных функций и поддержание адекватного уровня сознания до выяснения первопричины нарушений и их устранения. Лечение комы, проводимое в ОРИТ, включает следующие направления:
Одновременно с интенсивной терапией врачи осуществляется дифференциальную диагностику комы. После установления варианта коматозного состояния к лечению подключают профильных детских специалистов: эндокринолога, гастроэнтеролога, инфекциониста и т.д. Если врачи подозревают закрытую ЧМТ или объемное церебральное новообразование, ребенку необходима помощь нейрохирургов.
Прогноз и профилактика
Кома — крайне тяжелое состояние, которое без лечения заканчивается летальным исходом, поэтому прогноз определяется своевременностью и адекватностью терапии. При ранней коррекции патологии и устранении ее первопричины удается восстановить уровень бодрствованиям и неврологические функции. Длительное и глубокое нарушение сознания у ребенка считается прогностически неблагоприятным. Профилактика включает устранение этиологических факторов комы.
Последствия перинатального поражения центральной нервной системы с атонически–астатическим синдромом
Общая информация
Краткое описание
Союз педиатров России
Год утверждения (частота пересмотра): 2016 (пересмотр каждые 3 года)
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Этиология и патогенез
Наиболее частыми причинами последствий перинатального поражения ЦНС с атонически- астатическим синдромом являются перинатальные поражения центральной нервной системы гипоксически-ишемического генеза: церебральная ишемия II, III степени, внутричерепное кровоизлияние II, III степени. Поражение лобных долей, мозжечка, лобно-мосто-мозжечкового пути.
Наиболее часто геморрагический инфаркт и ишемия развиваются у плодов и новорожденных в области перивентрикулярных сплетений – субэпендимально в сочетании с поражением вещества мозга. Кровоизлияние может происходить также в боковые желудочки мозга и в субарахноидальное пространство. Помимо описанных изменений, морфологическим субстратом гипоксии, как правило, является полнокровие мозга, его общий или локальный отек.
В патогенезе гипоксически-травматических и гипоксически-ишемических энцефалопатий причины и следствия меняются местами, переплетаются в сложных «порочных кругах». Нарушение гемодинамики (макро- и микроциркуляции) приводят к многовариантным метаболическим сдвигам (нарушение кислотно-основного состояния и электролитного баланса, дестабилизация клеточных мембран, гипоксемия и тканевая гипоксия), а эти сдвиги в свою очередь усугубляют расстройства микроциркуляции.
У недоношенных детей повреждающее действие внутриутробной гипоксии потенцируется незрелостью сосудов головного мозга, дезадаптацией в интранатальном периоде.
Установлено, что повреждающее воздействие различных факторов может реализоваться как в форме быстрой гибели клетки (нейрональный некроз), так и в форме отсроченной, замедленной гибели – апоптоз.
Эпидемиология
Диагностика
• Раннюю диагностику формирующегося детского церебрального паралича рекомендуется проводиться на первом году жизни ребенка: при своевременном выявлении у него задержки моторного и психо-речевого развития, нарушений мышечного тонуса, повышении сухожильных рефлексов, несвоевременной редукции безусловных рефлексов и задержке формирования установочных реакций [6, 7, 18].
Комментарии: для проведения дифференциального диагноза с болезнями обмена веществ
Дифференциальный диагноз
Лечение
— Гинкго двулопастного листьев экстракт (Код АТХ: N06DX02) 0,02 на в 2 приема, курс 2 месяца.
— Витамины (В1, В6, В12)