Гомологический ряд алканов
Алканы (парафины) – линейные органические углеводороды, атомы которых соединены одинарными связями. Они служат топливом для машинных механизмов, а в микробиологической промышленности применяется с целью получения белков.
Изомерия и гомологический ряд
Для алканов свойственны следующие виды изомерии.
Гомологи алканов в соответствии с систематической номенклатурой называются по следующей схеме.
Таблица гомологического ряда и номенклатура алканов
| Формула | Название |
| CH4 | метан |
| C2H6 | этан |
| C3H8 | пропан |
| C4H10 | бутан |
| C5H12 | пентан |
| C6H14 | гексан |
Электронное строение
Имеют форму тетраэдра. Следовательно, гибридные облака одинаковы. Углы между облаками — 109° 28’. Связи одинарны. Атомы углерода в алканах находятся в 
Связь «углерод-углерод» неполярна. Длина ее — 0,154 нм, а энергия – 350 КДж/моль. Данная связь довольно прочная, поэтому реакции проходят в жестких условиях.
Физические свойства
Температуры плавления и кипения зависит от длины молекулы. Чем больше главная цепь, тем температура выше. Первые пять алканов гомологического ряда находятся в газовом состоянии. Углеводороды, содержащие с 5 до 15 атомов, — жидкости. Последующие алканы – твердые.
Газоорбразные и твердые не имеют запаха, в отличие от жидкостей. Все парафины бесцветны и не растворимы в воде.
Способы получения
Алканы в природе находят в:
Природные смеси трудно разделимы, поэтому есть синтетические метод.
Такая реакция сопровождается увеличением углеродной цепи в структурной формуле. Она часто используется для симметричных молекул, т.к. из нескольких исходных веществ получается смесь.
R-Cl + 2 Na + Cl-R’ → R-R’ + R-R + R’-R’ + 2 NaCl
Химические свойства
Алканы – это органические соединения, которым не свойственны реакции присоединения. Для этого класса характерны:
Связь «углерод-водород» разрывается гомолитически, т.е. каждому оторвавшемуся атому достается по одному электрону. В процессе образуются радикалы.
Реакции замещения водорода
Позднее был разработан метод парофазного нитрования. В нем используется азотная кислота в парах при температуре 250°С.
Реакции разложения
1. Дегидрирование и дегидроциклизация
Дегидрирование – процесс отщепления водорода. Идет в присутствии никеля, платины, железа.
В реакциях с соединениями из 2-4 атомов углерода рвутся связи «углерод-водород» и образуются углеводороды с кратными связями.
Алканы с пятью и более атомами углерода образуют цикл. Реакции происходят в присутствии платины.
Алканы с углеродной цепью из шести и более атомов образуют замкнутые циклы.
Проводится при температуре до 1500°С. Нагревают долго и медленно.
Если нагревать быстро, то образуется ацетилен.
Это разложение молекулы на короткие алканы и алкены. Существуют:
Реакции окисления алканов
Парафины – это малополярные соединения. Не окисляются в нормальных условиях.
Алканы под действием кислорода образуют углекислый газ и воду.
При недостатке кислорода:
2. Окисление под действием катализатора
Это один из способов синтеза уксусной кислоты, метанола или муравьиной кислоты в промышленных масштабах.
Изомеризация алканов
Под действием температуры и катализаторов из неразветвленных парафинов образуются изомеры алканов.
Газообразные алканы используют как топливо, а жидкие – в качестве растворителей. Вазелин – один из представителей твердых алканов. Он широко применяется в медицине.
Алканы в нормальных условиях инертны и их реакции протекают в жестких условиях. Из-за своей предельности им характерны реакции присоединения. Им свойственен радикальный механизм. Алканы – это составная часть нефти, которая применяется во многих сферах. Поэтому парафины имеют большое значение в жизни человека.
Какие типы изомерии характерны для алканов
I. АЛКАНЫ (предельные углеводороды, парафины)
Алканы – алифатические (ациклические) предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными) связями в неразветвленные или разветвленные цепи.
Алканы – название предельных углеводородов по международной номенклатуре.
Парафины– исторически сложившееся название, отражающее свойства этих соединений (от лат. parrum affinis – имеющий мало сродства, малоактивный).
Предельными, или насыщенными, эти углеводороды называют в связи с полным насыщением углеродной цепи атомами водорода.
Простейшие представители алканов:

Теперь можно вывести общую формулу алканов. Число атомов углерода в ряду алканов примем за n, тогда число атомов водорода составит величину 2n+2. Следовательно, состав алканов соответствует общей формуле CnH2n+2.
Поэтому часто используется такое определение:
Химическое строение (порядок соединения атомов в молекулах) простейших алканов – метана, этана и пропана – показывают их структурные формулы. Из этих формул видно, что в алканах имеются два типа химических связей:
Электронные и структурные формулы отражают химическое строение, но не дают представления о пространственном строении молекул, которое существенно влияет на свойства вещества.
Пространственное строение, т.е. взаимное расположение атомов молекулы в пространстве, зависит от направленности атомных орбиталей (АО) этих атомов. В углеводородах главную роль играет пространственная ориентация атомных орбиталей углерода, поскольку сферическая 1s-АО атома водорода лишена определенной направленности.
Четыре σ-связи углерода направлены в пространстве под углом 109 о 28′, что соответствует наименьшему отталкиванию электронов. Поэтому молекула простейшего представителя алканов – метана СН4 – имеет форму тетраэдра, в центре которого находится атом углерода, а в вершинах – атомы водорода:
 |  |
Для записи удобно использовать пространственную (стереохимическую) формулу.
1. Различия в порядке соединения атомов в молекулах (т.е. в химическом строении) приводят к структурной изомерии. Строение структурных изомеров отражается структурными формулами. В ряду алканов структурная изомерия проявляется при содержании в цепи 4-х и более атомов углерода, т.е. начиная с бутана С4Н10.
Причиной проявления структурной изомерии в ряду алканов являетсяспособность атомов углерода образовывать цепи различного строения.Этот вид структурной изомерии называется изомерией углеродного скелета.
Например, алкан состава C4H10 может существовать в виде двух структурных изомеров:
а алкан С 5 Н 12 – в виде трех структурных изомеров,отличающихся строением углеродной цепи:
При выводе структурных формул изомеров используют следующие приемы.
Алканы, начиная с этана H3C–СН3, существуют в различных пространственных формах (конформациях), обусловленных внутримолекулярным вращением по σ-связям С–С, и проявляют так называемую поворотную (конформационную) изомерию.
Различные пространственные формы молекулы, переходящие друг в друга путем вращения вокруг σ-связей С–С, называют конформациями или поворотными изомерами (конформерами).
Поворотные изомеры молекулы представляют собой энергетически неравноценные ее состояния. Их взаимопревращение происходит быстро и постоянно в результате теплового движения. Поэтому поворотные изомеры не удается выделить в индивидуальном виде, но их существование доказано физическими методами. Некоторые конформации более устойчивы (энергетически выгодны) и молекула пребывает в таких состояниях более длительное время.
то возможно существование двух соединений с одинаковой структурной формулой, но отличающихся пространственным строением. Молекулы таких соединений относятся друг к другу как предмет и его зеркальное изображение и являются пространственными изомерами.
Изомерия этого вида называется оптической, изомеры – оптическими изомерами или оптическими антиподами:

Молекулы оптических изомеров несовместимы в пространстве (как левая и правая руки), в них отсутствует плоскость симметрии.
Таким образом,
оптическими изомерами называются пространственные изомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное изображение.
Оптическая изомерия проявляется в органических веществах различных классов и играет очень важную роль в химии природных соединений.
Какие типы изомерии характерны для алканов
Изомерия – явление существования соединений, которые имеют одинаковый состав (одинаковую молекулярную формулу), но разное строение. Такие соединения называются изомерами.
1. Вид изомерии, при которой вещества отличаются друг от друга порядком связи атомов в молекуле, называется структурной изомерией. Строение структурных изомеров отражается структурными формулами.
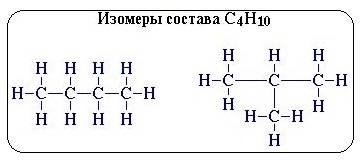
2. Если в молекулах одинакового состава и одинакового химического строения возможно различное взаимное расположение атомов в пространстве, то наблюдается пространственная изомерия (стереоизомерия).
В этом случае использование структурных формул недостаточно и следует применять модели молекул или пространственные (стереохимические) формулы.
2.1. Углеводородные цепи молекул алканов могут вращаться вокруг простых связей, принимать различные геометрические формы и переходить друг в друга.
Различные геометрические формы молекул, переходящие друг в друга путем поворота вокруг C–C связей, называются конформациями или поворотными изомерами (конформерами), а данный вид изомерии – конформационной (поворотной) изомерией.
2.2. Для предельных углеводородов, начиная с гептана, характерен еще один вид пространственной изомерии, когда два изомера относятся друг к другу как предмет и его зеркальное изображение (подобно тому, как левая рука относится к правой). Такие различия в строении молекул называют зеркальной, или оптической изомерией.
Алканы
Алканы – это предельные углеводороды, содержащие только одинарные связи между атомами С–С в молекуле, т.е. содержащие максимальное количество водорода.
Гомологический ряд алканов
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Все алканы легче воды, не растворимы в воде и не смешиваются с ней.
Строение алканов
В молекулах алканов встречаются химические связи C–H и С–С.
Связь C–H ковалентная слабополярная, связь С–С – ковалентная неполярная. Это одинарные σ-связи. Атомы углерода в алканах образуют по четыре σ-связи. Следовательно, гибридизация атомов углерода в молекулах алканов – sp 3 :



Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:

Это соответствует тетраэдрическому строению молекулы.
| Например, в молекуле метана CH4 атомы водорода располагаются в пространстве в вершинах тетраэдра, центром которого является атом углерода |


Молекулам линейных алканов с большим числом атомов углерода соответствует зигзагообразное расположение атомов углерода.
| Наример, пространственное строение н-бутана — зигзагообразное |
Изомерия алканов
Структурная изомерия
Для алканов характерна структурная изомерия – изомерия углеродного скелета.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета отличаются строением углеродного скелета.
| Например. Для н-бутана (алкана с линейной цепью) существует изомер с разветвленным углеродным скелетом – изобутан |
| Бутан | Изобутан |
 |  |
С увеличением числа атомов углерода в молекуле увеличивается количество изомеров, соответствующих данной формуле.
Количество изомеров в ряду алканов:
| Молекулярная формула | Число структурных изомеров |
| CH4 | 1 |
| C2H6 | 1 |
| C3H8 | 1 |
| C4H10 | 2 |
| C5H12 | 3 |
| C6H14 | 5 |
| C7H16 | 9 |
| C8H18 | 18 |
| C9H20 | 35 |
| C10H22 | 75 |
Оптическая изомерия
Если атом углерода в молекуле связан с четырьмя различными заместителями (атомами или атомными группами), например:
то возможно существование двух соединений с одинаковой структурой, но различным пространственным строением.Молекулы таких соединений относятся друг к другу, как зеркальные изображение и предмет. При этом никаким вращением нельзя получить одну молекулу из другой.
Номенклатура алканов
| Например, алкан имеет название 2-метилпропан. Для простейших алканов (метан, этан, пропан, бутан и изобутан) используют тривиальные названия. Начиная с пятиатомного углероводорода, в названии неразветвленных (нормальных) алканов используют корень, который показывает число атомов углерода в молекуле, и добавляют соответствующий суффикс (для алканов – ан, для алкенов – ен, и т.д.). Название разветвленных алканов строится по следующим правилам: 1. Выбирают главную углеродную цепь. При этом считают, что углеводородные радикалы, которые не входят в главной цепь, являются в ней заместителями. При этом главная цепь должна быть самой длинной. Например, в молекуле на рисунке главной является цепь, отмеченная на рисунке а:
Главная цепь должна быть самой разветвленной. Например, в молекуле, изображенной на рисунках а и б, выделены цепи с одинаковым числом атомов углерода. Но главной будет цепь, изображенная на рисунке а, т.к. от нее отходит 2 заместителя, а от цепи на рисунке б – только один:
2. Нумеруют атомы углерода в главной цепи так, чтобы атомы углерода, которые соединены с заместителями, получили минимальные возможные номера. Причем нумерацию следует начинать с более близкого к старшей группе конца цепи. 3. Называют все радикалы, указывая впереди цифры, которые обозначают их расположение в главной цепи. Например, 2-метилпропан:
Для одинаковых заместителей эти цифры указывают через запятую, при этом количество одинаковых заместителей обозначается приставками ди- (два), три- (три), тетра- (четыре), пента- (пять) и т.д. Например, 2,2-диметилпропан или 2,2,3-триметилпентан. 4. Названия заместителей со всеми приставками и цифрами располагают в алфавитном порядке. Например: 2,2-диметил-3-этилпентан. 5. Называют главную углеродную цепь, т.е. соответствующий нормальный алкан. Например, название молекулы на рисунке:
Химические свойства алкановАлканы – предельные углеводороды, поэтому они не могут вступать в реакции присоединения. Для предельных углеводородов характерны реакции: Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов. Поэтому для алканов характерны только радикальные реакции. Алканы устойчивы к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагируют с концентрированными кислотами, щелочами, бромной водой. 1. Реакции замещенияВ молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С. 1.1. ГалогенированиеАлканы реагируют с хлором и бромом на свету или при нагревании. При хлорировании метана сначала образуется хлорметан:
При хлорировании алканов с углеродным скелетом, содержащим более 3 атомов углерода, образуется смесь хлорпроизводных.
Бромирование протекает более медленно и избирательно.
|

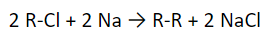

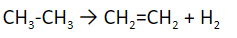
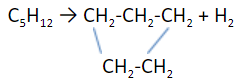
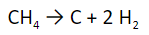

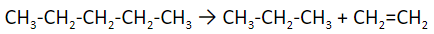
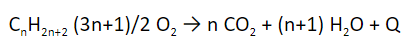
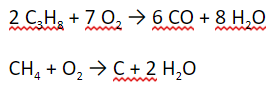
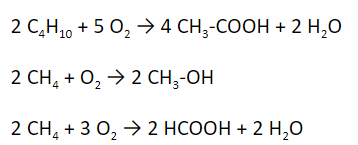





















 Хлорметан может взаимодействовать с хлором и дальше с образованием дихлорметана, трихлорметана и тетрахлорметана:
Хлорметан может взаимодействовать с хлором и дальше с образованием дихлорметана, трихлорметана и тетрахлорметана:





















