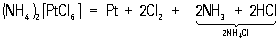Что представляют собой металлы платиновой группы
Металлы платиновой группы имеют своё название – «платиноиды». К металлам платиновой группы относятся шесть драгоценных металлов, а именно: платина, палладий, родий, рутений, иридий и осмий. Общей характерной особенностью для всех этих драгоценных металлов является то, что они имеют серебристо-белый цвет и обладают каталитическими свойствами, которые позволяют им ускорять химические реакции. Эти драгоценные металлы являются химически стойкими, облают высокой электропроводностью и могут выдерживать достаточно высокие температуры. Детальнее об особенностях, формах, перспективах инвестиций, а также ценовой политике данных драгоценных металлах пойдёт речь в этой статье.
Платина и палладий
Из всех драгоценных металлов платиновой группы именно платина и палладий являются классическими банковскими товарами.
Сферы применения платины в процентном соотношении ко всему объёму потребления данного драгоценного металла выглядят следующим образом:
Палладий обладает сходными с платиной свойствами, в связи с чем сферы применения этого драгоценного металла практически идентичны описанным выше.
Ввиду того, что платина и палладий являются банковскими металлами, им присущи традиционные формы инвестиций (за исключением возможности приобретения памятных и (или) инвестиционных монет):
Сегодня перспективы инвестиций в платину и палладий обусловлены стабильным спросом на эти драгоценные металлы, который исходит, в основном, со стороны промышленности. Эксперты утверждают, что отрицательная динамика показателе промышленного спроса на платину и палладий практически невозможна, в связи с чем рост рыночной стоимости на эти драгоценные металлы – неизбежен.
Родий
В феврале 2015 года многие авторитетные издания заявили о возможности появления на мировом рынке драгоценных металлов нового «участника»-металла – родия. Такие заявления являются совершенно небеспочвенными, поскольку элементарный анализ динамики стоимости родия за последний год позволяет прийти к выводу о том, что цена на этот драгоценный металл за указанный промежуток времени выросла на 65%. С учётом превалирующей, в целом, на рынке драгоценных металлов тенденции к снижению котировок данной группы товаров, такая тенденция заставляет задуматься организаторов рынка о выводе родия на новый уровень.
После рекордного роста цен на родий стоимость 1 тройской унции этого драгоценного металла стала снижаться, что, несомненно, предоставляет инвесторам уникальную возможность направлять свои инвестиции именно в этот драгоценный металл сегодня.
Важно отметить, что абсолютным рекордом стоимости 1 тройской унции родия, зафиксированным в 2008 году, стала отметка в 10100 долларов США.
Эксперты отрасли инвестиций в драгоценные металлы отмечают, что стремительное развитие отрасли автомобильной промышленности, которая на 80% обеспечивает мировое потребление родия, и в дальнейшем будет оставаться главным потребителем этого драгоценного металла.
На фоне этого также важно отметить, что предложение родия на рынке постоянно сокращается. Причиной этому является то, что родий является побочным продуктом, получаемым при добыче главных металлов платиновой группы – платины и палладия.
Относительно альтернативных форм инвестиций в родий важно отметить, что эксперты настаивают на существовании двух эффективных возможностей, а именно:
Это важно! Сегодня на рынке драгоценных металлов в свободной продаже находятся слитки родия массой одна десятая и одна четвёртая тройской унции, то есть 3,11 и 7,77 граммов, соответственно.
Рутений
Рутений – драгоценный металл платиновой группы, имеющий серебристо-белый цвет с серым оттенком. Рутений является химическим аналогом платины. В чистом виде этот драгоценный металл – достаточной хрупкий, в связи с чем его применение в чистом виде в ювелирной промышленности невозможно. Однако рутений в исключительных случаях используют в ювелирной отрасли в качестве легирующего материала.
Инвестиции в рутений сегодня можно осуществлять путём:
В целом, сегодня перспективы инвестиций в рутений ограничиваются рынком вторичных драгоценных металлов, однако возможно в ближайшем будущем этот драгоценный металл выйдет на новый уровень.
Иридий
Иридий является самым редким драгоценным металлом платиновой группы. По таким характеристикам как плотность и устойчивость иридий уступает только осмию, все остальные драгоценные металлы платиновой группы несравнимы с иридием в этом плане.
Основные характеристики иридия:
Сферы применения иридия:
В целом, иридий имеет широкую сферу использования, но, в то же время, он не торгуется на рынке драгоценных металлов.
Осмий
Многие современные интернет-издания говорят об осмии как одном из наиболее дорогостоящих драгоценных металлов. Подтвердить или опровергнуть этот факт мы не можем, однако приведём здесь альтернативные точки зрения относительно реальной стоимости осмия и возможности введения его на рынок драгоценных металлов.
Одни эксперты говорят о том, что осмий является самым дорогим драгоценным металлом, указывая на его уникальную плотность, которая составляет 22,61 г/см3. Сплавы, содержащие в своём составе осмий, отличаются высокой износостойкостью и долговечностью. Осмий применяют при производстве высокоточного измерительного оборудования, изготовлении краёв хирургических инструментов и много другого. Как правило, осмий используют в сплаве с другим драгоценным металлом платиновой группы – иридием.
А знаете ли Вы, что сплавы осмия с иридием встречаются в природе. Это так называемый осмистый иридий, или невьянскит, и иридистый осмий, или сысертскит.
Отличительными особенностями осмия являются:
Относительно предположительной стоимости осмия мнения экспертов и аналитиков здесь расходятся: одни утверждают, что цена осмия едва достигает 20 долларов за 1 грамм драгоценного металла; другие, указывая на уникальные свойства осмия и его незаменимость, говорят о цене в 200 долларов за грамм.
Драгоценные металлы платиновой группы уникальны по своей сути. Каждый из этих драгоценных металлов имеет свою сферу применения в современном мире. Надеемся, что в скором времени эти драгоценные металлы станут полноправными участниками рынка драгоценных металлов.
Платиновые металлы
Пл а тиновые мет а ллы, платиноиды, химические элементы второй и третьей триад VIII группы периодической системы Менделеева. К ним принадлежат: рутений (Ruthenium) Ru, родий (Rhodium) Rh, палладий (Palladium) Pd (лёгкие платиновые металлы, плотность
12 г/см 3 ); осмий (Osmium) Os, иридий (Iridium) lr, платина (Platinum) Pt (тяжёлые платиновые металлы, плотность
22 г/см 3 ). Серебристо-белые тугоплавкие металлы; благодаря красивому внешнему виду и высокой химической стойкости платиновые металлы наряду с Ag и Au называют благородными металлами.
Историческая справка. Имеются указания, что самородная платина в древности была известна в Египте, Эфиопии, Греции и Южной Америке. В 16 в. исп. конкистадоры обнаружили в Южной Америке вместе с самородным золотом очень тяжёлый белый тусклый металл, который не удавалось расплавить. Испанцы назвали его платиной — уменьшительным от исп. plata — серебро. В 1744 исп. морские офицер Антонио де Ульоа привёз образцы Pt в Лондон. Они вызвали живой интерес учёных Европы. Самостоятельным металлом Pt, которую первоначально считали белым золотом, была признана в середине 18 в.
В 1803 английский учёный У. Х. Волластон обнаружил в самородной платине палладий, получивший это название от малой планеты Паллады (открытой в 1802), и родий, названный так по розовато-красному цвету его солей (от греч. rh ó don — роза). В 1804 английский химик Смитсон Теннант в остатке после растворения самородной Pt в царской водке открыл ещё 2 металла. Один из них получил название иридий вследствие разнообразия окраски его солей (от греч. í ris, род. падеж í ridos — радуга), другой был назван осмием по резкому запаху его четырёхокиси (от греч. osm á — запах). В 1844 К. К. Клаус при исследовании остатков от аффинажа (очистки) уральской самородной Pt в Петербургском монетном дворе открыл ещё один платиновый металл — рутений (от позднелат. Ruthenia — Россия).
Согласно давно установившейся традиции, платиновые металлы принято помещать в VIII группу периодической системы элементов. В соответствии с этим следовало ожидать, что все платиновые металлы должны иметь высшую степень окисления +8. Однако это наблюдается только у Ru и Os, прочие же платиновые металлы проявляют валентность не выше +6. Объясняется это тем, что у атомов Ru и Os остаются незаполненными соответственно внутренние подуровни 4f и 5f. Поэтому для атомов Ru и Os возможно возбуждение не только с подуровней 5s и 6s на подуровни 5p и 6p, но и с подуровней 4d и 5d на подуровни 4f и 5f. Вследствие этого в атомах Ru и Os появляется по 8 непарных электронов и валентность +8. Электронные конфигурации атомов Rh, lr, Pd, Pt такой возможности не допускают. Поэтому в некоторых вариантах таблицы Менделеева эти элементы (а также Со и Ni) выносят за пределы VIII группы. Все платиновые металлы легко образуют комплексные соединения, в которых имеют различные степени окисления и различные координационные числа. Комплексные соединения платиновых металлов, как правило, окрашены и очень прочны.
Химические свойства платиновых металлов имеют много общего. Все они в компактном виде (кроме Os) малоактивны. Однако в виде т. н. черни (мелкодисперсного порошка) платиновые металлы легко адсорбируют S, галогены и др. неметаллы. (Чернь обычно получают восстановлением платиновых металлов из водных растворов их соединений.) Компактные Ru, Rh, Os, lr, будучи сплавлены с Pt, Zn, Pb, Bi, переходят в раствор при действии царской водки, хотя она не действует на эти платиновые металлы, взятые отдельно.
Семейство платиновых металлов можно разделить на 3 диады (двойки), образованные двумя стоящими один под другим лёгким и тяжёлым платиновыми металлами, а именно: Ru, Os; Rh, lr; Pd, Pt.
При нагревании с O2 и сильными окислителями Ru и Os образуют легкоплавкие кристаллы — четырёхокиси (тетроксиды) — оранжевую RuO4 и желтоватую OsO4. Оба соединения летучи, пары их имеют неприятный запах и весьма ядовиты. При действии восстановителей превращаются в низшие окислы RuO2 и OsO2 или в металлы. Со щелочами RuO4 образует рутенаты, например рутенат калия K2RuO по реакции:
При действии хлора K2RuO4 превращается в перрутенат калия:
Четырёхокись OsO4 даёт с KOH комплексное соединение K2[OsO4(OH)2]. С фтором и др. галогенами Ru и Os легко реагируют при нагревании, образуя соединения типа RuF3, RuF4, RuF5, RuF6. Осмий даёт подобные же соединения, кроме OsF3; существование OsF8 не подтверждено. Весьма интересны комплексные соединения Ru с ксеноном Xe [RuF6] (канадский химик Н. Бартлетт, 1962), а также с молекулярным азотом — [(NO)(NH3)4 N2Ru (NH3)4 NO] CI (советский химик Н. М. Синицын, 1962) и [Ru (NH3)5N2] Cl2 (канадский химик А. Аллен, 1965).
На компактные Rh и lr царская водка не действует. При прокаливании в O2 образуются окислы Rh2O3 и Ir2O3, разлагающиеся при высоких температурах.
Pd легко растворяется при нагревании в HNO3 и концентрированной H2SO4 с образованием нитрата Pd (NO3)2 и сульфата PdSO4. На Pt эти кислоты не действуют. Царская водка растворяет Pd и Pt, причём образуются комплексные кислоты — тетрахлоропалладиевая кислота H2[PdCl4] и гексахлороплатиновая — коричнево-красные кристаллы состава H2[PtCl6] × 6H2O Из её солей наибольшее значение для технологии платиновых металлов имеет хлороплатинат аммония (NH4)2[PtCl6] — светло-жёлтые кристаллы, малорастворимые в воде и почти не растворимые в концентрированных растворах NH4CI. При прокаливании они разлагаются по реакции:
При этом Pt получается в мелкораздробленном виде (т. н. платиновая губка, или губчатая платина).
Получение. Разделение платиновых металлов и получение их в чистом виде очень сложно вследствие большого сходства их химических свойств; это требует большой затраты труда, времени, дорогих реактивов. Для получения чистой Pt исходные материалы — самородную платину, платиновые шлихи (тяжёлые остатки от промывки платиноносных песков), лом (негодные для употребления изделия из Pt и её сплавов) обрабатывают царской водкой при подогревании. В раствор переходят: Pt, Pd, частично Rh, lr в виде комплексных соединений H2[PtCl6], H2[PdCl4], Нз [RhCl6] и H2[IrCl6], а также Fe и Cu в виде FeClз и CuCl2. Нерастворимый в царской водке остаток состоит из осмистого иридия, хромистого железняка (FeCrO2), кварца и др. минералов.
Из раствора осаждают Pt в виде (NH4)2[PtCl6] хлористым аммонием. Но чтобы в осадок вместе с Pt не выпал lr в виде аналогичного нерастворимого соединения (NH4)2[lrCl6] (остальные платиновые металлы NH4Cl не осаждает), предварительно восстанавливают Ir (+4) до Ir (+3) (например, прибавлением сахара C12H22O11 по способу И. И. Черняева). Соединение (NH4)3[IrCl6] растворимо и не загрязняет осадка.
Хлороплатинат аммония отфильтровывают, промывают концентрированным раствором NH4CI (в котором осадок практически не растворим), высушивают и прокаливают. Полученную губчатую платину спрессовывают, а затем оплавляют в кислородно-водородном пламени или в электрической печи высокой частоты. Из фильтрата, оставшегося после осаждения (NH4)2[PtCl6], и из осмистого иридия извлекают прочие платиновые металлы путём сложных химических операций. В частности, для перевода в растворимое состояние нерастворимых в царской водке платиновых металлов и осмистого иридия используют спекание с перекисями BaO2 или Na2O2. Применяют также хлорирование — нагревание смеси Pt-концентратов с NaCl и NaOH в струе хлора.
В результате аффинажа получают труднорастворимые комплексные соединения: гексахлорорутенат аммония (NH4)3[RuCl6], дихлорид тетрамминдиоксоосмия [OsO2(NH3)4] Cl2, хлорпентамминдихлорид родия [Rh (NH3)5CI] Cl2, гексахлороиридат аммония (NH4)2[lrCl6] и дихлордиаммин палладия [Pd (NH3)2] Cl2. Прокаливанием перечисленных соединений в атмосфере H2 получают платиновые металлы в виде губки, например
Губчатые платиновые металлы сплавляют в вакуумной электрической печи высокой частоты.
Применяют и др. способы аффинажа, в частности основанные на использовании ионитов.
Основным источником получения платиновых металлов служат сульфидные медно-никелевые руды, месторождения которых находятся в СССР (Норильск, Красноярский край), Канаде (округ Садбери, провинция Онтарио), ЮАР и др. странах. В результате сложной металлургической переработки этих руд благородные металлы переходят в т. н. черновые металлы — нечистые никель и медь. Платиновые металлы собираются почти полностью в черновом Ni, a Ag и Au — в черновой Cu. При последующем электролитическом рафинировании Ag, Au и платиновые металлы осаждаются на дне электролитической ванны в виде шлама, который отправляют на аффинаж.
Что такое металлы платиновой группы
Металлы платиновой группы (МПГ, Платиновая группа, Платиновые металлы, Платиноиды) — коллективное обозначение шести переходных металлических элементов (рутений, родий, палладий, осмий, иридий, платина), имеющих схожие физические и химические свойства, и, как правило, встречающихся в одних и тех же месторождениях. В связи с этим, имеют схожую историю открытия и изучения, добычу, производство и применение. Металлы платиновой группы являются благородными и драгоценными металлами. В природе, чаще всего встречаются, в полиметаллических (медно-никелевых) рудах, а также в месторождениях золота и платины. Иногда, металлы платиновой группы подразделяют на две триады:
рутений, родий и палладий — лёгкие платиновые металлы, а
платина, иридий и осмий — тяжёлые платиновые металлы.
Платина и металлы её группы встречаются в природе в весьма рассеянном состоянии. Геохимически все эти элементы связаны с ультраосновными и основными породами. Известно около полусотни минералов платиновой группы. Платина, иридий, палладий в горных породах и месторождениях развиты как в самородном виде, так и в виде твёрдых растворов и интерметаллических соединений с Fe, Ni, Cu, Sn, реже Au, Os, Pb, Zn, Ag.
Генетические группы и промышленные типы месторождений
1. Магматические
а. хромит-платиновые месторождения (уральский тип)
б. месторождения комплексных платина-хромит-медно-никелевых руд (бушвельдский тип)
в. ликвационные медь-никель-платиновые месторождения (норильский тип)
2. Гидротермальные
3. Россыпи
Все платиновые металлы светло-серые и тугоплавкие, платина и палладий пластичны, осмий и рутений хрупкие. Красивый внешний вид благородных металлов обусловлен их инертностью.
Платиновые металлы обладают высокой каталитической активностью в реакциях гидрирования, что обусловлено высокой растворимостью в них водорода. Палладий способен растворить до 800—900 объёмов водорода, платина — до 100.
Все платиновые металлы химически довольно инертны, особенно платина. Они растворяются лишь в «царской водке» с образованием хлоридных комплексов:
Промышленное производство платины первоначально велось в Америке. Лишь в 1819 году платиновые россыпи были впервые обнаружены на Урале близ Екатеринбурга. С тех пор Россия становится ведущим производителем платины, а, с момента открытия, и платиноидов.
В настоящее время, почти 90 % всего объема производства металлов платиновой группы разделено между платиной и палладием, остальные добываются и продаются в небольших количествах.
95 % запасов и 90 % производства МПГ сосредоточены в двух крупных месторождениях —
Бушвельдском комплексе, находящемся на территории Южно-Африканской Республики, и в
Норильском рудном районе, расположенном в России.
В рудах Бушвельда содержание платины втрое выше, чем палладия,
в то время как в Норильске наблюдается обратное соотношение.
Поэтому, ЮАР является крупнейшим мировым производителем платины, а Россия — палладия.
Запасы
Содержание платиновых металлов в земной коре (кларк) оценивается, как 10−8 % для платины, 10−9 % для палладия и 10−11 % для остальных платиновых металлов.
Общие запасы металлов платиновой группы на начало 2009 года оцениваются в 100 млн кг.
Причем распределены они, также неравномерно:
ЮАР (63,00 млн кг разведанных запасов при 70,00 млн кг общих),
Россия (6,20/6,60),
США (0,90/2,00),
Канада (0,31/0,39).
В России почти вся добыча металлов платиновой группы целиком сосредоточена в рамках «Норильского никеля» (15 % мирового производства платины и 55 % производства палладия).
С середины 1970−х годов главной сферой применения платины и палладия стала автомобильная промышленность.
В электротехнической промышленности из металлов платиновой группы изготовляют контакты с большой степенью надёжности (стойкость против коррозии, устойчивость к действию образующейся на контактах кратковременной электрической дуги).
В технике слабых токов при малых напряжениях в цепях используются контакты из сплавов золота с платиной, золота с серебром и платиной. Для слаботочной и средненагруженной аппаратуры связи широко применяют сплавы палладия с серебром (от 60 до 5 % палладия).Магнитные сплавы металлов платиновой группы с высокой коэрцитивной силой употребляют при изготовлении малогабаритных электроприборов. Сопротивления (потенциометры) для автоматических приборов и тензометров делают из сплавов металлов платиновой группы (главным образом палладия с серебром, реже с другими металлами). У них малый температурный коэффициент электрического сопротивления, малая термоэлектродвижущая сила в паре с медью, высокое сопротивление износу, высокая температура плавления, они не окисляются.
Металлы платиновой группы идут на изготовление деталей, работающих в агрессивных средах — технологические аппараты, реакторы, электрические нагреватели, высокотемпературные печи, аппаратуру для производства оптического стекла и стекловолокна, термопары, эталоны сопротивления и др.
При изготовлении инструментов металлы платиновой группы позволяют получить уникальные свойства по прочности, корозостойкости и долговечности.
Металлы платиновой группы используются в чистом виде, как биметалл и в сплавах (см. Платиновые сплавы). Химические реакторы и их части делают целиком или только покрывают фольгой из металлов платиновой группы. Покрытые платиной аппараты применяют при изготовлении чистых химических препаратов и в пищевой промышленности. Когда химической стойкости и тугоплавкости платины или палладия недостаточно, их заменяют сплавами платины с металлами, повышающими эти свойства: иридием (5-25 %), родием (3-10 %) и рутением (2-10 %). Примером использования металлов платиновой группы в этих областях техники является изготовление котлов и чаш для плавки щелочей или работы с соляной, уксусной и бензойной кислотами; автоклавов, дистилляторов, колб, мешалок и др.
Сплавы иридия с осмием, а также золота с платиной и палладием используют для изготовления компасных игл, напаек «вечных» перьев.
Высокие каталитические свойства некоторых металлов платиновой группы позволяют применять их в качестве катализаторов, например, платину применяют при производстве серной и азотной кислот.
Что такое платина: как выглядит, из чего состоит, где используется, как отличить
Сейчас ювелиры называют платину королевой цветных металлов, и этот титул ей достался не просто так. Так что же такое платина? Это благородный металл, который в том числе является биржевым товаром.
Металл ценят за его замечательный внешний вид, прочность, пластичность и многое другое. Но так было не всегда — положительные свойства материала заметили только в 18 веке.
«Плохое серебро» или «серебришко» — именно так платину назвали европейцы первый раз, когда с ней столкнулись. И современное название платины так и переводится. Испанское слово «plata» переводится как серебро, а при добавлении уменьшительно-ласкательного суффикса получается «platina» или «серебришко».
Зато сегодня этот металл считается одним из лучших благодаря своим удивительным качествам. Его активно используют в промышленности и, конечно, при изготовлении ювелирных украшений.
Свойства платины: физические, химические и другие характеристики
Платина или платинум — один из элементов таблицы Менделеева. Этот металл занимает 78 место среди других химических элементов и обозначается символом Pt. Материал плотный, твердый, но очень пластичный, что объясняет его популярность в ювелирном деле.
Физические свойства платины
Тяжелый тугоплавкий металл серебристо-белого цвета, один из самых плотных материалов — платина в два раза плотнее свинца. Также металл очень стабилен и обладает хорошей электропроводностью. Платина не поддается коррозии и не окисляется на воздухе даже при накаливании. Так как материал устойчив к вакууму, его с успехом применяют в космической технике.
При нагревании твердый платинум становится очень пластичным. Из разогретого материала можно сделать тончайшую фольгу или проволоку.
Металл обладает следующими физическими свойствами:
По показателю твердости платина почти в два раза превосходит золото. Аурум (именно так по-другому называется золото) может похвастаться лишь 2-2,4 баллами по шкале Мооса.
Материал настолько прочный, что изделие можно полностью сделать из платины. Это довольно редко, ведь чистые серебро и золото слишком мягкие и без примесей буквально гнутся в руках.
Также стоит уточнить по поводу магнитных свойств. Во многих источниках написано, что магнит — верный способ проверить подлинность украшения из платины. И хотя чистая платина не магнитится, это не всегда касается ювелирных изделий. Так как этот металл очень редкий и дорогой, его обычно используют с небольшим количеством примесей.
Сплав платины состоит из нескольких металлов. В качестве примесей чаще всего используют медь или палладий, но также могут добавить кобальт и даже золото. И если медь, палладий и золото не обладают магнитными свойствами, то кобальт в эту группу не входит. Даже 5% этого металла хватит, чтобы сплав магнитился. То есть, такой способ нельзя считать самым надежным.
Другие материалы, входящие в состав сплава, также могут изменить свойства платины.
Например, серебро, медь и рутений улучшают ее электросопротивление. Никель и осмий делают металл более твердым, а вот палладий и родий – наоборот – мягким.
Химические свойства платины
Металл легко поддается обработке давлением — ковке, прокатке, волочению, но отличается высокой химической стойкостью. Платина является одним из самых инертных (такие вещества или металлы, которые «неохотно» вступают в реакции) хим. элементов и растворяется только в горячей «царской водке», цианистом калии и расплавленных щелочах.
Несмотря на свою инертность, элемент участвует во многих химических реакциях в качестве катализатора, то есть ускорителя.
После накаливания платина сохраняет свой естественный цвет.
Также при нагревании платина реагирует с кислородом. В результате реакции образуются летучие оксиды.
Металлическая платина абсолютно безопасна для человека и не может вызывать аллергии даже у чувствительных людей. Но это не касается платиновой черни (порошок из крупинок платины, который получают в ходе реакций. В основном используют в качестве катализатора). В ее состав входит ядовитый теллур, который может привести к общей интоксикации организма.
Кроме того, для создания украшений обычно используют платиновый сплав. Если в нем присутствует никель, он тоже может стать причиной аллергии на платину. При длительном ношении у чувствительных людей возникает сыпь, покраснение кожи и зуд.
Как выглядит платина
Платинум обладает красивым бело-серебристым цветом. Внешне платина очень сильно напоминает серебро, поэтому многим может показаться, что это одно и то же. На самом деле все совсем не так. Материалы отличаются физическими и химическими свойствами.
Также металл можно спутать с белым золотом, но второй сплав обладает более выраженным белым оттенком и глянцевым блеском.
Какая бывает проба у платины
Чистую платину в ювелирном деле не используют. И если в случае с серебром и золотом такое решение связано с мягкостью металла, то причина использования исключительно платиновых сплавов кроется в совсем другом.
Этот материал крайне редко встречается в природе и отличается высокими показателями твердости, прочности и устойчивости. Использовать платину в больших объемах для ювелирных изделий просто нецелесообразно, тем более стоит она слишком дорого.
Платиновые сплавы внешне не отличаются от чистого элемента. Это металлы серовато-белого оттенка с серебристым блеском.
Лигатура (именно так называются примеси в сплаве) может быть разной. Обычно для этого используют один или несколько металлов из этого списка:
Некоторые ювелиры могут использовать другие элементы, например, никель или рутений.
Все изделия из драгоценных металлов, в том числе и из платины, обязательно должны обладать клеймом с пробой, которая указывает, какой процент примесей присутствует в этом изделии. Например, 950 проба обозначает, что на килограмм такого сплава приходится 50 грамм или 5% примесей. Из этого же следует, что чем выше проба, тем дороже стоит сплав
Именно клеймо с пробой подтверждает то, что украшение все же выполнено из дорогостоящего материала и что оно соответствует сплаву той или иной пробы. Оттиск может отсутствовать только на переплавленных изделиях или украшениях ручной работы.
По принятой в России метрической системе, существует только четыре варианта платиновых проб:
Последняя, самая высокая проба обычно используется только изготовления слитков платины.
Такая же система действует во Франции, Германии, Австрии, Польше и многих других странах Европы. А вот в Канаде и США для обозначения качества сплава используют каратную систему. Четыре платиновые пробы, указанные выше, в каратной системе выглядят так (соответственно):
Также учитывайте, что в разных странах само клеймо тоже может отличаться. Например, на украинских украшениях может быть изображен трезубец, а на старинных английских изделиях изображали рыбу.
Где используется платина?
Всем известно, что платина применяется для создания ювелирных украшений, ведь металл отличается высокими показателями твердости и пластичности. Кроме того, платиновые изделия радуют своими внешними данными: серебристый цвет и характерный блеск делают украшения очень востребованными среди покупателей.
До середины прошлого века всего лишь несколько процентов добываемого драгоценного металла отводилась для сферы медицины. Но сегодня ситуация изменилась, и спрос на платину растет в геометрической прогрессии. Скорее всего, это связано с развитием исследований, которые выявили преимущества платины над другими металлами.
На сегодняшний момент платина необходима в следующих сферах жизни:
Применение платине нашлось и в банковском деле. Этот благородный металл является предметом инвестирования: из него отливают слитки.
Платина нужна при производстве азотной кислоты и других химических веществ. В этом случае элемент выступает в качестве катализатора, ускоряющего слишком медленные реакции. Для этого используют не чистую платину, а ее сплав с родием. В противном случае производство веществ было бы слишком дорогим.
Также металл играет роль катализатора в нефтепереработке. С его помощью из нефти получают бензин. И если для создания азотной кислоты платину используют в виде сетки, то для использования в обработке нефти из нее делают порошок. Конечно, можно использовать и другие катализаторы, например, алюминий или молибден, но платинум более долговечный и эффективный.
Использование платины в электротехнике обусловлено стабильными электрическими и механическими свойствами. Материал хорошо проводит ток, а также отличается приличным показателем теплопроводности. Обычно платиновые сплавы используют для изготовления контактов, а соединение платины с кобальтом позволяет создавать мощные магниты.
Применение платины в медицинской отрасли помогает сохранить жизни тысячи больным. Дело в том, что аналогов этому материалу просто нет. Изделия из других металлов не устойчивы к окислению, поэтому для такой реакции не пригодны.
В полевых условиях инструменты из платины стерилизуют в пламени спиртовой горелки.
Также платину часто используют для создания имплантов для людей с нарушениями слуха. Кроме того, существует мнение, что этот материал помогает бороться с раком. На основе этого металла изготовлены многие препараты, помогающие людям преодолеть онкологию.
Как и где добывают платину
Платина — редчайший элемент в земной коре. Именно ее редкостью и отличными свойствами можно объяснить ее высокую стоимость.
Основные места добычи платины — это месторождения меди и никеля. Из них добывают драгоценный металл вместе с другими материалами. В ультраосновных (породы, в которых содержится много кремнезема) породах также встречаются небольшие платиновые вкрапления.
Природные руды с высоким содержанием платинума (до 75%) встречаются очень редко.
В месторождениях с платиной часто встречаются металлы платиновой группы, которые еще считают ее «спутниками».
Кроме этого, в разных породах драгметалл могут сопровождать разные материалы:
Существует два типа месторождения платины:
В мире есть несколько лидеров по добыче платины. В их число входят следующие страны:
Добыча платины в России началась с приблизительно 1824 года. В какой-то период царская знать даже выпускала монеты из этого материала.
Одна из самых известных компаний, добывающих платину на Урале, является «Русская платина». Она добывает драгметалл в самом богатом российском месторождении — прииске «Кондер». За сутки добыча материала составляет около 30 кг, а за год — около 3,5 тонн.
Чистая платина в природе не встречается. Металл образует смеси с другими веществами:
Платиновая руда не однородна, а включает в себя вкрапления драгоценного платинума, которые выглядят будто бы небольшие зерна.
Самородным металлом называют только те «куски», в которых содержится около 70-90% чистой платины. Но самородки платины, на 90% состоящие из платинума, — большая редкость. В основном Pt добывают в виде железистой платины, в которой содержится примерно 20-50% железа.
В природе существует не только железистая платина. Самородки классифицируют в зависимости от того, какой еще компонент содержится в руде. Есть несколько вариантов:
Как определить платину в домашних условиях и отличить от других металлов
И хотя популярность платины стремительно растет, далеко не все знают, как выглядит этот металл. По этой причине риск нарваться на мошенников и купить подделку довольно высокий.
Чтобы не стать жертвой обмана, лучше всего обратиться за помощью к ювелиру. И хотя это не совсем дешевая услуга, это самый надежный способ купить подлинное изделие. Но если вы не хотите обращаться к мастеру, существует несколько более-менее проверенных методов проверки платины на подлинность.
Чем платина отличается от серебра
Аргентум имеет более серый оттенок, в то время как платина светлая и блестящая. Через время серебро тускнеет, теряет свой блеск, а платинум нет.
Проверить на подлинность изделие из платины, можно тестом:
Также можно воспользоваться раствором аммиака. Возьмите ватную палочку, опустите в раствор и оставьте капельку на украшении. На серебряном изделии останутся темные пятна, а на платину раствор никак не подействует.
Распознаем: платина или нержавейка
А вот от нержавеющей стали платину отличить практически невозможно. Дело в том, что оба материала не реагирует на большинство веществ, известных на сегодняшний день химии. Внешне металлы похожи настолько, что их не отличить друг от друга.
Пара обручальных колец из стали стоят около 500 рублей, а такие же украшения из платины обойдутся в 20 или даже 30 тысяч.
Чтобы отличить платину от нержавейки, можно воспользоваться одним из трех способов:
Отличие от палладия
Чтобы отличить платину от палладия, можно провести проверку йодом. Для этого эксперимента понадобится йод, пипетка и салфетка. Необходимо капнуть раствор на украшение и подождать пару минут. Если ничего не произойдет — перед вами изделие из платины. Тот же самый вывод можно сделать, если йод станет еще более темным. А вот если на изделии останутся пятна или жидкость поменяет оттенок на более светлый, перед вами палладий.
Магические свойства платины
В отличие от золота, платина не хранит негативные воспоминания и мысли. Именно поэтому по своим магическим свойствам металл считается самым “чистым” и “светлым”.. Энергию платинума нельзя направить на людей, предметы или исполнение желаний, поэтому из него не делают амулеты.
Главное действие платины заключается в том, что она смягчает влияние камней на своего владельца.
Благодаря этому металлу минералы не так сильно влияют на характер и жизнь людей. Это очень полезно, если камень вам не подходит.
Так как платину соотносят с планетой Нептун, то этот металл покровительствует Рыбам и Раку. Именно этим знакам зодиака можно постоянно носить украшения из этого материала. Девам и Стрельцам металл подарит успокоение, а Скорпиону поможет улучшить интуицию и связь с потусторонним миром. Возможно, что одаренным Скорпионам платина поможет обрести дар ясновидения.
А вот Водолеям, Близнецам, Львам и Тельцу носить платину не рекомендуется. На них ношение этого металла окажет отрицательное воздействие.
Овну, Козерогу и Весам можно надевать украшения из платинума, но периодически снимать и откладывать его. Так вы сможете избежать негатива в вашей жизни, но и на положительные изменения рассчитывать не нужно.
Стоимость платины
Цена на платину меняется каждый день. В период с 2016 по 2019 ее стоимость выросла с 600 до 900 долларов за тройскую унцию.
Унция – мера величины, которая равна 31 грамму и используется для измерения драгоценных металлов. В одном килограмме 32,15 таких унций.
Из этого следует, что увеличилась и стоимость платины за 1 грамм. Считается, что это наиболее выгодный металл для инвестирования.
Сколько стоит 1 грамм платины? Около 2300 рублей за грамм. То есть, за 1 кг этого драгоценного металла можно вполне приобрести автомобиль.
Чтобы приблизительно понимать цену платины, лучше ее сравнить с другими металлами или драгоценностями.
. палладий?
Цена за тройскую унцию палладия составляет примерно 2300 долларов. Это означает, что палладий дороже платины более чем в два раза.
. бриллиант?
Ограненный алмаз — это, пожалуй, самый дорогой драгоценный камень. Его стоимость только начинается от 20 000 р за небольшую вставку весом 0,24 карата. Конечно, он будет намного дороже платины.
. серебро?
Цена за одну тройскую унцию составляет 27 долларов. Это означает, что платина почти в 30 раз дороже серебра.
. титан?
Стоимость сортового титана начинается от 0,6 долларов за тройскую унцию. Конечно, цена на платину значительно выше титана.
В заключении хотелось бы сказать, что платина — один из самых необычных металлов. Она обладает удивительными свойствами и используется во многих отраслях. Кроме того, платинум — отличный вариант, куда можно вложить деньги. Металл постоянно дорожает, а украшения из него будут радовать прекрасным внешним видом.