Куриный эмбрион как экспериментальный и сырьевой объект для биологии, медицины и биотехнологии
История исследовательского интереса к куриному эмбриону, как к истоку развития эмбриологии и биологии. Его современное использование рядом наук. Анализ ценности физико-химических и биологических процессов происходящих с используемыми зародышами кур.
| Рубрика | Биология и естествознание |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 26.07.2013 |
| Размер файла | 13,3 K |
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
Куриный эмбрион как экспериментальный и сырьевой объект для биологии, медицины и биотехнологии
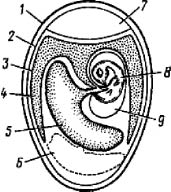
Интерес к куриному эмбриону, как объекту исследования, появился еще у Аристотеля, который стоит у истоков эмбриологии и биологии развития. С XVII века ряд ученых сделали открытия, используя в качестве объекта исследований, куриный эмбрион. Поэтому невозможно переоценить значение куриного эмбриона не только на этапе становления, но и на дальнейших этапах развития учения об онтогенезе. Использование куриного эмбриона имеет свои особенности: это доступная и управляемая система, благодаря чему можно получать результаты практически с помощью всех известных методов; работа с куриным эмбрионом, может быть реализована на любом этапе онтогенеза. Эмбрион является экологически чистым максимально изолированным от внешней среды объектом, что снижает вероятность спонтанного влияния внешних факторов в процессе эксперимента.
Куриный зародыш является объектом экспериментального изучения закономерностей эмбрионального развития. Наибольшее число исследований выполнено в условиях искусственной инкубации, что позволило испытать влияние различных внешних факторов на общие закономерности развития организма. При этом сам процесс инкубации, как основной способ получения экспериментальной эмбриональной ткани, сопровождается неизбежными потерями. В связи с этим эксперименты с куриными эмбрионами не противоречат принципам биоэтики.
Существует ряд методов, позволяющих экспериментировать с зародышем «in situ», внутри яйцевых оболочек.
На зародышах производят изоляцию, которая достигается в условиях культивирования «in vitro», для чего используют технику пересадок различных органов и тканей на хориоаллантоис эмбриона; удаление частей зародыша.
Сведения о физико-химических и биологических процессах, обусловливающих высокую биологическую активность тканей куриного эмбриона, расширяют спектр применения эмбриональных тканей, благодаря чему зародыш используют во многих областях биологии, медицины и биологической промышленности.
Зародыши кур используют в микробиологии и вирусологии для определения патогенности и степени вирулентности изучаемого микроорганизма. Кроме того, на эмбрионах проводят различные опыты: постановка реакции нейтрализации, определение инфекционного титра, изучение виростатических веществ и т. д.
Вышеописанные свойства обусловили использование куриного эмбриона, ставшего классическим, в биологической промышленности при производстве противовирусных вакцин и диагностикумов. Высокая пролиферативная способность клеток эмбриона, при создании оптимальных условий выращивания вируса, позволяет получить достаточное накопление вирусного материала.
При производстве бактериальных вакцин куриные эмбрионы используются в качестве компонента питательной среды, что существенно повышает прирост бактериальной массы культивируемых микро организмов (Тюменцева И.С., Косик Н.В., Ржепаковский И.В., 2005).
Известно, что наиболее эффективные и перспективные иммуностимуляторы и препараты c иммуномодулирующими свойствами (стволамин, ряд специфических цитаминов, плацентоль, экстракт плаценты и др.) получены из растущих эмбриональных и плацентарных тканей животных, а иногда и человека. Но использование таких тканей ограничено эпизоотическими проблемами, сложностью получения достаточного количества эмбрионального материала с необходимыми параметрами, невозможностью управляемости развитием и соображениями биоэтики. Поэтому куриный эмбрион является наиболее доступным, рентабельным, высокоактивным сырьевым субстратом, не только не уступающим по своим качествам, но и превосходящий, по ряду показателей эмбриональные плацентарные ткани других животных.
Вышеперечисленные особенности эмбриональной ткани положены в основу биотехнологии тканевых препаратов из эмбриональной ткани, разработанных сотрудниками проблемной научно-исследовательской лаборатории экспериментальной иммуноморфологии, иммунопатологии и иммунобиотехнологии Ставропольского государственного университета. Именно использование эмбриональных тканей в сочетании с оптимально выбранными технологиями их обработки, позволили получить много компонентные биологически активные препараты «СТЭМБ», «СТЭМБ-М1», и «ЭСРМ», содержащие биогенные стимуляторы, в том числе низкомолекулярные белки, цитамины, цитокины, аминокислоты, витамины, ферменты, гормоны и другие вещества в оптимальных количественных и качественных соотношениях. куриный эмбрион биология
Таким образом, куриный эмбрион является не только интересным экспериментальным объектом, позволившим получить сведения о практически всех закономерностях эмбрионального развития, но и важнейшим материалом для осуществления актуальных проблемных исследований в других областях биологии и медицины, а также ценнейшим сырьем для биотехнологической промышленности.
Размещено на Allbest.ru
Подобные документы
контрольная работа [21,0 K], добавлен 10.01.2011
Теоретические основы, предмет, объект и закономерности биологии. Сущность, анализ и доказательство аксиом теоретической биологии, обобщенных Б.М. Медниковым и характеризующих жизнь и отличающуюся от нее нежизнь. Особенности генетической теории развития.
реферат [47,8 K], добавлен 28.05.2010
Общая характеристика науки биологии. Этапы развития биологии. Открытие фундаментальных законов наследственности. Клеточная теория, законы наследственности, достижения биохимии, биофизики и молекулярной биологии. Вопрос о функциях живого вещества.
контрольная работа [28,1 K], добавлен 25.02.2012
Методология современной биологии. Философско-методологические проблемы биологии. Этапы трансформации представлений о месте и роли биологии в системе научного познания. Понятие биологической реальности. Роль философской рефлексии в развитии наук о жизни.
реферат [22,0 K], добавлен 30.01.2010
Промышленное использование биологических процессов на основе микроорганизмов, культуры клеток, тканей и их частей. История возникновения и этапы становления биотехнологии. Основные направления, задачи и методы: клонирование, генная и клеточная инженерия.
презентация [1,5 M], добавлен 22.10.2016
Научная электронная библиотека
Перетрухина А. Т., Блинова Е. И.,
Глава 3. МЕТОДЫ КУЛЬТИВИРОВАНИЯ МИКРОБОВ
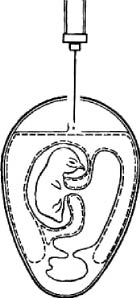
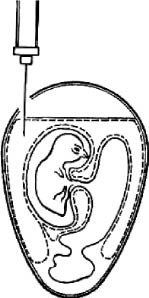
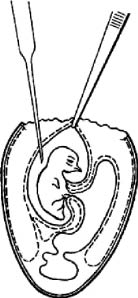
Рис. 2. Заражение куриного эмбриона на ХАО через естественную воздушную камеру
(по Николау)
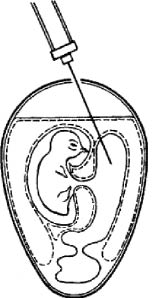
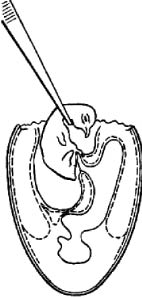
Рис. 3. Заражение куриного эмбриона в аллантоисную полость (по Николау)
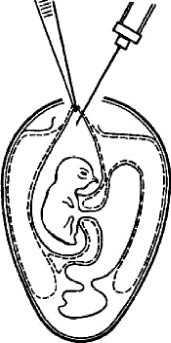
Заражение через искусственную воздушную камеру применяют чаще первого, так как оно обеспечивает контакт вируссодержащего материала с большей поверхностью ХАО и, следовательно, ведет к образованию большего количества вируса. Для заражения эмбриона этим методом его помещают в штатив горизонтально зародышем вверх. В скорлупе делают два отверстия: одно небольшое над центром воздушной камеры (предназначено для отсасывания из нее воздуха), а другое диаметром 0,2-0,5 см сбоку, со стороны зародыша. Сложность метода в том, что, делая второе отверстие, необходимо осторожно снять вначале кусочек скорлупы, затем скользящим движением, не повреждая ХАО, сдвинуть подскорлупную оболочку в сторону так, чтобы через образовавшийся дефект мог пройти воздух. После этого резиновой грушей через первое отверстие отсасывают воздух из естественной воздушной камеры (рис. 4, а). В результате через боковое отверстие наружный воздух устремляется внутрь, образуя искусственную воздушную камеру, дном которой является ХАО (рис. 4, б).
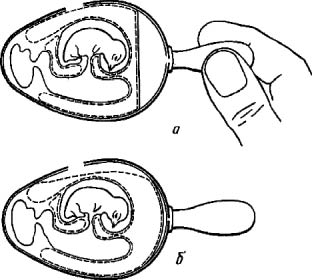
Рис. 4. Заражение куриного эмбриона на ХАО через искусственную воздушную камеру (по Николау и др.)
Через боковое отверстие на поверхность ХАО наносят инфекционную жидкость и отверстие закрывают кусочком лейкопластыря. Закрывать первое отверстие нет необходимости, так как внутренний листок подскорлупной оболочки при этом методе заражения не нарушается и продолжает выполнять роль барьера для микрофлоры окружающей среды.
Дальнейшую инкубацию эмбрионов, зараженных этим методом, проводят в горизонтальном положении боковым отверстием вверх.
Заражение в желточный мешок. Большей частью им пользуются для размножения хламидий, а также вирусов болезни Марека, ринопневмонии лошадей, катаральной лихорадки овец и др. Заражают эмбрионы 5-7-дневного, а иногда и 2-3-дневного возраста (вирус лихорадки долины РИФ). Используют два варианта заражения (рис. 6).
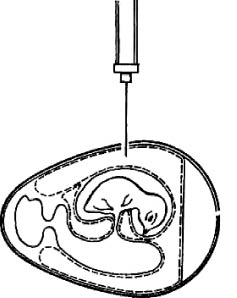
Рис. 5. Заражение куриного эмбриона в амниотическую полость (по Николау и др.)
Рис. 6. Заражение куриного эмбриона в желточный мешок (по Николау и др.)
Рис. 7. Заражение куриного эмбриона в амнион открытым способом (по Николау и др.)
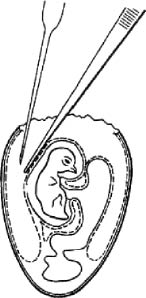
Рис. 8. Отсасывание аллантоисной жидкости (по Николау)
Рис. 9. Отсасывание амниотической жидкости (по Николау и др.)
ПАТОЛОГИЯ В РАЗВИТИИ ЭМБРИОНОВ С/Х ПТИЦЫ
Цель занятия. Научиться определять причины аномалий в развитии эмбрионов и их гибели.
Содержание и методика проведения занятия. Для установления причины гибели эмбрионов применяют патологоанатомическое вскрытие. Наиболее распространенные причины гибели эмбрионов при инкубации яиц, свободных от возбудителей инфекционных заболеваний: биологическая неполноценность инкубационных яиц и нарушение режима инкубации. В некоторых случаях наблюдается массовая гибель эмбрионов, обусловленная летальными и полулетальными генами.
Основные признаки гибели эмбрионов в результате неполноценности инкубационных яиц.
При авитаминозе А эмбрион отстает в росте. Отмечаются слабая пигментация пуха и ног, бледный желток, повышенное отложение мочекислых солей на оболочках эмбриона. Если авитаминоз А сочетается в авитаминозом D или неполноценным протеиновым питанием птицы родительского стада, то наблюдается значительное отложение солей в почках, мочеточниках и других внутренних органах.
При недостатке витаминов группы В эмбрионы погибают в большинстве случаев на 12-16-й день инкубации. Если эмбрион погиб на ранних стадиях инкубации, то у него нарушена дифференцировка зародышевых листков и оболочек. У эмбрионов старших возрастов не полностью использован белок. В полости аллантоиса откладывается большое количество мочекислых солей. На почках заметны кристаллы солей в виде беловатых отложений. Оперение недоразвито. Кончики перьев загнуты, они имеют «курчавый» вид. В некоторых случаях нижняя часть клюва недоразвита, а верхняя переразвита и изогнута книзу, образуя так называемый попугаев клюв. Кожа в области головы и шеи отечная. Голова большая, ноги укорочены и искривлены. При недостатке витамина В12 нарушены процессы кроветворения. Печень темно-красного цвета, дряблая. В конце инкубации пух и клюв приклеиваются к скорлупе, в результате чего вывод затрудняется и эмбрион погибает.
Многие из признаков недостаточности витаминов группы В характерны и для белковой интоксикации, которая возникает при даче птице родительского стада в избыточном количестве протеиновых кормов животного происхождения.
В старых яйцах, хранившихся длитечьное время, гибель эмбриона наступает на ранней стадии инкубации, поэтому такие яйца ошибочно относят к неоплодотворенным. Одним из характерных признаков при этом является аморфоз. Зародыш имеет вид бесформенного сгустка темно-серого цвета, располагающегося на внутренней поверхности подскорлупных оболочек.
Основные признаки гибели эмбрионов в результате нарушения режима инкубации.
При длительном перегреве ускоряется развитие эмбриона, аллантоис замыкается преждевременно, наклев начинается рано, вывод растянут. У цыплят, погибших при выводе, наблюдается неправильное положение, невтянутый большой желточный мешок или неиспользованный белок.
При недогреве яиц развитие эмбрионов запаздывает. Желточный мешок имеет темно-зеленый цвет. Возникает отечность в области головы и шеи. Скорлупа после вывода сырая, с комками неиспользованного белка.
При высокой влажности в яйце накапливается большое количество клейкой околоплодной жидкости. При наклеве молодняк заглатывает ее и погибает. Перья и клюв приклеиваются к скорлупе, что затрудняет вывод. Кишечный тракт погибших эмбрионов переполнен жидкостью.
При недостаточной влажности масса яиц значительно падает, усиливается воздействие высоких температур, что вызывает отклонения в развитии эмбрионов. Во время вывода оболочки пересыхают и уплотняются, эмбрион не может освободиться от скорлупы.
При нарушении газообмена в середине инкубации отмечаются переполнение кровью сосудов аллантоиса, резкая гиперемия желточного мешка и внутренних органов. При нарушении газообмена во второй половине инкубации наблюдается неправильное положение эмбрионов: голова, как правило, повернута в сторону острого конца яйца.
Неправильное поворачивание яиц приводит к слипанию белка с подскорлупными оболочками на остром конце яйца и к ненормальному смыканию аллантоиса, когда значительная часть белка остается за его пределами. В результате белок полностью не используется и нарушается питание эмбриона.
Вскрытие яиц с погибшими эмбрионами. Техника вскрытия яиц с погибшими эмбрионами сходна с техникой вскрытия яиц с живыми эмбрионами. Однако в данном случае необходимо тщательно соблюдать ветеринарные требования, работать в резиновых перчатках, предварительно смазав руки вазелином.
Вскрыв яйцо и удалив оболочки, определяют положение эмбриона. Нормальным считается такое положение, при котором тело эмбриона расположено вдоль длинной оси яйца, шея изогнута, голова находится под правым крылом, кончик клюва выступает из-под крыла и направлен в сторону воздушной камеры, ноги согнуты в суставах и прижаты к телу.
После определения положения эмбриона пинцетом осторожно извлекают его из яйца и осматривают содержимое скорлупы. Оболочки скорлупы должны быть слегка розового цвета, без околоплодной жидкости и утолщений. Обращают внимание на отсутствие большого количества мочекислых солей, неиспользованного белка или переполненных кровью участков. Затем осматривают сам эмбрион. Отмечают общее его развитие, состояние желточного мешка, отсутствие дефектов на туловище, голове, ногах. Затем эмбрион вскрывают, предварительно поместив в чашку Петри, залитую воском, и прикрепив его препаровальными иглами. Острыми ножницами разрезают по средней линии кожу живота по направлению от клоаки к голове. Желточный мешок удаляют так, чтобы не повредить его оболочку и не запачкать брюшную полость. Кожу отворачивают, разрезают грудную полость и осматривают сначала сердце, разрезая левую и правую его половины и отмечая наполнение его кровью, а затем легкие. Разрезают бронхи, трахею и гортань и определяют наличие в них содержимого, указывающего на какое-либо заболевание.
После этого осматривают печень, селезенку, мышечный желудок, железистый желудок, почки, делают разрез их тканей, надрезают кожу вокруг головы и шеи, разрезают кости черепа, обнажают мозг. При этом обращают внимание на отсутствие кровоизлияний, гиперемии, анемичности и других отклонений в состоянии тканей внутренних органов. Делают заключение о причинах гибели эмбриона.
Задание 1. Изучите причины гибели зародышей в разные периоды инкубации. Просмотрите на овоскопе 5-7 яиц с погибшими эмбрионами. Определите возраст гибели эмбрионов. Проведите патологоанатомическое вскрытие погибших эмбрионов и определите причину их гибели.
Куриный эмбрион как объект эксперимента для изучения развития сердечно-сосудистой системы
Полный текст
Аннотация
В настоящее время врожденные сердечно-сосудистые заболевания, в том числе врожденные пороки сердца, вносят значительный вклад в структуру заболеваемости и смертности детей во всем мире. В связи с этим эксперименты, позволяющие изучать развитие сердечно-сосудистой системы (ССС) на ранних этапах онтогенеза, представляются весьма перспективными источниками информации для создания теоретической основы знаний о врожденной патологии системы кровообращения. Использование куриных эмбрионов заложило основу для экспериментального изучения физиологии и патологии развития ССС. Благодаря накопленному теоретическому и экспериментальному материалу о закономерностях развития куриного эмбриона и его органов, стало возможным изучение этиологии и патогенеза многих сердечно-сосудистых заболеваний.В связи с доступностью, крупными размерами в сравнении с другими представителями Aves, простотой манипуляций и культивирования, куриные эмбрионы послужили моделью для описания развития и васкуляризации сердца, при этом, ввиду высокой консервативности многих ключевых механизмов раннего онтогенеза, полученные при этом данные возможно экстраполировать на человека. Работа с куриными эмбрионами составила основу для получения человеком знаний в области эмбриогенеза сердечно-сосудистой системы – формирование миокарда, эпикарда, эндокарда, коронарного сосудистого русла, камер сердца и магистральных сосудов.С развитием новых биомедицинских технологий, в первую очередь методик прижизненной визуализации, расширился круг возможных вмешательств на ССС куриного эмбриона.С учетом указанных преимуществ и совершенствования экспериментальных методик, модели на основе куриных эмбрионов не теряют актуальность и по сегодняшний день.
Ключевые слова
Полный текст
Использование куриных эмбрионов заложило основу для экспериментального изучения физиологии и патологии сердечно-сосудистой системы (ССС). В связи с доступностью, крупными размерами, простотой манипуляций и культивирования куриные эмбрионы служат моделью для изучения закладки, развития и васкуляризации сердца. При этом, ввиду высокой консервативности многих ключевых механизмов раннего онтогенеза, полученные данные могут быть экстраполированы на человека. Этому способствовала разработка методик для in ovo, ex ovo, in vitro исследований биохимии, генетики, физиологии и патологии различных аспектов морфогенеза сердца [1, 2]. Именно на куриных эмбрионах изучались роль клеток эндокарда в закладке коронарных сосудов во время трабекуляции миокарда и механизм образования аорты, а также формирование проэпикарда и эпикарда [3].
Роль проэпикарда в формировании коронарного русла
Современные данные о роли проэпикарда (ПЭ) в формировании коронарного русла основаны на исследованиях, проведенных на куриных эмбрионах. Развитие коронарных сосудов начинается, когда мезотелиальные клетки ПЭ перемещаются из зачатка печени к поверхности сердца, где они дифференцируются в клеточные линии, составляющие различные отделы сердца. У цыплят ПЭ возникает из мезотелиальных клеток, расположенных вдоль каудальной границы перикардиальной полости, которые легко выявляются методами световой микроскопии и хорошо поддаются экспериментальным манипуляциям [4].
Клетки ПЭ, связанные с процессом инициирования трабекуляции мигрируют к сердцу, формируя его внешний слой – эпикард, который интегрируется в стенку миокарда, что приводит к началу формирования коронарной сосудистой сети и увеличению числа фибробластов в стенке миокарда [5]. Неудачное слияние ПЭ с сердцем приводит к формированию дефектов коронарного кровообращения и истончению миокарда [6].
Эксперименты с мечением клеток ПЭ флуоресцентными белками и β-галактози-дазой выявляют окрашенные соответствующим способом гладкие миоциты и эндотелиоциты коронарных артерий у зрелых эмбрионов, что подтверждает гипотезу о формировании коронарных артерий непосредственно из ПЭ [3]. Предотвращение прикрепления клеток ПЭ к сердцу у цыплят препятствует развитию коронарных сосудов. Это также подтверждает необходимость клеток ПЭ для образования коронарных сосудов [7]. Достигнутые успехи в понимании механизмов развития коронарных сосудов, происхождения эндотелиальных клеток сердца, а также уникальные свойства куриных эмбрионов делают их полезной экспериментальной моделью. Когда меченные перепелиные клетки ПЭ пересаживаются в развивающийся куриный эмбрион, они приводят к развитию в сердце цыпленка-реципиента гладкомышечных клеток и фибробластов, при этом, в их коронарных артериях и эндокарде отсутствуют эндотелиальные клетки. Для развития эндотелиоцитов эмбриону-реципиенту требуется, помимо ПЭ клеток, еще и трансплантация печени перепела [8].
При исследовании культур клеток ПЭ, полученных от куриных эмбрионов, выявлен ряд регуляторных механизмов, приводящих эпикардиальный эпителий к эпителиальному мезенхимальному переходу (ЭМП) и клеточной дифференциации, которая необходима для развития коронарных сосудов [9]. В процессе своего развития клетки подвергаются ЭМП, что приводит к изменениям морфологии, полярности и подвижности клетки. Эксперименты на куриных эмбрионах помогли определить функцию хемокинов во время ЭМП в сердце [10].
Эксперименты на эмбрионах способствовали пониманию ключевых механизмов развития сердечного клапана на ранних стадиях морфогенеза и выявили гетерогенность эндокардиальных клеток в эмбриональном сердце. Структурный анализ эмбрионального сердца выявил трансформацию эндокардиальных клеток в богатых матриксом клапанообразующих областях сердца – эндокардиальных подушках [11]. Разработка системы культивирования in vitro для оценки эмбриональной клапанообразующей ткани [12] предоставила возможность четкого описания процесса трансформации эндокардиальных клеток, на основе чего разработана система скрининга и идентификации морфогенов, которые регулируют клеточную трансформацию. В ходе культивирования на коллагеновом геле при использовании определенных областей сердечной трубки, стало возможным выделить заинтересованные типы клеток и изучить механизмы их трансформации в ходе развития клапанов сердца. В большинстве исследований используется область сердечной трубки, которая лежит между общим предсердием и желудочком, так называемая атриовентрикулярная подушка (АВП), где образуются приточные клапаны. Трансформация имплантированной АВП широко изучалась в экспериментах на эмбрионах птиц [13, 14]. Данные эксперименты показали, что эндокард подушек функционально отличается от эндокарда, перекрывающего желудочек [14]. Описание гетерогенности эндокардиальных клеток, при использовании эмбриона, имеет решающее значение для понимания ранних этапов развития клапанов и разработки аналогичных экспериментальных методик у других организмов.
Использование метода эксплантатов in vitro привело к идентификации ключевых регуляторов трансформации эндокардиальных клеток. Классическим примером является идентификация роли трансформирующего фактора роста β (TGFβ) в развитии сердца. Добавление лигандов, нейтрализующих антисывороток или антисмысловых олигонуклеотидов к культуре экспланта позволило выявить специфические лиганды TGFβ и рецепторы, которые регулируют трансформацию эндокардиальных клеток [15]. Значительное совершенствование метода эксплантатов достигнуто благодаря технологии использования вирусных векторов для введения генов в АВП или эндокардиальные клетки желудочка. В первоначальных экспериментах использовали инкубацию эксплантов с культуральной жидкостью, содержащей вирусный вектор для введения генов в эндокардиальные клетки, что зачастую приводило к неэффективному заражению эндокардиальных клеток. Первоначально этот подход был использован для идентификации роли атипичного рецептора TGFβ типа III (TGFβR3) при трансформации эндокардиальных клеток. Более поздние ex ovo модификации этого метода, за счет использования новых способов культивирования [16], позволили проводить манипуляции на эмбрионе вне яйца, благодаря этому раствор, содержащий вирус, мог быть введен непосредственно в просвет сердечной трубки на этапе ее развития до присоединения к сосудистой сети [17]. Инъекция раствора, содержащего аденовирус, приводит к высокоэффективному инфицированию эндокардиальных клеток по всей трубке сердца. Впоследствии в АВП или эксплантах желудочков проводится подсчет количества инфицированных эндокардиальных клеток, которые подверглись трансформации. В экспериментах использовался перенос аденовирусного гена для исследования функции TGFβR3 в эндокардиальных клетках. Сверхэкспрессия этого рецептора в желудочковых эндокардиальных клетках, которые обычно не имеют TGFβR3, приводит к их трансформации после добавления TGFβ-лиганда. Эти исследования на курином эмбрионе идентифицировали ключевые сигнальные молекулы, которые регулировали трансформацию эндокардиальных клеток и способствовали разработке подобной системы для in vitro исследования у мыши, что позволило дополнить данные полученные на куриных эмбрионах [18]. Постоянный интерес к трансформации эндокардиальных и эндотелиальных клеток, как при развитии клапанов, так и в выявлении механизмов, лежащих в основе трансформации эндокардиальных клеток, свидетельствует о том, что исследования на куриных эмбрионах по-прежнему актуальны.
Сердечный нейральный гребень
Сердечный нейральный гребень необходим для нормального развития и дальнейшего функционирования ССС. Клетки нейрального гребня могут быть получены из нервных складок, расположенных между серединами отических плакод и каудальной частью 3-го сомита. Особенностью клеток данного вида является возможность дифференцировки в различные типы мезенхимальных клеток, которые участвуют в развитии ССС, в дополнение к нейрогенным клеткам.
Эксперименты с использованием эмбрионов птиц, особенно куриных химер, позволили провести анализ миграции и дифференцировки клеток нейрального гребня [21]. Этот подход показал важную роль клеток нейрального гребня в развитии сердца. В частности, данные клетки вносят вклад в развитие аорто-легочной и конотрункальной перегородки.
В экспериментах на куриных эмбрионах также было обнаружено, что хемокиновый стромальный клеточный фактор (SDF1) и его родственный рецептор Cxcr4 важны для миграции в сердце клеток сердечного нейрального гребня. Было показано, что SDF1 действует как хемоаттрактант. Нарушение сигнализации SDF1 вызывало сердечные аномалии, в т.ч. неполное септирование аорты, легочного ствола и дефекты межжелудочковой перегородки [22].
Камеры сердца
В ходе завершения процесса формирования сердечной петли, начинается дифференцировка отделов сердца на два предсердия и два желудочка. Появление предсердий начинается с появления перегородки с дорсокраниальной стенки предсердия на стадии 14 по Гамбургеру-Гамильтону. В экспериментах на куриных эмбрионах было выявлено, что миокардиально-эндокардиальные взаимодействия координируют формирование клапанов [23], которые регулируют кровоток в сердце. Кроме того, полимеразная цепная реакция микроРНК выявила профили их экспрессии в предсердных, желудочковых и атриовентрикулярных областях развивающегося сердца цыпленка. В частности, miR-23b, miR-199a и miR-15a имели повышенную экспрессию во время раннего развития атриовентрикулярного канала, а анализ генов-мишеней свидетельствует о том, что они участвуют в регуляции путей передачи ЭМП [24].
Стенки камер сердца также подвергаются морфологическим изменениям. Вначале миокардиальный слой стенок желудочков образует выпячивания, называемые трабекулами, которые выступают в просвет камеры и покрываются слоем эндокарда. Процесс образования трабекул начинается со стадии 16 по Гамбургеру-Гамильтону. На протяжении всех стадий эмбрионального развития, увеличенная площадь поверхности сердца, создаваемая трабекулами, играет важную роль в васкуляризации и процессе доставки кислорода к сердцу.
Гемодинамика и ангиогенез
Куриный эмбрион, благодаря доступности для наблюдения и различных манипуляций, играл важную роль в ранних описаниях сосудистой системы позвоночных, сделанных Уильямом Гарвеем и Марчелло Мальпиги. С современными неинвазивными системами визуализации куриный эмбрион служит надежной моделью для мониторинга сосудистой сети in vivo. Когда развивающийся куриный эмбрион освобождается из яйца и культивируется ex ovo, хориоаллантоисная оболочка естественным образом расширяется, обнажая его сосудистую сеть и обеспечивая удобный доступ для долгосрочных экспериментов по ее визуализации.
Характер кровотока в развивающемся сердце играет значительную роль в морфогенезе сердца. В ответ на воздействие силы тока крови, культивируемые сердечные эндотелиальные клетки, перестраивают свой цитоскелет и изменяют экспрессию генов [25]. Чтобы связать такого рода данные, полученные в условиях in vitro с интактным сердцем куриного эмбриона, применяется ряд методов количественного анализа внутрисердечных потоков in vivo. Используя визуализацию in vivo, было показано, что высокочастотные сдвиговые вихревые флуктуации в развивающемся сердце оказывают более существенные воздействия, чем это можно было бы ожидать в столь малых структурах при низких значениях числа Рейнольдса. Чтобы проверить значимость этих сдвиговых сил in vivo, проводились эксперименты с блокированием тока крови, что приводило к образованию сердец с аномальной третьей камерой, нарушением формирования сердечной петли и образования клапанов. Сходство этих дефектов с некоторыми врожденными пороками сердца свидетельствует о важности внутрисердечной гемодинамики как ключевого эпигенетического фактора в эмбриональном кардиогенезе [25].
Роль эпигеномной регуляции в формировании ССС куриного эмбриона
МикроРНК участвуют в регуляции таких биологических процессов как пролиферация клеток, дифференцировка, апоптоз и поддержание нормальной клеточной физиологии. Аберрантная экспрессия или делеция микроРНК связана с аномальной дифференцировкой кардиомиоцита, нарушением развития сердца и сердечной дисфункцией. Несколько микроРНК были обнаружены в сердечной мышце и клетках миотомов скелетных мышц куриных эмбрионов.
Последовательность miR-1 играет важную роль, регулируя процесс кардиогенеза и миогенеза; miR-1 транскрибируется генами miR-1-1 и miR-1-2 [26]. Обнаружить транскрипты miR-1 удавалось в формирующейся сердечной трубке, начиная с дифференцировки кардиомиоцитов с 9-10 вплоть до стадии 22 по Гамбургеру-Гамильтону [26].
Избыточная экспрессия miR-1 приводит к остановке формирования сердца, развитию тонкостенных желудочков и сердечной недостаточности, что обусловлено преждевременной дифференцировкой и пролиферацией дефектных кардиомиоцитов [27].
Дифференцировка клеток в сердце регулируется различными факторами транскрипции: bHLH, hand1 и hand2, экспрессия которых регулирует развитие левого и правого желудочка, соответственно. Экспрессия фактора транскрипции hand2 зависит от isl-1, а hand1 – от nkx2-5 [28]. nkx2-5 взаимодействует с семейством транскрипционных факторов t-box и является одним из элементов активации или подавлении экспрессии генов, необходимых для дифференциации структур сердца. Выраженность экспрессии фактора nkx2-5 не существенна для образования синусового узла [29]. Однако, взаимодействие nkx2-5 с tbx2 или tbx3 приводит к репрессии гена, регулирующего предсердный натрийуретический пептид и коннексина-40 во время дифференцировки проводящей системы сердца, в том числе синоатриального узла [30, 31].
Заключение
Таким образом, эксперименты, позволяющие изучать развитие сердечно-сосудистой системы на ранних этапах онтогенеза, представляются весьма перспективными источниками информации для создания теоретической основы знаний о врожденной патологии системы кровообращения.
Использование куриных эмбрионов заложило основу для экспериментального изучения физиологии и патологии развития сердечно-сосудистой системы. Благодаря накопленному теоретическому и экспериментальному материалу о закономерностях развития куриного эмбриона и его органов, стало возможным изучение этиологии и патогенеза многих сердечнососудистых заболеваний. Работа с куриными эмбрионами заложила основу для получения человеком знаний в области эмбриогенеза сердечно-сосудистой системы – о формировании миокарда, эпикарда, эндокарда, коронарного сосудистого русла, камер сердца и магистральных сосудов.
С развитием новых биомедицинских технологий, в первую очередь методик прижизненной визуализации, расширился круг возможных вмешательств на сердечно-сосудистую систему куриного эмбриона. С учетом указанных преимуществ и совершенствования экспериментальных методик, модели на основе куриных эмбрионов не теряют актуальность и по сегодняшний день.