МКБ-10
Общие сведения
Синдром Шмидта (аутоиммунный полигландулярный синдром 2 типа, тиреоадренокортикальная недостаточность) – симптомокомплекс, состоящий из первичного гипокортицизма и гипотиреоза (реже гипертиреоза). Впервые он был описан в 1926 немецким эндокринологом М. Шмидтом. Данный синдром является самым распространенным вариантом полиэндокринных нарушений аутоиммунного генеза (встречается у 1,4-4,5 человек на 100 000 населения). Соотношение женщин и мужчин составляет 3:1. Средний возраст манифестации болезни – 30-35 лет. В единичных случаях синдром наблюдается у детей.
Причины
Точная этиология синдрома Шмидта неизвестна. Многие исследователи причисляют его к группе наследственно обусловленных заболеваний с аутосомно-рецессивным типом наследования. Генетическим маркером предрасположенности к синдрому Шмидта считаются определенные антигены главного комплекса гистосовместимости – HLA-B8, HLA-DW3.
Также в качестве доказательства связи некоторых гаплотипов с возникновением патологии рассматривается тот факт, что наиболее распространены случаи синдрома Шмидта среди близких родственников, чем среди чужих людей. Риск развития данного синдрома повышается при наличии у человека других аутоиммунных заболеваний, таких как синдром Шегрена, дерматомиозит, ревматоидный артрит и т. д.
Патогенез
В силу неизвестных причин в генетически предрасположенном организме происходит нарушение регуляции Т-клеточного иммунитета, а именно, чрезмерная активация Т-киллеров и Т-хелперов, подавление Т-супрессоров. Это приводит к аутоиммунному поражению эндокринных органов-мишеней (щитовидной железы и коркового вещества надпочечников) – развивается их деструкция, атрофия, снижение выработки гормонов.
Дефицит альдостерона вызывает водно-электролитный дисбаланс, снижение сосудистого тонуса, недостаточность кортизола снижает сопротивляемость к различным стрессорным факторам (главным образом к инфекциям), повышает порог чувствительности кардиомиоцитов и гладкомышечных клеток сосудов к катехоламинам, нарушает глюконеогенез и гликогенолиз в печени.
Из-за низкого уровня кортизола по принципу обратной связи увеличивается концентрация адренокортикотропного и меланоцитостимулирующего гормона, обусловливающего избыточное отложение меланина в коже. Дефицит трийодтиронина и тироксина замедляет все метаболические процессы в организме (окислительно-восстановительные реакции, синтез и катаболизм), что нарушает функционирование всех органов и систем, в первую очередь центральной нервной, сердечно-сосудистой.
Симптомы АПГС 2 типа
Проявления ХНН
В подавляющем большинстве случаев синдром Шмидта манифестирует с надпочечниковой недостаточности. Клиническая картина развивается постепенно, в течение нескольких месяцев или даже лет. Возникают общая и мышечная слабость, потеря аппетита, снижение веса. Практически во всех случаях наблюдаются признаки гипогликемии – чувство страха, дрожь во всем теле, потливость, тахикардия. Характерным признаком считается гиперпигментация кожи, она приобретает коричнево-бронзовый оттенок.
Особенно выражены изменения на открытых участках тела (лицо, шея, кисти рук), зонах, подверженных трению (подмышечные, паховые, ладонные складки, локтевые и коленные сгибы), сосках молочных желез. Также пигментируется слизистая оболочка полости рта – десна, мягкое, твердое небо покрываются серо-черными пятнами. Увеличенная щитовидная железа у многих пациентов вызывает дискомфорт в области шеи.
Вследствие слабого сосудистого тонуса наблюдаются симптомы пониженного артериального давления – головокружение, ортостатическая гипотензия, потеря сознания (обмороки). Нередки диспепсические явления – боли в животе (могут быть приступообразными), тошнота, рвота, диарея. Из-за сниженной сопротивляемости к инфекциям больные синдромом Шмидта подвержены частым респираторным вирусным заболеваниям.
Симптомы гипотиреоза
Примерно через 7-10 лет после манифестации синдрома Шмидта возникает аутоиммунный тиреоидит, в первые месяцы протекающий бессимптомно (фазы эутиреоза и субклинического гипотиреоза). Через некоторое время наступает манифестный гипотиреоз. Больные становятся сонливыми, заторможенными, у них ухудшаются когнитивные функции (память, внимание). Появляется отечность, особенно выраженная на лице, шее, руках, ломкость, выпадение волос, ногтей. Язык утолщается, на его поверхности остаются следы от зубов.
Из-за ослабления двигательной функции кишечника возникают запоры. Иногда развиваются боли в конечностях по типу радикулопатий вследствие отечности и сдавления нервных корешков и волокон. Наиболее типичен карпальный туннельный синдром. Возможны изменения психики в виде депрессивных расстройств, психозов. Из-за метаболических сдвигов в миокарде, больные нередко испытывают ноющие боли в области сердца. У женщин часто встречаются нарушения менструального цикла.
Симптомы тиреотоксикоза
Диффузный токсический зоб (ДТЗ) при синдроме Шмидта наблюдается крайне редко и считается, скорее, его атипичным вариантом. Больные становятся раздражительными, у них часто сменяется настроение, ухудшается сон, вплоть до бессонницы. Характерны постоянный субфебрилитет, тремор всего тела, артериальная гипертензия. Еще один типичный признак гипертиреоза – офтальмопатия, проявляющаяся экзофтальмом, двоением в глазах.
Осложнения
Наиболее грозным осложнением синдрома Шмидта, часто приводящим к летальному исходу, считается адреналовый криз – острая надпочечниковая недостаточность, при которой возникает высокая лихорадка, сильные абдоминальные боли, резкое падение артериального давления (сосудистый коллапс). Из-за низкой инфекционной сопротивляемости, больные имеют высокий риск пневмоний, менингита, туберкулеза.
Еще одним осложнением, связанным с высоким уровнем смертности, является гипотиреоидная кома. При гипотиреозе возможно скопление большого количества жидкости в серозных полостях (перикарде, плевральной, брюшной полости). Выраженная отечность мягких тканей глотки может привести к синдрому обструктивного апноэ сна. При тиреотоксикозе часто возникает фибрилляция предсердий, при которой возрастает риск образования тромбов и кардиоэмболического инсульта.
Диагностика
Пациентов с синдромом Шмидта курирует врач-эндокринолог. В диагностике патологии важное значение имеет физикальное обследование. Во время осмотра обращают на себя внимание утолщение и сухость кожи, холодные конечности, снижение или отсутствие сухожильных рефлексов. При аускультации сердца часто можно выслушать приглушенность сердечных тонов, замедление ЧСС. Для верификации диагноза назначаются:
Дифференциальную диагностику синдрома Шмидта следует проводить по преобладающим в клинической картине симптомам. Гиперпигментацию кожи и слизистых нужно отличать от болезни Иценко-Кушинга, гемохроматоза. Признаки гипогликемии могут наблюдаться при инсулиноме, незидиобластозе. Мышечную слабость необходимо дифференцировать с мышечными дистрофиями.
Лечение синдрома Шмидта
Консервативная терапия
Начало терапии больных всегда проводится в условиях стационара (отделение эндокринологии). Основу лечения составляет постоянная гормональная терапия. При достижении улучшения общего состояния пациента, регресса клинической симптоматики и нормализации лабораторных показателей можно уменьшить дозу препарата до поддерживающей, но прием остается пожизненным. При консервативной терапии синдрома Шмидта используют следующие средства:
При сочетании хронической надпочечниковой недостаточности и гипотиреоза лечение всегда нужно начинать с коррекции гипокортицизма. Это связано с тем, что левотироксин ускоряет клиренс глюкокортикоидов в печени, и его назначение пациенту с некомпенсированной ХНН может спровоцировать развитие острой надпочечниковой недостаточности.
Хирургическое лечение
При безуспешности консервативной терапии гипертиреоза (частые рецидивы) или непереносимости лекарств прибегают к хирургическому удалению щитовидной железы – тотальной тиреоидэктомии. До проведения оперативного вмешательства необходимо достигнуть состояния эутиреоза (нормализации показателей тиреоидных гормонов) тиреостатиками либо большими дозами йодида калия. После удаления железы назначается левотироксин в заместительной дозе.
Прогноз и профилактика
При своевременной диагностике и грамотно проведенной терапии синдром Шмидта имеет благоприятный прогноз. Продолжительность жизни пациента может ничем не отличаться от таковой в общей популяции. Основные причины смерти при декомпенсированном гормональном дефиците – тяжелые генерализованные инфекции, адреналовый криз, микседематозная кома.
Так как точные причины возникновения заболевания неизвестны, методов первичной профилактики не существует. Вторичная профилактика (предупреждение осложнений) заключается в регулярном контроле за клиническими (общее самочувствие пациента, артериальное давление) и лабораторными показателями (концентрация ТТГ, глюкозы, калия).
Другая и неуточненная недостаточность коры надпочечников (E27.4)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Первичный гипокортицизм/аддисонова болезнь:
· врожденная форма;
· приобретенная форма.
Врожденная форма:
· гипоальдостеронизм;
· адренолейкодистрофия;
· синдром Оллгрова;
· врожденная гипоплазия коры надпочечников;
· семейный изолированный дефицит глюкокортикоидов.
Приобретенная форма:
· аутоиммунный и инфекционный адреналит;
· амилоидоз и опухолевые метастазы.
Вторичный гипокортицизм:
· врожденная форма;
· приобретенная форма.
Третичная недостаточность коры надпочечников:
· врожденная форма;
· приобретенная форма.
Врожденная форма:
· недостаточность выработки кортиколиберина
· множественную недостаточность гипоталамуса,
Приобретенная форма:
· деструкции тканей гипоталамуса.
По тяжести как первичную, так и вторичную надпочечниковую недостаточность делят:
· легкая степень тяжести;
· средняя степень тяжести;
· тяжелая степень тяжести.
По выраженности клинических проявлений ХНН:
· явная форма;
· латентная форма.
На фоне лечения ХНН возможно выделение следующих фаз:
· декомпенсация;
· субкомпенсация;
· компенсация.
Клиническая картина
Cимптомы, течение
При хронической надпочечниковой недостаточности
Диагностические критерии
Жалобы
:
· судорожный синдром;
· гиперпигментация кожи;
· приступы гипогликемии (потеря сознания, дрожь,потоотделение);
· постоянная слабость;
· повышенная утомляемость;
· снижение аппетита, потеря массы тела;
· повторная рвота, тошнота, диарея на фоне заболеваний, высокая температура, стресс;
· тяга к соленой пище.
Анамнез:
· наличие у пациента заболевания, одним из компонентов которого может быть ХНН;
· наличие близких родственников, страдающих наследственными формами ХНН.
· туберкулез/амилоидоз в анамнезе;
Физикальное обследование:
· гиперпигментация кожных покровов и слизистых оболочек (локальная или диффузная);
· бледность/сероватый оттенок кожи;
· низкое АД;
· дефицит массы тела/резкая потеря массы тела.
NB! Ни одно из клинических проявлений не является строго специфическим критерием диагностики ХНН и требует лабораторного подтверждения (УД-B) [3]
Диагностика
Лабораторная диагностика
Лабораторные исследования (УД–B):
· уровень кортизола в сыворотке (время забора крови с 8.00);
· уровень АКТГ в плазме крови (время забора крови 8.00);
· ОАК;
· ОАМ;
· глюкоза в сыворотке крови;
· уровень калия в сыворотке крови;
· уровень натрия в сыворотке крови;
· ренин в плазме крови (активность ренина плазмы – АРП).
Уровень кортизола в сыворотке:
Таблица – 1. Оценка уровня базального кортизола (УД–B) [2].
| Кортизол, нмоль/л | Вероятность диагноза НН |
| менее 150 | Вероятна НН |
| 150—500 | Сомнительна НН |
| более 500 | Исключается НН |
Уровень АКТГ в плазме крови:
· при значительно повышенном уровне АКТГ (более 150 пг/мл) и уровне кортизола менее 500 нмоль/л диагноз первичной НН может быть установлен.
NB! При уровне АКТГ менее 150 пг/мл и уровнекортизола менее 500 нмоль/л, требуется дополнительный стимуляционный тест с синактеном (УД–B) [2].
NB! Если пациент получает терапию глюкокортикоидами, то исследование уровня базального кортизола и АКТГ не достоверно, рекомендуется переход ко II этапу диагностики с помощью стимуляционных проб.
Анализ суточной мочи, слюны на уровень свободного кортизола:
· повышение уровня свободного кортизола.
NB! Определение метаболитов стероидогенеза в суточной моче (17-ОКС) не является информативным и нe рекомендуется для диагностики НН (УД – E) [2].
При острой надпочечниковой недостаточности :
Определение электролитов в сыворотке крови:
· резкое снижение содержания натрия (гипонатриемия) и хлоридов. Уровень натрия может быть 130 мэкв и ниже.
· гиперкалиемия до 5-6 мэкв, иногда этот показатель достигает 8 мэкв;
· изменение соотношение Na/K (снижение до 20 и ниже).
Определение глюкозы в сыворотке крови:
· гипогликемия;
Биохимический анализ крови:
· повышение уровня мочевины, остаточного азота.
КЩС крови:
· повышение гематокрита, уменьшение щелочности крови.
ОАМ:
· характерным является снижение выделения натрия с мочой, которое составляет менее 10 г за сутки;
Для диагностики центрального гипокортицизма используются тест с инсулином, тест с метирапоном и стимуляционная проба с КРГ.
Схема 4. Алгоритм диагностики вторичного гипокортицизма.
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований
Таблица – 1. Дифференциальный диагноз первичной и вторичной ХНН
| Показатель | ХНН | |
| первичная | вторичная | |
| гипотония | + | + |
| Снижение массы тела | + | + |
| Гипогликемия | + | + |
| Гиперпигментация кожи и слизистых | + | нет |
| Уровень кортикотропинав крови | ↑ | ↓ |
| Сопутствующий гипотиреоз | редко | часто |
| Сопутствующий гипогонадизм | редко | часто |
| Отставание в росте | нет | часто |
| Уровень кортизола в крови | ↓ | ↓ |
| Экскрекция кортизола с мочой | ↓ | ↓ |
| Уровень ТТГ в крови | ↓ норма (синдром Шмидта) | ↓ |
| Уровни Т3 и Т4 | норма | ↓ |
| Дефицит СТГ | Нет | часто |
| Уровни ЛГ ФСГ в крови | норма | ↓ |
| Проба с КРГ | положительная | отрицательная |
| Проба с кортикотропином | Отрицательная | положительная |
Лечение (амбулатория)
Немедикаментозное лечение:
Режим: III (щадящий режим, избегать острых стрессовых ситуаций, переохлаждений).
Диета: стол № 15 (питание, обогащенное поваренной солью и аскорбиновой кислотой).
Медикаментозное лечение:
На амбулаторном этапе медикаментозная терапия заключается в постоянной заместительной терапии стероидными препаратами, как глюкокортикостероидами, так и минералокортикоидами.
Перечень основных лекарственных средств (имеющих 100% вероятность применения):
| Лекарственная группа | Международное непатентованное наименование ЛС | Способ применения | Уровень доказательности |
| ГКС | гидрокортизон H02AB09 | 15-25 мг/стукив двух или трех разделенных дозах в день, наибольшая доза должна быть принята утром, при пробуждении, на следующий либо в начале дня (2 часа после обеда; две дозы лечебного препарата) или в обед, а после обеда (три дозы препаратов) | А |
| кортизона ацетат H02AB10 | 20-35 мг/сутки в двух или трех разделенных дозах в день, наибольшая доза должна быть принята утром, при пробуждении, на следующий либо в начале дня (2 часа после обеда; две дозы лечебного препарата) или в обед, а после обеда (три дозы препаратов) | А | |
| преднизолон Н02АВ06. | 3-5 мг/сут, вводят перорально один или два раза в день | В | |
| Минералортикоиды | H02AA02 флудрокортизон | начальная доза 50-100 мкг у взрослых. В летние месяцы дозу может быть увеличена до 0.2 мг в день для компенсации потери электролитов с потоотделением. В случае повышения АД на фоне терапии рекомендуется добавить антигипертензивную терапию и продолжить флудкортизон | А |
*применение после регистрации на территории РК.
Хирургическое вмешательство: нет.
Дальнейшее ведение :
· обучение больного, страдающего любой формой хронической надпочечниковой недостаточности, регулярному приему адекватных доз глюко- и минералокотрикоидных препаратов, а также самостоятельному увеличению их дозировок вдвое при любых стрессах (интеркуррентные заболевания, операции, эмоциональные напряжения и другие).
Контроль адекватности заместительной терапии 1 раз в 6 месяцев включает:
· исследование калия, натрия крови;
· АРП;
· осмотр эндокринолога 1 раз в 6 месяцев с оценкой динамики массы тела, АД, жалоб, анализом причин острых состояний (если таковые были за прошедший период с момента предыдущего осмотра) (УД-B).Обследование с учетом причины ХПНН для выявления новых компонентов синдрома или коррекции уже назначенной терапии дополнительных компонентов совместно с другими специалистами.
Индикаторы эффективности лечения:
· устранение клинических и лабораторных признаков гипокортицизма.
Лечение (стационар)
Карта наблюдения пациента, маршрутизация пациента
Немедикаментозное лечение
Режим:
· II (щадящий режим);
· I при развитии острой надпочечниковой недостаточности.
Диета: стол № 15(должна содержать увеличенное количество калорий, белков, углеводов, витаминов, с достаточным количеством поваренной соли до 3-10 г/сут).
Медикаментозное лечение:
Проводится заместительной гормональной терапией, как глюкокортикостероидами так и минералокортикоидами. Дозы варьируются в зависимости от состояния пациента и коморбидного фона.
Перечень основных лекарственных средств (имеющих 100% вероятность применения):
Ведение пациентов со вторичными бактериальными инфекциями и сопутствующими заболеваниями, отягощающие ХНН, ведется согласно утвержденным клиническим протоколам МЗ РК.
Хирургическое вмешательство: нет.
Индикаторы эффективности лечения:
· устранение клинических и лабораторных признаков гипокортицизма.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
· первичная верификация диагноза (проведение тестов);
· развитие сопутствующей патологии (вирусные, бактериальные инфекции, стрессы и тд).
Показания для экстренной госпитализации:
· развитие надпочечникового криза.
Первичная хроническая надпочечниковая недостаточность на фоне аутоиммунного полигландулярного синдрома
Надпочечниковая недостаточность – это тяжелое эндокринное заболевание, обусловленное недостаточной секрецией гормонов коры надпочечников, являющееся результатом нарушения функционирования одного или нескольких звеньев гипоталамо-гипофизарно-надпочечниковой системы. Клиническая картина надпочечниковой недостаточности, связанная с деструкцией надпочечников туберкулезного происхождения, впервые в 1855 г. была описана английским врачом Томасом Аддисоном (Thomas Addison, 1793-1860 гг.) и поэтому синонимом первичной хронической надпочечниковой недостаточности является термин «болезнь Аддисона».
В клинической практике в зависимости от скорости развития клинических симптомов заболевания выделяют острую (ОНН) и хроническую надпочечниковую недостаточность (ХНН). ХНК в соответствии с локализацией патологического процесса разделяется на первичную 1-ХНН – уменьшение продукции гормонов коры надпочечников в самих надпочечниках; вторичную 2-ХНН — снижение или отсутствие секреции адренокортикотропного гормона гипофиза (АКТГ); третичную 3-ХНН — неспособность гипоталамуса вырабатывать кортикотропин-рилизинг-гормон.
Принципиальным аспектом при обсуждении этиологии 1-ХНН является аутоиммунный полигландулярный синдром (АПС). АПС представляет собой первичное аутоиммунное поражение двух и более периферических эндокринных желез, приводящее, как правило, к их недостаточности, часто сочетающееся с различными органоспецифическими неэндокринными заболеваниями аутоиммунного генеза. В настоящее время на основании клинических и иммуногенетических особенностей выделяют АПС 1-го и 2-го типов (АПС-1 и АПС-2).
АПС-2 – наиболее распространенный, но менее изученный вариант АПС. В свою очередь самым частым вариантом АПС-2 является синдром Шмидта, представляющий собой сочетание 1-ХНН и аутоиммунных тиреопатий (аутоиммунный тиреоидит или диффузный токсический зоб). Реже встречается сочетание 1-ХНН с сахарным диабетом I типа (синдром Карпентера).
Многие из заболеваний в рамках АПС-2 ассоциированы с антигенами гистосовместимости НLА-В8, НLА-DR3, НLА-DR4, НLА-DR5. Тем не менее в настоящее время не выявлено каких-либо существенных иммуногенетических различий между изолированными аутоиммунными эндокринопатиями и таковыми в рамках АПС-2. В большинстве случаев АПС-2 встречается спорадически, однако описано немало случаев семейных форм, при которых заболевание наблюдается у разных членов семьи в нескольких поколениях. АПС-2 примерно в 8 раз чаще встречается у женщин, манифестирует в среднем возрасте (между 20 и 50 годами), при этом интервал между клиническим дебютом его отдельных компонентов может составить более 20 лет. У 40-50% больных с исходно изолированной хронической НН (1-ХНН) рано или поздно развивается другая аутоиммунная эндокринопатия.
АПС-1 (APECED-Autoimmune polyendocrinopathy-candidiasis-ectodermal-dystrophy, MEDAC-Multiple Endocrine Deficiency Autoimmune Candidiasis, кандидо-полиэндокринный синдром) редкое заболевание с аутосомно-рецессивным типом наследования или встречающееся реже спорадически, для которого характерна классическая триада, описанная Уайткером: слизисто-кожный кандидоз, гипопаратиреоз, 1-ХНН. АПС-1 дебютирует, как правило, в детском возрасте. В подавляющем большинстве случаев первым проявлением является слизисто-кожный кандидоз, развивающийся в первые 10 лет жизни, чаще в возрасте около 2 лет, при этом наблюдается поражение слизистых оболочек полости рта, гениталий, а также кожи, ногтевых валиков, ногтей, реже встречается поражение желудочно-кишечного тракта (ЖКТ), дыхательных путей. На фоне слизисто-кожного кандидоза у 84% пациентов появляется гипопаратиреоз, который у 88% больных развивается в первые 10 лет, а позднее (иногда через десятки лет) диагностируется надпочечниковая недостаточность. С меньшей частотой вышеперечисленная симптоматика сопровождается первичным гипогонадизмом, хроническим активным гепатитом, алопецией, витилиго, пернициозной анемией.
Наиболее существенным открытием последних лет в области исследования АПС является открытие гена, мутации которого приводят к развитию АПС-1. Этот ген расположен на хромосоме 21q22.3 и получил название AIRE-1 (от autoimmune regulator). Открытие гена AIRE-1 имеет важное общемедицинское значение. Генетический компонент предполагается в качестве одного из принципиальных факторов развития большинства аутоиммунных заболеваний. Однако с позиции генетики аутоиммунные заболевания относятся к полигенным или заболеваниям с наследственной предрасположенностью.
При динамической оценке соотношения частоты изолированной 1-ХНН и 1-ХНН в рамках АПС было выявлено, что если в 30-50-х годах ХХ века 1-ХНН в рамках АПС встречалась в 13% случаев, то к 80-90-м годам этот показатель вырос до 34%, в связи с чем можно сделать вывод об очередном этапе патоморфоза болезни Аддисона, который заключается в постепенном переходе этой патологии в разряд АПС, в первую очередь АПС-2.
По степени тяжести, как первичную, так и вторичную надпочечниковую недостаточность делят на формы: легкую, среднюю и тяжелую. По выраженности клинических проявлений ХНН делится на явную и латентную. На фоне лечения ХНН возможно выделение следующих фаз: декомпенсация, субкомпенсация и компенсация.
Патогенез хронической надпочечниковой недостаточности заключается в том, что клиническая картина становится заметной после разрушения 90 % объема ткани надпочечников, т.е. болезнь Аддисона развивается постепенно. Прогрессирующий дефицит кортизола и альдостерона приводит к нарушениям углеводного, белкового, липидного и водно-солевого обменов. Развивается гипонатриемическая дегидратация с гиперкалиемией, гипохлоремией, гипогликемией и кетозом. Уменьшение объема циркулирующей плазмы приводит к нарастанию внутриклеточной дегидратации с развитием метаболического ацидоза, выраженной артериальной гипотензии (вплоть до коллапса), снижением сердечного выброса и клубочковой фильтрации (вплоть до анурии). При первичной ХНН дефицит кортизола приводит к гиперпродукции АКТГ гипофизом (отрицательная обратная связь), что объясняет появление гиперпигментации.
Клиническая картина. Первичная ХНН (1ХНН) характеризуется незаметным началом и медленным нарастанием утомляемости, мышечной слабости, потери аппетита, снижения массы тела, гиперпигментации кожи и слизистых оболочек, гипотензии и иногда гипогликемии. Выраженная общая и мышечная слабость (астения) вначале возникает периодически во время стрессов. На ранних стадиях астения увеличивается к концу дня и проходит после ночного отдыха, в дальнейшем нарастает и становится постоянными, приобретая характер адинамии. Наряду с физической адинамией развивается психическая астенизация, вплоть до развития психозов. Мышечная слабость является результатом нарушения углеводного (гипогликемия) и электролитного (гипонатриемия) обменов.
Потеря массы тела является постоянным симптомом надпочечниковой недостаточности и связана с понижением аппетита, нарушением всасывания в кишечнике, рвотой, диареей, дегидратацией.
Гипогликемические состояния у больных с хронической надпочечниковой недостаточностью могут возникать как натощак, так и через 2-3 часа после приема пищи, богатой углеводами. Приступы сопровождаются слабостью, чувством голода, потливостью. Гипогликемия развивается в результате снижения секреции кортизола, уменьшения глюконеогенеза, запасов гликогена в печени.
Нарушения функции ЦНС встречаются более чем у половины больных и проявляются снижением умственной деятельности и памяти, апатией, раздражительностью.
Со стороны почек нередко отмечается никтурия на фоне снижения клубочковой фильтрации и почечного кровотока.
Прекращение секреции надпочечниковых андрогенов у мужчин мало влияет на состояние половых функций, если сохранена функция яичек. Однако у женщин это может определять снижение либидо и играет определенную роль в уменьшении и полном исчезновении подмышечного и лобкового оволосения.
У небольшой части больных при длительном наличии гипокортицизма отмечается наличие кальцификации ушных хрящей (вероятно, обусловленное возникающей гиперкальциемией).
Синдром Нельсона развивается у больных через разные промежутки времени после тотальной адреналэктомии. Клиническая картина при синдроме Нельсона характеризуется лабильным течением ХНН, прогрессирующей гиперпигментацией кожных покровов, АКТГ-продуцирующей опухолью гипофиза, офтальмологическими и неврологическими нарушениями.
Диагноз ХНН устанавливается на основании субъективного (жалобы, анамнез заболевания, жизни), объективного и лабораторно-инструментального исследования. Прямым подтверждением гормональной недостаточности коры надпочечников являются исследования уровня кортизола в крови в утренние часы и свободного кортизола в суточной моче. Как первичная, так и вторичная надпочечниковая недостаточность проявляются снижением содержания кортизола в крови, но часто содержание кортизола в плазме крови в утренние часы имеет нормальные или пограничные значения, что требует дальнейшего обследования.
Исследование АКТГ в плазме крови позволяет дифференцировать первичную и вторичную ХНН. Уровень АКТГ более 100 пг/мл, определенный с помощью РИА или иммуноферментного анализа, при наличии клиники надпочечниковой недостаточности, однозначно свидетельствует о ее первичном генезе. При вторичной ХНН, как правило, отмечается снижение уровня АКТГ крови.
В общем анализе крови при хронической надпочечниковой недостаточности часто выявляется нормохромная или гипохромная анемия, умеренная лейкопения, относительный лимфоцитоз и эозинофилия. Ускорение СОЭ отмечается лишь при наличии сопутствующего активного воспалительного процесса.
Основой современной этиологической диагностики аутоиммунной болезни Аддиссона считается выявление в крови больных антител к 21-гидроксилазе (Р450с21), которые являются высокоспецифичным маркером аутоиммунного адреналита, протекающего как в форме изолированной болезни Аддисона, так и в составе АПГС I и II типов.
Учитывая то, что первичная ХНН аутоиммунного генеза часто сочетается с другими аутоиммунными эндокринопатиями, необходимо скрининговое определение в сыворотке крови больных с первичной ХНН органоспецифических антител (к тиреоглобулину, тиреопероксидазе, гонадам, островковым клеткам поджелудочной железы), а также определения у них уровня кальциемии, фосфатемии, гликемии, ЛГ, ФСГ, свободного тироксина (св. Т4), ТТГ для исключения первичной недостаточности паращитовидных, половых, щитовидной желез и островкового аппарата поджелудочной железы.
Для подтверждения туберкулезного генеза ХНН обязательно проводятся рентгенологическое исследование органов грудной клетки и малого таза. Проба Манту, а также посев мочи и мокроты на выявление микобактерий туберкулеза в ряде случаев помогают подтвердить диагноз туберкулезного процесса в надпочечниках.
Увеличение надпочечников, выявленное на КТ, может иметь место не только при туберкулезе, но и при метастазах в надпочечники, грибковых инфекциях. Основная роль в трудных случаях дифференциальной диагностики отводится тонко игольной аспирационной биопсии надпочечников под контролем ультразвукового исследования (УЗИ) или КТ.
Для установления причины вторичной ХНН необходимо проведение обзорной рентгенографии черепа (боковая проекция) и магнитно-резонансной томографии (МРТ) головного мозга для исключения опухолевого процесса в гипоталамо-гипофизарной области.
Трудоспособность и профилактика. Больным с хронической надпочечниковой недостаточностью показан перевод на легкую работу с нормированным рабочим днем, исключая ночные смены, командировки, тяжелую физическую нагрузку. В период декомпенсации гипокортицизма больные считаются нетрудоспособными. При тяжелой форме надпочечниковой недостаточности показан перевод на инвалидность.
В течение полугода на базе 3-ей ГКБ г. Минска им. Е.В Клумова наблюдалось четыре пациента с клинически ярко выраженным течением криза первичной хронической надпочечниковой недостаточности на базе аутоиммунного полигландулярного синдрома.
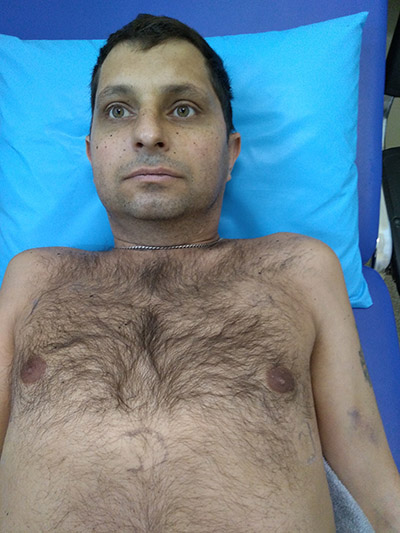
Больной Ц., 37 лет, был доставлен в стационар СП в тяжёлом состоянии с жалобами на общую слабость, недомогание, тошноту, многократную рвоту, сердцебиение, затруднение дыхания, резкое похудание (на 36 кг в течение полугода). Считает себя больным около 2-х месяцев, причины не знает. С 28.11.18.по 18.12. 2018. находился на стационарном лечении в кардиологическом отделении 2-ой ГКБ с диагнозом Неревматические поражения митрального клапана. МАС: Пролапс передней створки МК 1 ст. с минимальной регургитацией. Острый алиментарно-токсический гепатит, умеренная ст. активности. ХСН ФК 1. Неполная БПНПГ.
Самочувствие резко ухудшилось после нервного стресса (решался квартирный вопрос): снизился аппетит, появилась тошнота, рвота, общая слабость и недомогание, упало артериальное давление.
Кожно-венерические заболевания, туберкулёз отрицает, в детском возрасте часто болел бронхитом, при проведении реакции Манту запомнил «цифру 8», в юношеском возрасте перенёс инфекционный гепатит. Аллергии не наблюдалось, вредные привычки не отмечает.
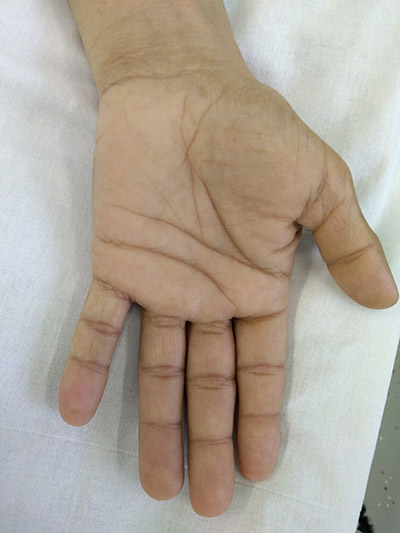
Рис. 1. Больной Ц. (37 лет), с первичной хронической надпочечниковой недостаточностью: выраженное отложение пигмента на лице, около сосочковых ареолах, на ладонных складках разгибательных поверхностей суставов кистей рук.
Кардиологическая триада: КФК-МБ 18,1 нг/мл, Миоглобин 500 нг/мл, Тропонин 0,05 нг/мл.
Общий анализ мочи: с/ж, прозрачная, уд.в.1030, кет., белок – 0,06, ураты.
Общий анализ крови: Er 3,2 ×10 12 /л, L 9,32 ×10 12 /л, Нв-105 г/л, э-1%, п- 2%, с- 63%, с-28%, м-6%, СОЭ 3 мм/час.
УЗИ органов брюшной полости: печень КВР-3 мм, ПЭР-92 мм, не увеличена, контуры ровные, эхогенность и проводимость нормальная, эхоструктура однородная.
Заключение: изменения печени по типу стеатоза. Диффузные изменения поджелудочной железы.
В обеих почках «подчёркнут» рисунок пирамид – справа пирамидки 8 мм, слева – 7,5 мм. Кровоток при ЦДК не изменён: ЛСК справа – 58 см/сек, слева ЛСК – 60 см/сек, ИР – 0,54, область надпочечников свободна.
Заключение: УЗ-картина может соответствовать воспалительному заболеванию почек. Уростаза не выявлено.
УЗИ щитовидной железы: Без эхоструктурной патологии.
КТ органов брюшной полости, КТ костного аппарата.
Заключение: Патологических изменений надпочечников не выявлено.
ЭКГ: ритм синусовый, неполная блокада ПНПГ.
При назначении минерало- и глюкокортикоидов в должных дозах на фоне антибактериального и симптоматического лечения быстро наблюдалась положительная динамика: нормализовалось АД, появился аппетит, уменьшилась слабость, восстановился сон.
Пациент был переведен в эндокринологическое отделение 1-ой ГКБ г. Минска.
После стационарного лечения в течение 9-ти дней больной в удовлетворительном состоянии был переведен на амбулаторное лечение.
врачи отделения ультразвуковой диагностики
УЗ 3-я ГКБ г. Минска им. Е.В. Клумова:
заведующая отделением Максимова Т.В., врач Ванькович Е.А.