Бронхолегочная дисплазия у недоношенных детей
Нередко у недоношенных детишек после применения искусственной вентиляции легких (ИВЛ) развивается бронхолегочная дисплзия (БЛД). Возникает она благодаря нескольким факторам: это и собственно незрелость легких недоношенных детей, и интенсивный режим ИВЛ. Заболевание характеризуется полной ремиссией к 3-м годам жизни ребенка.
Почему возникает БЛД?
БЛД может возникать в результате дефицита сурфактанта (пленки, выстилающей альвеолы и препятствующей их спадению), отека легких, длительного применения высоких концентраций кислорода (повреждение свободными разикалами кислорода и т.д.), ИВЛ, воспаления, воздействия бактерий и вирусов и др. В результате действия вышепепречисленных факторов повреждаются практически все структурные компоненты незрелой легочной ткани, что приводит к хроническому нарушению функции легких и замещению здоровой ткани участками фиброза.
Как проявляется БЛД?
При наличии бронхолегочной дисплазии у ребенка отмечается бледность кожи и цианоз, учащается дыхание до 80-100 в мин, дыхание происходит с помощью дополнительной мускулатуры (межреберные мышцы). При выслушивании фонендоскопом: ослабленное дыхание, хрипы, либо жесткое дыхание. Если развивается тяжелая форма БЛД, то повреждаются и другие органы: сердце, почки, печень (ввиду перегрузки малого круга кровообращения).
Как наблюдаться у специалистов после выписки из стационара и на что обращать внимание?
Обязательно наблюдение участкового педиатра, с целью подбора терапии в периоды обострения, своевременного лечения рахита, коррекции анемии. Наблюдение пульмонолога, с целью подбора лечения, либо коррекции терапии БЛД, оценки функции внешнего дыхания.
Также важно следить за питанием малыша. Необходима прибавка в весе, избегание задержки роста. (достигается за счет повышенной каллорийности питания 140-150 ккал/кг/сутки, у матерей кормящих грудным молоком за счет обогащения молока усилителями, либо подбор специальной смеси).
Как часто наблюдаться у специалистов?
В зависимости от тяжести БЛД наблюдение специалистов происходит:
С чем связаны периоды обострения заболевания?
Блд у детей что это

Поиск
Современные подходы к диагностике и лечению бронхолегочной дисплазии
Статья содержит обзор данных литературы по этиологии, патогенезу и диагностике бронхолегочной дисплазии у новорожденных. Приводятся доказательные методы лечения данного заболевания с позиции современной медицины.
Current approaches to diagnosis and treatment of bronchopulmonary dysplasia
This article contains a review of the literature on the etiology, pathogenesis and diagnosis of bronchopulmonary dysplasia in infants. Conclusive methods treatment of this disease from the position of modern medicine are provided.
Бронхолегочная дисплазия (БЛД) — это полиэтиологическое хроническое заболевание морфологически незрелых легких, развивающееся у новорожденных, главным образом глубоконедоношенных детей, в результате интенсивной терапии респираторного дистресс-синдрома (РДС) и/или пневмонии. Протекает это заболевание с преимущественным поражением бронхиол и паренхимы легких, развитием эмфиземы, фиброза и/или нарушением репликации альвеол [2, 3]. Проявляется БЛД зависимостью от кислорода в возрасте 28 суток жизни и старше, бронхообструктивным синдромом и симптомами дыхательной недостаточности; для него характерны специфические рентгенологические изменения в первые месяцы жизни и регресс клинических проявлений по мере роста ребенка.
Частота БЛД обратно пропорциональна гестационному возрасту и массе тела при рождении. Так, у детей с весом при рождении 501-750 г, по результатам различных исследований, БЛД отмечается в 35-67%, а у детей с массой тела 1251-1500 г при рождении — в 1-3,6% случаев [1].
Первоначально БЛД рассматривалась как результат повреждающего действия кислорода и ИВЛ на легкие новорожденного, что нашло отражение в классической формуле A. Philip (1975): «кислород+давление+время». В настоящее время БЛД рассматривается как полиэтиологическое заболевание [3, 5]. Факторами, способствующими развитию БЛД, являются:
Бронхолегочная дисплазия у детей. Клинические рекомендации.
Бронхолегочная дисплазия у детей
Оглавление
Ключевые слова
Высокоразрешающая компьютерная томография
Искусственная вентиляция легких
Открытый артериальный проток
Респираторный дистресс синдром
Шкала балльной оценки тяжести течения БЛД
Список сокращений
ЖКТ- Желудочно-кишечный тракт
ИВЛ- Искусственная вентиляция легких
Термины и определения
В данных клинических рекомендациях новые и узконаправленные термины не употребляются.
1. Краткая информация
1.1 Определение
Бронхолегочная дисплазия (БЛД) – это полиэтиологическое хроническое заболевание морфологически незрелых легких, развивающееся у новорожденных, главным образом глубоко недоношенных детей, в результате интенсивной терапии респираторного дистресс-синдрома (РДС) и/или пневмонии. Протекает с преимущественным поражением бронхиол и паренхимы легких, развитием эмфиземы, фиброза и/или нарушением репликации альвеол; проявляется зависимостью от кислорода в возрасте 28 суток жизни и старше, бронхообструктивным синдромом и симптомами дыхательной недостаточности; характеризуется специфичными рентгенографическими изменениями в первые месяцы жизни и регрессом клинических проявлений по мере роста ребенка [1].
1.2 Этиология и патогенез
Бронхолегочная дисплазия является мультифакториальным заболеванием (табл. 1).
Малая масса тела при рождении ( 0,5, высокие PIP и MAP
CPAP или ИВЛ с FiO2 0,3-0,4, невысокие PIP и MAP
Сразу после рождения
Отсроченно (через несколько дней-недель), характерен «светлый» промежуток
Интерстициальный отек, сменяемый гиперинфляцией, буллами, лентообразными уплотнениями
Равномерное затенение («затуманенность»), негомогенность легочной ткани с мелкими или более крупными уплотнениями, в тяжелых случаях повышенная воздушность
1.3 Эпидемиология
Отмечается увеличение частоты формирования БЛД по мере уменьшения гестационного возраста и массы тела ребенка при рождении. У детей с гестационным возрастом менее 29 недель и массой тела при рождении менее 750г частота формирования БЛД может достигать 65 – 67%, в то время как у детей с гестационным возрастом более 32 недель и массой тела при рождении более 1250г – всего лишь 1 – 3,6% [1].
1.4 Кодирование по МКБ-10
1.5 Примеры диагнозов
«Бронхолегочная дисплазия, классическая форма, тяжелое течение, неполная ремиссия, хроническая дыхательная недостаточность».
При формулировке диагноза необходимо обязательно указывать тяжесть течения заболевания. В возрасте до 28 суток жизни диагноз БЛД не может быть установлен, до 28 суток жизни правомочны такие формулировки как «формирование БЛД» или «группа риска по БЛД».
Диагноз «бронхолегочная дисплазия» правомерен в качестве самостоятельного у детей до 3-летнего возраста, у детей после 3 лет БЛД указывается как заболевание, имевшее место в анамнезе. При ведении медицинской документации для оценки степени тяжести БЛД необходимо указывать вид респираторной терапии и состояние кислородозависимости ребенка в значимые для определения тяжести заболевания сроки.
1.6 Классификация
Тяжесть и прогноз БЛД определяет степень кислородозависимости, оцененная в 36 нед. постконцептуального возраста (ПКВ – возраст, суммирующий срок гестации и срок постнатальной жизни в неделях) у детей, родившихся с гестационным возрастом менее 32 недель, на 56 день жизни у детей с гестационным возрастом более 32 недель или при выписке, если она наступит раньше (1А) [3] (табл. 3).
Степень тяжести БЛД
Диагностические критерии для детей различного
гестационного возраста при рождении
Время и условия оценки
36 недель постконцептуального возраста или выписка домой (что наступит раньше)
От 28 до 56 дня после рождения или выписке домой (что наступит раньше)
Терапия кислородом более 21% в течение 28 сут*
Дыхание комнатным воздухом в 36 нед. или при выписке
Дыхание комнатным воздухом на 56 день или при выписке
Потребность в кислороде менее 30% в 36 нед. или при выписке
Потребность в кислороде менее 30% на 56 день жизни или при выписке
Потребность в кислороде более 30% и/или PPV**, NCPAP*** в 36 нед. или при выписке
Потребность в кислороде более 30% и/или PPV**, NCPAP*** на 56 день жизни или при выписке
*За одни сутки лечения принимают кислородотерапию продолжительностью не менее 12 ч
** PPV (positive pressure ventilation) – вентиляция под положительным давлением
***NCPAP (nose continious positive airway pressure) – постоянное положительное давление в дыхательных путях через носовые катетеры
В соответствие с классификацией БЛД Американского торакального общества (ATS) и Российского респираторного общества, кроме тяжести заболевания, выделяются клинические формы (классическая и новая БЛД недоношенных, БЛД доношенных), которые целесообразно рассматривать как отдельные фенотипы болезни [4]. Отечественная классификация выделяет также периоды заболевания (обострение, ремиссия) и осложнения. В фазе ремиссии состояние больного определяется тяжестью течения заболевания и наличием осложнений. Фаза обострения заболевания характеризуется ухудшением состояния больного, что проявляется усилением симптомов бронхиальной обструкции, развитием острой дыхательной недостаточности, у тяжелых больных на фоне хронической, как правило, при присоединении острого респираторного заболевания, чаще всего респираторно-синцитиальной вирусной инфекции (РСВИ).
К осложнениям БЛД, согласно отечественной классификации, относятся хроническая дыхательная недостаточность, острая дыхательная недостаточность на фоне хронической, ателектаз, легочная гипертензия, легочное сердце, системная артериальная гипертензия, недостаточность кровообращения, гипотрофия.
2. Диагностика
2.1 Жалобы и анамнез
Классическая форма БЛД развивается обычно у пациентов в результате тяжелого поражения легких, требующего ИВЛ с «жесткими режимами» и высокими концентрациями кислорода. Кроме РДС, такое поражение легких у недоношенных детей может явиться результатом врожденной пневмонии/сепсиса, вызванного стрептококком группы В (Streptococcus
В отличие от детей с классической БЛД, которым требуется многодневная ИВЛ с высоким содержанием кислорода, пациенты с новой БЛД нередко в первые дни и недели жизни имеют минимальную потребность в кислороде. И только после нескольких дней или недель («медовый месяц») у этих детей начинается прогрессирующее ухудшение функции легких, которая характеризуется увеличением потребности в вентиляции и кислорода и признаков текущей дыхательной недостаточности. Следовательно, особенностью клинической картины новой БЛД также является позднее, отсроченное развитие кислорозависимости [5]. Длительная кислородозависимость у таких пациентов часто обусловлена функционирующим ОАП или инфекцией [6].
У доношенных зрелых новорожденных факторами, предрасполагающими к развитию БЛД, являются синдром аспирации мекония, сепсис, нозокомиальная пневмония, персистирующая легочная гипертензия, гипоплазия легкого, диафрагмальная грыжа, пролонгированная ИВЛ, проводимая в связи с хирургические вмешательствами.
2.2 Физикальный осмотр
Первым признаком возможного формирования БЛД является затяжное течение РДС. Клиническая картина БЛД представлена симптоматикой хронической дыхательной недостаточности у недоношенных новорожденных детей, зависимых от высоких концентраций кислорода во вдыхаемом воздухе и ИВЛ в течение более или менее продолжительного времени. Стойкая дыхательная недостаточность развивается после первичного улучшения состояния на фоне ИВЛ. При легком течении наблюдается невозможность снижения концентрации кислорода и смягчения параметров ИВЛ в течение 1-2 недель, удлинение периода выздоровления после дыхательной недостаточности; в тяжелых – на фоне ИВЛ сохраняется гипоксемия, гиперкапния, «снять» ребенка с ИВЛ не удается в течение нескольких месяцев. Реинтубации являются фактором риска тяжелого течения заболевания (1С) [2].
При объективном исследовании обычно выявляют бледные кожные покровы, с цианотичным оттенком. На фоне терапии глюкокортикостероидами возможно развитие кушингоидного синдрома. Грудная клетка эмфизематозно вздута, характерны тахипноэ до 80-100 в минуту, одышка с западением межреберных промежутков и втяжением грудины, симптом «качелей» (западение грудины при вдохе в сочетании с усиленным участием в акте дыхания мышц брюшного пресса), затрудненный удлиненный выдох. Перкуссия грудной клетки не проводится детям с ОНМТ и ЭНМТ в связи с риском интракраниальных кровоизлияний. Для аускультативной картины БЛД типичны ослабление дыхания и крепитация, отражающие развитие интерстициального отека, и появление свистящих, мелкопузырчатых хрипов при отсутствии сердечной недостаточности. К проявлениям бронхообструктивного синдрома (БОС) у недоношенных детей с БЛД относятся также эпизоды падения сатурации кислорода, клинически сопровождающиеся свистящими хрипами, ослабленным дыханием, затруднением вдоха и выдоха, ригидностью грудной клетки, падением растяжимости и увеличением резистентности дыхательных путей. У части пациентов с БЛД возможен стридор, при его развитии требуется исключить постинтубационное повреждение гортани. У ребенка, находящегося на ИВЛ, трактовка физикальных изменений в легких затруднена.
Клиническая картина новой формы БЛД характеризуется длительной кислородозависимостью и, в то же время, сравнительно редким возникновением БОС. Тогда как БЛД доношенных часто протекает с длительными, стойкими, резистентными к терапии бронхообструктивными эпизодами.
2.3 Лабораторная диагностика
Рекомендуется проведение клинического анализа крови [1,2].
(Сила рекомендации 1; уровень доказательств С)
Комментарии: у большинства больных с БЛД выявляет анемию, нейтрофилез и эозинофилию.
Рекомендовано исследование кислотно-основного состояния и мониторинг оксигенации в спокойном состояниик [1,2].
(Сила рекомендации 1; уровень доказательств С)
Комментарии: у кислородозависимых младенцев с БЛД возможны эпизоды десатурации и гипоксии при стрессе, энтеральном кормлении, чрезмерном возбуждении, бронхоспазме. Идеальным для мониторинга оксигенации является транскутанная пульсоксиметрия. Дети с высокой легочной гипертензией и длительно кислородозависимые нуждаются в пролонгированной пульсоксиметрии.
Рекомендуется контроль системного артериального давления [1,2].
(Сила рекомендации 1; уровень доказательств С)
Комментарии: рекомендуется как на стационарном этапе, так и при каждом амбулаторном визите пациента в связи с возможностью такого осложнения БЛД как системная артериальная гипертензия.
2.4 Инструментальная диагностика
Рекомендовано проведение рентгенографии грудной клетки [1,2].
(Сила рекомендации 1; уровень доказательств С)
Комментарии: рентгенография грудной клетки необходима для выявления и оценки выраженности вздутия легочной ткани, фиброзных, интерстициальных и кистозных изменений.
Рекомендовано проведение высокоразрешающей компьютерной томографии (КТ) [1,2].
(Сила рекомендации 1; уровень доказательств С)
Комментарии: КТ необходима в следующих случаях:
1) при проведении дифференциальной диагностики с другими бронхолегочными заболеваниями, например, ИЗЛ;
2) при повторных пневмотораксах;
3) при задержке клинического выздоровления и персистенции респираторных симптомов, не объяснимых тяжестью БЛД;
4) при необходимости верификации хронического заболевания легких в исходе БЛД, например, при подозрении на развитие облитерирующего бронхиолита;
5) для исключения врожденных пороков развития легких. Для объективизации данных ВРКТ-исследований в настоящее время применяется отечественная рентгенологическая шкала балльной оценки степени тяжести БЛД (табл.4) [7].
Клиника, принципы терапии и исходы бронхолегочной дисплазии
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
НИИ пульмонологии С.-Пб. ГМУ им. акад. И.П.Павлова, Детская областная клиническая больница, Санкт-Петербург
Б ронхолегочная дисплазия (БЛД) – заболевание легких, развивающееся преимущественно у недоношенных детей в периоде новорожденности, после острого эпизода дыхательных расстройств, требующих искусственной вентиляции легких (ИВЛ). БЛД формируется в результате воздействия многих факторов, среди которых наибольшее значение придается незрелости легких и ИВЛ с жесткими параметрами. Сочетанное действие высокой концентрации кислорода и положительного давления на выдохе, а также баротравма при длительной механической вентиляции играют основную роль в развитии болезни. Диагностическими критериями БЛД в периоде новорожденности являются сохраняющиеся респираторные симптомы, ИВЛ не менее 3 суток, потребность в кислородотерапии не менее 28 дней.
Морфологическое исследование при БЛД выявляет хронический бронхиолит с утолщением стенки и сужением просвета за счет перибронхиолярного склероза, гипертрофию гладкой мускулатуры мелких бронхов и бронхиол, деструкцию межальвеолярных перегородок и эмфизематозную перестройку легочной паренхимы.
В период с 1992 по 2000 г.г. с диагнозом БЛД наблюдались 96 детей в возрасте от 1 месяца до 7 лет. Дети рождались в тяжелом и крайне тяжелом состоянии с признаками дистресс-синдрома новорожденных, что требовало применения ИВЛ длительностью от нескольких дней до нескольких месяцев. В периоде новорожденности отмечались тахипноэ, цианоз, кислородозависимость в течение 28 дней и более, стойкие физикальные изменения в легких (ослабление дыхания, затруднение выдоха, сухие свистящие хрипы, влажные мелкопузырчатые хрипы и крепитация). В раннем периоде у детей на рентгенограммах определялись признаки болезни гиалиновых мембран («воздушная» бронхограмма, ателектазы и дистелектазы на фоне интерстициального отека), симптомы утечки воздуха (интерстициальная эмфизема, пневмомедиастинум, пневмоторакс).
Наблюдение за детьми позволило выявить легкое, тяжелое и среднетяжелое течение болезни. Легкое течение характеризовалось отсутствием тахипноэ в покое и аускультативных изменений в легких, которые обычно появлялись при присоединении вирусной инфекции. Не отмечалось отставания в физическом развитии и признаков легочного сердца. Рентгенологическое исследование грудной клетки выявляло умеренные признаки вздутия. При среднетяжелом течении тахипноэ появлялось при физической нагрузке (плач, беспокойство, кормление), симптомы обструкции были выражены умеренно и нарастали при вирусной инфекции. Инструментальное исследование у части больных обнаруживало признаки легочного сердца. При рентгенографии грудной клетки отмечались вздутие легочной ткани, участки локального пневмосклероза, у отдельных больных – кардиомегалия. Дети с тяжелым течением БЛД имели тахипноэ в покое, усиливающееся при физической нагрузке и вирусной инфекции. Больные значительно отставали в физическом развитии, имелись выраженные аускультативные симптомы обструкции. Эхокардиография выявляла признаки легочного сердца (легочную гипертензию, дилатацию и гипертрофию правого желудочка). При рентгенологическом исследовании наблюдалось значительное вздутие, буллы, множественные участки пневмосклероза, гиповентиляции, перибронхиальные изменения, кардиомегалия, выбухание ствола легочной артерии.
Обычно течение БЛД волнообразное. При наслоении респираторной вирусной инфекции значительно нарастала дыхательная недостаточность, и в ряде случаев требовалась интенсивная терапия или даже реанимационное пособие.
Характер воспаления слизистой дыхательных путей изучали с помощью цитоморфологического исследования бронхиальных смывов. Воспалительные изменения слизистой бронхов характеризовались повышением числа нейтрофилов и лимфоцитов, выявлением пластов дедифференцированного метаплазированного эпителия, что свидетельствовало о длительно сохраняющемся повреждении эпителиального слоя слизистой оболочки бронхов. Выраженность этих изменений коррелировала с тяжестью течения заболевания.
Лечение БЛД включало проведение оксигенотерапии для поддержания сатурации кислорода в пределах 94–96%, назначение стероидных препаратов с целью ликвидации воспалительных изменений в слизистой оболочке дыхательных путей и бронхолитических препаратов, а также витаминов А и Е. В ряде случаев возникала необходимость в применении мочегонных средств. Успех лечения больных зависит также от адекватного энергетического обеспечения, которое достигалось увеличением калорийности пищи в 1,5–2 раза и дотацией белка до 3–3,5 г на 1 кг веса ребенка.
Клинические симптомы бронхиальной обструкции, обусловленные гиперреактивностью и воспалительными изменениями слизистой оболочки, диктуют необходимость назначения стероидных препаратов. При БЛД предпочтение отдавалось ингаляционным стероидам в виде дозированных аэрозолей или жидких форм, которые доставлялись в дыхательные пути при помощи специального спейсера с маской (аэрочамбер или бебихалер) или небулайзера. Начинали с низких доз, которые повышали до минимально эффективной, терапию продолжали до стойкого клинического и рентгенологического улучшения (от 1 месяца до 2,5 лет). Ухудшение состояния требовало удвоения дозы на 2–3 недели. При достижении клинико–лабораторной ремиссии базисную терапию ингаляционными стероидами постепенно отменяли.
Ингаляционные бронходилататоры высокооэффективны при БЛД, что определяется гипертрофией гладкой мускулатуры бронхов, отмечаемой при морфологических исследованиях. Использовались адреномиметики (сальбутамол) и холинолитики (атровент), а также комбинированные формы (беродуал) в виде дозированных ингаляторов через спейсер или жидких форм через небулайзер, в возрастных дозировках сроком от 10 дней до 3 месяцев, обычно совместно с ингаляционными стероидами.
Важным моментом для благоприятного исхода болезни является сотрудничество врача и родителей больного, которые должны знать, что следует делать регулярно, а что – во время ухудшения состояния при наслоении респираторной инфекции. Кроме того, необходимо постоянное мониторирование состояния больного ребенка с целью коррекции лечебных мероприятий (родители должны вести дневник состояния ребенка, отмечать частоту дыхания и частоту сердечных сокращений во сне, а также до и после приема лекарств).
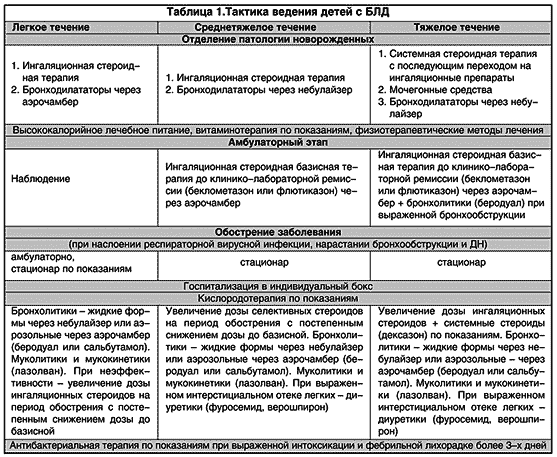
Исходя из того, что наиболее тяжелое состояние у больных с БЛД отмечается на фоне вирусной инфекции, родителям рекомендовалось соблюдение строгого охранительного режима для ребенка; при угрозе инфицирования с профилактической целью назначался интерферон интраназально. Если инфицирования избежать не удавалось, то дозировка базисных препаратов (ингаляционных стероидов) и симптоматических средств изменялась с учетом индивидуальных особенностей ребенка и характера заболевания. При длительном обострении (более 7 дней) с фебрильной температурой более 3 дней, нарастающими катаральными симптомами и дыхательной недостаточностью проводилась антибактериальная терапия коротким курсом (7–10 дней) с учетом выделенной микрофлоры. Тактика ведения больных с БЛД на разных этапах наблюдения и при разной степени тяжести представлена в табл. 1.
Длительное динамическое наблюдение (в течение 2–5 лет) 83 больных БЛД позволило уточнить прогноз этого состояния в раннем детском возрасте. Стратегия этапного наблюдения и противовоспалительная терапия использовались у 76 детей из 83. Дети со среднетяжелой формой болезни (51 ребенок), получавшие противовоспалительную терапию, не нуждались в госпитализации по поводу обострений заболевания (до назначения терапии требовалась госпитализация 2–3 раза в месяц), и к 3 годам у них удалось добиться клинического выздоровления. Однако при этом сохранялись рентгенологические изменения в виде умеренного вздутия и интерстициальной реакции. Дети, имеющие тяжелую форму болезни (25 больных), также получали противовоспалительную терапию, однако клинического выздоровления удалось добиться у 18 больных (73%), 5 детей (23%) умерли в течение первых 1,5 лет жизни, у 1 ребенка (4%) сформировался хронический бронхиолит. Часть больных с БЛД (7 детей из 83) не получали базисную терапию, так как наблюдались в различных лечебных учреждениях с ошибочным диагнозом «рецидивирующая пневмония с обструктивным синдромом». Из них 1 ребенок умер (14%), а у 6 больных (84%) сформировалась тяжелая форма хронического бронхиолита, что послужило основанием для назначения инвалидности.