Сравнение эффективности биологической терапии у пациентов с псориазом
Актуальность
В последние годы проводится все больше и больше исследований, посвященных изучению биологической терапии у больных псориазом.
Одним из потенциальных препаратов для лечения псориаза является мирикизумаб (блокатор p19 субъединицы интерлейкина-23).
Его эффективность и безопасность в сравнении с плацебо и сецикинумабом (анти-интерлейкин-17) изучались в исследовании OASIS-2.
Методы
В мультицентровое рандомизированное клиническое исследование включили 1465 пациентов с умеренным или тяжелым псориазом.
Пациентов рандомизировали в одну из 4 групп: мирикизумаб 250 мг подкожно каждые 4 недели с последующим переходом на 250 мг препарата каждые 8 недель, начиная с 16 недели. Вторая группа получала мирикизумаб 250 мг каждые 4 недели с переходом на 135 мг каждые 8 недель с 16 недели. Третья группа получала сецикинумаб 300 мг еженедельно на протяжении 4 недель и затем каждые 4 недели начиняя с 4 недели. Четвертая группа получала плацебо каждые 4 недели и затем мирикизумаб 250 мг каждые 4 недели с 16 по 32 неделю и затем 1 раз в 8 недель.
В качестве первичных конечных точек выбрил выбраны: процент пациентов, достигших показателя Physician’s Global Assessment (sPGA) 0 или 1 с улучшением как минимум на 2 балла, по сравнению с исходным показателем, и доля пациентов с PASI 90 на 16 неделе, по сравнению с плацебо.
Основными вторичными конечными точками были выбраны: PASI 75 и PASI 100, по сравнению с плацебо на 16 неделе; sPGA 0 или 1 и PASI 90 non-inferiority, по сравнению с сецукинумабом на 16 неделе; sPGA 0 или 1, PASI 90 и PASI 100 superiority, по сравнению с сецукинумабом на 52 неделе.
Результаты
Генно-инженерная биологическая терапия
Что такое современная биологическая терапия псориаза?
Наша иммунная система защищает организм от инфекций и раковых клеток. Но иногда из-за генетических изменений, под воздействием стресса, инфекции или травмы происходит сбой. В результате отдельные компоненты иммунной системы сохраняют активность, даже когда организму ничего не угрожает. Так развивается хроническое воспаление.
В случае с псориазом это воспаление протекает главным образом в коже, суставах, кровеносных сосудах. Все генно-инженерные биологические препараты вводятся подкожно с помощью шприцев или автоинжекторов, в поддерживающем режиме по определенной схеме.
Роль цитокинов в развитии псориаза
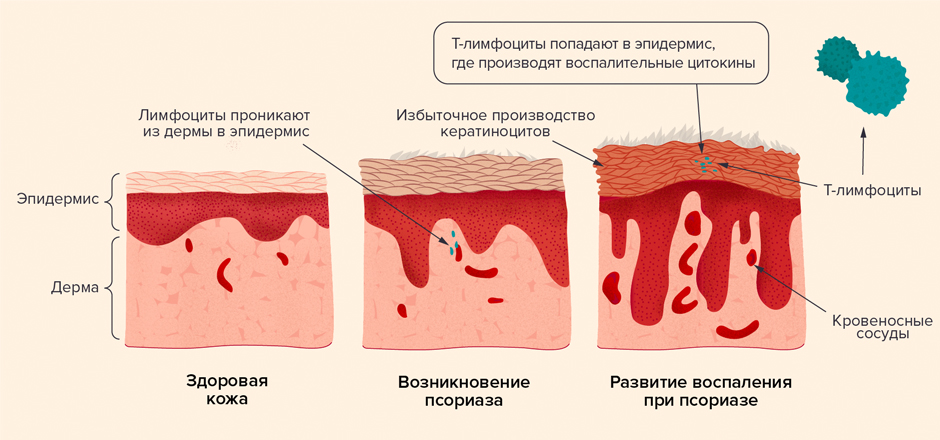
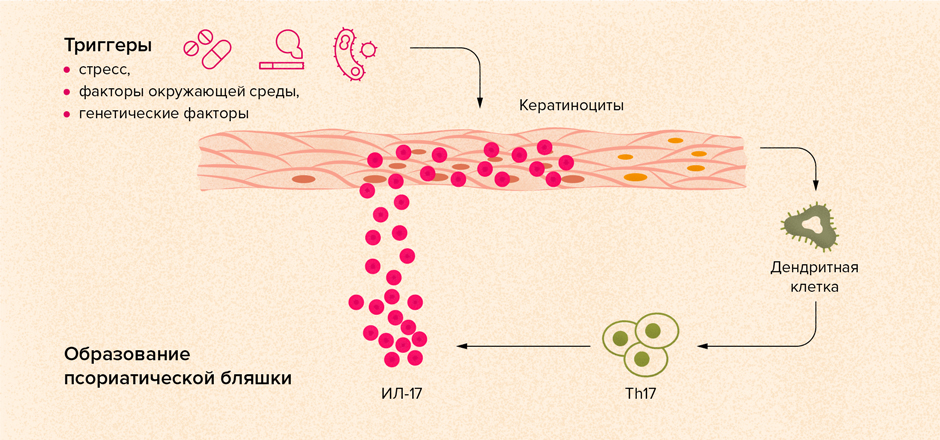
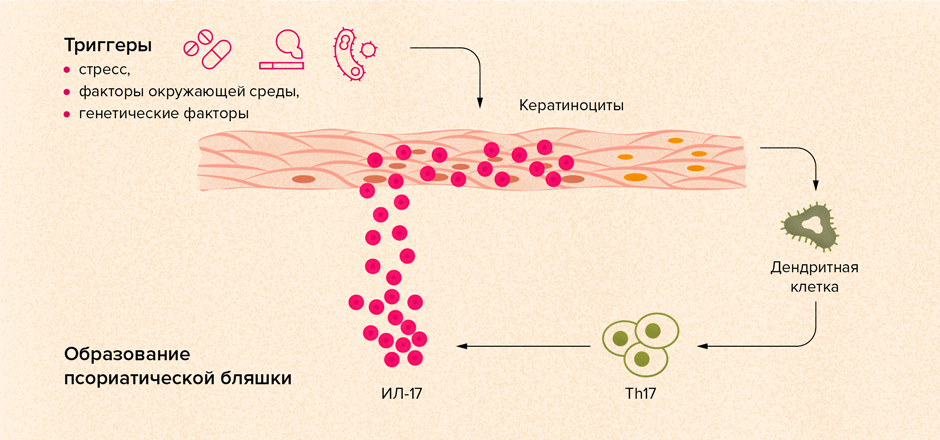
Ведущую роль в развитии псориаза играют различные клетки иммунной системы. Они вырабатывают небольшие молекулы — провоспалительные цитокины. Именно эти молекулы — основные стимуляторы воспаления. В развитии псориаза участвуют такие цитокины, как фактор некроза опухоли (ФНО), интерлейкины (ИЛ)-1, 6, 12, 17, 23, интерфероны [1].
Эти молекулы заставляют клетки иммунной системы расти, делиться, переходить в активное состояние, скапливаться в месте воспаления, а также вырабатывать все новые и новые цитокины. Чтобы остановить действие цитокинов, в норме иммунная система вырабатывает регуляторные Т-клетки [2]. Однако у людей с псориазом этих клеток образуется мало, поэтому ничто не мешает воспалению развиваться, вызывать все более тяжелые изменения и поражать другие органы и системы.
Системная терапия для лечения псориаза
Поскольку псориаз развивается по вине гиперактивной иммунной системы, которая поражает различные органы и системы, для лечения среднетяжелых и тяжелых форм псориаза применяют системную терапию. Как правило, применяется 2 вида системной терапии:
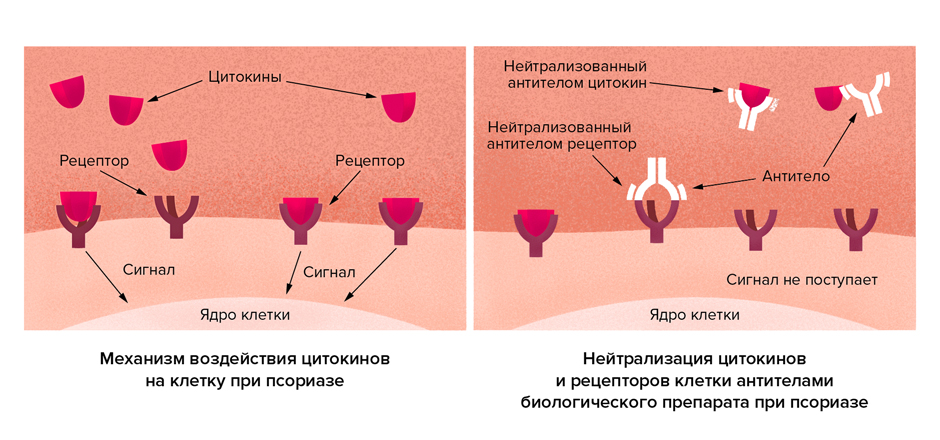
Основное отличие ГИБП от системных иммуносупрессоров в том, что биологическая терапия действует узконаправленно на определенное звено воспаления. Системные иммуносупрессоры, в свою очередь, разрушают иммунные клетки неразборчиво, а значит, влияют на всю защитную систему организма.
ГИБП состоят из антител — специфических избирательных белков, которые реагируют лишь на одну определенную мишень. Они очень прочно связываются со своей мишенью и блокируют ее активность.
Комментарий врача. Достижение фармакотерапии: биологические препараты, фото результатов
Благодаря высокой избирательности ГИБП и способности к формированию прочной связи с вредоносными агентами, выраженный терапевтический эффект развивается быстро.
Так, клинические исследования показали, что при применении блокаторов ИЛ-17 уже через 12 недель терапии у 65–85% пациентов на 75% снижается тяжесть и распространенность псориатических поражений, а у трети пациентов кожа полностью очищается [3–6]. Такой эффект сохраняется при регулярном приеме лечения согласно зарегистрированным показаниям. Подобные результаты считались практически недостижимыми до появления современных биологических препаратов.
Согласно действующим в Российской Федерации клиническим рекомендациям [7], ГИБП применяются:
При блокировке ИЛ-17 очень быстро формируется выраженный эффект. Ослабевают все проявления псориаза, при этом клетки иммунной системы остаются неповрежденными и продолжают выполнять большинство своих защитных функций.
Согласно действующим в Российской Федерации клиническим рекомендациям, ГИБП применяются:
Врач-дерматолог Бакулев А.Л. отвечает на важные вопросы о генно-инженерной биологической терапии
Виды ГИБП для лечения псориаза
Согласно зарегистрированным показателям, для терапии псориаза применяются биологические препараты, блокирующие 3 группы цитокинов:
Ингибитор интерлейкина-17
Относительно недавно была доказана ведущая роль Т-лимфоцитов 17-го типа в развитии и прогрессировании псориаза [8,9]. Они вырабатывают ключевой для псориаза провоспалительный цитокин — интерлейкин-17 (ИЛ-17).
ИЛ-17 передает сигнал различным типам клеток. Одни начинают активно делиться и расти. Другие включаются в процессы воспаления. Так, под влиянием ИЛ-17 в суставах развивается хроническое воспаление. Костная ткань разрушается, могут даже формироваться костные разрастания. В стенках кровеносных сосудов ИЛ-17 участвует в формировании атеросклеротических изменений: в сосудах образуются «бляшки», которые нарушают кровоток, из-за чего органы могут не получать достаточное количество крови. Все это ведет к нарушению функции органов [10]. В коже и в тканях суставов пациентов с псориазом обнаруживается большое количество клеток, которые синтезируют ИЛ-17, поэтому воздействие на этот цитокин рассматривается исследователями как очень перспективное направление в лечении многих ревматоидных и иммуновоспалительных заболеваний [8].
Ингибитор ИЛ-17 воздействует на основной цитокин, вызывающий воспаление при псориазе, — ИЛ-17. Благодаря его блокировке формируется устойчивый терапевтический ответ. Блокада ИЛ-17 не несет в себе тех рисков, которые появляются при блокаде ФНО или ИЛ-12/23 [11], таких как увеличение частоты онкологических заболеваний и лимфом. Наиболее частыми для ИЛ-17 являются инфекции дыхательных путей и нейтропения (снижение числа определенного вида иммунных клеток), но риска развития новообразований, лимфом, хронической сердечной недостаточности при применении ингибиторов ИЛ-17 на текущий момент не выявлено.
Ингибитор интерлейкина-12/23
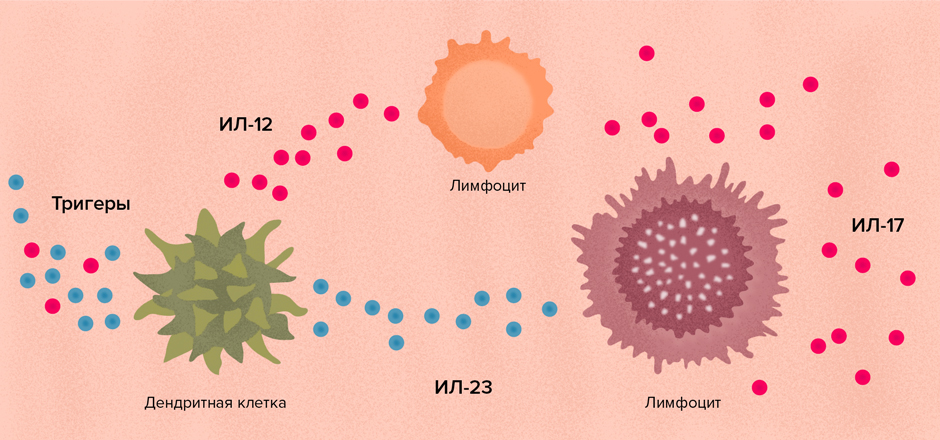
Ингибитор ИЛ-12/23 возник благодаря последующим исследованиям механизма развития псориаза [12]. Ученые обнаружили, что ИЛ-12 и ИЛ-23 не влияют непосредственно на клетки кожи, однако активируют Т-клетки 1-го или 17-го типов. Эти клетки вызывают выраженный воспалительный процесс в коже. Блокада ИЛ-12 и ИЛ-23 также широко применяется в терапии псориаза, но терапевтический эффект может развиваться чуть дольше, чем при применении других биологических препаратов.
Ингибиторы фактора некроза опухоли
Первыми для лечения пациентов с псориазом стали использоваться ингибиторы ФНО. ФНО — очень мощный провоспалительный цитокин. При псориазе ФНО активизирует иммунные клетки, но не оказывает прямого влияния на клетки кожи [13].
Для препаратов этого класса впервые было отмечено такое явление, как ускользание эффекта: эффективность терапии снижалась спустя некоторое время (1-2 года) [14].
Блокада ФНО при помощи биологической терапии широко применяется при псориазе и дает терапевтический эффект. Однако ингибиторы ФНО могут вызвать повышенную восприимчивость организма к инфекционным заболеваниям, включая туберкулез, а также увеличение риска развития ряда онкологических заболеваний — новообразований и лимфом [13].
Обострения псориаза зачастую возникают без видимой на то причины, поэтому так важна адекватная, своевременная и наиболее эффективная терапия. Основной целью лечения является как можно более длительная ремиссия пациента, а также повышение качества его жизни. Все это позволяет обеспечить современная биологическая терапия, которая показала свою эффективность в лечении псориаза. Биологические препараты относительно безопасны, однако их применение требует постоянного наблюдения со стороны специалиста во избежание проявления нежелательных реакций.
Изоляция —
не выход
Смотрите истории людей, преодолевающих псориаз, в нашем спецпроекте.
Безопасность биологических препаратов у пациентов с псориазом и псориатическим артритом: анализ данных регистров пациентов
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Цель: изучение безопасности различных биологических препаратов, применяемых для лечения пациентов с псориазом и псориатическим артритом (ПА) в реальной клинической практике (по данным регистров пациентов).
Материал и методы: проводился систематический поиск публикаций с использованием базы данных PubMed. Для анализа отобраны 17 оригинальных статей, содержащих данные по безопасности/выживаемости биологической терапии из 9 регистров пациентов с псориазом/ПА.
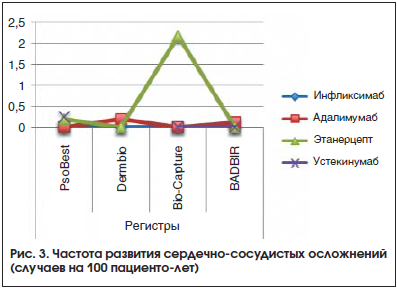
Результаты: в регистре PSOLAR частота возникновения серьезных инфекционных осложнений составила 2,49 случая на 100 пациенто-лет для инфликсимаба, 1,97 – для адалимумаба, 1,47 – для этанерцепта, 0,83 – для устекинумаба. В регистре PsoBest частота инфекций на 100 пациенто-лет была следующей: для инфликсимаба – 1,3, для адалимумаба – 0,52, для этанерцепта – 1,0, для устекинумаба – 0,5. Отмечена следующая частота малигнизации: для инфликсимаба – 0 на 100 пациенто-лет, для адалимумаба – 0,5, для этанерцепта – 0,2, для устекинумаба – 0,7. Частота осложнений на 100 пациенто-лет, представленная в регистре Bio-Сapture, составила: инфекционные осложнения – 0,93 на фоне терапии этанерцептом, сердечно-сосудистые осложнения – 2,18 для этанерцепта, частота малигнизаций – 2,81 для группы этанерцепта и 1,8 для группы адалимумаба. По данным регистра BADBIR, количество инфекционных осложнений на 100 пациенто-лет составило 2,6 для инфликсимаба, 1,02 – для адалимумаба, 0,1 – для этанерцепта, 1,1 – для устекинумаба; сердечно-сосудистые осложнения на 100 пациенто-лет – 0,12 для адалимумаба; частота малигнизации – 0,16 для адалимумаба, 0,2 – для этанерцепта, 0,18 – для устекинумаба. В регистре Biobadaderm частота развития туберкулеза на 100 пациенто-лет составила 0,6 для инфликсимаба, 0,27 – для адалимумаба. По данным регистра Dermbio, наибольшая длительность терапии была характерна для инфликсимаба, в регистре BADBIR наибольшей выживаемостью среди впервые назначенных генно-инженерных биологически препаратов (ГИБП) обладал устекинумаб.
Выводы: регистры пациентов обладают большими возможностями в изучении всех аспектов назначения биологической терапии, в т. ч. в выявлении рисков и осложнений терапии в реальной клинической практике. Вместе с тем разнородность данных не позволяет проводить прямые сравнения безопасности отдельных препаратов. Для оценки профиля безопасности отдельных ГИБП необходимо оценивать всю совокупность имеющихся данных.
Ключевые слова: псориаз, псориатический артрит, регистры пациентов, биологические препараты, безопасность, нежелательные явления.
Для цитирования: Лыткина К.А., Зянгиров Р.Р. Безопасность биологических препаратов у пациентов с псориазом и псориатическим артритом: анализ данных регистров пациентов. РМЖ. 2016;22:1511-1516.
Ключевые слова: псориаз, псориатический артрит, регистры пациентов, биологические препараты, безопасность, нежелательные явления.ns. Patient registries provide valuable information on the safety profile and other aspects of biological therapy in a real-world clinical settings. However, the comparability of the data from different registries is limited due to their heterogeneity. Comprehensive analysis of all available data should be performed to assess the safety profile of biologic preparations.
Key words: psoriasis, psoriatic arthritis, patient registries, biologics, safety, adverse events.
For citation: Lytkina K.A.1, Zyangirov R.R.2 Safety of biological preparations in psoriasis and psoriatic arthritis: data analysis from patient registries // RMJ. 2016. № 22. P. 1511–1516.
Освещена безопасность биологических препаратов у пациентов с псориазом и псориатическим артритом
Введение
Материал и методы
Результаты
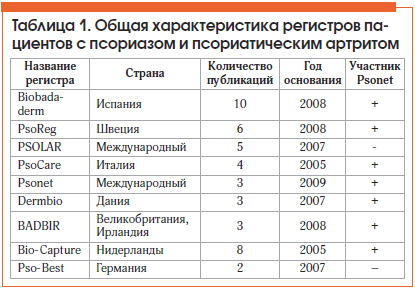
Общая характеристика отобранных для анализа регистров пациентов представлена в таблице 1. Большинство регистров содержит данные о пациентах, проживающих в странах Европы. Исключение составляет PSOLAR – международный регистр, который начинался в США, а в настоящий момент объединяет 12 стран Американского континента и Европы. Кроме того, сетевой регистр Psonet аккумулирует данные из различных национальных регистров (в основном из стран Западной Европы, а также Австралии и Израиля). Часть регистров посвящена анализу побочных эффектов проводимой терапии, другая часть направлена на изучение выживаемости отдельных видов генно-инженерной терапии и связи выживаемости терапии с ее безопасностью [5].
В публикациях по 8 регистрам содержатся данные о побочных эффектах ГИБП с частотой их встречаемости на 100 пациенто-лет (или возможностью расчета этой величины), публикации по регистру PsoReg носят описательный характер.
В таблице 2 суммированы данные по частоте серьезных НЯ из различных регистров.
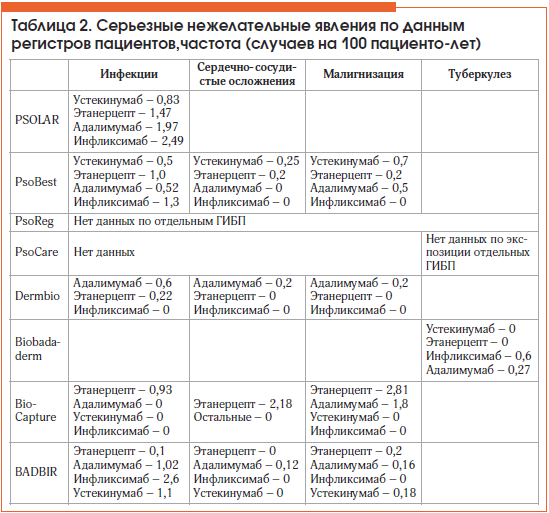
Серьезные инфекции
Туберкулез
Малигнизация
Данные о частоте развития злокачественных опухолей у пациентов, получавших ГИБП, представлены на рисунке 2.
В регистре ProBest [8] общая доля малигнизации (исключая немеланомный рак кожи) составила 0,46 на 100 пациенто-лет в группе традиционной системной терапии и 0,49 на 100 пациенто-лет в группе ГИБП (р>0,05, разница статистически незначима). Статистически значимой разницы между различными препаратами (устекинумаб, этанерцепт, адалимумаб и инфликсимаб) в риске малигнизации (исключая немеланомный рак кожи), а также в риске возникновения немеланомного рака кожи или меланомы кожи, выявлено не было (табл. 2).
По данным регистра Bio-Сapture [9], у 9 пациентов наблюдалось 11 случаев малигнизации. У 48-летнего пациента во время терапии этанерцептом трижды зарегистрированы случаи развития злокачественных новообразований, а именно плоскоклеточного рака кожи и карциномы пищевода. У другого пациента развились 2 случая базальноклеточного рака кожи и 1 случай плоскоклеточного рака кожи в течение 6 мес. после начала терапии этанерцептом. У 66-летней женщины, получавшей терапию этанерцептом, был диагностирован рак молочной железы. Рак толстой кишки с метастазированием был выявлен у 76–летнего пациента, получавшего этанерцепт. Частота развития опухолей на фоне терапии отдельными ГИБП составила: 2,81 случая на 100 пациенто-лет для этанерцепта и 1,8 случая на 100 пациенто-лет для адалимумаба. У пациентов, получавших устекинумаб и инфликсимаб, случаев малигнизации не выявлено (табл. 2).
В регистре Dermbio описан 1 случай рака яичников у пациентки, получавшей адалимумаб (0,2 случая на 100 пациенто-лет) [12].
По данным регистра BADBIR, частота малигнизации на фоне терапии этанерцептом составила 0,2 на 100 пациенто-лет, на фоне терапии устекинумабом – 0,18 на 100 пациенто-лет, в группе адалимумаба – 0,16 на 100 пациенто-лет. Статистически значимых различий в частоте встречаемости малигнизации на фоне перечисленных препаратов не выявлено. В группе инфликсимаба случаев малигнизации не отмечено [13].
Сердечно-сосудистые осложнения
Выживаемость терапии ГИБП
Длительность проводимой различными препаратами терапии проанализирована в регистрах Dermbio и BADBIR.
В регистре Dermbio основными причинами прекращения терапии явились потеря эффекта (75%) и побочные эффекты (12%). Наилучшую выживаемость среди ингибиторов ФНО-альфа показал инфликсимаб – через 4 года его приема 70% пациентов остаются на данной терапии [12].
По данным регистра BADBIR, выживаемость биологической терапии первым ГИБП через 1 год составляла 77%, а к концу 3-го года терапии падала до 53%. Предикторами прекращения терапии ГИБП явились женский возраст, текущий статус курильщика, терапия этанерцептом или инфликсимабом. В противовес этому, наличие ПА или терапия устекинумабом явились предикторами длительности проводимой терапии. Прекращало терапию из-за развития побочных эффектов примерно одинаковое количество пациентов во всех 4-х группах ГИБП. Устекинумаб, назначенный в качестве первого ГИБП, продемонстрировал наибольшую выживаемость терапии у пациентов с псориазом [13].
Генно-инженерная биологическая терапия
Что такое современная биологическая терапия псориаза?
Наша иммунная система защищает организм от инфекций и раковых клеток. Но иногда из-за генетических изменений, под воздействием стресса, инфекции или травмы происходит сбой. В результате отдельные компоненты иммунной системы сохраняют активность, даже когда организму ничего не угрожает. Так развивается хроническое воспаление.
В случае с псориазом это воспаление протекает главным образом в коже, суставах, кровеносных сосудах. Все генно-инженерные биологические препараты вводятся подкожно с помощью шприцев или автоинжекторов, в поддерживающем режиме по определенной схеме.
Роль цитокинов в развитии псориаза
Ведущую роль в развитии псориаза играют различные клетки иммунной системы. Они вырабатывают небольшие молекулы — провоспалительные цитокины. Именно эти молекулы — основные стимуляторы воспаления. В развитии псориаза участвуют такие цитокины, как фактор некроза опухоли (ФНО), интерлейкины (ИЛ)-1, 6, 12, 17, 23, интерфероны [1].
Эти молекулы заставляют клетки иммунной системы расти, делиться, переходить в активное состояние, скапливаться в месте воспаления, а также вырабатывать все новые и новые цитокины. Чтобы остановить действие цитокинов, в норме иммунная система вырабатывает регуляторные Т-клетки [2]. Однако у людей с псориазом этих клеток образуется мало, поэтому ничто не мешает воспалению развиваться, вызывать все более тяжелые изменения и поражать другие органы и системы.
Системная терапия для лечения псориаза
Поскольку псориаз развивается по вине гиперактивной иммунной системы, которая поражает различные органы и системы, для лечения среднетяжелых и тяжелых форм псориаза применяют системную терапию. Как правило, применяется 2 вида системной терапии:
Основное отличие ГИБП от системных иммуносупрессоров в том, что биологическая терапия действует узконаправленно на определенное звено воспаления. Системные иммуносупрессоры, в свою очередь, разрушают иммунные клетки неразборчиво, а значит, влияют на всю защитную систему организма.
ГИБП состоят из антител — специфических избирательных белков, которые реагируют лишь на одну определенную мишень. Они очень прочно связываются со своей мишенью и блокируют ее активность.
Комментарий врача. Достижение фармакотерапии: биологические препараты, фото результатов
Благодаря высокой избирательности ГИБП и способности к формированию прочной связи с вредоносными агентами, выраженный терапевтический эффект развивается быстро.
Так, клинические исследования показали, что при применении блокаторов ИЛ-17 уже через 12 недель терапии у 65–85% пациентов на 75% снижается тяжесть и распространенность псориатических поражений, а у трети пациентов кожа полностью очищается [3–6]. Такой эффект сохраняется при регулярном приеме лечения согласно зарегистрированным показаниям. Подобные результаты считались практически недостижимыми до появления современных биологических препаратов.
Согласно действующим в Российской Федерации клиническим рекомендациям [7], ГИБП применяются:
При блокировке ИЛ-17 очень быстро формируется выраженный эффект. Ослабевают все проявления псориаза, при этом клетки иммунной системы остаются неповрежденными и продолжают выполнять большинство своих защитных функций.
Согласно действующим в Российской Федерации клиническим рекомендациям, ГИБП применяются:
Врач-дерматолог Бакулев А.Л. отвечает на важные вопросы о генно-инженерной биологической терапии
Виды ГИБП для лечения псориаза
Согласно зарегистрированным показателям, для терапии псориаза применяются биологические препараты, блокирующие 3 группы цитокинов:
Ингибитор интерлейкина-17
Относительно недавно была доказана ведущая роль Т-лимфоцитов 17-го типа в развитии и прогрессировании псориаза [8,9]. Они вырабатывают ключевой для псориаза провоспалительный цитокин — интерлейкин-17 (ИЛ-17).
ИЛ-17 передает сигнал различным типам клеток. Одни начинают активно делиться и расти. Другие включаются в процессы воспаления. Так, под влиянием ИЛ-17 в суставах развивается хроническое воспаление. Костная ткань разрушается, могут даже формироваться костные разрастания. В стенках кровеносных сосудов ИЛ-17 участвует в формировании атеросклеротических изменений: в сосудах образуются «бляшки», которые нарушают кровоток, из-за чего органы могут не получать достаточное количество крови. Все это ведет к нарушению функции органов [10]. В коже и в тканях суставов пациентов с псориазом обнаруживается большое количество клеток, которые синтезируют ИЛ-17, поэтому воздействие на этот цитокин рассматривается исследователями как очень перспективное направление в лечении многих ревматоидных и иммуновоспалительных заболеваний [8].
Ингибитор ИЛ-17 воздействует на основной цитокин, вызывающий воспаление при псориазе, — ИЛ-17. Благодаря его блокировке формируется устойчивый терапевтический ответ. Блокада ИЛ-17 не несет в себе тех рисков, которые появляются при блокаде ФНО или ИЛ-12/23 [11], таких как увеличение частоты онкологических заболеваний и лимфом. Наиболее частыми для ИЛ-17 являются инфекции дыхательных путей и нейтропения (снижение числа определенного вида иммунных клеток), но риска развития новообразований, лимфом, хронической сердечной недостаточности при применении ингибиторов ИЛ-17 на текущий момент не выявлено.
Ингибитор интерлейкина-12/23
Ингибитор ИЛ-12/23 возник благодаря последующим исследованиям механизма развития псориаза [12]. Ученые обнаружили, что ИЛ-12 и ИЛ-23 не влияют непосредственно на клетки кожи, однако активируют Т-клетки 1-го или 17-го типов. Эти клетки вызывают выраженный воспалительный процесс в коже. Блокада ИЛ-12 и ИЛ-23 также широко применяется в терапии псориаза, но терапевтический эффект может развиваться чуть дольше, чем при применении других биологических препаратов.
Ингибиторы фактора некроза опухоли
Первыми для лечения пациентов с псориазом стали использоваться ингибиторы ФНО. ФНО — очень мощный провоспалительный цитокин. При псориазе ФНО активизирует иммунные клетки, но не оказывает прямого влияния на клетки кожи [13].
Для препаратов этого класса впервые было отмечено такое явление, как ускользание эффекта: эффективность терапии снижалась спустя некоторое время (1-2 года) [14].
Блокада ФНО при помощи биологической терапии широко применяется при псориазе и дает терапевтический эффект. Однако ингибиторы ФНО могут вызвать повышенную восприимчивость организма к инфекционным заболеваниям, включая туберкулез, а также увеличение риска развития ряда онкологических заболеваний — новообразований и лимфом [13].
Обострения псориаза зачастую возникают без видимой на то причины, поэтому так важна адекватная, своевременная и наиболее эффективная терапия. Основной целью лечения является как можно более длительная ремиссия пациента, а также повышение качества его жизни. Все это позволяет обеспечить современная биологическая терапия, которая показала свою эффективность в лечении псориаза. Биологические препараты относительно безопасны, однако их применение требует постоянного наблюдения со стороны специалиста во избежание проявления нежелательных реакций.
Изоляция —
не выход
Смотрите истории людей, преодолевающих псориаз, в нашем спецпроекте.