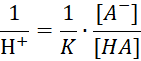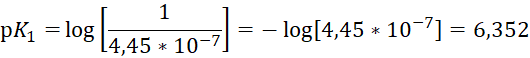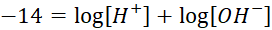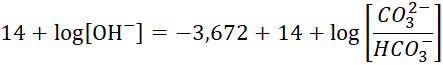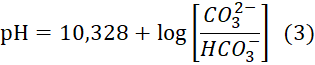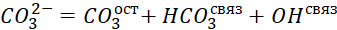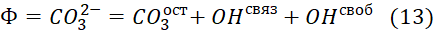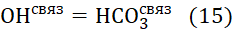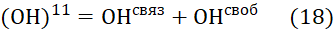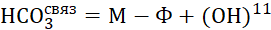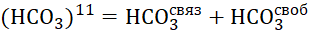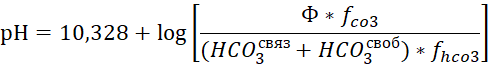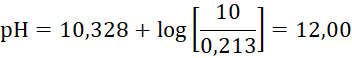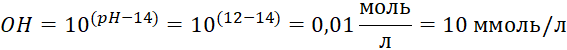Бикарбонаты в воде что это

Ремонт кулеров в Тамбове
Мы работаем для Вас в обычном режиме. Сделать заказ Вы можете по телефонам на сайте.
Бикарбонаты
Бикарбонаты – это соли угольной кислоты. Содержание бикарбонатов является важнейшим параметром для питьевой воды. Бикарбонаты попадают в воду из углекислого газа атмосферы и почвы. Также бикарбонаты образуются
в ходе растворения карбонатных пород. Измеряется содержание бикарбоната в количестве миллиграммов на один литр воды.
Бикарбонаты очень часто еще называют гидрокарбонатами, так как они хорошо растворяются в воде.
Если говорят про бикарбонаты в воде, то, как правило, подразумевается бикарбонат натрия (NaHCO3). Это вещество еще также часто называют пищевой или питьевой содой.
Бикарбонат натрия оказывает весьма позитивное воздействие на человеческий организм. Это вещество благотворно влияет на почки, способствует скорейшему выведению камней, обладает антисептическими свойствами, позволяет обеспечить должный уход за ротовой полостью. Однако повышенное содержание бикарбоната натрия может привести к обратному эффекту.
Также в воде содержатся бикарбонаты калия и магния, которые влияют на временную жесткость воды. Поэтому к концентрации карбонатов в питьевой воде выдвигаются повышенные требования. Нормой считается, если содержание гидрокарбонатов в питьевой воде не превышает 400 миллиграмм на литр.
Гидрокарбонаты в питьевой воде
Гидрокарбонаты в питьевой воде – это компоненты, определяющие ее щелочность. Их содержание в воде объясняется несколькими процессами:
Гидрокарбонаты в питьевой воде уменьшают количество водородных ионов, приводят к уменьшению кислотности и повышению щелочности. Благодаря высокой концентрации гидрокарбонатов некоторые минеральные воды могут использоваться для лечения гастритов и повышенной кислотности желудочного сока. В умеренных концентрациях гидрокарбонат-ионы необходимы качественной питьевой воде для поддержания нормальной щелочности, оптимального значения рН и приемлемых органолептических характеристик.
Зачем насыщать воду гидрокарбонатами
Гидрокарбонаты в воде нужны для того, чтобы корректировать водородный показатель pH воды и улучшить ее вкусовые свойства. Если щелочность низкая, уровень pH будет нестабилен вследствие низкой буферной емкости такой воды. Низкая (практически нулевая) щелочность и пониженные уровни рН характерны, в частности, для воды после очистки обратным осмосом.
Гидрокарбонаты в воде (природной) – это прежде всего соли кальция и магния (гидрокарбонаты этих элементов существуют только в растворенном состоянии). При нагреве и кипячении растворенные гидрокарбонаты элементов жесткости частично перейдут в нерастворимые карбонаты, и вода станет мягче.
При необходимости (например, после обратного осмоса) гидрокарбонаты в воде можно повысить, используя специально разработанные для этого модификации минеральной добавки «Северянка Бикарбонат». Помимо повышения щелочности питьевой воды и коррекции рН, эта добавка улучшает её вкусовые качества.
Полезные качества и показания к применению гидрокарбонатной минеральной воды
Каждый хоть раз сталкивался с симптомами гастрита или другими проблемами пищеварения. Для облегчения этих состояний приходится пить дорогостоящие препараты.
Но ведь легче предотвратить появление недуга. Гидрокарбонатная минеральная вода – альтернатива для профилактики и лечения отклонений в работе ЖКТ.
Что это за минералка?

Такие воды являются родниковыми, они обогащаются минеральными соединениями благодаря омовению и частичному растворению ископаемых, находящихся под землей.
Классификация
Прежде, чем отправиться в магазин, надо ознакомиться с разнообразием щелочных вод и разобраться в их отличиях.
Гидрокарбонатные воды делят по следующим признакам:
| Вид | Вместимость солей, г/л |
| Столовая | До 3 |
| Лечебно-столовая | 3-10 |
| Лечебная | Более 10 |
Среди всех вод 2 вида, выпускаемых в бутылках, гидрокарбонатные составляют приблизительно 30%. Они содержат много кислых солей угольной кислоты, до 15% хлоридов в виде поваренной соли.
По показателю вместимости солей и назначению применения двууглекислые воды делят на:
Польза от применения
Щелочная минералка:
Воду с бикарбонатами рекомендуют употреблять при нарушениях функций ЖКТ и мочевыделительной системы. Терапия помогает устранить такие неприятные симптомы, как изжога, отрыжка.
Как сделать выбор?
Минеральная вода предназначена для устранения различных отклонений, а не для утоления жажды. Применять ее следует по рекомендациям врача. Особенно дело касается лечебной воды.
В идеале пить минералку непосредственно из источника. Но для тех, у кого нет возможности отправиться на курорт, повсеместно продают минералку в бутылках.
Также существуют природные воды, изначально содержащие углекислоту. Их не подвергают искусственному газированию.

Желательно брать воду в стеклянной таре, так как пластик, при нарушении условий температурного режима хранения, выделяет вредные вещества, которые попадают в напиток.
Цена не является показателем высокого качества. Чаще всего, это признак отдаленности источника. Воды, разлитые в Европейских странах, стоят на порядок выше, чем добываемые в России и ближайшем зарубежье, ведь на их транспортировку затрачивают немалые средства.
Названия популярных марок
Некоторые бренды минералки заслужили доверие покупателей и высокую репутацию благодаря качеству и оздоровительным свойствам воды. Их названия используют как символ здоровья и долголетия.
Слабощелочные
Список лучших столовых вод:
Щелочные
Столово-лечебные воды пользуются наибольшей популярностью, имеют более насыщенный состав. Они помогают вылечить различные недуги, но при этом у них относительно мягкий вкус.
Самые знаменитые марки:
Сильнощелочные
Сильнощелочные воды обладают выраженным лечебным эффектом, применяются только по назначению врача. Для них характерен яркий специфический вкус. Пить такую воду следует в строго ограниченном количестве.
Наиболее распространенными являются:
От каких болезней помогает избавиться?
Если заболевание достаточно серьезное, одной водой вылечиться не удастся. Но при комплексной терапии, минералка дает положительные результаты и ускоряет выздоровление.
Ощелачивающие воды принимают при следующих болезнях:
Длительность, время приема и суточную норму указывает врач после осмотра, опроса пациента, тщательных исследований и постановки диагноза.
Противопоказания

Детям до трех лет также следует отказаться от этого лечебного напитка. Так как у малышей еще не сформированы ферменты, способные расщепить сложные элементы для полноценного усвоения.
Правила употребления для укрепления здоровья
Максимальную пользу несет свежая вода из источника, бутилированная – менее эффективна, но зато доступна в любом городе.
Важно принимать воду правильно. Для лучшего всасывания полезных компонентов следует пить ее неспеша в предписанном объеме.
Основные моменты при лечении минералкой:
| Диагноз | Когда пить |
| Профилактика | За 30 минут до еды |
| Язва желудка | После еды |
| Гастрит с пониженной кислотностью | Во время еды |
| Гастрит с повышенной кислотностью | Через час после еды |
При ухудшении состояния стоит перестать пить щелочную воду и записаться на прием к врачу.
Заключение
Устранение неприятных симптомов проще и приятней проводить натуральными средствами, чем медикаментами. Минеральные вещества необходимы для нормального функционирования ЖКТ. Но надо помнить, что минералка – это не просто жидкость, и что пить ее надо с учетом вышеприведенной информации.
Щёлочность, гидрокарбонат-ион
Щёлочность
Описание: многоуровневый интегральный параметр, отражающий концентрацию анионов слабых органических и неорганических кислот в воде, в основном — угольной. Характеризует направленность гидро- и геохимических процессов, коррозионной агрессивности воды по отношению к бетону, стали, отопительным котлам, парогенераторам.
Методы определения: титриметрия с использованием индикаторов, потенциометрическое определение.
Типы щёлочности
| Тип | Обусловленность |
|---|---|
| Свободная щелочность | Наличие в воде карбонат-ионов CO 2− 3 и гидроксильных ионов OH − в водах с pH > 8,3 |
| Карбонатная щелочность | Наличие в воде продуктов диссоциации угольной кислоты — карбонатов CO 2− 3 и гидрокарбонатов HCO − 3, находящихся в равновесии |
| Общая щелочность | Наличие в воде анионов слабых неорганических и органических кислот, титруемых сильной кислотой |
Методики, используемые в Испытательном центре МГУ определения концентрации гидрокарбонатов в природных средах
| Нормативный документ на методику | Метод определения | Оборудование |
|---|---|---|
| Вода | ||
| ГОСТ 31957-2012 | титриметрия | вспомогательное оборудование |
| РД 52.24.493-2006 | титриметрия | вспомогательное оборудование |
| Почва | ||
| ГОСТ 26424-85 | титриметрия | весы |
Распространённость: гидрокарбонаты HCO − 3, карбонаты CO 2− 3, гидроксид-ион OH − и ионы слабых органических и неорганических кислот появляются в природной воде естественным образом в процессе растворения в воде углекислого газа, минералов и вмещающих пород при контакте воды с почвой. Поэтому практически все типы вод характеризуются щёлочностью отличной от нуля. Щёлочность тесно связана с показателем pH, поэтому разные щёлочности могут не присутствовать в воде одновременно.
Нормирование
С нормированием щёлочностей дела обстоят сложно. Сама по себе эта группа параметров в воде не нормируется. Однако нормируются гидрокарбонаты (только в бутилированной воде), частично обуславливающие значение щёлочностей. Содержание карбонатов напрямую не нормируются, но, если учесть, что в питьевой воде строго нормируется pH, свободная щёлочность в питьевой воде должна быть равна нулю.
Предельно допустимая концентрация (ПДК) гидрокарбонатов в различных типах вод
| Нормирование | ПДК, мг/л |
|---|---|
| Бутилированная вода первой категории СанПиН 2.1.4.1116-02 | 0–400 |
| Бутилированная вода высшей категории СанПиН 2.1.4.1116-02 | 30–400 |
| Вода систем централизованного водоснабжения СанПиН 2.1.4.1074-01 | — |
| Водные объекты рыбохозяйственного значения Приказ Минсельхоза РФ № 552 | — |
| Объекты рекреационного водопользования СанПиН 2.1.5.980-00 | — |
| Вода плавательных бассейнов СанПиН 2.1.2.1188-03 | — |
| Сточные воды в бытовых системах водоотведения Постановление Правительства РФ № 644 | — |
| Сточные воды в ливневых системах водоотведения Постановление Правительства РФ № 644 | — |
Польза и вред
Несмотря на то, что щёлочность не нормируется в большей части типов вод (кроме бутилированной), у щёлочности есть физиологическое воздействие: при употреблении воды с повышенной щёлочностью неизбежны негативные последствия для организма. Наиболее опасна свободная щёлочность. Общую и карбонатную щёлочности (при отсутствии свободной) лучше контролировать по содержанию гидрокарбонатов. Их содержание не должно превышать 400 мг/л.
При повышенной щёлочности наблюдается:
Методы очистки воды
Появление в питьевой воде свободной щёлочности говорит о наличии загрязнения источника.
При загрязнении источника такими загрязнителями очистка воды, как правило, не целесообразна — необходимо проводить очистку самого источника. В случае, если без очистки воды не обойтись, предпочтительнее использовать обратный осмос.
Щёлочность — важный интегральный параметр состояния воды. Повышенное содержание свободной щёлочности говорит о загрязнении источника. Общая и карбонатная щёлочности позволяют судить о происходящих в воде процессах и о балансе карбонатов и гидрокарбонатов, а также о связи этого баланса с показателем pH. Также параметры используются для оценки пригодности воды для использования в технологических процессах и устройствах, например парогенераторах, отопительных котлах, бойлерах и т.д.
Влияние различных форм углекислоты в воде на ее значение рН
В данной статье рассмотрены вопросы нахождения в воде различных форм углекислоты. Показана важность измерения значения рН при определении соотношений бикарбонатов, карбонатов и гидратов. В статье представлена методика расчёта значения рН воды в зависимости от соотношения в воде различных форм углекислоты. Разработанная методика адаптирована для расчета значения рН воды в щелочном диапазоне. В статье представлены результаты расчетов по данной методике и приведено сравнение расчетных и опытных данных.
Известно, что углекислый газ содержится в воде в связанной, полусвязанной и свободной форме. К связанной форме относятся карбонат – ионы (СО3 2- ), к полусвязанной бикарбонат – ионы (НСО3 — ) и к свободной форме угольная кислота растворенная (Н2СО3) и газообразная (СО2).
Общее количество углекислого газа в воде определяется как сумма всех трех форм.
Количество (концентрация форм углекислоты) выражена в ммоль/л.
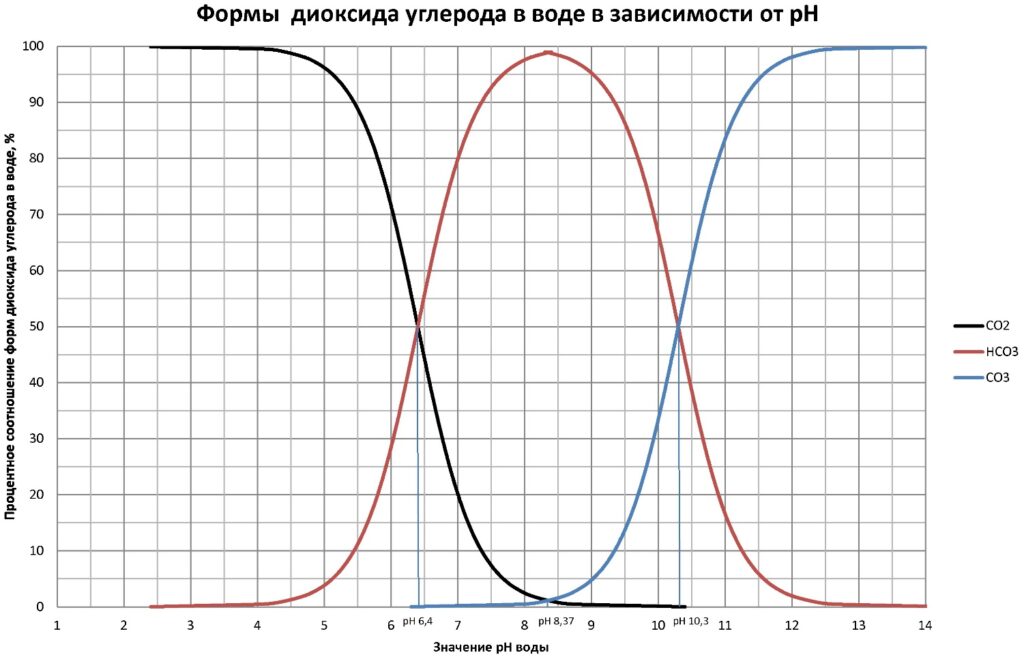
Данные формы углекислоты находятся в определенном равновесии. Принято говорить, что процентное соотношение концентраций различных форм углекислоты зависит от значения рН воды. Так, при значении рН воды 8,37 в воде практически отсутствует свободная форма углекислоты и, соответственно, присутствует бикарбонат-ион и начинает появляться карбонат-ион (рис.1).
Соотношение между угольной кислотой, карбонатами и бикарбонатами установлено экспериментально и зависит от значения рН воды (Уравнение Хендерсона-Хассельбальха для диссоциации углекислоты и бикарбоната):
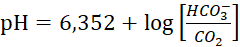
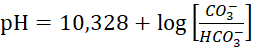
где, 6,352 – отрицательный логарифм константы диссоциации угольной кислоты в воде по 1-й стадии;
10,328 – отрицательный логарифм константы диссоциации угольной кислоты в воде по 2-й стадии;
Как видно из графика (рис.1) изменение количества одной формы углекислоты приводит к изменению соотношения двух других форм углекислоты. При этом изменяется значение рН воды.
Рисунок 1
Здесь необходимо пояснить как была получена форма записи для уравнений (2) и (3).
Уравнение диссоциации кислоты в воде можно записать в общем виде:
HA – кислота, где Н + – ион водорода и A — – анион кислоты.
Константу равновесия (диссоциации) данной химической реакции можно записать в виде:
Данное уравнение можно записать следующим образом вынося ион водорода в левую часть:
Затем записать в виде десятичного логарифма, взятого с обеих сторон:
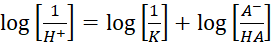
Тогда, уравнение (4) легко преобразуется в уравнения (2) и (3).
Можно сказать, что при растворении в воде диоксида углерода происходит уменьшение рН воды за счет появления в воде иона водорода. Т.к. уравнение (2) есть ни что иное как форма записи уравнения химической реакции диоксида углерода и воды, то в зависимости от количества образующихся в результате реакции конечных продуктов, иона водорода (Н + ) и бикарбоната (НСО3 — ), будет устанавливаться и значение рН.
Это можно наглядно проследить по рисунку 1. Если в воде, после растворения начального количества диоксида углерода, находятся одинаковые количества диоксида углерода и образовавшегося, в результате химической реакции СО2 с водой, бикарбоната (по 50%), то значение рН такой воды составит 6,352 ед. рН.
Рассмотрим пример. В обессоленной воде растворяют С= 0,3 ммоль/л диоксида углерода. Значение рН такой воды можно определить по формуле:
По рисунку 1 определим процентное содержание в такой воде диоксида углерода и бикарбоната. Получаем примерно 3,5% газообразного диоксида углерода СО2 прореагировало с водой с образованием бикарбоната. Это говорит о том, что только 3,5 процента диоксида углерода реагирует с обессоленной водой. При этом количество образующегося иона водорода можно подсчитать как
При этом вода со значением рН равным 4,94 содержит
Значения практически равны. Незначительная погрешность определяется погрешностью визуального определения процента соотношения диоксида углерода к бикарбонату при помощи рисунка 1.
Увеличение концентрации диоксида углерода в воде приводит к уменьшению доли диоксида углерода, вступившего в реакцию с водой с образованием угольной кислоты. Но за счет общего увеличения концентрации диоксида углерода в воде рН такой воды будет уменьшаться до значения 4,0. Ниже этого значения диоксид углерода практически в воде не растворяется.
Рассмотрим пример, в котором в воде, содержащей диоксид углерода, содержится так же бикарбонат натрия (NaHCO3). В этом случае расчет значения рН возможен с использованием уравнения (2).
В воде находятся следующие концентрации углекислоты и бикарбоната натрия: концентрация Ссо2=0,3 ммоль/л; концентрация Снсо3=0,8 ммоль/л
Соответственно, используя уравнение (2) можно записать,
При помощи рисунка 1 определим долю диссоциации (взаимодействия диоксида углерода с водой) в случае нахождения в воде бикарбоната. Получаем, что около 22 % в воде диоксида углерода и 78 % бикарбоната.
При этом вода со значением рН равным 6,96 содержит водорода
Что говорит о том, что только (0,00011/0,3) *100=0,036% диоксида углерода вступает в реакцию с водой с образованием угольной кислоты. Т.е. практически весь диоксид углерода находится в воде в газообразном состоянии (или иногда называют адсорбированном состоянии).
Диссоциация диоксида углерода в данном случае значительно меньше (0,036%) при той же концентрации диоксида углерода в воде, чем в первом примере (в первом примере 3,5 %), из-за того, что в воде уже содержится продукт диссоциации угольной кислоты — бикарбонат.
Далее необходимо более подробно рассмотреть процесс растворения угольной кислоты в воде по двум стадиям.
Запишем уравнения реакций:
Диссоциация по первой стадии происходит в соответствии с константой диссоциации К1, и доля диоксида углерода, образовавшего в воде углекислоту, можно определить по значению рН такой воды при помощи уравнения (2) или рисунка (1).
Диссоциация диоксида углерода по второй стадии при нормальных условиях не происходит. Дело в том, что по второй стадии диссоциации подвергается образовавшийся в первой стадии бикарбонат. Для того что бы бикарбонат подвергся диссоциации с образованием карбоната и угольной кислоты, угольная кислота должна быть удалена из процесса. Тогда из бикарбоната будет образовываться карбонат. Данный процесс наблюдается, например, при кипении воды, содержащей бикарбонат натрия.
Очевидно, что удаление из воды углекислоты приведет к увеличению значения рН. Это видно по рисунку 1. Чем больше бикарбоната переходит в карбонат в соответствии с (6), тем выше значение рН. Т.е. процентное содержание бикарбоната в воде падает и, соответственно, вырастает процентное содержание карбоната.
Данное условие с использованием константы диссоциации К2 представлено в виде уравнения (3).
Для понимания процесса повышения значения рН, диссоциацию по второй стадии удобнее представить в следующем виде:
Фактически уравнение (7) представляет из себя процесс диссоциации карбонатов в воде. При растворении карбоната в воде образуются 2 равные мольные доли бикарбоната и гидрата. Именно появление гидрата в воде увеличивает значение рН воды, т.е. соотношение водород — гидрат увеличивается в сторону гидрата.
Выразим константу равновесия Kг химической реакции (7).

Данная константа есть константа гидролиза карбоната в воде.
Выразим из уравнения константы гидролиза (8) гидрат:
По аналогии с выражением (4) можно записать:
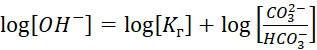

При помощи уравнения (10) можно определить значение рН воды в зависимости от соотношения карбонатов к бикарбонатам.
Добавим к правой и левой частям уравнения (10) число 14. Получаем,
В результате используя уравнение гидролиза карбонатов и константу гидролиза после преобразований получаем уравнение (3), которое было изначально получено для процесса диссоциации угольной кислоты по второй стадии. Это обстоятельство чрезвычайно важно и позволяет сделать следующий вывод. Увеличение значение рН воды при увеличении соотношения карбонат-бикарбонат происходит за счет гидролиза образующихся карбонатов с образованием гидратов и бикарбонатов. Так же как уменьшение значения рН при изменении соотношения диоксид углерода – бикарбонат происходит за счет взаимодействия диоксида углерода с водой с образованием водород иона и бикарбоната.
Понимая, что карбонаты гидролизуются в воде по уравнению (7), уравнение (3) можно записать в следующем виде:
Т.к. карбонаты в воде гидролизуются с образованием бикарбоната и гидрата, то исходное количество карбоната (СО3 2- ) гидролизует на равное количество в молях на гидрат (ОН связ ) и бикарбонат (НСО3 связ ) и остаточное количество самого карбоната (СО3 ост ). В результате можно записать,
Гидрат (ОН своб ) и бикарбонат (НСО3 своб ), условно назовем их свободными, это ионы, полученные не в результате гидролиза исходного значения карбоната. Возможно, привнесенные в воду растворением бикарбоната натрия и едкого натра.
Очевидно, что значение числителя в уравнении (11) равно изначальному количеству карбонатов участвующему в гидролизе плюс количество гидрата привнесенному дополнительно (полученного не в результате гидролиза). Хотя физическая модель такой системы будет рассматривать «свободный» гидрат как продукт гидролиза изначального карбоната. Соответственно, численно в молях значение числителя будет равно значению, полученному при определении щелочности такой воды по фенолфталеину (Ф).
Рассмотрим структуру титрования пробы соляной кислотой по содержанию в ней бикарбонатов, карбонатов и гидратов. Концентрации щелочей указаны в мг-экв/л, в строгом соответствии с количеством ушедшей на титрование соляной кислоты.
При титровании водород ион (Н) соляной кислоты связывает гидроксил ион в натрий хлор и карбонат при натрии в бикарбонат. Соответственно, при фенолфталеиновом индикаторе оттитровывается полностью гидроксил ион и половина карбонат иона. Т.е. после обесцвечивания фенолфталеина в воде останутся только бикарбонаты (рН 8,1-8,3), часть из которых относится к карбонатам и образовалась в результате их разрушения соляной кислотой.
Знаменатель в уравнении (11) будет равен сумме бикарбоната полученного в процессе гидролиза (НСО3 связ ) и бикарбоната, полученного не в результате гидролиза (НСО3 своб ).
Соответственно, уравнение (11) можно записать в виде
Используя уравнение (11) и (12) мною была разработана методика определения значения рН воды по значениям щелочности по фенолфталеину (Ф) и метилоранжу (М) полученных в результате анализа воды на щелочность по ГОСТ 31957-2012. «Вода. Методы определения щелочности и массовой концентрации карбонатов и гидрокарбонатов».
Необходимо отметить, что для дальнейших расчетов вводится допустимое упрощение: В дальнейшем предполагается, что щелочность по метилоранжу (М) определена как общая щелочность минус щелочность по фенолфталеину (Ф).
Можно записать, значения щелочности по (Ф) и по (М):
Так же можно записать, что
Значение рН связано с концентрацией гидрата в воде по уравнению:
Зная значения по (Ф) и (М) в моль/л с использованием уравнений (11) – (16) можно определить значение рН воды для данных значений (Ф) и (М). Методика определения значения рН представлена на рисунке 2.
Изначально рассчитывается массив данных (ОНрН; рН) 16 по формуле (16). Для этого задается значение рН от 8,5 до 14 с определенным шагом. Графическое отображение решения уравнения (16) представлено на рисунке 3.
Затем расчет ведется по двум направлениям.
Первое направление:
Если значение (Ф) больше (М).
В этом случае концентрация «свободного» гидрата определяется как

Задаемся концентрацией (ОН) 11 (для расчета по уравнению (11)) равной 0,0001 моль/л.
В данном случае свободный бикарбонат отсутствует, НСО3 своб =0. (В соответствии с ГОСТ 31957-2012)
Соответственно, общая концентрация бикарбоната определяется только концентрацией бикарбоната полученного в результате гидролиза карбоната (НСО3 связ ).
Тогда, с учетом условия (15) и подстановки ОН своб по (17) в уравнение (18) получаем,
Второе направление:
Если значение (Ф) меньше (М).
Для примера рассчитаем значение рН водного раствора карбоната натрия концентрацией 10 ммоль/л.
Анализ показывает, что значение Ф=10 ммоль/л и М=10 ммоль/л
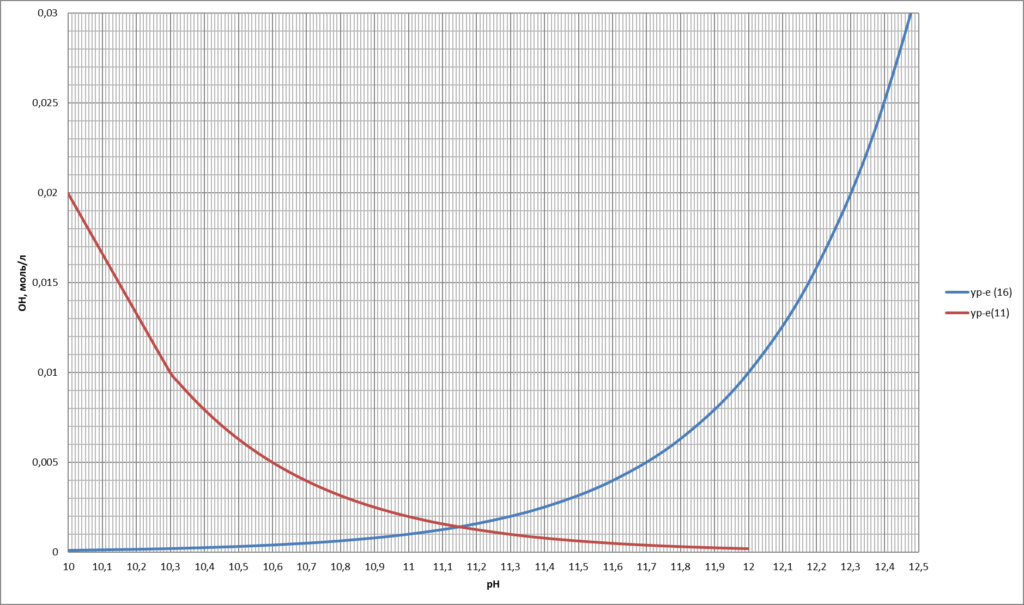
Далее, задаваясь значением рН в интервале 8,5 – 14 по уравнению 16 определяем значение ОНрН. График функции по уравнению (16) в диапазоне значений рН от 10 до 12 представлен на рисунке 3.
Затем задаваясь значением (НСО3) 11 производим расчет рН по уравнению (12). График функции по уравнению (12) в диапазоне значений (НСО3) 11 от 0,000213 до 0,01 представлен на рисунке 3.
Здесь необходимо отметить, что уравнение (3) или (11) или (12) имеет физический смысл только при значении бикарбоната не менее 0,000213 моль/л.
Из рисунка 3 видно, что точка пересечения двух функций дает единственное значение рН равное 11,16. Данное, такое же, значение так же можно получить через константу гидролиза.
Необходимо отметить, что данное значение рН получено при использовании концентраций, а не активностей. Поэтому расчетное значение рН несколько отличается от реального рН раствора такой концентрации. Ниже будет рассмотрено каким образом на основании представленных расчетов получить значение рН равное реально измеренному значению рН раствора.
Рисунок 3
Очевидно, что присутствие в воде «свободных» гидратов или бикарбонатов будет влиять на степень гидролиза карбоната.
Для наглядного представления об изменении степени гидролиза карбоната были проведены расчеты по разработанной методике на основании опыта. Для опыта был взят раствор карбоната натрия концентрацией 10 ммоль/л. Затем раствор принудительно продували воздухом. В результате диоксид углерода из воздуха начал поглощаться водой. В результате образующаяся угольная кислота нейтрализует гидрат в бикарбонат с увеличением концентрации бикарбоната и уменьшением концентрации гидрата и карбоната, из которого в результате гидролиза получается гидрат.
На рисунке 4 представлены зависимости изменения концентрации бикарбоната, карбоната и гидрата в зависимости от рН при продувке раствора воздухом.
Как можно видеть, при растворении в воде 10 ммоль/л карбоната натрия образуется 1,46 ммоль/л бикарбоната и 1,46 ммоль/л гидрата. При этом расчетный рН равен 11,16. Доля диссоциировавшего карбоната составила 1,46/10=0,146 (14,6%). По рисунку 1 видно, что данной доли также соответствует рН 11,16.
Затем раствор насыщается диоксидом углерода. Происходит связывание гидрата, который образовался в процессе гидролиза в бикарбонат по уравнению реакции:
Через определенные промежутки времени раствор анализировался на Ф и М и на основании этих данных рассчитывалось значение рН и концентрация бикарбонатов, карбонатов и гидратов.
Из рисунка 4 видно, что сразу после растворения карбоната натрия (СО3 исх ) в растворе в результате гидролиза образовались гидрат (ОН) и бикарбонат (НСО3) в равных долях. Затем углекислота связывает гидрат в бикарбонат и при значении рН 10,6 концентрация бикарбоната составила 4,4 ммоль/л, а гидрата 0,4 ммоль/л и карбоната 7,6 ммоль/л. Т.е. 4,2/2+0,4/2+7,6=10 ммоль/л исходного карбоната. При этом значение щелочности по фенолфталеину составило 8 ммоль/л, а метилоранжу 12 ммоль/л.
Здесь необходимо отметить, что концентрация карбоната и бикарбоната по ГОСТ 31957-2012 будет равна СО3 исх =8 ммоль/л, НСО3 исх =4 ммоль/л. Как можно видеть данный гост не учитывает гидролиз карбонатов в воде и определяет количество карбонатов бикарбонатов и гидратов без учета процесса гидролиза. При этом по госту количество карбонатов подлежащих гидролизу определяется верно, но не учитывается количество образующихся в результате гидролиза бикарбонатов и гидратов, что не дает возможность рассчитать рН такой воды от значения рН выше 10,0 — 10,5.
Как мы можем видеть при рН 10,0 гидролиз карбонатов настолько незначителен, что при достаточно большой концентрации бикарбонатов это практически не вызывает большой ошибки в расчете рН по уравнению (3)
В качестве примера рассмотрим известный буферный раствор со значением рН 10,00 (при 25 0 С), который содержит 25 ммоль/л Na2CO3 и 25 ммоль/л NaHCO3. Известно, что расчетное значение рН такого раствора без учета коэффициентов активности будет 10,328. Рассчитаем рН такого раствора по разработанной методике. Очевидно, щелочность по фенолфталеину равна 25 ммоль/л и по метилоранжу 50 ммоль/л. Графическое решение уравнений (11) и (16) представлено на рисунке 5. Расчет по предложенной методике показывает, что значение рН равно 10,326, что дает ошибку только на 0,002 ед. рН.
Если рассматривать раствор, где Ф равно М, то в соответствии с ГОСТ 31957-2012 в данном растворе вообще отсутствует бикарбонат и, соответственно, нет возможности рассчитать рН данного раствора. Это неверно, т.к. в растворе присутствует бикарбонат как продукт гидролиза карбоната (НСО3 связ ). Т.о. используя предложенную методику можно рассчитать рН раствора при любых соотношениях Ф к М.
Как видно из рисунка 4, при рН 9,4 количество бикарбоната составило 16 ммоль/л, количество карбоната 2 ммоль/л и количество гидрата 0,0025 ммоль/л. Т.е. чем больше продуктов гидролиза в растворе, тем меньше степень гидролиза. При этом количество поглощенного диоксида углерода из воздуха составило 8 ммоль/л.
Рисунок 4 Зависимости различных форм углекислоты и гидрата от значения рН для случая Ф =М
Рассмотренная методика использует концентрации ионов. В результате рассчитанные значения рН не совпадают с реально измеренными значениями рН. Чем больше ионная сила раствора, тем больше будут расхождения между рассчитанным и измеренным значением. Для того чтобы расчётные и измеренные значения рН совпадали необходимо в расчетах использовать активность ионов. Известно, что активность ионов определяется как произведение концентрации иона на его коэффициент активности.
На рисунке 7 представлена зависимость коэффициентов активности ионов НСО3 и СО3 от ионной силы. Зависимость построена на основании решения уравнения
fi – коэффициент активности иона,
I – ионная сила раствора, моль/л.
Для получения расчетного значения рН равного измеренному необходимо в формуле (3) использовать активности карбоната и бикарбоната. Т.о. после расчета рН по разработанной методике для получения реального значения рН необходимо значение карбоната в уравнение (11) или (12) умножить на коэффициент активности карбоната, взятый при соответствующей ионной силе раствора и значение бикарбоната умножить на коэффициент активности бикарбоната.
К примеру, для раствора 25 ммоль/л Na2CO3 и 25 ммоль/л NaHCO3 рассчитанное значение рН составляет 10,328. Умножим соответствующие ионы на их коэффициенты активности.
Для этого определяем ионную силу раствора
Сi – концентрация иона, ммоль/л.
При данной ионной силе коэффициент активности для карбоната равен 0,37, для бикарбоната 0,775. (рисунок 7)
Таким образом получено расчетное значение рН равное измеренному при температуре 25 0 С. Необходимо четко понимать, что рассчитанные значения будут совпадать с измеренными только при температуре 25 0 С. Влияние температуры на измерение рН довольно существенно, особенно при высоких значениях рН, и изменение рН от температуры для каждого раствора должно быть определено индивидуально. Зависимость рН от температуры носит линейный характер. Поэтому достаточно определить только коэффициент наклона. Данная проблема не рассматривается в статье.
К примеру, определим значение рН для раствора 20 ммоль/л NaOH + 10 ммоль/л NaHCO3. Выше было определено расчетное значение рН для концентраций – 12,02.
Определим ионную силу раствора. Фактически в растворе содержится (по ГОСТ 31957-2012) 10 ммоль/л Na2CO3 и 10 ммоль/л NaOH. Тогда,
Коэффициенты активности при данной ионной силе равны:
Используем для упрощения уравнение (12). С учетом коэффициентов активности получаем:
Данное значение рН будет определяться при температуре раствора 25 0 С.
Мною было проведено довольно много опытов с растворами, содержавшими различные соотношения Ф к М. В среднем расчетные и измеренные значения рН имели различия не более 0,05 ед. рН, что в условиях существующей погрешности измерений является очень хорошим показателем. Во избежание щелочной погрешности измерение рН проводилось до значений не более 12,5.
Стоит сказать, что данная методика разрабатывалась для технологии контроля котловой воды паровых котлов низкого и среднего давления. Значение рН котловой воды рабочего котла не может превышать 12,5. Поэтому меня интересовали прежде всего растворы в диапазоне рН от 8,5 до 12,5. На момент написания данной статьи (07.02.2020) подана заявка № 2020100737 (от 14.01.2020) на патент «Способ контроля и регулировки водно-химического режима парового котла», которая включает в себя данную методику как часть контроля попадания солей жесткости в котловую воду.
Рисунок 7
Хочу отметить еще один момент. Изначально было сложно понять, что значение Ф можно умножать на коэффициент активности карбоната. Если в воде изначально присутствует только карбонат, то здесь всё понятно. Но если в воде присутствует «свободный» гидрат, который получен не в результате гидролиза карбонатов? Анализ физического смысла уравнения (3) говорит о том, что величина фенолфталеиновой щелочности (гидрат и карбонат) обеспечивает количественную характеристику в определении рН, а значение бикарбоната обеспечивает качественную характеристику. Т.е. чем на меньшую величину мы делим, тем большее значение получаем, но при этом полученное значение рН не может быть больше того, что потенциально содержит в себе фенолфталеиновая щелочность. Если при растворении бикарбоната в воде производить отгонку углекислоты, то образующийся карбонат будет гидролизоваться с образованием гидрата. После отгонки более половины углекислоты в такой воде появится «свободный» гидрат. Т.е. фенолфталеиновая щелочность станет больше чем метилоранжевая (Ф=>М). Тем не менее это именно тот гидрат, который образовался от изначального количества бикарбоната. В соответствии с рисунком 1 получается, что именно оставшееся количество бикарбоната обеспечивает значение рН при том, что вся остальная часть, представляемая щелочностью при фенолфталеине, предполагается, что находится в форме карбоната.
Проведем простой эксперимент. В деионизированной воде было растворено 10 ммоль/л едкого натра. При этом измеренное значение рН такого раствора составило 11,86. Ионная сила раствора равна 0,01. Коэффициенты активности при данной ионной силе равны:
Как видно, без учета коэффициента активностей, при подстановке в уравнение (3) в качестве бикарбонатов значения константы гидролиза карбонатов (минимальное значение, при котором уравнение (3) имеет физический смысл 0,000213 или для ммоль 0,213) получаем значение рН, полностью определяемое концентрацией гидратов в растворе. Т.е. если бы в деионизированной воде растворили 10 ммоль/л NaOH.
При этом с учетом коэффициентов активностей получаем:
Как видно, даже при отсутствии в воде карбонатов использование данной методики расчета с определенными допущениями (минимальной концентрацией бикарбоната 0,213 ммоль/л) позволяет получить расчетное значение рН равное измеренному.
Интересно, что коэффициент активности NaOH в воде при ионной силе равной 0,01 равен 0,9. При этом измеренное значение рН раствора концентрацией 10 ммоль/л (I=0,01) при 25 0 С равно 11,86. Это предполагает, что при измерении рН коэффициент активности NaOH будет определятся не как коэффициент активности гидрата. К примеру, для данной концентрации едкого натра (0,01 моль/л) коэффициент активности гидрата будет равен 0,724, а не 0,9.
СОН – активность гидрата, ммоль/л.
Эксперименты при разных концентрациях гидрата и разной ионной силе подтверждают возможность использования уравнения (3), с учетом минимальной концентрации бикарбоната 0,000213 моль/л, в расчетах значения рН при растворении в воде по крайней мере едкого натра при использовании коэффициентов активностей для карбоната и бикарбоната.
Выводы: