Азотистая кислота
Характеристики и физические свойства азотистой кислоты
Она имеет две таутомерные формы: NO(OH) и N(H)O2(преобладает при комнатной температуре в растворе). Концентрированные растворы – голубые, разбавленные растворы – бесцветные. В форме NO(OH) проявляет слабые кислотные свойства, в форме N(H)O2 кислотой не является.
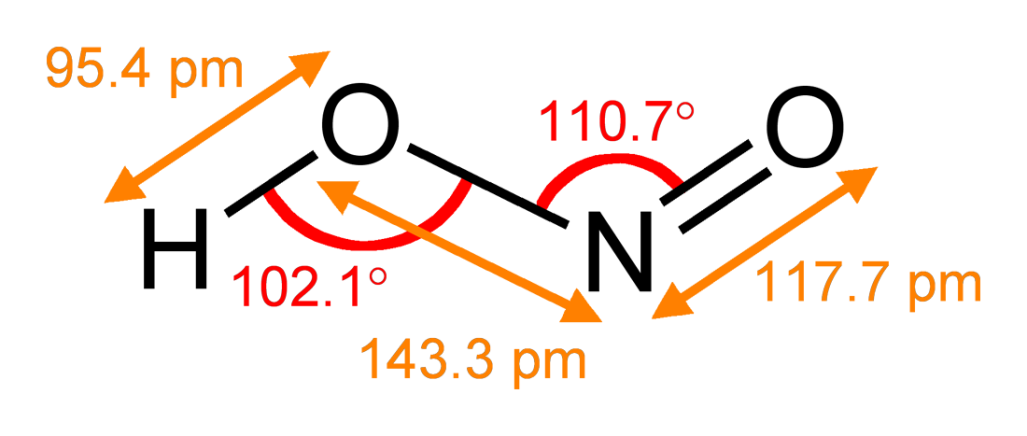
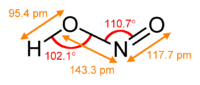
Рис. 1. Строение молекулы азотистой кислоты.
Таблица 1. Физические свойства азотистой кислоты.
Молярная масса, г/моль
Температура плавления, o С
Температура кипения, o С
Растворимость в воде, г/100мл
Получение азотистой кислоты
При действии разбавленной серной кислоты на раствор какого-нибудь нитрита происходит образование свободной азотистой кислоты:
Химические свойства азотистой кислоты
Азотистая кислота в водном растворе диссоциирует на ионы. Её соли носят название нитриты.
Азотистая кислота нейтрализуется щелочами (1), гидратом аммиака (2):
Реагирует с атомным водородом (3), кислородом (4), пероксидом водорода (5, 6):
Проявляет окислительно-восстановительные свойства (7 — 10):
Применение азотистой кислоты
Азотистая кислота нашла применение в органическом синтезе, в частности, для получения ароматических аминов и солей диазония.
Примеры решения задач
Коэффициент активности молекул азотной кислоты равен единице.
Найдем рН раствора азотистой кислоты:
Для расчета показателя основности раствора используют следующую формулу:
Среда раствора – нейтральная.
Копирование материалов с сайта возможно только с разрешения
администрации портала и при наличие активной ссылки на источник.
Азотистая кислота
| Азотистая кислота | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Азотистая кислота |
| Химическая формула | HNO2 |
| Физические свойства | |
| Состояние (ст. усл.) | твердое |
| Отн. молек. масса | 47.0134 а. е. м. |
| Молярная масса | 47.0134 г/моль |
| Плотность | 1.685 (жидк) г/см³ |
| Термические свойства | |
| Температура плавления | 42.35 °C |
| Температура кипения | 158 °C |
| Химические свойства | |
| pKa | 3.4 |
| Растворимость в воде | 548 г/100 мл |
| Классификация | |
| Рег. номер CAS | [7782-77-6] |
Азо́тистая кислота HNO2 — слабая одноосновная кислота, существует только в разбавленных водных растворах, окрашенных в слабый голубой цвет, и в газовой фазе. Соли азотистой кислоты называются нитритами или азотистокислыми. Нитриты гораздо более устойчивы, чем HNO2, все они токсичны.
Содержание
Строение
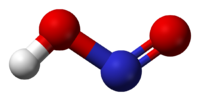
В газовой фазе планарная молекула азотистой кислоты существует в виде двух конфигураций цис- и транс-. При комнатной температуре преобладает транс-изомер.
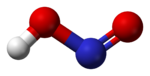 |  |
| транс-изомер | цис-изомер |
Вторая структура является более устойчивой. Так, для цис-HNO2(г) DG°f = −42,59 кДж/моль, а для транс-HNO2(г) DG = −44,65 кДж/моль.
Химические свойства
В водных растворах существует равновесие:
При нагревании раствора азотистая кислота распадается с выделением NO и образованием азотной кислоты:
HNO2 является слабой кислотой. В водных растворах диссоциирует (KD=4,6·10 −4 ), немного сильнее уксусной кислоты. Легко вытесняется более сильными кислотами из солей:
Азотистая кислота проявляет как окислительные, так и восстановительные свойства. При действии более сильных окислителей (пероксид водорода, хлор, перманганат калия) окисляется в азотную кислоту:


В то же время она способна окислять вещества, обладающие восстановительными свойствами:
Получение
Азотистую кислоту можно получить при растворении оксида азота (III) N2O3 в воде:
Также она получается при растворении в воде оксида азота (IV) NO2:
Применение
Азотистая кислота применяется для диазотирования первичных ароматических аминов и образования солей диазония. Нитриты применяются в органическом синтезе при производстве органических красителей.
Физиологическое действие
Азотистая кислота токсична, причём обладает ярко выраженным мутагенным действием, поскольку является деаминирующим агентом.
Источники
Ссылки
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | — | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | Н | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Азотистая кислота» в других словарях:
азотистая кислота — Неустойчивая в концентрированном виде одноосновная кислота; мутаген, вызывающий появление транзиций в результате реакции дезаминирования пуриновых и пиримидиновых оснований: HNO2. [Арефьев В.А., Лисовенко Л.А. Англо русский толковый словарь… … Справочник технического переводчика
азотистая кислота — nitrous acid азотистая кислота. Hеустойчивая в концентрированном виде одноосновная кислота; мутаген, вызывающий появление транзиций
азотистая кислота — nitrito rūgštis statusas T sritis chemija formulė HNO₂ atitikmenys: angl. nitrous acid rus. азотистая кислота ryšiai: sinonimas – vandenilio dioksonitratas (1–) … Chemijos terminų aiškinamasis žodynas
Азотистая кислота — HNO2, одноосновная, нестойкая, довольно слабая кислота, существующая только в разбавленных холодных водных растворах. Структурная формула HO N = О. Константа диссоциации А. к. 4,5․10 4 при 18°C. Образуется наряду с азотной кислотой при… … Большая советская энциклопедия
Азотистая кислота — ангидрид N2О3, гидрат NOOH. Получается одновременно с азотноватым ангидридом при нагревании азотной кислоты с мышьяковистой кислотой в виде бурого, вызывающего сильный кашель газа, сгущающегося на сильном холоде в синюю жидкость, закипающую при… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
АЗОТИСТАЯ КИСЛОТА — HNO2, бесцв. в во, существующее в виде паров или водного р ра. Нагревание паров или их конденсация, а также концентрирование водных р ров приводят к разложению А. к.: в парах по р ции 2HNO2 NO + NO2 + Н 2 О, в p pe 3HNO2 HNO3 + 2NO + Н 2 О.… … Химическая энциклопедия
АЗОТИСТАЯ КИСЛОТА — HNO2. Существует в разбавл. вод. р рах. Применяется в органич. синтезе, гл. обр. для диазотирования. Соли и эфиры А. к. наз. нитритами … Естествознание. Энциклопедический словарь
АЗОТИСТАЯ КИСЛОТА И ЕЕ ПРЕПАРАТЫ — АЗОТИСТАЯ КИСЛОТА И ЕЕ ПРЕПАРАТЫ. А. к. не применяется в терапии, но большое значение имеют ее соли и эфиры, к рые, расщепляясь в организме, действуют, гл. обр., питрозо группой (NO). Особенно чувствительными к этой группе являются окончания… … Большая медицинская энциклопедия
Кислота — У этого термина существуют и другие значения, см. Кислота (значения) … Википедия
Тартроновая кислота — или оксималоновая принадлежит к трехатомно двуосновным спиртокислотам (см.). Состав ее C3H4O5 = СООН СН(ОН) СООН. Она является первым членом гомологического ряда кислот СnH2n 2O5, к которому принадлежат следующие кислоты: яблочная C4H6O5;… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Азотистая кислота. Свойства азотистой кислоты.
Азотистая кислота HNO2 имеет слабый характер. Весьма неустойчива, может быть только в разбавленных растворах:
2HNO2 
Соли азотистой кислоты называются нитритами или азотистокислыми. Нитриты гораздо более устойчивы, чем HNO2, все они токсичны.
Атом азота в азотистой кислоте имеет промежуточную степень окисления +3 и в связи с этим он может быть и окислителем, и проявлять восстановительные свойства:
Строение азотистой кислоты.
В газовой фазе планарная молекула азотистой кислоты существует в виде двух конфигураций цис- и транс-:
Химические свойства азотистой кислоты.
В водных растворах существует равновесие:

Нагреваясь, раствор азотистой кислоты распадается с выделением NO и образованием азотной кислоты:

HNO2 в водных растворах диссоциирует (KD=4,6·10 −4 ), немного сильнее уксусной кислоты. Легко вытесняется более сильными кислотами из солей:

Азотистая кислота проявляет окислительные и восстановительные свойства. При действии более сильных окислителей (пероксид водорода, хлор, перманганат калия) происходит окисление в азотную кислоту:



Кроме того, она может окислять вещества, которые обладают восстановительными свойствами:

Получение азотистой кислоты.
Азотистую кислоту получают при растворении оксида азота (III) N2O3 в воде:

Кроме того, она образуется при растворении в воде оксида азота (IV) NO2:
Применение азотистой кислоты.
Азотистая кислота применяется для диазотирования первичных ароматических аминов и образования солей диазония. Нитриты применяются в органическом синтезе в производстве органических красителей.
Физиологическое действие азотистой кислоты.
Азотистая кислота является токсичной и обладает ярко выраженным мутагенным действием, так как является деаминирующим агентом.
Азотистая кислота (HNO2): строение, свойства, синтез.
Содержание:
В азотистая кислота слабая неорганическая кислота, химическая формула которой HNO2. Он находится в основном в водном растворе бледно-голубого цвета. Он очень нестабилен и быстро разлагается на оксид азота, NO, и азотную кислоту, HNO.3.
Обычно он находится в водном растворе в виде нитритов. Кроме того, он естественным образом поступает из атмосферы в результате реакции оксида азота с водой. Там, особенно в тропосфере, азотистая кислота вмешивается в регулирование концентрации озона.
Решение HNO показано на изображении выше.2 где ценится характерный бледно-голубой цвет этой кислоты. Он синтезируется растворением триоксида азота N2ИЛИ3, в воде. Точно так же это продукт подкисления растворов нитрита натрия при низких температурах.
HNO2 Он не имеет коммерческого использования, поскольку используется в форме нитрита для консервирования мяса. С другой стороны, он используется в производстве азокрасителей.
Он используется вместе с тиосульфатом натрия при лечении пациентов с отравлением цианидом натрия. Но это мутагенный агент, и считается, что он может вызывать замены в основаниях цепей ДНК посредством окислительного дезаминирования цитозина и аденина.
Азотистая кислота имеет двойное поведение, поскольку она может действовать как окислитель или как восстановитель; то есть он может быть уменьшен до NO или N2, или окислиться до HNO3.
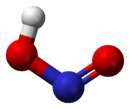
Состав азотистой кислоты
На верхнем изображении показана молекулярная структура азотистой кислоты с использованием модели сфер и столбиков. Атом азота (синяя сфера) расположен в центре структуры, образуя двойную связь (N = O) и одинарную связь (N-O) с атомами кислорода (красные сферы).
Обратите внимание, что атом водорода (белая сфера) связан с одним из атомов кислорода, а не напрямую с азотом. Итак, зная это, структурная формула HNO2 это [HO-N = O] или [NO (OH)], и такой связи H-N нет (как может предполагать химическая формула).
Их структуры могут принимать две формы: цис- или транс-, называемые геометрическими изомерами. В цис-изомере атом H затмевается соседним атомом кислорода; в то время как в транс-изомере оба находятся в анти- или противоположных положениях.
В цис-изомере вероятно образование внутримолекулярного водородного мостика (OH-NO), который может нарушить межмолекулярные (ONOH-ONOH).
Свойства
Химические названия
-Диоксоназотная кислота (III)
-Hydroxydoxydonitrogen (систематическое название IUPAC)
Физическое описание
Бледно-голубая жидкость, соответствующая раствору нитрита.
Молекулярный вес
Константа диссоциации
Это слабая кислота. Его pKa составляет 3,35 при 25 ° C.
Температура плавления
Это известно только в растворе. Следовательно, его температуру плавления невозможно вычислить, равно как нельзя выделить кристаллы.
Точка кипения
Образование соли
Пожарный потенциал
Воспламеняется в результате химических реакций. Может взорваться при контакте с трихлоридом фосфора.
Разложение
Это очень нестабильное соединение, и в водном растворе оно разлагается на оксид азота и азотную кислоту:
Восстановитель
Реагирует с ионами I – и вера 2+ в форме нитрита калия с образованием оксида азота:
Нитрит калия в присутствии ионов олова восстанавливается с образованием закиси азота:
Нитрит калия восстанавливается цинком в щелочной среде с образованием аммиака:
Окислитель
Азотистая кислота не только является восстановителем, но и может вмешиваться в процессы окисления. Например: он окисляет сероводород, превращаясь в оксид азота или аммиак, в зависимости от кислотности среды, в которой происходит реакция.
Азотистая кислота в кислой среде с pH может окислять иодид-ион до йода.
Номенклатура
В HNO2 Ему могут быть присвоены другие названия, в зависимости от вида номенклатуры. Азотистая кислота соответствует традиционной номенклатуре; диоксоназотная кислота (III), к номенклатуре запасов; и диоксонитрат водорода (III) к систематическому.
Синтез
Азотистая кислота может быть синтезирована растворением триоксида азота в воде:
Другой метод приготовления состоит из реакции нитрита натрия, NaNO.3, с минеральными кислотами; такие как соляная кислота и бромистоводородная кислота. Реакцию проводят при низкой температуре, и азотистая кислота расходуется на месте.
Старший брат3 + H + => HNO2 + Na +
Ион H + это происходит из HCl или HBr.
Риски
Учитывая его свойства и химические характеристики, имеется мало информации о прямых токсических эффектах HNO.2. Возможно, некоторые вредные эффекты, которые, как считается, вызывает это соединение, на самом деле вызваны азотной кислотой, которая может быть произведена при расщеплении азотистой кислоты.
Отмечается, что HNO2 он может оказывать вредное воздействие на дыхательные пути и вызывать раздражающие симптомы у пациентов с астмой.
В форме нитрита натрия он восстанавливается дезоксигемоглобином, образуя оксид азота. Это мощное сосудорасширяющее средство, которое вызывает расслабление гладких мышц сосудов; доза LD50 для перорального употребления людям оценивается в 35 мг / кг.
Токсичность нитрита натрия проявляется сердечно-сосудистым коллапсом с последующей тяжелой гипотензией из-за сосудорасширяющего действия оксида азота, производимого из нитрита.
Двуокись азота, NO2присутствует в загрязненном воздухе (смог), при определенных условиях может выделять азотистую кислоту; которые, в свою очередь, могут реагировать с аминами с образованием нитрозаминов, гамма канцерогенных соединений.
Аналогичная реакция происходит с сигаретным дымом. Были обнаружены остатки нитрозамина на внутренней обшивке автомобилей для курения.
Приложения
Производство солей диазония
Азотистая кислота используется в промышленности при производстве солей диазония в результате реакции с ароматическими аминами и фенолами.
Соли диазония могут образовывать яркие азосоединения, которые используются в качестве красителей, а также служат качественным тестом на наличие ароматических аминов.
Удаление азида натрия
Азотистая кислота используется для удаления азида натрия (NaN3), который потенциально опасен из-за своей склонности к взрыву.
2 NaN3 + 2 HNO2 => 3 N2 + 2 NO + 2 NaOH
Синтез оксимов
Азотистая кислота может реагировать с кетонными группами с образованием оксимов. Они могут быть окислены с образованием карбоновых кислот или восстановлены с образованием аминов.
Этот процесс используется при коммерческом получении адипиновой кислоты, мономера, используемого при производстве нейлона. Он также участвует в производстве полиуретана, а его сложные эфиры являются пластификаторами, в основном в ПВХ.
В солевом виде
Азотистая кислота в форме нитрита натрия используется для обработки и консервирования мяса; так как он предотвращает рост бактерий и способен реагировать с миоглобином, давая темно-красный цвет, что делает мясо более привлекательным для потребления.
Эта же соль используется вместе с тиосульфатом натрия при внутривенном лечении отравления цианидом натрия.
Ссылки
5 измерений устойчивости и их характеристики
Как быть более активным на работе: 8 практических советов