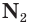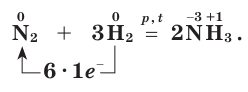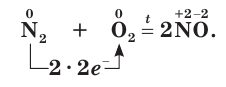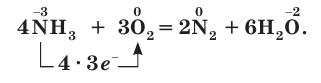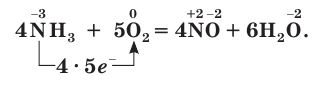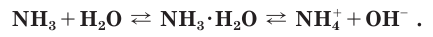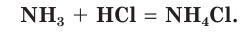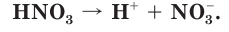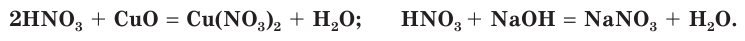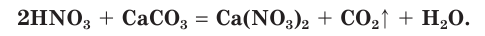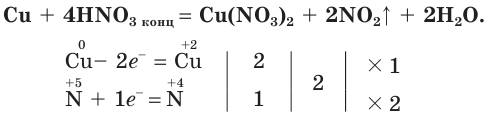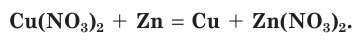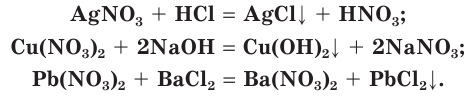Азот что представляет собой
Полезное
Смотреть что такое «АЗОТ» в других словарях:
АЗОТ — (N) химический элемент, газ, без цвета, вкуса и запаха; составляет 4/5 (79 %) воздуха; уд. вес 0,972; атомный вес 14; сгущается в жидкость при 140 °С. и давлении 200 атмосфер; составная часть многих растительных и животных веществ. Словарь… … Словарь иностранных слов русского языка
АЗОТ — АЗОТ, хим. элемент, симв. N (франц. AZ), порядковый номер 7, ат. в. 14,008; точка кипения 195,7°; 1 л А. при 0° и 760 мм давл. весит 1,2508 г [лат. Nitrogenium («порождающий селитру»), нем. Stickstoff («удушающее… … Большая медицинская энциклопедия
АЗОТ — (лат. Nitrogenium) N, химический элемент V группы периодической системы, атомный номер 7, атомная масса 14,0067. Название от греческой a отрицательная приставка и zoe жизнь (не поддерживает дыхания и горения). Свободный азот состоит из 2 атомных… … Большой Энциклопедический словарь
азот — а м. azote m. <араб. 1787. Лексис.1. алхим. Первая материя металлов металлическая ртуть. Сл. 18. Пустился он <парацельс> на конец по свету, предлагая всем за весьма умеренную цену свой Лауданум и свой Азот, для изцеления всех возможных… … Исторический словарь галлицизмов русского языка
АЗОТ — (Nitrogenium), N, химический элемент V группы периодической системы, атомный номер 7, атомная масса 14,0067; газ, tкип 195,80 шС. Азот основной компонент воздуха (78,09% по объему), входит в состав всех живых организмов (в организме человека… … Современная энциклопедия
Азот — (Nitrogenium), N, химический элемент V группы периодической системы, атомный номер 7, атомная масса 14,0067; газ, tкип 195,80 °С. Азот основной компонент воздуха (78,09% по объему), входит в состав всех живых организмов (в организме человека… … Иллюстрированный энциклопедический словарь
Азот — (хим. знак N, атомный вес 14) один из химических элементов;бесцветный газ, не имеющий ни запаха, ни вкуса; очень мало растворим вводе. Удельный вес его 0.972. Пикте в Женеве и Кальете в Париже удалосьсгустить азот, подвергая его высокому давлению … Энциклопедия Брокгауза и Ефрона
Азот — N (лат. Nitrogenium * a. nitrogen; н. Stickstoff; ф. azote, nitrogene; и. nitrogeno), хим. элемент V группы периодич. системы Mенделеева, ат.н. 7, ат. м. 14,0067. Oткрыт в 1772 англ. исследователем Д. Pезерфордом. При обычных условиях A.… … Геологическая энциклопедия
АЗОТ — муж., хим. основание, главная стихия селитры; селитротвор, селитрород, селитряк; он же главная, по количеству, составная часть нашего воздуха (азота 79 объемов, кислорода 21). Азотистый, азотный, азотовый, азот в себе содержащий. Химики различают … Толковый словарь Даля
азот — органоген, нитроген Словарь русских синонимов. азот сущ., кол во синонимов: 8 • газ (55) • неметалл … Словарь синонимов
Азот — это газ, который гасит пламя, так как не горит и не поддерживает горения. Его получают фракционной перегонкой жидкого воздуха, хранят под давлением в стальных баллонах. Азот применяют, в основном, для производства аммиака и цианамида кальция, а… … Официальная терминология
Азот что представляет собой
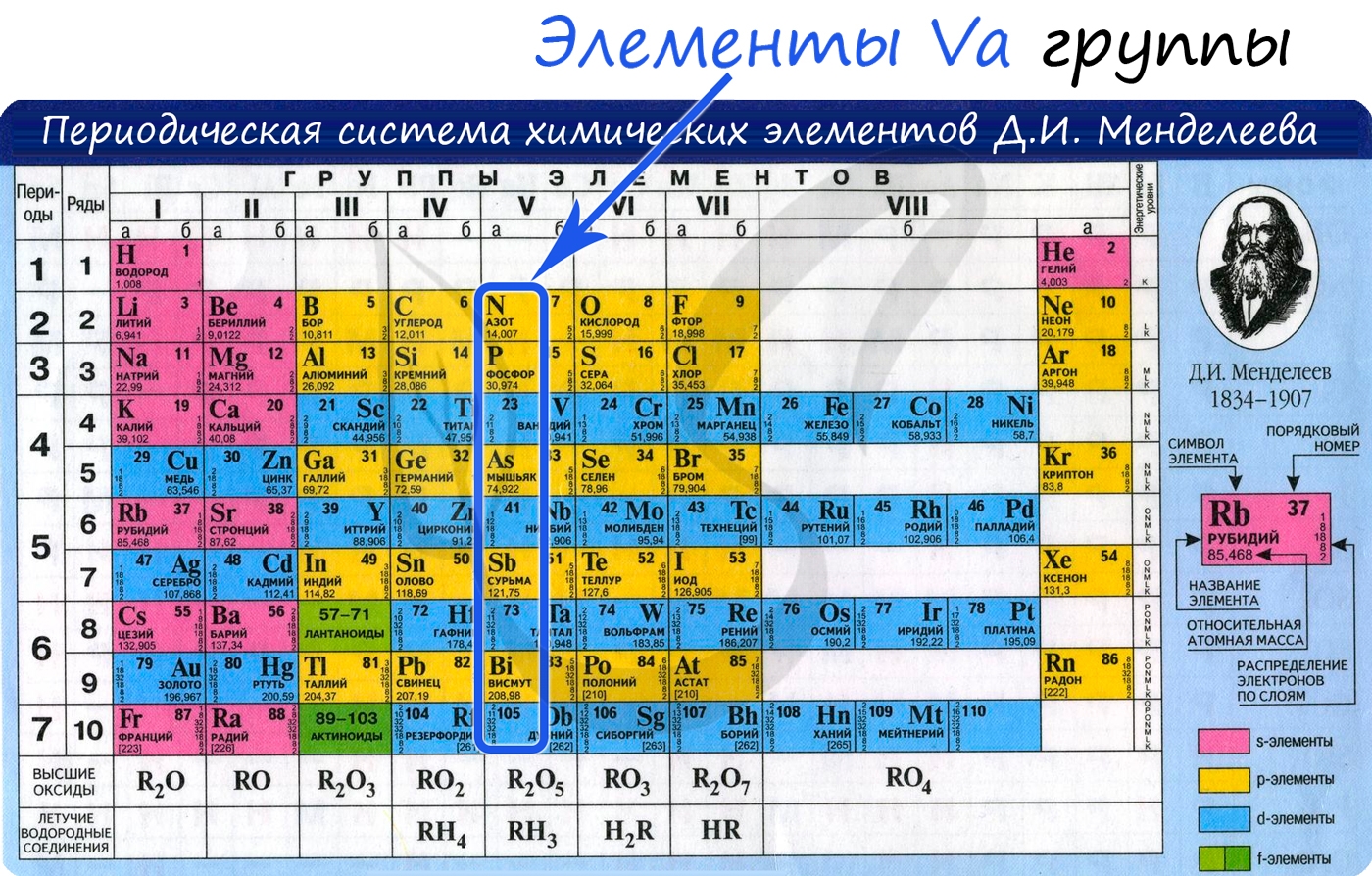
Общая характеристика элементов Va группы
От N к Bi (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
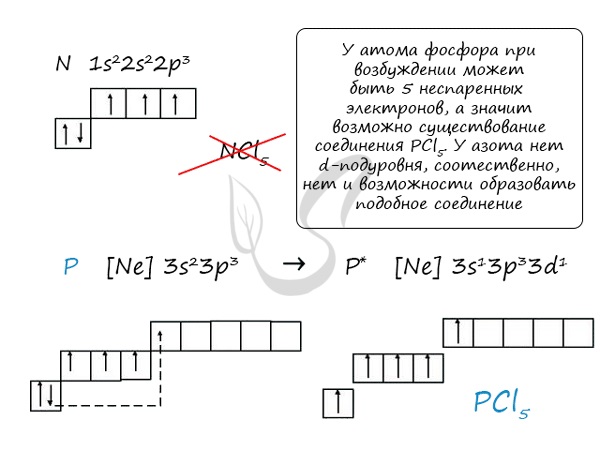
Основное и возбужденное состояние азота
Сравнивая возможности перемещения электронов у азота и фосфора, разница становится очевидна.
Природные соединения
Селитры являются распространенными азотными удобрениями, которые обеспечивают быстрый рост и развитие растений, повышают урожайность. Однако, следует строго соблюдать правила их применения, чтобы не превысить допустимые концентрации.
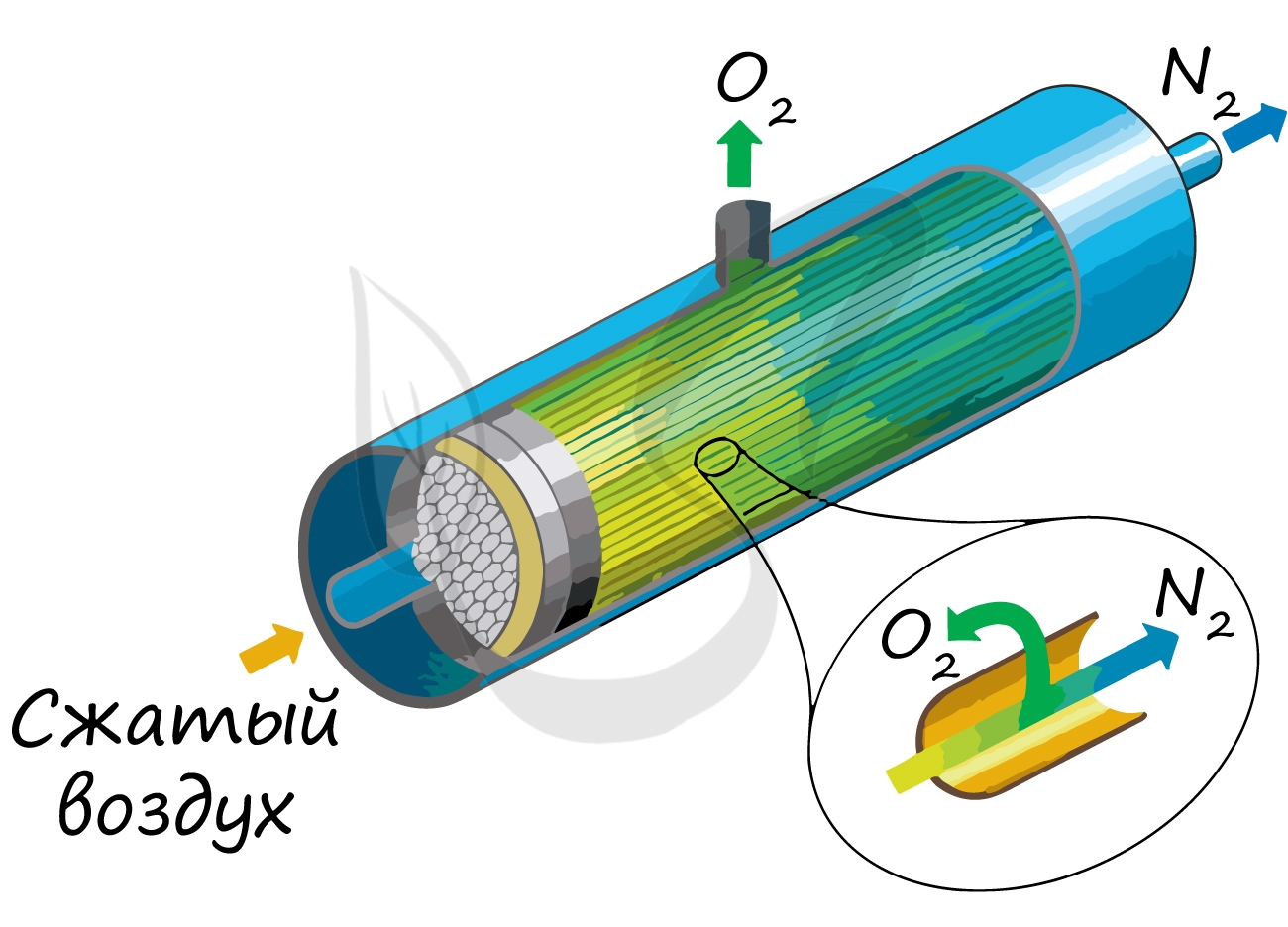
В промышленности азот получают путем сжижения воздуха. В дальнейшем путем испарения из сжиженного воздуха получают азот.
Применяют и метод мембранного разделения, при котором через специальный фильтр из сжатого воздуха удаляют кислород.
В лаборатории методы не столь экзотичны. Чаще всего получают азот разложением нитрита аммония
Также азот можно получить путем восстановления азотной кислоты активными металлами.
Молекула азота отличается большой прочностью из-за наличия тройной связи. Вследствие этого многие реакции эндотермичны: даже горение азота в кислороде сопровождается поглощением тепла, а не выделением, как обычно бывает при горении.
Без нагревания азот взаимодействует только с литием. При нагревании реагирует и с другими металлами.
Важное практическое значение имеет синтез аммиака, который применяется в дальнейшим при изготовлении удобрений, красителей, лекарств.
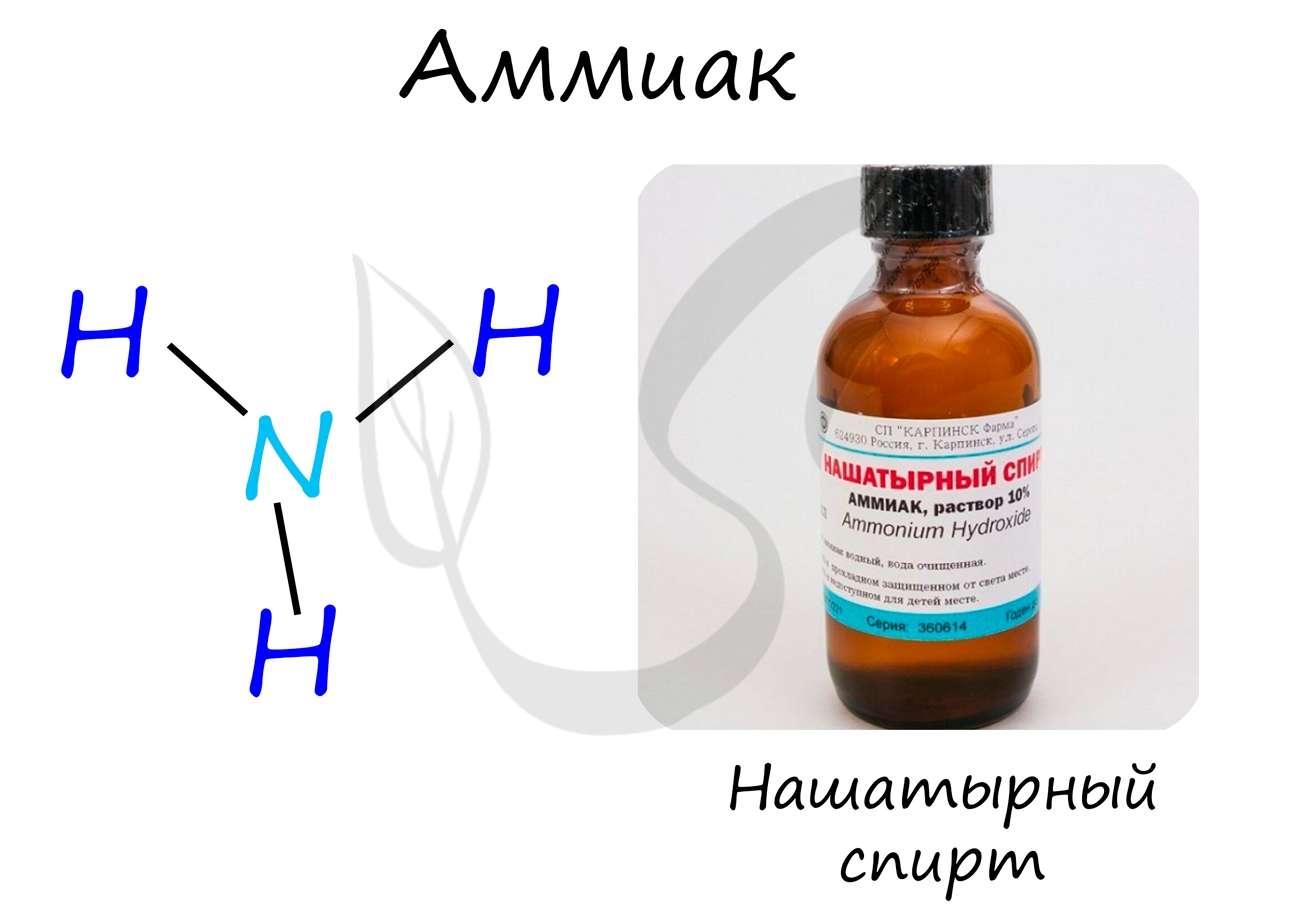
Аммиак
Бесцветный газ с резким едким запахом, раздражающим слизистые оболочки. Раствор концентрацией 10% аммиака применяется в медицинских целях, называется нашатырным спиртом.
В промышленности аммиак получают прямым взаимодействием азота и водорода.
В лабораторных условиях сильными щелочами действуют на соли аммония.
Аммиак проявляет основные свойства, окрашивает лакмусовую бумажку в синий цвет.
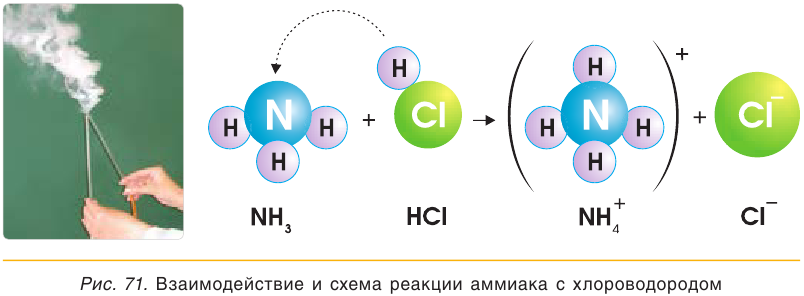
Как основание аммиак способен реагировать с кислотами с образованием солей.
NH3 + HCl → NH4Cl (хлорид аммония)
Горение аммиака без катализатора приводит к образованию азота в молекулярном виде. Окисление в присутствии катализатора сопровождается выделением NO.
Соли аммония
В воде ион аммония подвергается гидролизу с образованием нестойкого гидроксида аммония.
Получают N2O разложением нитрата аммония при нагревании:
Оксид азота I разлагается на азот и кислород:
В промышленных масштабах оксид азота II получают при каталитическом окислении аммиака.
При н.у. жидкость синего цвета, в газообразной форме бесцветен. Высокотоксичный, приводит к тяжелым ожогам кожи.
При охлаждении газов образуется оксид азота III.
Бурый газ, имеет острый запах. Ядовит.
В лабораторных условиях данный оксид получают в ходе реакции меди с концентрированной азотной кислотой. Также NO2 выделяется при разложении нитратов.
Проявляет высокую химическую активность, кислотный оксид.
Как окислитель NO2 ведет себя в реакциях с фосфором, углеродом и серой, которые сгорают в нем.
Если растворение в воде оксида проводить в избытке кислорода, образуется азотная кислота.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Содержание:
Азот — химический элемент и простое вещество:
Неметалл азот N в периодической системе химических элементов открывает VA-группу, в которой также расположены неметаллы фосфор Р и мышьяк As и металлы сурьма Sb и висмут Bi.
Свойства атомов элементов VA-группы, а также свойства их простых веществ закономерно изменяются с ростом их атомного номера: неметаллические свойства ослабевают, а металлические — усиливаются.
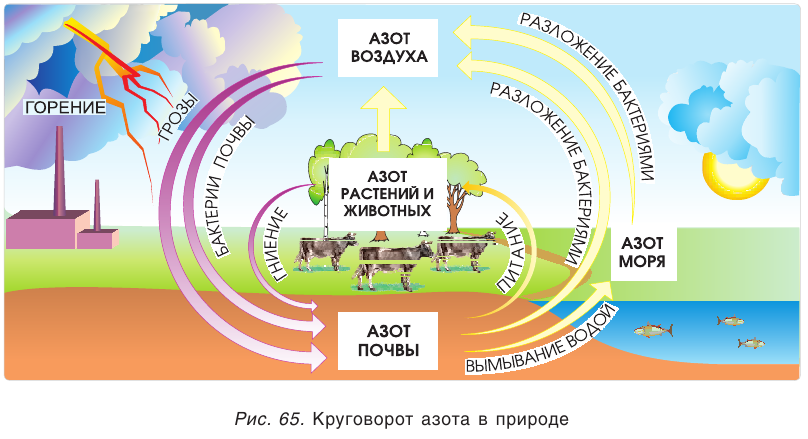
Азот в природе
В природе химический элемент азот находится в виде простого вещества
Строение атомов
В атоме азота 7 электронов, из них 5 располагаются на внешнем электронном слое: 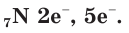
В соединениях с кислородом атом азота проявляет максимальную положительную степень окисления, равную +5, как, например, в азотной кислоте
Строение и физические свойства простого вещества
Простое вещество азот состоит из двухатомных молекул 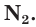
При обычных условиях азот — бесцветный газ, без вкуса и запаха, не поддерживает дыхания и горения, не ядовит. Молекулы азота неполярны, поэтому азот мало растворим в воде. Животные в атмосфере чистого азота погибают из-за того, что лишаются необходимого для дыхания кислорода. С этим связано название азота, происходящее от греческого а — отрицательная приставка, зое — жизнь, т. е. непригодный для жизни.
При повышении давления растворимость азота в тканях организма человека увеличивается. Это приводит к состоянию «азотного наркоза»: водолаз перестает уверенно управлять своими движениями. Поэтому при погружении на большие глубины вместо сжатого воздуха пользуются искусственной дыхательной смесью, в которой азот заменен гелием.
Химические свойства азота
Простое вещество азот 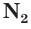
Окислительные свойства азота проявляются в реакциях с водородом и активными металлами. Так, при высокой температуре (t) и большом давлении (p) азот соединяется с водородом в присутствии катализатора, образуя аммиак:
При обычных условиях азот реагирует только с литием, образуя нитрид лития:
С другими металлами азот взаимодействует при высоких температурах.
Восстановительные свойства азота проявляются при его взаимодействии с кислородом. Азот реагирует с кислородом при температуре около 3000 °С, образуя оксид азота(II):
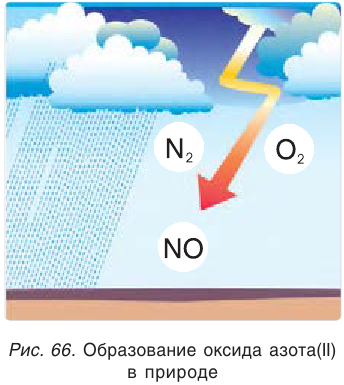
Эта реакция может также протекать при пропускании электрического разряда через смесь газов, например при разряде молнии во время грозы (рис. 66).
Применение азота
Применение азота обусловлено присущими ему свойствами инертного газа. Он используется для продувки и очистки систем трубопроводов и пожаротушения. В атмосфере азота замедляются процессы окисления и гниения, что позволяет увеличить сроки хранения лекарственных препаратов и пищевой продукции — мясных изделий, орехов, чипсов, масла, кофе, пива и др. Поэтому азот используется при их упаковке, а также для создания определенной атмосферы в овощехранилищах.
Жидкий азот, температура которого равна –196 °С, применяется для глубокого охлаждения и вымораживания, в косметологии.
В химической промышленности азот применяется при производстве минеральных удобрений и для синтеза аммиака.
Аммиак
Одним из важнейших соединений азота является аммиак 
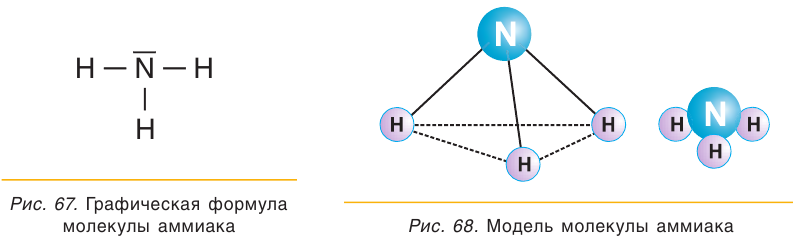
Молекула аммиака имеет форму пирамиды (рис. 68).
Химические связи между атомом азота и атомами водорода в молекуле 

Физические свойства аммиака
Аммиак — бесцветный газ, с резким характерным запахом, ядовит. Он хорошо растворим в воде. В одном объеме воды при комнатной температуре растворяется около 700 объемов аммиака.
Водный раствор с массовой долей аммиака, равной 3 %, в быту называется нашатырным спиртом, под таким же названием он продается в аптеке. В технике водный раствор с массовой долей аммиака, равной 25 %, называют аммиачной водой.
Медики используют водные растворы аммиака (нашатырный спирт) в повседневной практике: ватка, смоченная в нашатырном спирте, выводит человека из обморочного состояния, не причиняя вреда.
При увеличении давления или охлаждении аммиак легко сжижается. Жидкий аммиак при испарении поглощает много теплоты, поэтому его применяют в холодильных установках, а также для получения искусственного льда в спортивных сооружениях.
Химические свойства аммиака
Для аммиака характерны реакции окисления и соединения.
Степень окисления атома азота в аммиаке равна –3, поэтому аммиак проявляет восстановительные свойства, окисляясь кислородом и другими окислителями. Реакция горения аммиака в кислороде описывается уравнением:
В присутствии катализатора (платины) аммиак реагирует с кислородом с образованием оксида азота(II) NO:
Эта реакция лежит в основе промышленного способа получения азотной кислоты. Подробнее этот процесс вы изучите в 11-м классе.
Запомните!
Смеси аммиака с кислородом или воздухом могут взрываться при нагревании, поэтому они опасны
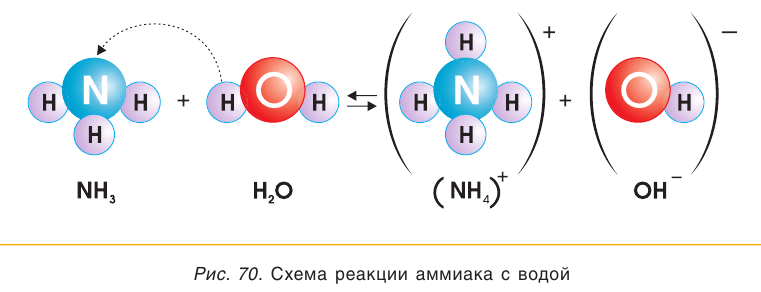
С водой и кислотами аммиак вступает в реакции соединения. Колбу, заполненную аммиаком и закрытую пробкой со вставленной в нее трубочкой, опустим в воду, к которой добавлено несколько капель фенолфталеина (рис. 69). Внутри колбы начнет бить малиновый «фонтан».
При растворении аммиака в воде происходит химическая реакция с образованием гидрата аммиака 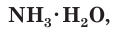


Раствор аммиака в воде (аммиачная вода) за счет присутствия в нем гидроксид-ионов обладает свойствами слабого основания, поэтому в опыте, иллюстрирующем растворимость аммиака в воде, «фонтан» окрашивается в малиновый цвет. Если вместо фенолфталеина в воду добавить лакмус, то раствор окрасится в синий цвет.
Поскольку реакция взаимодействия аммиака с водой обратима, в растворе помимо катионов аммония 

При взаимодействии аммиака с кислотами образуются соли аммония, например хлорид аммония 
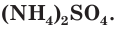
Аммиак способен реагировать и с другими кислотами. Эти реакции протекают без изменения степени окисления атомов азота.
Применение аммиака
По объемам производства в мире аммиак занимает одно из первых мест — ежегодно получают около 100 млн т этого соединения. Аммиак выпускается в жидком виде или в виде водного раствора — аммиачной воды.
Огромные количества аммиака используются для получения азотной кислоты, которая идет на производство удобрений и множества других продуктов.
Из аммиака получают различные соли аммония и мочевину (карбамид).
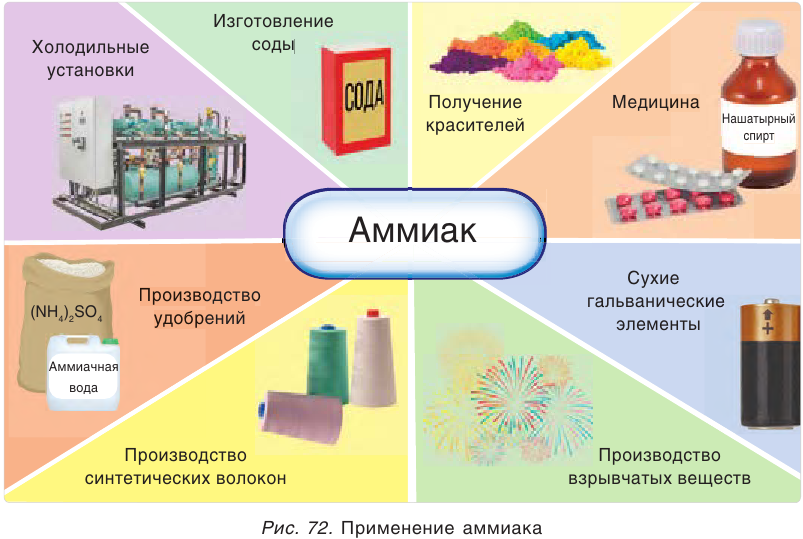
Аммиак используется также для получения синтетических волокон, лекарственных препаратов, взрывчатых веществ, красителей (рис. 72).
Азотная кислота
Азотная кислота 
Модель молекулы азотной кислоты представлена на рисунке 73.
Физические свойства азотной кислоты
Азотная кислота 
Азотная кислота — сильный электролит, в водном растворе практически полностью диссоциирует на ионы:
Присутствие в разбавленном водном растворе 
Химические свойства азотной кислоты
Подобно другим кислотам, азотная кислота вступает в реакции с осно Ђвными оксидами и основаниями. При этом образуются соли азотной кислоты — нитраты:
Азотная кислота как сильная кислота взаимодействует с солями более слабых кислот. На рисунке 75 показано растворение раковины моллюска, состоящей в основном из карбоната кальция, под действием азотной кислоты с выделением углекислого газа:
Азотная кислота проявляет окислительные свойства по отношению к металлам, но в отличие от других кислот реагирует с большинством металлов, кроме благородных.
При этом водород обычно не выделяется.
Продуктами взаимодействия азотной кислоты с металлами являются нитраты металлов и соединения азота со степенью окисления атомов меньшей, чем в азотной кислоте. Например, если поместить в колбу обрезки медной проволоки и осторожно (в вытяжном шкафу!) прилить к ним концентрированную азотную кислоту, то сразу начнет выделяться «бурый газ» — оксид азота(IV) (рис. 76):
Один объем азотной и три объема соляной кислоты образуют смесь, называемую царской водкой. Она способна растворять даже «царя металлов» — золото.
Азотная кислота способна окислять и другие вещества, как неорганические, так и органические. Поэтому с азотной кислотой надо обращаться крайне осторожно: не проливать, не допускать попадания на кожу (азотная кислота реагирует с белками, вследствие чего на коже образуются желтые пятна), на одежду (разрушаются шерсть и натуральный шелк).
Применение азотной кислоты и нитратов
Азотная кислота — одноосновная кислота, образующая соли нитраты.
Из предыдущего параграфа вы уже знаете, что нитраты образуются при взаимодействии азотной кислоты с различными химическими веществами: металлами, оксидами и гидроксидами металлов, солями слабых кислот.
При обычных условиях нитраты — твердые кристаллические вещества. Все они хорошо растворимы в воде.
Нитраты являются сильными электролитами. При диссоциации этих солей в качестве катионов образуются ионы металлов (или аммония), а в качестве анионов — нитрат-ионы:
В больших количествах нитраты ядовиты.
Нитраты участвуют во всех обменных реакциях, характерных для солей. Они взаимодействуют с металлами, при этом более активный металл вытесняет менее активные из растворов их солей:
Реакции с кислотами, щелочами и солями протекают, если в результате образуются нерастворимые соединения, а нитрат-ионы остаются в растворе, например:
Все нитраты термически неустойчивы. При нагревании они разлагаются с образованием кислорода. Подробнее с этими реакциями вы познакомитесь в курсе химии 11-го класса.
Книга была переведена на многие европейские языки, и чуть ли не два столетия оставалась самой популярной научной работой по артиллерии. В свое время по книге Казимира Семеновича учились Ньютон, российский император Петр I и французский император Наполеон I. Основоположник российской космонавтики К. Э. Циолковский ссылался в некоторых своих работах на труды Казимира Семеновича.
Применение азотной кислоты и нитратов:
Азотная кислота широко используется для получения минеральных удобрений, лекарственных препаратов, взрывчатых веществ и ракетного топлива, полимерных материалов, красителей и т. п.
Очень широка и область применения нитратов. Они используются в качестве удобрений, как окислители — в пиротехнических смесях, для производства стекла.
Нитрат серебра(I) 
Нитраты используются для обработки и консервирования пищевых продуктов. Так нитрат натрия NaNO3 в строго определенном количестве добавляют в мясо при изготовлении колбас. Он восстанавливается микроорганизмами до нитрита натрия NaNO2, который препятствует окислению мяса и способствует сохранению розового цвета мясных изделий. Присутствие нитритов в колбасе необходимо еще и по другой причине: они предотвращают развитие микроорганизмов, выделяющих ядовитые вещества.
При копировании любых материалов с сайта evkova.org обязательна активная ссылка на сайт www.evkova.org
Сайт создан коллективом преподавателей на некоммерческой основе для дополнительного образования молодежи
Сайт пишется, поддерживается и управляется коллективом преподавателей
Whatsapp и логотип whatsapp являются товарными знаками корпорации WhatsApp LLC.
Cайт носит информационный характер и ни при каких условиях не является публичной офертой, которая определяется положениями статьи 437 Гражданского кодекса РФ. Анна Евкова не оказывает никаких услуг.