Микрофлора и аутоиммунные заболевания
АУТОИММУННЫЕ ЗАБОЛЕВАНИЯ И КИШЕЧНЫЙ МИКРОБИОМ
ВЗАИМОСВЯЗЬ АУТОИММУНИТЕТА С СОСТОЯНИЕМ КИШЕЧНОГО МИКРОБИОМА

Аутоиммунный процесс (аутоиммунитет) — это форма иммунного ответа, индуцированная аутоантигенами в условиях нормы и патологии.
В широком смысле понятие «аутоиммунные болезни» включает все расстройства, в этиологии и/или патогенезе которых в качестве первичных либо вторичных компонентов участвуют аутоантитела и/или аутосенсибилизированные лимфоциты.
В одних случаях нарушение толерантности является первичным и может быть причиной развития заболевания, в других, особенно при длительных хронических заболеваниях (например, хронический пиелонефрит, хронический простатит и др.), — вторичным и может быть следствием заболевания, замыкая «порочный круг» патогенеза. Нередко у одного больного развивается несколько аутоиммунных заболеваний, особенно это относится к аутоиммунным эндокринопатиям.
Среди заболеваний, которые относятся к данной группе недугов, следует отметить ревматоидный артрит, ряд аутоиммунных заболеваний щитовидной железы. Также аутоиммунным является механизм развития сахарного диабета первого типа, рассеянного склероза, системной красной волчанки. Существуют также некоторые синдромы, которые имеют аутоиммунную природу.
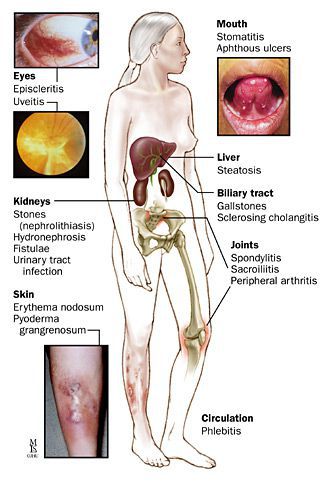
Рис. 1. Аутоиммунные заболевания
На сегодняшний день нет точных сведений и о механизме развития заболеваний такого типа. Согласно общему определению, возникновение аутоиммунных болезней провоцирует нарушение общих функции иммунной системы или же ее некоторых компонентов.
Таблица 1. Аутоиммунные заболевания: список наиболее часто встречающихся и основной патогенез их развития
Болезни ЖКТ (аутоиммунные)
Аутоиммунные заболевания возникают из-за неспецифического ответа иммунитета — он начинает атаковать собственный организм. Могут быть поражены любые ткани и органы, в том числе желудочно-кишечного тракта. Аутоиммунные болезни ЖКТ представлены описанными ниже.
Хронический атрофический гастрит (типа А)
Образование аутоантител против компонентов клеток слизистой оболочки желудка приводит к их функциональным нарушениям, атрофии, гибели и ахлоргидрии. Аутоантитела против париетальных клеток обнаруживаются как в сыворотке крови, так и в желудочном соке ОдА, 1дб. В норме белок, синтезируемый париетальными клетками слизистой желудка, называемый внутренним фактором Касла, связывается с витамином В12, и образовавшийся комплекс транспортируется через слизистую оболочку кишки. Аутоантитела против внутреннего фактора, связываясь с ним, блокируют его и препятствуют переносу витамина В12. Это приводит к развитию витамин В12-дефицитной анемии.
Хронический атрофический гастрит типа А составляет 3-5 % всех форм гастритов. Он сопровождается поражением слизистой оболочки в основном фундального отдела и тела желудка. Происходит гибель желез слизистой оболочки желудка, уменьшается количество главных и обкладочных клеток. Развиваются воспалительные инфильтраты и процессы фиброза.
Хронический атрофический гастрит (типа А) — это аутоиммунное заболевание, ассоциируемое с аутоантителами против внутреннего фактора Касла, а также против главных и париетальных клеток слизистой оболочки желудка.
Симптомы
Заболевание развивается в основном в среднем и пожилом возрасте. После еды появляется ощущение тяжести в надчревной области и переполнения желудка. Аппетит снижен. Отмечается диарея, чередующаяся с запорами. Хронический атрофический гастрит часто сочетается с витамин В12-дефицитной анемией, сахарным диабетом 1-го типа, тиреоидитом, первичным гипопаратиреозом.
Лечение
Проводят заместительную терапию:
1) при секреторной недостаточности желудка (желудочный сок, соляная кислота с пепсином и др.);
2) при снижении экскреторной функции поджелудочной железы (холензим, мезим форте и др.).
Назначают препараты, усиливающие репаративные процессы и т. д. Осуществляют терапию витамин В12-дефицитной анемии. При развитии синдрома дисбактериоза назначают пробиотики.
Целиакия
Патология ассоциирована с HLA-DR3- и Н1_А-В8-антигенами. Расщепление глютенов приводит к образованию глиадинов — пептидов, которые из-за недостаточности пептидаз накапливаются в организме, оказывая на него аллергическое и токсическое действие.
Другой тип гастрита — тип В (хронический хеликобактерный гастрит) — наиболее распространенная патология среди всех видов хронического гастрита, вызванная бактерией Helicobacter pylori. Является важнейшим язвообразующим фактором.
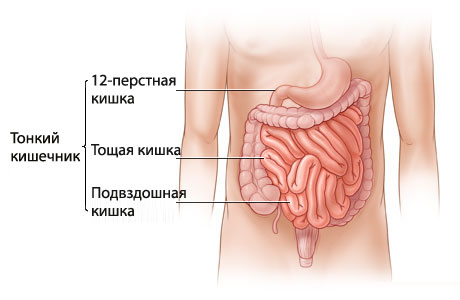
Целиакия (глютеновая энтеропатия) — непереносимость протеинов клейковины (глютенов) пшеницы и других злаков в виде хронического иммунного воспаления верхних отделов тонкой кишки, сопровождающегося атрофией ворсинок, гиперплазией крипт, мальабсорбцией и диареей.
В слизистой оболочке тонкой кишки увеличивается количество клеток, отвечающих за развитие гуморального и клеточного иммунитета: внутриэпителиальных лимфоцитов, плазмоцитов, продуцирующих IgM, эозинофилов и тучных клеток. Появляются антитела против глиадина и антиретикулиновые антитела.
Возрастает количество Т-лимфоцитов, взаимодействующих с глиадином. Сходный патогенез с целиакией актуален в отношении другого глютенчувствительного заболевания — герпетиформного семейного дерматита.
Симптомы
Отмечается упорный понос, обильный пенистый стул, метеоризм, потеря массы тела, анорексия и слабость. Может развиться герпетиформный дерматит.
Лабораторная диагностика
Кожные пробы на глиадин развиваются через 6-8 ч. Изучают биоптаты тощей или двенадцатиперстной кишки. В сыворотке крови выявляются антитела против глиадина. Определяют также антитела против тканевой трансглютаминазы. В результате нарушения проницаемости слизистых оболочек возможно появление антител против различных пищевых антигенов.
Лечение
Применяется безглютеновая диета путем исключения из питания продуктов из пшеницы, ржи, ячменя, овса. По показаниям применяют кортикостероиды и иммунодепрессанты
Неспецифический язвенный колит
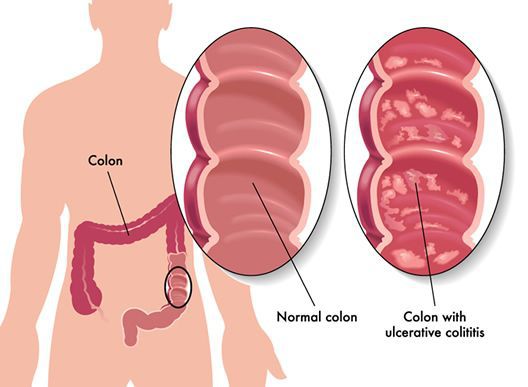
Неспецифический язвенный колит — хроническое рецидивирующее воспалительное заболевание толстой кишки с язвенно-деструктивными изменениями ее слизистой оболочки.
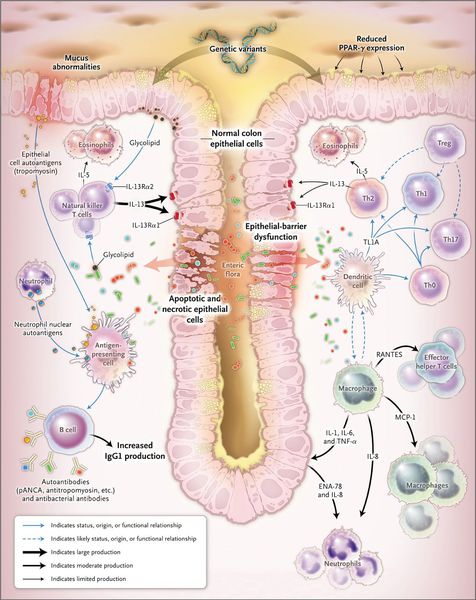
У больных развивается диарея с кровью или слизью и округлые язвы поверхности слизистой оболочки. Происходит инфильтрация собственной пластинки слизистой эозинофилами, лимфоцитами, тучными клетками и нейтрофилами. Процесс распространяется от прямой кишки в проксимальные отделы кишечника. Гиперрегенерация ведет к формированию псевдополипов. Возможно развитие токсического мегаколона и карциномы толстой кишки, а также развитие внекишечных осложнений — увеита и артрита. Неспецифический язвенный колит также ассоциирован с IgА-аутоиммунным гепатитом и первичным билиарным циррозом. Слизистая оболочка имеет высокий уровень ИЛ-5, что предполагает активность Тн2. В пользу аутоиммунной природы заболевания свидетельствует присутствие антинейтрофильных цитоплазматически: антител (А1МСА) и ассоциация с некоторыми аутоиммунными болезнями.
Симптомы
Неспецифический язвенный колит развивается остро в течение 1-2 дней, больных отмечаются три синдрома поражении кишки: нарушение стула, геморрагический болевой синдромы. Возможны внекишечные проявления:
При постепенном развитии заболевания наблюдается в основном только ректальное кровотечение.
Лабораторная диагностика. Тяжесть проявления неспецифического язвенного колита сопровождаются увеличением СОЭ (при редком лейкоцитозе).
Лечение. При остром начале болезни назначают сульфасалазин и аминосалицилаты.
Болезнь Крона (гранулематозный колит)
Это хроническое гранулематозное сегментарное воспаление пищеварительного тракта в виде терминального илеита или регионарного энтероколита
Воспалительный процесс развивается сегментарно: пораженные сегменты кишки чередуются с непораженными участками («прыжки кенгуру»). Чаще в процесс вовлекается терминальный отдел подвздошной кишки (терминальный илеит). Реже одновременно повреждаются тонкая и толстая кишки. Воспаление захватывает все слои стенки кишки. В толще стенки образуются лимфоцитарные гранулемы, гранулемы, включающие гигантские и эпителиоидные клетки, абсцессы и глубокие проникающие язвы, из-за чего слизистая оболочка приобретает вид «булыжной мостовой». Формируются стеноз и воспалительные конгломераты. Кишка деформируется, приобретая вид «садового шланга». Возможно образование кишечных свищей.
Симптомы
При остром начале болезни развиваются симптомы региональной энтерита в виде резкой боли в правой подвздошной области и лихорадки. Возможны явления острого аппендицита.
Чаще наблюдается постепенное нарастание нарушений: схваткообразная боль в животе, периодически неустойчивый стул и другие функциональные нарушения. В разгаре болезни развиваются упорные поносы, а иногда — запоры. Возможна длительная ремиссия. Токсико-аллергические осложнения чаще наблюдаются при локализации процесса в толстой кишке.
Лабораторная диагностика
В пользу болезни Крона свидетельствует наличие в сыворотке крови пациента антител к пищевым аллергенам и к условно патогенным бактериям-комменсалам кишечника. Могут появляться также анти тела против поверхностных структур эпителиоцитов кишки.
Лечение
При обострении назначают сульфасалазин, аминосалицилаты (месалазин, олсалазин) и/или кортикостероиды. В течение ремиссии больные мо гут получать комбинацию из азатиоприна, метотрексата и циклоспорина А. Возможно хирургическое вмешательство (по решению лечащего врача).
Аутоиммунные заболевания кишечника (болезнь Крона, язвенный колит) и желудка
Аутоиммунный гастрит.
Аутоиммунный гастрит относится к частым аутоиммунным заболеваниям и наиболее частым аутоиммунным заболеванием желудочно-кишечного тракта (ЖКТ). Этому заболеванию в 30% случаев сопутствуют другие аутоиммунные патологические состояния: аутоиммунные заболевания щитовидной железы, алопеция и витилиго. Аутоиммунный гастрит протекает субклинически и редко является поводом обращения пациентов к врачу. В его основе лежит аутоиммунная реакция, направленная против обкладочных (париетальных) клеток желудка, а также против внутреннего фактора (фактора Кастла). Обкладочных клеток больше в теле желудка, поэтому обычно аутоиммунный гастрит проявляется атрофией фундальных отделов, по сравнению с антральным гастритом при инфекции Helicobacter pylori. Для деффиринцаильной диагностики гастрита, ассоциированного с аутоиммунной реакцией и связанного с инфекцией Helicobacter pylori, используется тест Серологическое обследование гастритов типов А и В. Обкладочные клетки желудка вырабатывают соляную кислоту и внутренний фактор Кастла, необходимый для всасывания витамина В12 в кишечнике. Уничтожение обкладочных клеток ведет к гипоацидному гастриту, мальабсорбции, железодефицитной и пернициозной анемиям.
Антитела к обкладочным (париетальным) клеткам желудка.
Париетальные (обкладочные) клетки желудка вырабатывают соляную кислоту и внутренний фактор Кастла, необходимый для всасывания витамина В12 (кобаламина) в кишечнике. Основным антигеном антител к париетальным клеткам желудка (АПКЖ) является бета-субъединица Н+/К+ АТФ-азы, мембрано-ассоциированного ионного насоса, который участвует в закислении содержимого желудка. Аутоантитела являются комплемент-фиксирующими и непосредственно участвуют в разрушении популяции обкладочных клеток и развитии атрофического гастрита. Не отмечается взаимосвязи между обнаружением аутоантител к париетальным клеткам желудка и антральным гастритом, основной этиологической причиной которого является инфекция Helicobacter pylori. Титры аутоантител не коррелируют с тяжестью атрофии слизистой желудка, поэтому их мониторинг не целесообразен. Антитела к обкладочным клеткам желудка отмечаются у 90% больных с атрофическим гастритом и пернициозной анемией. Другие проявления дефицита витамина В12, обусловленные аутоиммунным гастритом, включают полиневрит, фуникулярный миелоз, атаксию, истощение мышц и снижение рефлексов. Нарушение закисления желудка приводит также к нарушению всасывания железа в тонком кишечнике, поэтому аутоиммунный гастрит, связанный с присутствием аутоантител к парительным клеткам желудка, может также приводить к развитию железодефицитной анемии с характерной клиникой этого состояния. Макроцитарная анемия обусловлена дефицитом эритропоэза в связи с нехваткой витамина В12. Анемия развивается через несколько лет после развития аутоиммунного гастрита, поскольку в норме в печени человека сохраняется значительный запас витамина. Анемия проявляется увеличением среднего размера эритроцита, повышением цветного показателя, характерными изменениями нейтрофилов, низким количеством ретикулоцитов, тромбоцитопенией и лейкопенией. Кроме того отмечается мегалобластная трансформация в костном мозге.
Антитела к внутреннему фактору (фактору Кастла).
Внутренний фактор (фактор Кастла) представляет собой гликопротеин массой 72 кДа, который секретируется в просвет желудка и связывает и транспортирует в стенку кишки витамина В12 (кобаламина). Аутоантитела к внутреннему фактору способны вызывать нарушение его функции как за счет блокады его связывания с витамином, так и препятствуя адсорбции комплекса в тонком кишечнике. Антитела к внутреннему фактору являются более специфичными по сравнению с антителами к парительным клеткам желудка при диагностике пернициозной анемии и дефицита витамина В12, однако встречаются только у 60% больных с аутоиммунным гастритом.
Комплексная оценка аутоантител при подозрении на аутоиммунный гастрит позволяет повысить точность лабораторной диагностики данного состояния (Диагностика гастрита типа А и пернициозной анемии).
Диагностика воспалительный заболеваний кишечника (болезнь Крона и язвенный колит).
Болезнь Крона (БК) и язвенный колит (ЯК) представляют собой хронические, рецидивирующие, идиопатические расстройства ЖКТ. При этом БК характеризуется иммунным, трансмуральным, сегментарным, гранулематозным воспалением ЖКТ различной протяженности от полости рта до анального отверстия, с развитием местных и системных осложнений, а ЯК — поражением только толстой кишки с обязательным вовлечением прямой, и воспаление при этом чаще всего ограничивается слизистой оболочкой кишечника и носит диффузный характер. Болезнь Крона и язвенный колит представляют собой наиболее частые формы ВЗК в европейской популяции и за последние несколько лет наблюдается стабильное повышение заболеваемости и распространенности данных заболеваний в развитых и развивающихся странах (5,6 на 100,000 в год в некоторых странах Европы). По данным Американского центра по эпидемическому контролю болезней примерно 1,4 млн. человек популяции США страдают от воспалительных заболеваний кишечника. В Германии распростраенность оценивается в пределах 1/500 до 1/800 взрослого населения. В Санкт-Петербурге по данным городского центра ВЗК на учете стоит 5,500 пациентов. Диагноз БК и ЯК, согласно международным и отечественным клиническим рекомендациям по диагностике и лечению ВЗК, устанавливается на основании всесторонней оценки клинической картины заболеваний, данных эндоскопических, радиологических, гистологических и лабораторных методов исследований. В 2011 году были опубликованы данные, рекомендующие рутинное использование панелей серологических маркеров для диагностики или мониторинга ВЗК в клинической практике. Но аутоантитела при ВЗК имеют ограниченную диагностическую ценность в первичной диагностике вследствие их низкой чувствительности.
Серологические маркеры диагностики болезни Крона. Антитела к пекарским дрожжам Sacchаromyces cerevisiae и антитела к экзокринной части поджелудочной железы и антигену GP2.
Антитела к пекарским дрожжам Sacchаromyces cerevisiae (ASCA) являются основным лабораторным маркером болезни Крона. Кроме антител к антигенам пекарских дрожжей, при болезни Крона появляются антитела к другим комменсальным организмам ЖКТ. Так, при этом заболевании появляются антитела антигенам кишечной палочки, псевдомонад, а также антигенам полисахаридной стенки многих микроорганизмов. Основными иммуногенными эпитопами антител к сахаромицетам являются также компоненты полисахаридов, в том числе маннотетроза и маннотриоза.
Антитела к сахаромицетам выявляются при болезни Крона с частотой, составляющей около 50% (30-70%). Антитела могут быть представлены IgG или IgA, обладая общей специфичностью для диагностики болезни Крона составляющей 93%. Частота выявления ASCA не зависит от географического района и демографии обследованных групп, что указывает на универсальность иммунологического механизма, лежащего в основе иммунной реакции против клеток сахаромицет. Характерно, что антитела к сахаромицетам часто отмечаются у родственников больных воспалительными заболеваниями кишечника (20-25%). У клинически здоровых лиц ASCA могут быть выявлены у 1-3% лиц общей популяции. При болезни Крона антитела к сахаромицетам могут появляться до клинического дебюта заболевания. При болезни Крона у пациентов с ASCA заболевание течет тяжелее, что связано с частыми эпизодами кишечной непроходимости, кроме того заболевание лучше отвечает на терапию блокаторами фактора некроза опухоли-альфа. В то же время, титры антител не коррелируют с клинической активностью процесса. Антитела к сахаромицетам могут использоваться для дифференциальной диагностики болезни Крона и неспецифического язвенного колита, поскольку встречаемость антител у больных с язвенным колитом не превышает 10%. Редко ASCA встречаются при первичном билиарном циррозе, первичном склерозирующем холангите, целиакии. Отсуствие антител к сахаромицетам (ASCA) не исключает вероятности болезни Крона.
Антитела к центроацинарным клеткам реагируют с цитоплазмой ацинарных клеток поджелудочной железы или с глобулярными структурами в протоках поджелудочной железы. Причина появления антител к ацинарным клеткам при БК остается неизвестной. Поражение поджелудочной железы иногда отмечается при ВЗК, однако не обнаружено взаимосвязи между панкреатитом и появлением антител к панкреоцитам. Вероятно, это связано с преимущественной экскрецией большинства антигенов в составе сока поджелудочной железы. Описано несколько антигенов ацинарных клеток, в частности гликопротеин GP2, который экскретируются поджелудочной железой в просвет кишечника. Антитела к экзокринной части поджелудочной железы отмечаются у 10-20% пациентов с болезнью Крона, несколько чаще у сравнительно молодых пациентов. Крайне редко антитела к центроацинарным клеткам поджелудочной железы могут отмечаться при других заболеваниях ЖКТ. Обнаружение антител к экзокринной части поджелудочной железы указывает на высокую вероятность БК и требует углубленного клинического и инструментального обследования. В сочетании с другими клиническими, инструментальными и лабораторными находками выявление антител позволяет поставить диагноз БК.
Изучение антигенных мишеней антител к центроацинарным клеткам привело к описанию белка GP2 (гликопротеина 2 типа) который является основным антигеном экскреторных гранул зимогенов. Обладая высокой структурной гомологией с белком Тамм-Хорсфала в моче, гликопротеин GP2 в просвете кишечника выполняет антибактериальную функцию, связываясь с фимбриями бактерий. Кроме того гликопротеин GP2 обладает антиапоптотическим и пролиферативным действием на энтероциты, таким образом, выступая в качестве протективного фактора. Антитела к GP2 классов IgGи IgA отмечаются у 30-35% пациентов с болезнью Крона, независимо от присутствия ASCA, поэтому совместное использование обоих маркеров позволяет выявить серологические признаки заболевания у 60-70% пациентов. Антитела к GP2 чаще отмечаются у более молодых больных.При БК антитела к GP2 антигену отмечаются при илиоколите, стриктурирующей формах заболевания с частым перианальным воспалением. Антитела к GP2 редко отмечаются у больных с неспецифическим язвенным колитом и менее чем у 3% здоровых лиц. Антитела к GP2 могут отмечаться при других заболеваниях ЖКТ, в том числе целиакии.
Серологические маркеры диагностики язвенного колита. Антитела к цитоплазме нейтрофилов (АНЦА) IgA и Антитела к бокаловидным клеткам кишечника (БКК).
Антинейтрофильные цитоплазматические антитела (АНЦА) были впервые описаны при гранулематозных васкулитах. При системных васкулитах в качестве основных антигенов антинейтрофильных антител выступает ряд ферментов содержащихся в азурофильных гранулах нейтрофилов. К известным антигенным мишеням АНЦА относятся протеиназа-3, миелопероксидаза, лактоферрин, эластаза, белок BPI и катепсин G. Антинейтрофильные антитела также используются в качестве диагностических маркеров при воспалительных заболеваниях кишечника, однако при этих заболеваниях большинство антигены аутоантител плохо изучено. Метод непрямой иммунофлюоресценции остается «золотым стандартом» выявления антинейтрофильных антител, поскольку позволяет определить как частые антигены (такие как протеиназа-3 или миелопероксидаза), так и редкие мишени аутоантител, которые охарактеризованы недостаточно хорошо. Для клинической диагностики воспалительных заболеваний кишечника целесообразно дополнять выявление антинейтрофильных антитела класса IgA выявлением антинейтрофильных цитоплазматических антител класса IgG.
Антитела к цитоплазме нейтрофилов часто отмечаются при аутоиммунной патологии желудочно-кишечного тракта. Они встречаются при язвенном колите (70%), болезни Крона (2-7%), аутоиммунном гепатите (50%), первичном склерозирующем холангите (40%), первичном биллиарном циррозе (5%), болезни Шенлейн-Геноха (70%) и васкулитах при ревматоидном артрите (5-10%). При неспецифическом язвенном колите выявление высоких титров антинейтрофильных антител отмечается у больных с тяжелым течением заболевания. Повышенный титр АНЦА IgA указывает на вероятный диагноз язвенного колита и ассоциированного с ним первичного склерозирующего холангита.
Бокаловидные клетки кишечника (БКК) вырабатывают слизь, которая защищает слизистую кишки от агрессивных факторов содержимого кишки. Такие клетки, имеющие форму чаши (бокала), можно обнаружить во всех отделах кишечника, однако их число максимально в прямой кишке, особенно в криптах толстого кишечника. Основным антигеном БКК являются муцины – семейство гликопротеинов, состоящие из белка и углеводной последовательности. Как центральный белок, так и углеводная цепь являются мишенью антител при неспецифическом язвенном колите (НЯК).
Наличие антител к БКК тесно связано с язвенным колитом. Антитела к БКК часто отмечаются у пациентов с ЯК 15-40%, редко встречаются при болезни Крона, других орган-специфических аутоиммунных заболеваниях и очень редко у здоровых лиц. Также антитела к БКК могут встречаться при аутоиммунной энтеропатии – редком состоянии, связанном со снижением числа бокаловидных клеток, виллезной атрофией и воспалением в тонком кишечнике. Аутоиммунная энтеропатия проявляется рецидивирующией диареей, нарушением всасывания, кроме того она часто бывает связана с другими аутоиммунными заболеваниями и полиэндокинопатиями. Другим важным серологическим тестом на аутоиммунную энтеропатию является Определение антител к энтероцитам методом непрямой иммунофлюоресценции для диагностики аутоиммунной энтеропатии.
Что такое неспецифический язвенный колит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Куракин А. А., проктолога со стажем в 10 лет.
Определение болезни. Причины заболевания
Неспецифический язвенный колит (или просто язвенный колит) — хроническое воспаление толстой кишки аутоиммунного характера. Данное заболевание относится к группе воспалительных заболеваний толстого кишечника.
Эпидемиология
Заболевание преобладает в развитых странах Европы и Северной Америки. Язвенный колит встречается в 20-260 случаев на 100 000 человек. С каждым годом число заболевших увеличивается. [2]
Чаще всего болеют лица в возрасте от 21 до 42 лет, а также пациенты после 54 лет. Самые опасные периоды в развитии язвенного колита — это первый год болезни (из-за быстрого развития воспаления при фульминантном течении появляются осложнения, опасные для жизни) и десятый год (за этот период развиваются злокачественные новообразования).
Факторы риска до сих пор до конца не изучены. Существует следующая закономерность:
Этиология
Происхождение язвенного колита на сегодняшний день неизвестно. Существуют следующие теории развития заболевания:
Симптомы неспецифического язвенного колита
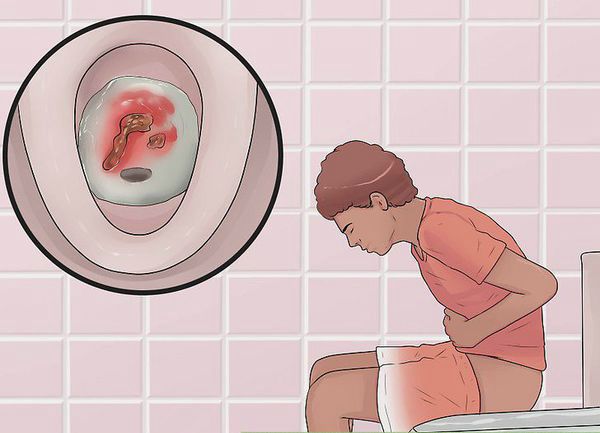
Первые признаки заболевания: кровь и слизь в стуле, диарея, боли в животе, повышение температуры тела.
Основными симптомами неспецифического язвенного колита кишечника являются:
Заболевание хроническое — симптомы возникают только при обострении, при ремиссии их может не быть.
Характер преобладающей симптоматики зависит от тяжести заболевания и вовлечённого в воспалительный процесс отдела толстого кишечника. Например, при тотальном поражении наблюдается частый жидкий стул с большим количеством крови в кале, боли в животе спастического характера. При тяжёлом течении присоединяются симптомы общей интоксикации (лихорадка, тошнота, рвота, слабость).
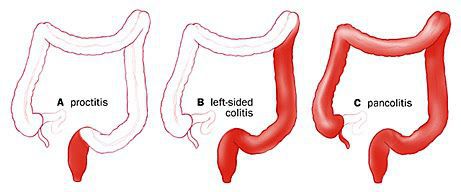
При поражении дистальных отделов толстого кишечника (проктит) чаще возникает запор, ложные позывы на дефекацию, тенезмы, в кале обнаруживаются следы алой крови, слизи или гноя. Для оценки тяжести язвенного колита предложены критерии Truelove и Witts.
Патогенез неспецифического язвенного колита
При язвенном колите происходит каскад воспалительных реакций. В результате воздействия триггерного (инициирующего) фактора стимулируются Т- и В-лимфоциты, что, в свою очередь, приводит к образованию иммуноглобулинов М и G. Дефицит Т-супрессоров усиливает аутоиммунный ответ. Образование иммуноглобулинов М и G приводит к появлению иммунных комплексов и активации сиcтемы комплемента, который обладает цитотоксическим действием. В очаг воспаления проникают нейтрофилы и фагоциты, при этом высвобождаются медиаторы воспаления.
Одним из механизмов патогенеза язвенного колита является нарушение барьерной функции слизистой оболочки толстой кишки и регенераторной функции.
Реакция организма на стресс с патологическим нейрогуморальным ответом приводит к активизации аутоиммунного процесса. Часто больные язвенным колитом имеют эмоциональную нестабильность.
Классификация и стадии развития неспецифического язвенного колита
По распространённости процесса различают:
По степени тяжести течения: [3]
По характеру течения:
Язвенный колит — это хроническое заболевание, при котором бывают периоды, когда возникает обострение и периоды, когда симптомы затухают или не выявляются — стадия ремиссии. Язвенный колит может обостряться без явной причины, однако чаще это происходит под воздействием стресса, неправильного питания и приёме некоторых лекарств.
Осложнения неспецифического язвенного колита
Местные осложнения
К местным осложнениям относятся:
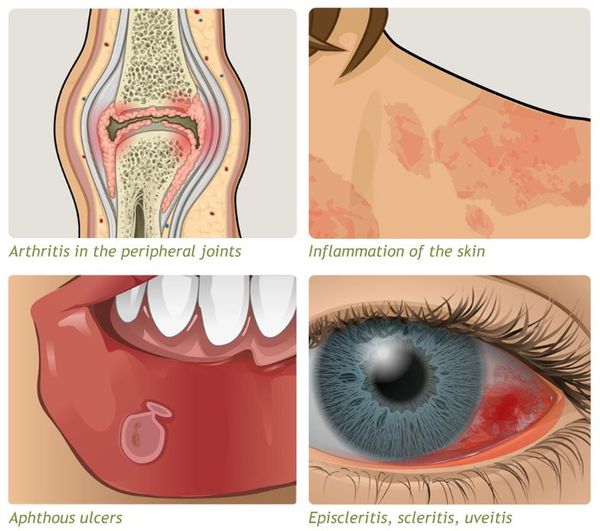
Системные осложнения
Проявляются внекишечными симптомами, причина которых до сих пор не изучена. Чаще поражаются ротовая полость, кожа, суставы.
К системным осложнениям относятся:
Диагностика неспецифического язвенного колита
При диагностике в первую очередь оценивается клиника заболевания, анамнез, производится осмотр с обязательным пальцевым исследованием прямой кишки.
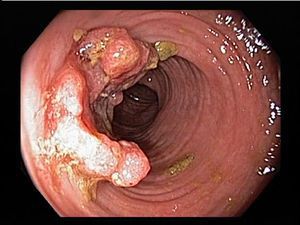
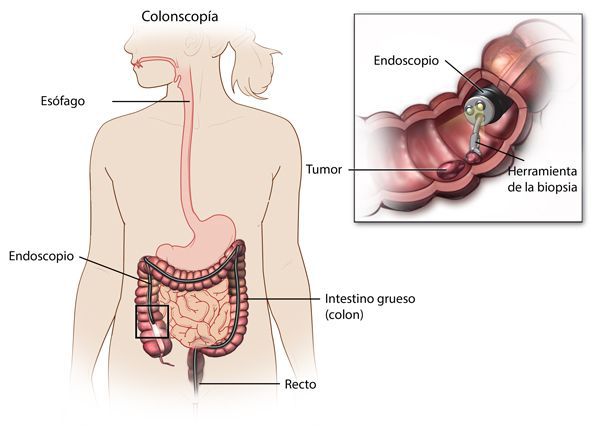
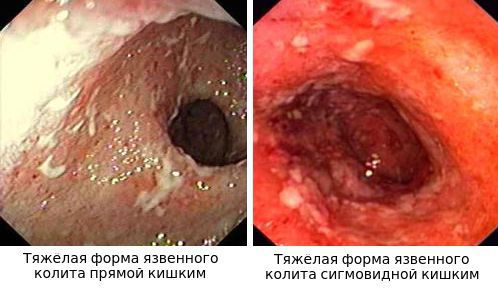
Наиболее важными в диагностике язвенного колита являются эндоскопические методы исследования: ректороманоскопия, колоноскопия с биопсией. Так же для уточнения диагноза применяются ирригоскопия, МСКТ-колоноскопия.
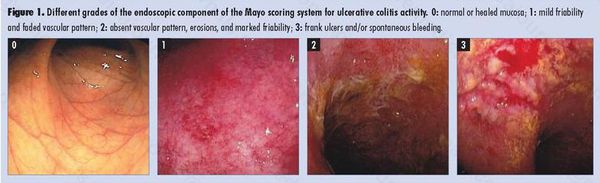
По эндоскопической картине можно определить степень воспаления толстого кишечника. Существуют четыре степени воспаления кишечника:
Язвы не проникают глубже подслизистого слоя.
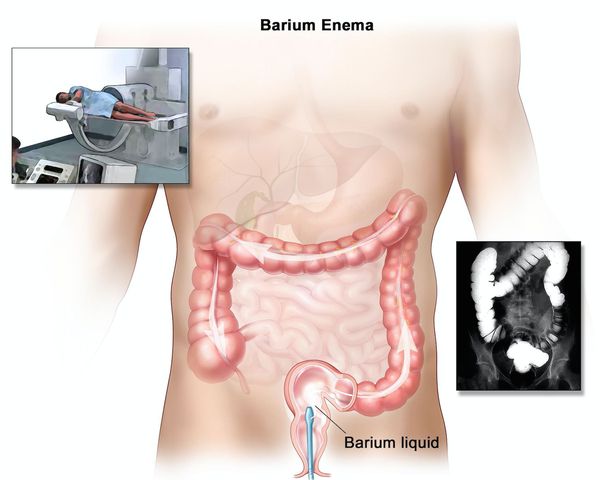
При рентгенологическом исследовании определяется:
Ирригоскопия помогает не только в диагносте язвенного колита, но и в выявлении серьёзных осложнений, таких как токсическая дилатация (чрезмерное расширение просвета толстой кишки).
Дифференциальный диагноз:
Лечение неспецифического язвенного колита
Тактика зависит от локализации поражения и тяжести течения. При дистальных формах заболевания течение обычно лёгкое, поэтому больные могут лечиться в амбулаторных условиях. Тотальное или левостороннее поражение чаще имеет тяжёлое течение, поэтому требует госпитализации и лечения в условиях стационара.
Диета
Назначаются диеты № 4, 4Б, 4В по Певзнеру. Цель диеты — уменьшить воспаление, бродильные и гнилостные процессы в кишечнике, нормализовать функции кишечника и других органов пищеварения. Блюда жидкие, полужидкие, протёртые, сваренные в воде или на пару. Исключены очень горячие и холодные блюда.
Разрешённые при язвенном колите продукты:
Запрещенные при язвенном колите продукты:
Консервативная терапия
К консервативной терапии относятся:
Аминосалицилаты являются препаратами первой линии и применяются в первую очередь. Для купирования атаки язвенного колита обычно требуется 3-6 недель терапии по 1-2 г/кг в сутки. После этого проводится противорецидивное лечение сульфасалазином (3 г/сут) или месалазином (2 г/сут).
При дистальном поражении (проктит) отдаётся предпочтение формам препарата в виде свечей. При левостороннем поражении — препаратам в форме пены для ректального применения. При тотальном поражении используют таблетированные формы препаратов.
При лечении данными препаратами ремиссия достигается в 74-81 % случаев.
Наиболее выраженным и эффективным противовоспалительным средством являются глюкокортикоиды.
Основными показаниями для лечения глюкокортикоидами являются:
При остром тяжёлом течении назначают внутривенное введение глюкокортикоидов (преднизолона не менее 120 мг/сут) 4-6 раз в день. Обязательно проводится коррекция водно-электролитного баланса, переливание компонентов крови, гемосорбция. Через неделю после внутривенного введения переходят на приём преднизолона внутрь. За это время проводится гастроскопия для исключения язвенной болезни желудка и двенадцатиперстной кишки.
При среднетяжёлой форме можно ограничиться пероральным приёмом преднизолона. Обычно преднизолон назначается в дозе 1,5-2 мг/кг массы тела в сутки. Максимальная доза 100 мг (у лиц пожилого возраста 60 мг).
Если отсутствуют побочные эффекты, то приём продолжают ещё 10-14 дней, затем снижают дозу на 10 мг каждые 10 дней. С 30-40 мг переходят на однократный приём преднизолона. С 30 мг дозу снижают по 5 мг в неделю. Обычно курс гормональной терапии составляет от 8 до 12 недель. Параллельно с гормонотерапией применяют аминосалицилаты до полной отмены гормонов.
При проктите применяются глюкокортикоиды ректально в микроклизмах. Обычно для этого используют гидрокортизон, применяют после дефекации 2 раза в день.
Побочные эффекты гормонотерапии:
Современным глюкокортикоидом является буденофальк (содержащий будесонид). Суточная доза составляет 3 мг будесонида (1 капсула) 4-6 раз в сутки.
При лечении глюкокортикоидами может возникнуть гормональная зависимость или даже гормонорезистентность, которая формируется у 20-35 % больных тяжёлым язвенным колитом. Гормональная зависимость — это ответ организма на лечение глюкокортикоидами, при котором возобновляется воспалительный процесс после снижения дозировки.
При отсутствии эффекта от гормональной терапии назначают препараты, обладающие иммуносупрессивным действием, а также биологическую терапию. Основными из них являются 6-меркаптопурин и азатиоприн — это препараты первой линии. Они помогают уменьшить дозу гормонов и отменить их в 62-71 % случаев. Лечение обычно начинают вместе с гормонотерапией. Максимальная суточная доза — 150 мг. Незначительное количество побочных эффектов, по сравнению с глюкокортикоидами, позволяет применять препарат на протяжении многих лет.
Также существует аналогичный препарат — метотрексат, который применяется при непереносимости азатиоприна или для ускорения лечебного эффекта. Внутрь или внутримышечно по 30 мг в неделю. Эффект наступает через 2-4 недели
Если отсутствует эффект от азатиоприна и 6-меркаптопурина, применяют препараты второй линии — это инфликсимаб и циклоспорин А.
При отсутствии эффекта от второго введения инфликсимаба и 7-дневного курса циклоспорина А показано хирургическое лечение.
Противорецидивное лечение
После купирования острых воспалительных процессов, назначают противорецидивную терапию аминосалицилатами на срок до 6 месяцев. В случае успешного лечения и отсутствии клинических и эндоскопических признаков заболевания, терапию отменяют.
В случае нестабильного эффекта от противорецидивного лечения терапию продлевают дополнительно сроком на 6 месяцев.
При неэффективности монотерапии аминосалицилатами добовляют к лечению иммуносупрессоры (азатиоприн или 6-меркаптопурин) и гормоны.
Пациентам с язвенным колитом, получающих консервативную терапию, необходимо постоянное наблюдение врача, регулярное эндоскопическое исследование с биопсией.
Хирургическое лечение
По статистике хирургическое лечение показано больным в 11-22 % случаев. Единственным способом радикального хирургического лечения язвенного колита является колпроктэктомия, то есть удаление всей толстой кишки. Основными показаниями к хирургическому лечению являются:
Послеоперационные осложнения
Возникают у ослабленных пациентов на фоне тяжёлого течения заболевания:
Особенности лечения в зависимости от формы и течения
Левосторонний колит или проктит низкой активности: свечи и пена салофальк.
Колит умеренной активности или распространённый: салофальк в таблетках, глюкокортикоиды.
Тяжёлое течение: салофальк в таблетках, глюкокортикоиды, инфузионная терапия, препараты железа, переливание плазмы и эритроцитарной массы, колпроктэктомия (удаление всей толстой кишки с формированием постоянной илеостомы — отверстия в брюшной полости, к которому прикрепляют калоприёмник).
Фульминантный колит: лечение такое же как и при тяжёлом течении.
Прогноз. Профилактика
При несвоевременном хирургическом лечении в послеоперационном периоде присоединяются другие осложнения в 59-81 % случаев, а летальность составляет от 11 до 49 %. При хирургическом лечении до возникновения тяжёлых кишечных осложнений (перфорация, токсическая дилатация и т. д.) эти цифры снижаются до 8-12 % и 0,5-1,5 % соответственно.
Таким образом, правильная диагностика, рациональная консервативная терапия и своевременное хирургическое лечение помогают добиться хороших результатов. В таком случае прогноз благоприятный. Но, в связи с длительным периодом нетрудоспособности, многие пациенты нуждаются в медико-социальной экспертизе и оформлении инвалидности.