Атипичная резекция легкого что это
а) Показания для атипичной торакоскопической резекции легкого:
— Плановые: удаление ограниченных патологических очагов, расположенных на поверхности легкого. Резекция показана после первого рецидива спонтанного пневмоторакса.
— Противопоказания: предшествующая торакальная операция или диффузное заболевание, поражающее все легкое.
— Альтернативные операции: торакотомия с атипичной резекцией/лобэктомией/пульмонэктомией.
б) Предоперационная подготовка:
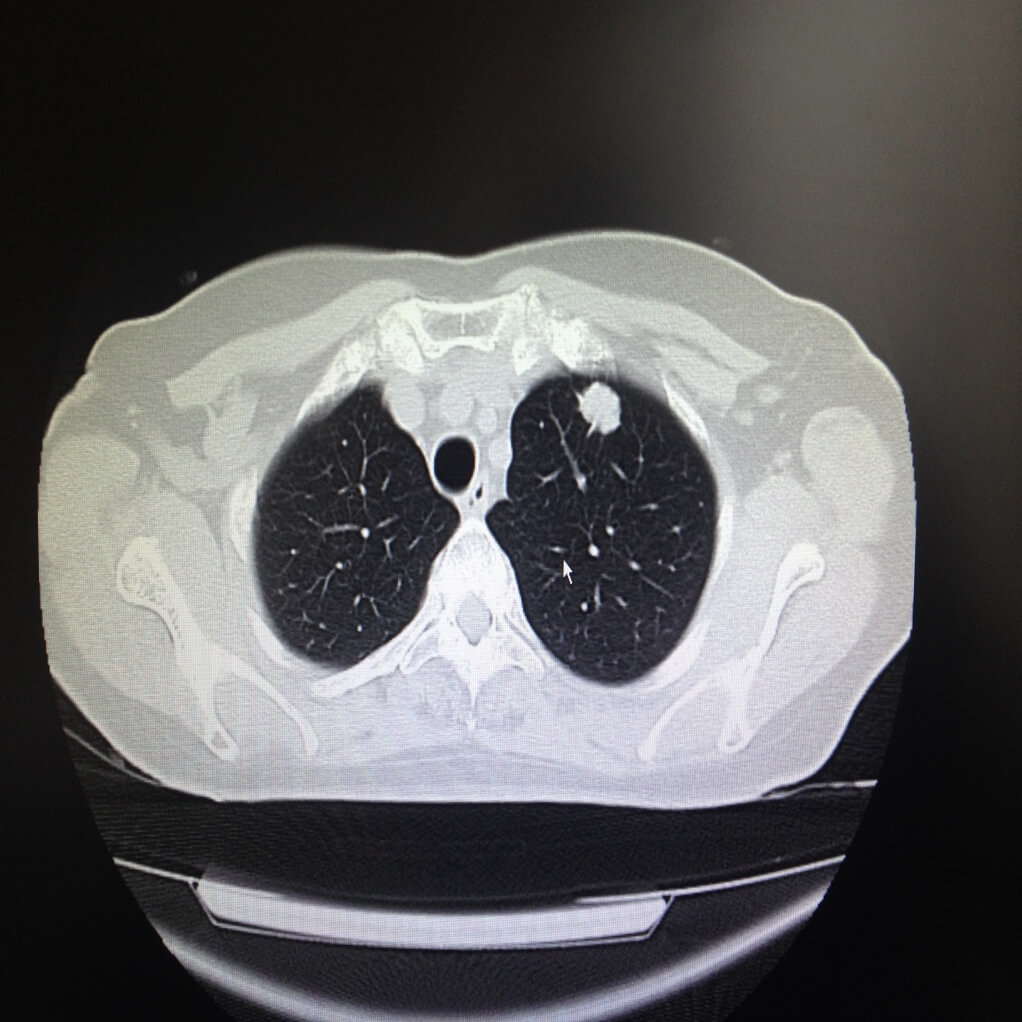
— Предоперационные исследования: рентгенография органов грудной клетки, компьютерная томография, подумайте об исследовании функции внешнего дыхания.
— Подготовка пациента: начало лечения с дренированием плевральной полости.
в) Специфические риски, информированное согласие пациента:
— Рецидив после удаления буллы или пузыря (менее 10% случаев)
— Кровотечение
— Подкожная эмфизема
— Инфекция (местная, эмпиема, пневмония)
— Повреждение нервов (межреберных, синдром Горнера)
— Может потребоваться переход к торакотомии
г) Обезболивание. Общее обезболивание (интубация).
д) Положение пациента. На боку, рука располагается горизонтально на уровне плеча.
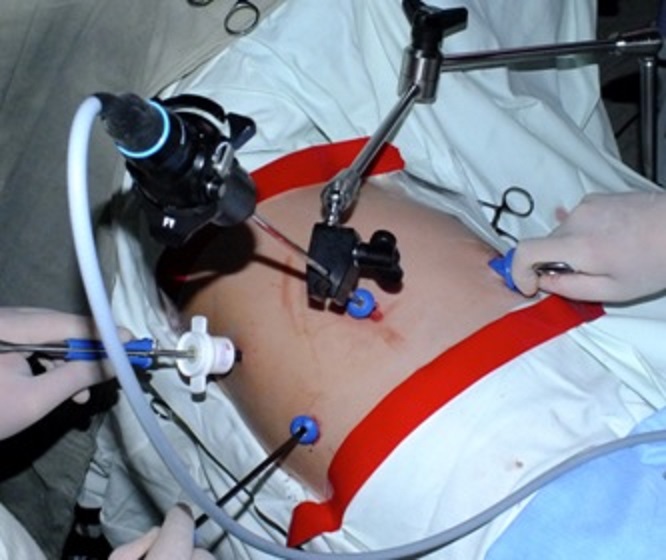
е) Доступ при торакоскопической атипичной резекции легкого. В подмышечном треугольнике, где мышечной ткани меньше: передний край широчайшей мышцы спины в пятом межреберье, под эндоскопическим контролем в седьмом межреберье по средней подмышечной линии, а также в пятом межреберье по заднему краю большой грудной мышцы.
ж) Этапы торакоскопической атипичной резекции легкого:
— Расположение, хирургическая бригада, доступы
— Клиновидное иссечение
— Проверка герметичности
— Дренаж
з) Анатомические особенности, серьезные риски, оперативные приемы:
— Небольшие пузыри можно перевязать у основания эндопетлей и иссечь.
— Плевродез: выскабливание париетальной плевры в области верхней грудной апертуры тупфером (абразионная техника) или аргоновоплазменная коагуляция. Альтернатива: выполнение плеврэктомии.
и) Меры при специфических осложнениях. При наличии выраженного утолщения плеврального покрова, плохом обзоре или кровотечении перейдите к открытой операции.
к) Послеоперационный уход после торакоскопической атипичной резекции легкого:
— Медицинский уход: пережмите плевральные дренажи и удалите их через 2 дня (предварительное условие: отсутствие утечки воздуха).
— Активизация: немедленно.
— Период нетрудоспособности: 2 недели.
л) Оперативная техника торакоскопической атипической резекции легкого:
— Положение пациента, хирургическая бригада, доступы
— Клиновидное иссечение
— Проверка герметичности
— Дренаж
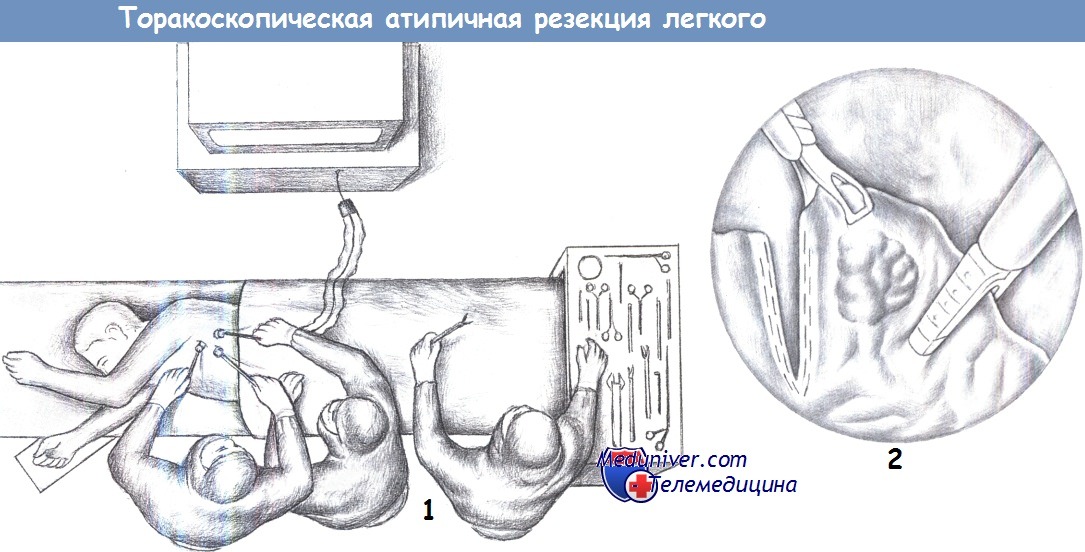
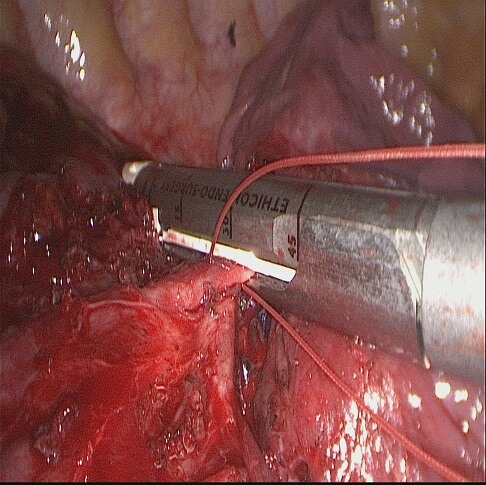
2. Клиновидное иссечение. Поверхностные узелки резецируются сшивающим аппаратом Endo-GIA. Для более глубоких узлов рекомендуется клиновидное иссечение двумя или более кассетами сшивающего аппарата Endo-GIA. Клиновидные иссечения нужно планировать так, чтобы вся иссеченная паренхима могла бы быть герметизирована и ушита аппаратом. Резецированный препарат извлекается в контейнере через место введения троакара.
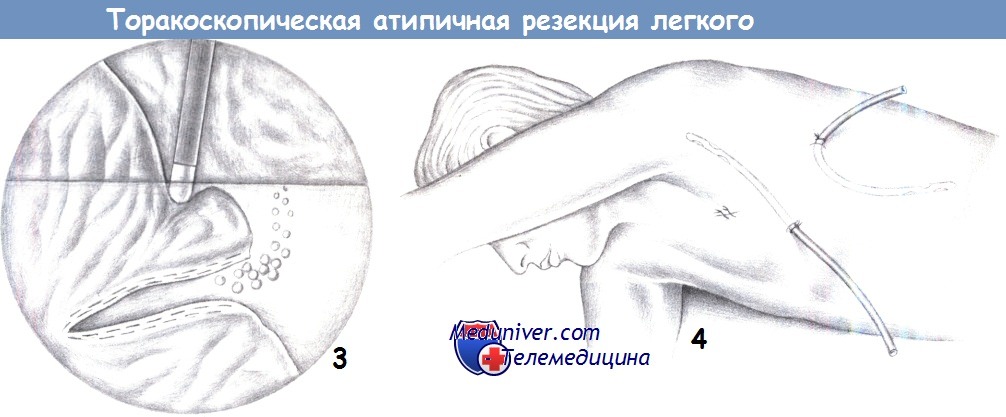
3. Проверка герметичности. Чтобы оценить проникновение воздуха через линию резекции после завершения прошивания аппаратом, рекомендуется проверка герметичности при заполнении плевральной полости водой. Для этого отключенное легкое нужно снова соединить с вентиляционной системой.
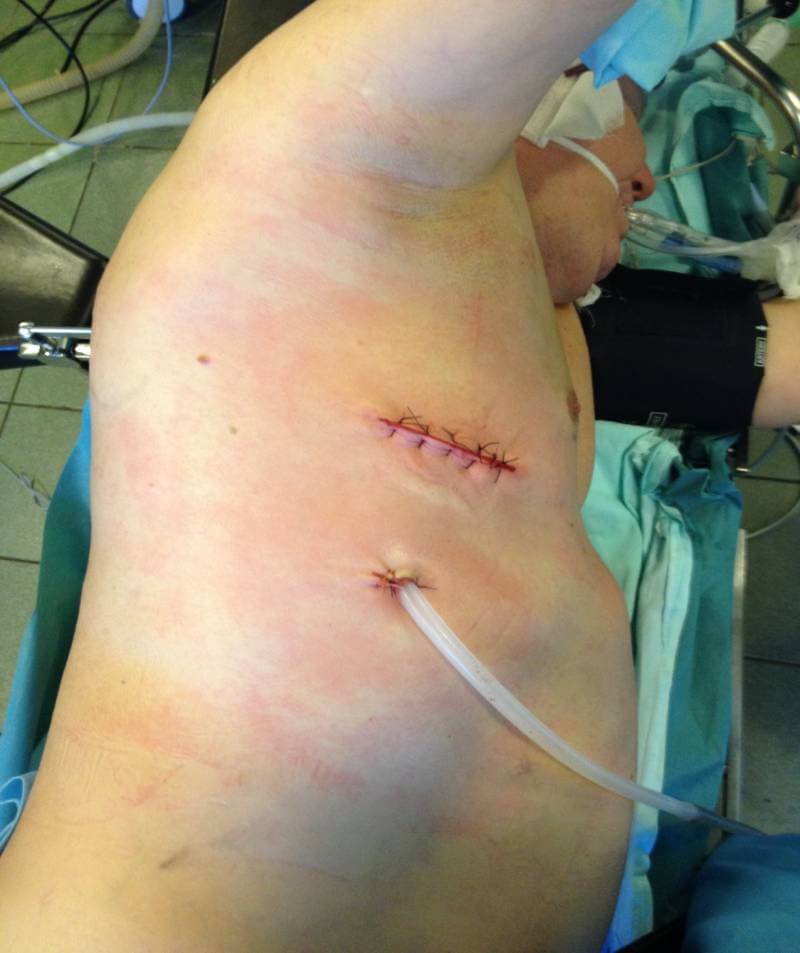
4. Дренаж. После расправления легкого, через места введения троакаров устанавливаются один или два плевральных дренажа.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Торакоскопические резекции легких
Важным принципом хирургического лечения рака является выполнение минимально травматичных операций, с тем, чтобы по возможности сохранить функции пораженного органа и сократить послеоперационный период. Это достигается широким применением малоинвазивных и органосохраняющих методик, преимущества которых очевидны и не вызывают сомнений ни у врачей, ни у пациентов. Большинство урологических, гинекологических и иных операций на органах брюшной полости давно уже выполняются с использованием лапароскопической техники, которая стала «золотым стандартом» современной хирургии.
Внедрение эндоскопических технологий в торакальной хирургии происходило значительно медленнее, и долгое время ограничивалось выполнением небольших диагностических операций (биопсии плевры, краевые резекции лёгких, дренирования плевральной полости). Это связано с особенностями анатомии грудной стенки (жесткий реберный каркас, ограничивающий свободу манипуляций), сложной анатомией легких и средостения (наличие близкорасположенных крупных сосудов, сокращения сердца), а также отсутствием одной несложной типовой операции (холецистэктомия в абдоминальной хирургии), которая бы позволила детально отработать эндоскопическую технику.
Хирургические вмешательства на легких и органах средостения сложны и требуют от хирурга высокой концентрации внимания, детального знания анатомии и точного выполнения всех этапов операции. Накопление большого опыта «открытой» торакальной хирургии, появление новых эндоскопических инструментов и механических аппаратов для разъединения тканей позволили расширить показания к торакоскопическим операциям. Неким промежуточным этапом перехода к полностью «закрытым» вмешательствам были видео-ассистированные резекции лёгких из мини-доступа, которые и сейчас широко выполняются в ряде клиник, но при этом не лишены многих недостатков классических «открытых» операций.
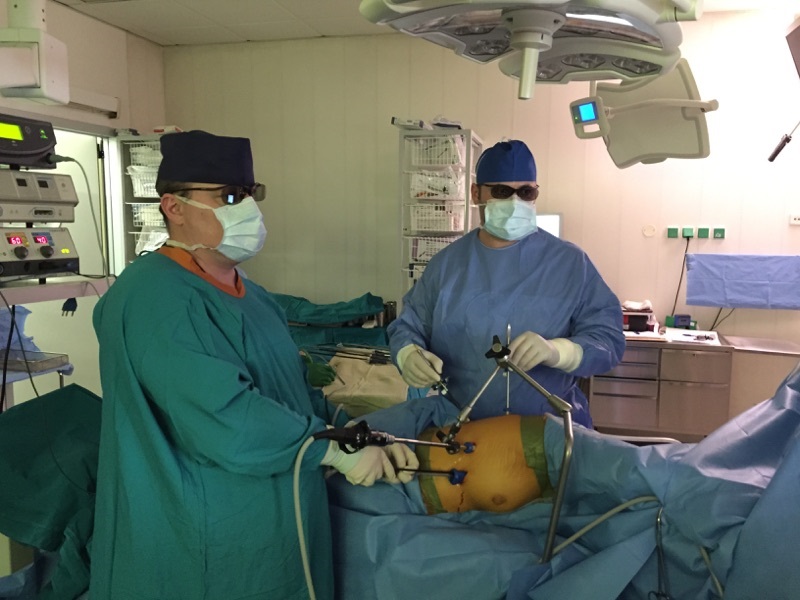
На сегодняшний день в нашей клинике при ранних стадиях периферического рака легкого (опухоль не более 5см в диаметре, без метастазов в лимфатических узлах) радикальная торакоскопическая лобэктомия уже стала стандартом хирургического лечения. Следует отметить, что при торакоскопических операциях по поводу злокачественных опухолей объем удаляемых тканей полностью соответствует таковому при «открытом» доступе, что сохраняет необходимую «онкологическую радикальность» вмешательства. За счет увеличения и высокой четкости изображения, в некоторых случаях, при торакоскопии удается более тщательно выполнить ревизию зоны операции и удалить пораженные ткани. Качественно иной уровень торакоскопической хирургии обеспечивает также применяемая нами система 3D-визуализации, аналоги которой используются в роботах «Da Vinci».
Торакоскопическая техника резекций легких в нашей клинике обладает рядом значительных преимуществ. Во время операции не используются ранорасширители, травмирующие межреберные нервы. Максимальный разрез до 4 см выполняется в конце операции с целью удаления опухоли, кисты или части легкого. Для визуализации операционного поля применяются специальные торакоскопы с гибким концом, что позволяет не менять положения камеры во время операции. Изменение поля зрения происходит за счет управления камерой при помощи специальных кнопок. Используются мягкие анатомические (соответствующие форме межреберного промежутка) троакары, а места установки портов ушиваются саморассасывающимися нитями.
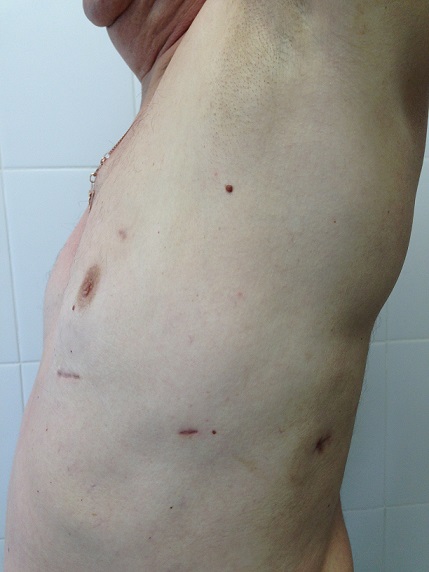
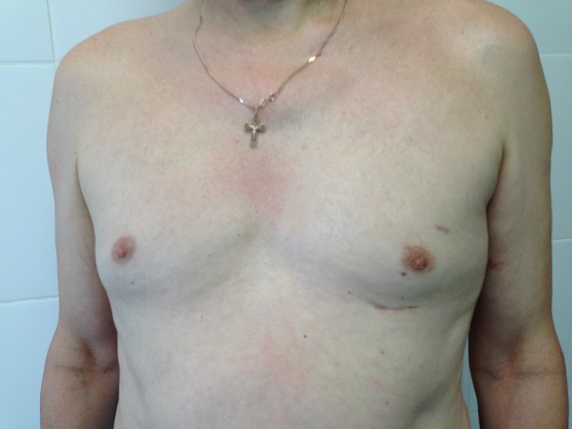
Применение сверхтонких инструментов (диаметром 3 и 5мм) и тончайшей гибкой оптики позволяет значительно уменьшить травматизацию тканей во время операции и существенно снижает интенсивность болевого синдрома в послеоперационном периоде, а в ряде случаев почти полностью его исключает. Точное выделение всех анатомических структур, применение современных сшивающих степлеров и систем гемостаза позволяет снизить интраоперационную кровопотерю до 50-100мл.
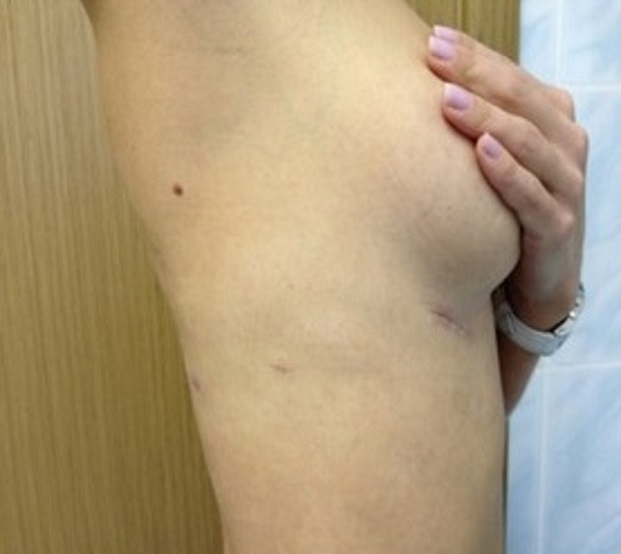
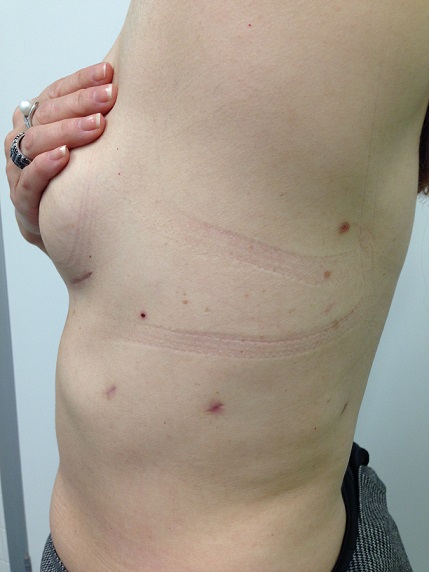
В нашей клинике все торакоскопические операции выполняются на самом современном оборудовании ведущих мировых производителей с использованием лучших расходных материалов. Оперирующие хирурги прошли обучение и стажировки в ведущих клиниках Франции, Бельгии и США. Некоторые операции выполнены впервые в России.
Лечение I и II стадий немелкоклеточного рака легкого
Для I и II стадий немелкоклеточного рака легкого (НМРЛ) характерно вовлечение в патологический процесс только одного легкого и отсутствие поражения средостения или каких-либо других структур. На раннем этапе выявляется не более 30% всех случаев НМРЛ [1].
Общие принципы терапии
Стадирование рака легкого осуществляется в соответствии с системой TNM. В настоящее время стадию НМРЛ определяют, основываясь на последней, 8-й редакции системы, принятой в 2016 году [1].
Таблица 1. Стадирование рака легкого по системе TNM 8 пересмотра [2].
| Стадия заболевания | ТХ | N0 | М0 |
|---|---|---|---|
| Стадия IA1 | T1a(mi) | N0 | M0 |
| T1a | N0 | M0 | |
| Стадия IA2 | T1b | N0 | M0 |
| Стадия IA3 | T1c | N0 | M0 |
| Стадия IB | T2a | N0 | M0 |
| Стадия IIA | T2b | N0 | M0 |
| Стадия IIB | T1a-c | N1 | M0 |
| T2a | N1 | M0 | |
| T2b | N1 | M0 | |
| T3 | N0 | M0 |
* T1a(mi) – минимально инвазивная карцинома.
Основным методом лечения I и II стадий НМРЛ является полная хирургическая резекция опухоли при отсутствии противопоказаний к операции. Для пациентов со II стадией НМРЛ показана адъювантная химиотерапия. Ее также может быть целесообразно назначать при стадии IB, особенно с признаками высокого риска. Пациентам с опухолями стадии IA после резекции адъювантная химиотерапия не показана [3].
Послеоперационная лучевая терапия показана только пациентам I и II стадии, у которых обнаружено опухолевое поражение в области резекции [4].
Лучевая терапия – альтернатива для пациентов, не являющихся кандидатами на хирургическое лечение вследствие сопутствующих заболеваний или отказа от операции [5]. Стереотаксической радиотерапии отдается предпочтение при опухолях с размерами менее 5 см. Обычное фракционирование показано пациентам с более массивными поражениями или при недоступности стереотаксической радиотерапии.
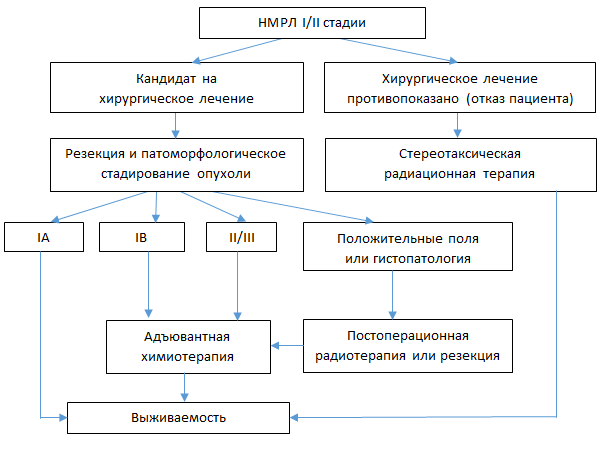
Алгоритм лечения потенциально резектабельного НМРЛ
Хирургическое лечение НМРЛ
Хирургическая лечение – стандартный подход при НМРЛ I и II стадии, а также в случае отсутствия доказательств вовлечения средостения до хирургической резекции.
Анатомическая резекция – лобэктомия
Процедурой выбора считается хирургическая резекция одной доли легкого, лобэктомия, имеющая важное преимущество по сравнению с пневмонэктомией в случаях, когда поражение может быть резецировано полностью, – способность сохранять легочную функцию [6]. При этом альтернативой открытой торакотомии считается видеоторакоскопия [7], обеспечивающая снижение инвазивности лечения ранней стадии НМРЛ.
Применение видеоторакоскопии позволяет снизить последствия хирургического вмешательства, в том числе уменьшить выраженность послеоперационного болевого синдрома, что особенно важно для пациентов с тяжелой сопутствующей патологией [8]. Кроме того, благоприятная переносимость видеоторакоскопии может увеличить комплайенс постоперационной адъювантной химиотерапии. Так, анализ данных 100 пациентов с НМРЛ после лобэктомии и последующей адъювантной химиотерапии показал, что при проведении вмешательства с помощью видеоторакоскопии гораздо реже приходилось откладывать назначение химиотерапии (18% против 58%) и снижать ее дозу (26% против 49%) по сравнению с открытой торакотомией [9].
Несмотря на то, что эффективность видеоторакоскопии по сравнению с обычными хирургическими методами не была подтверждена в рандомизированных исследованиях, ретроспективные данные позволяют сделать вывод о безопасности и эффективности лобэктомии с помощью видеоторакоскопии для пациентов с I стадией НМРЛ без ущерба для выживаемости 10.
Ограниченная (сублобарная) резекция может подразумевать анатомическую или неанатомическую сегментэктомию с удалением первичной опухоли, внутрилегочных, прикорневых и медиастинальных лимфатических узлов. Сублобарная резекция может быть терапией выбора для пациентов, которые не в состоянии перенести удаление всей доли легкого вследствие снижения функции легких, преклонного возраста или тяжелой сопутствующей патологии.
Результаты ряда исследований свидетельствуют, что сублобарная резекция связана с худшими показателями выживаемости по сравнению с лобэктомией [6,14]. По различным данным, при неанатомической резекции увеличивается частота местного рецидива на 5-10% [15]. Предложенная в качестве способа уменьшения частоты локального рецидива при сублобарной резекции интраоперационная брахитерапия, к сожалению, оказалась неэффективной, что подтверждено данными клинического исследования III фазы ALLIANCE [16], свидетельствующими об отсутствии существенной разницы между сублобарной резекцией с и без сочетания с интраоперационной брахитерапией.
Однако существует и противоположная точка зрения, утверждающая, что эффективность сублобарной резекции на ранних стадиях НМРЛ, особенно при размере поражения не более 2 см, может быть сравнима с результатом, полученным после лобэктомии [17].
Согласно рекомендациям Европейского общества торакальных хирургов 2006 года, целесообразно проводить систематическое удаление лимфоузлов во всех случаях с целью обеспечения полноты резекции [18]. Такая же тактика декларируется и в рекомендациях Британского торакального общества 2010 года [19].
Согласно федеральным российским рекомендациям, стандартным объемом медиастинальной лимфаденэктомии при операциях на правом легком считается удаление правых нижних паратрахеальных (трахеобронхиальных, паратрахеальных, претрахеальных) узлов, на левом легком – парааортальных, субаортальных, левых нижних паратрахеальных узлов, а также независимо от стороны операции – бифуркационных, параэзофагеальных и узлов легочной связки соответствующих сторон [15].
Согласно рекомендациям Европейского общества торакальных хирургов ESTS [20], у пациентов с минимальным получением образцов тканей лимфоузлов, независимо от местоположения первичной опухоли, необходимо исследовать следующие уровни лимфоузлов и удаленные узлы, при наличии таковых:
У пациентов с систематической радикальной средостеночной лимфаденэктомией вся доступная средостеночная жировая ткань, относящаяся к одной стороне тела, подлежит удалению, включая следующие уровни:
Пациенты, у которых не все упомянутые уровни лимфоузлов были удалены, автоматически классифицируются как имеющие «минимальное получение образцов ткани лимфоузлов».
При метастатическом поражении лимфоузлов средостения показана расширенная медиастинальная лимфаденэктомия, подразумевающая удаление превенозных, ретротрахеальных и верхних паратрахеальных узлов с окружающей клетчаткой соответствующей стороны [15].
При микроскопическом вовлечении опухолевых клеток по линии резекции (R1) прогноз заболевания значительно менее благоприятный по сравнению с резекцией с отрицательными микроскопическими полями (R0) [21,22].
Для пациентов со стадией IIB вследствие вовлечения в опухолевый процесс грудной стенки может быть показана резекция грудной стенки в едином блоке с опухолью и тканью легкого («en-bloc»). По данным ретроспективного исследования с участием 212 пациентов, это позволило достичь высоких показателей выживаемости в течение пяти лет [23].
Частота локального рецидива после хирургического вмешательства у пациентов с НМРЛ I и II стадии составляет, по разным данным, от 6% до 55% [24,25].
Адъювантная терапия
После потенциально радикальной резекции опухоли при НМРЛ существует вероятность прогрессирования заболевания вследствие отдаленного метастазирования или местного рецидива. Адъювантная химиотерапия после радикальных операций у некоторых больных на ранних стадиях заболевания (IB и II) позволяет улучшить безрецидивную и общую 5-летнюю выживаемость.
Клинические исследования, в которых в качестве адъювантной химиотерапии применялись современные схемы на основе цисплатина, продемонстрировали преимущество в выживаемости для пациентов с НМРЛ II стадии и, возможно, со стадией IB [26], но не подтвердили эффективность у пациентов со стадией IA [27].
Адъювантную терапию назначают после восстановления пациента от хирургического лечения (но не позже 8 недель), ее длительность в среднем составляет 3-4 цикла. Для химиотерапии можно использовать любые платиносодержащие комбинации с включением препаратов 3 поколения или этопозида. Наиболее изученными считаются комбинации винорельбина и цисплатина, гемцитабина и цисплатина, паклитаксела и карбоплатина [15].
Определенных рекомендаций по назначению таргетных препаратов в качестве адъювантной терапии на сегодня не существует. Данные ряда исследований свидетельствуют, что у пациентов с мутацией EGFR на ранней стадии заболевания (особенно на стадии IIIA после резекции опухоли) назначение в качестве адъювантного лечения эрлотиниба сопряжено с увеличением выживаемости без рецидива [26, 28]. Однако неизвестно, свидетельствуют ли эти результаты об улучшении общей выживаемости или о пролонгировании времени до рецидива.
В то же время в работе Kelly K с соавт. с участием 973 пациентов с НМРЛ и мутацией в гене EGFR [29] было показано, что адъювантная химиотерапия эрлотинибом не пролонгирует выживаемость без рецидива. Столь противоречивые данные свидетельствуют о необходимости дальнейших исследований эффективности ингибиторов тирозинкиназы в качестве адъювантной химиотерапии у EGFR-позитивных пациентов с НМРЛ.
Прогноз НМРЛ I и II стадии
У пациентов со стадией I и II НМРЛ на прогноз заболевания влияет ряд факторов, среди которых:
Постоперационное наблюдение
Целью постоперационного наблюдения после первичного лечения НМРЛ является раннее обнаружение рецидива или второго первичного рака легкого.
Физический осмотр, КТ грудной клетки рекомендовано проводить каждые 6 месяцев на протяжении первых двух лет после лечения, а затем – ежегодно [41]. Однако на конгрессе Европейского общества медицинской онкологии ESMO 2017 года в Мадриде были представлены результаты исследования с участием 1775 пациентов с полностью резецированным НМРЛ I-II-IIIA стадии, продемонстрировавшие отсутствие разницы в общей выживаемости между пациентами, проходящими КТ-сканирование каждые 6 месяцев в первые два года после операции, и пациентами, не делающими этого исследования.
Тем не менее, наблюдение на основе КТ по-прежнему остается оптимальным способом контроля из-за возможного развития повторного случая первичного рака у пациентов после полной резекции НМРЛ.
Хирургическое лечение рака легких
Хирургическое лечение рака легких показано, когда опухоль можно удалить одномоментно вместе с регионарными лимфоузлами. Кроме этого, учитывают локализацию опухоли, ее тип и стадию развития, общее состояние и возраст пациента.
В зависимости от перечисленных параметров хирургическое лечение рака легких бывает:
Цели радикального и условно радикального лечения — избавить больного от патологии. Паллиативная помощь направлена на временное улучшение его состояния.
При радикальной операции удаляют весь опухолевый комплекс — первичный очаг, клетчатку с путями метастазирования и регионарные лимфатические узлы. На начальных стадиях удаляют долю легкого — делают лобэктомию.
При хирургическом лечении рака правого легкого возможна билобэктомия — резекция двух долей. При местнораспространенном процессе проводят пульмонэктомию — удаляют все легкое с регионарными лимфоузлами разных групп. Кроме этого, возможны комбинированные операции с резекцией грудной стенки, перикарда, диафрагмы, предсердия, мышечной стенки пищевода, бифуркации трахеи.
Цены на платные услуги
| Торакальная хирургия | Цена, руб. |
| Дренирование плевральной полости эндоскопическим методом Гистологическое исследование оплачивается дополнительно | 3 900 руб. |
| Трансторакальная биопсия Гистологическое исследование оплачивается дополнительно | 4 800 руб. |
| Биопсия (игловая) легкого или образований средостения Гистологическое исследование оплачивается дополнительно | 5 500 руб. |
| Открытая биопсия легкого, образований средостения Гистологическое исследование оплачивается дополнительно | 21 230 руб. |
| Эндопротезирование трахеи и бронхов силиконовыми протезами | 41 360 руб. |
| Дренирование абсцесса легкого средней тяжести с последующим лечением | 5 500 руб. |
| Санация плевральной полости лекарственными препаратами при гнойных заболеваниях (1 процедура) | 4 800 руб. |
| Диагностическая торакоскопия | 11 770 руб. |
| Видеоторакоскопическая спланхикоэктомия (с одной стороны) | 24 970 руб. |
| Видеомедиастиноскопия | 22 000 руб. |
| Видеоторакоскопическая биопсия легкого Гистологическое исследование оплачивается дополнительно | 22 000 руб. |
| Видеоторакоскопическая плеврэктомия Гистологическое исследование оплачивается дополнительно | 26 400 руб. |
| Видеоторакоскопическая плеврэктомия с распылением склерозирующих препаратов Гистологическое исследование оплачивается дополнительно | 33 770 руб. |
| Видеоторакоскопическая буллэктомия с использованием одноразовых сшивающих аппаратов | 41 360 руб. |
| Видеоторакоскопическое удаление периферических образований легкого Гистологическое исследование оплачивается дополнительно | 26 400 руб. |
| Видеоторакоскопическое удаление образований средостения Гистологическое исследование оплачивается дополнительно | 32 230 руб. |
| Микроторакотомия с видеоподдержкой и использованием многоразовых сшивающих аппаратов | 22 000 руб. |
| Плеврэктомия Гистологическое исследование оплачивается дополнительно | 22 000 руб. |
| Плеврэктомия с декортикацией легкого Гистологическое исследование оплачивается дополнительно | 32 230 руб. |
| Краевая резекция легкого Гистологическое исследование оплачивается дополнительно | 22 000 руб. |
| Удаление новообразования легкого (атипичная резекция) Гистологическое исследование оплачивается дополнительно | 26 400 руб. |
| Удаление округлых периферических образований легких Гистологическое исследование оплачивается дополнительно | 26 400 руб. |
| Уменьшение объема легкого у больных ХОБЛ, крупнобуллезной или диффузной эмфиземой легких | 65 890 руб. |
| Декортикация легкого | 36 630 руб. |
| Лобэктомия 1 категории | 41 030 руб. |
| Лобэктомия 2 категории | 48 400 руб. |
| Билобэктомия | 48 400 руб. |
| Пневмонэктомия Гистологическое исследование оплачивается дополнительно | 48 400 руб. |
| Пневмонэктомия с клиновидной резекцией бифуркации трахеи Гистологическое исследование оплачивается дополнительно | 58 630 руб. |
| Пневмонэктомия с циркулярной резекцией бифуркации трахеи Гистологическое исследование оплачивается дополнительно | 58 630 руб. |
| Циркулярная резекция трахеи при новообразованиях и рубцовых стенозах Гистологическое исследование оплачивается дополнительно | 77 660 руб. |
| Резекция грудной клетки | 26 400 руб. |
| Операция при опухолях средостения Гистологическое исследование оплачивается дополнительно | 61 600 руб. |
| Торакопластика | 44 000 руб. |
| Эмболизация бронхиальных артерий при легочных кровотечениях и/или кровохарканьях | 22 000 руб. |
| Лечебно-диагностическая торакоскопия, введение лекарственных препаратов с целью плевродеза | 22 000 руб. |
| Лечебно-диагностическая видеоторакоскопия | 23 430 руб. |
| Лечебно-диагностическая видеоторакоскопия, введение лекарственных препаратов с целью плевродеза | 26 400 руб. |
| Дренирование плевральной полости и плевродез | 17 600 руб. |
| Видеоторакоскопия, дренирование плевральной полости и плевродез | 26 400 руб. |
| Видеоторакоскопия, биопсия плевры, дренирование плевральной полости и плевродез Гистологическое исследование оплачивается дополнительно | 27 830 руб. |