Выясняем причину субфебрильной температуры

На температуру тела влияет жара, влажность, слишком теплая одежда. У женщин наблюдается небольшой скачок температуры (на полградуса) в определенные дни менструального цикла. Но это будет разовое повышение. Поводом для беспокойства может стать повышение температуры от 37.2 до 37.9 в период больше месяца – это и есть субфебрильная температура.
Если субфебрильная температура держится более двух недель, и ее сопровождают такие симптомы, как быстрая утомляемость, плохой сон, одышка, то не следует откладывать прием терапевта. Часто субфебрилят сигнализирует о неполадках в организме, когда еще не появились другие симптомы.
Причины субфебрильной температуры

Если причиной повышенной температуры является инфекция, то для нее характерно:
Но существуют причины, когда у здорового человека наблюдается субфебрильная температура:
Такая температура не поддается действию жаропонижающих препаратов, легко переносится и не имеет выраженных суточных колебаний.
Выяснить причину поможет обследование.
Анализы и исследования при субфебрильной температуре.
Начинать следует всегда с врача-терапевта. Именно врач-терапевт направит на первичные анализы, а затем после полученных результатов порекомендует прием узкого специалиста: эндокринолога, кардиолога, гинеколога, отоларинголога, инфекциониста.
Повышена температура на протяжении более двух недель?
Если после полученных результатов причина не установлена, то пациента направляют сдать анализ крови:
Длительное повышение температуры после COVID-19
17 марта
У многих пациентов, переболевших COVID-19, нередко продолжается повышение температуры тела до 37,2 – 37,5. Почему же это происходит? Давайте разбираться.
Центр терморегуляции располагается в отделе головного мозга, который называется гипоталамус.
Гипоталамус управляет процессами эндокринной системы, которая тесно взаимосвязана с самыми важными для терморегуляции органами – это надпочечники и щитовидная железа. Так, при понижении температуры окружающей среды усиливается выделение гормонов щитовидной железы, ускоряющих обмен веществ и, как следствие усиливается теплообразование. При изменении погоды надпочечники выделяют в кровь гормоны, сужающие или расширяющие сосуды, в том числе кожи. Из-за этого меняется уровень теплоотдачи.
Физиологические колебания температуры тела в течение суток могут быть на 1-1,3 градуса. При чем, она всегда увеличивается к вечеру и может быть в норме с 16 до 18 часов в подмышечной области в пределах 37,0 – 37,2. Это связано с биоритмами и физиологическими процессами в организме (лактация, менструация у женщин, реакция на стресс, боль, приём пищи, физические нагрузки, особые климатические условия).
Известно, что коронавирус оказывает повреждающее действие на нервную систему. Т.е. колебания температуры тела объяснимы непосредственным поражением нервной системы. Восстановление происходит долго, иногда несколько месяцев.
Симптом субфебрильной температуры является проявлением постковидного синдрома, которое пока не лечится. Это своеобразный астенический синдром, возникший после с болезни, связанной с внушительным воспалительным процессом. Восстановление может протекать несколько месяцев.
Но нервной системе можно помочь восстановиться быстрее:
► Спать 7-9 часов каждую ночь.
► Если есть возможность, устраивать «тихий час» днем.
► Максимально снизить время, проведённое у экранов таких устройств как смартфон, планшет, компьютер или телевизор.
► Отдыхать достаточное количество времени.
► Поддерживать температуру в помещении на уровне 22 градусов, постоянно проветривать для доступа свежего воздуха.
► Соблюдать водный режим – циркулярный душ, контрастный душ.
► Питаться сбалансированно и правильно: употреблять много свежих фруктов и овощей, белка, никакого фастфуда, жареной пищи, алкоголя и кофеина. Возможно применение энтерального питания с повышенным содержанием белка и энергии, например Нутридринк Компакт Протеин по 125 г (1 пластиковая бутылочка) в сутки на протяжении 3-4 недель.
► Гулять на свежем воздухе и иметь регулярную легкую физическую нагрузку, (ЛФК, йога, особенно дыхательные практики, медитации).
► Прием витамина Д в профилактической дозировке 2000 МЕ в сутки, Магне В6 форте по 1 таб 3 р в сутки 1 месяц.
► Применение акупунктуры также признается доказательной медициной, как способ восстановления после перенесенных заболеваний.
Однако очень важно людям, имеющим проблемы с эндокринной системой, обратиться к эндокринологу и провести контроль показателей. Дополнительно можно определить в крови уровень железа, ферритина, витамина Д. Если в анализах будут отклонения, начать соответственное лечение. И в любом случае при появлении и сохранении в течение длительного времени субфебрильной температуры следует обратиться к врачу для выявления возможных проблем.
Что еще важно помимо измерения температуры тела?
Люди, находящиеся в процессе восстановления, особенно пожилые, должны регулярно контролировать пульс, артериальное давление, бдительно относиться к жалобам со стороны сердца, контролировать уровень кислорода с помощью пульсоксиметра. Нормальное насыщение кислородом составляет от 96 до 100% и не должно опускаться ниже 88% во время физической нагрузки. Поэтому важно измерять сатурацию до, во время и после тренировки.
Если после перенесенной коронавирусной инфекции вы не чувствуете себя как раньше, то в «Клинике Вся Медицина» действуют специальные программы реабилитации после COVID-19, которые помогут улучшить ваше самочувствие!
Узнать подробности можно по телефону +7 (351) 240-03-03 или по ссылкам:
Использование Нурофена для уточнения этиологии лихорадки неясного генеза
Опубликовано в журнале:
Практика педиатра, Март, 2007
Л.И. Васечкина, Т.К. Тюрина, педиатрическое отделение Московского областного научно-исследовательского клинического института им. М.Ф. Владимирского
Среди детей, поступающих в педиатрическое отделение Московского областного научно-исследовательского клинического института им. М.Ф. Владимирского (МОНИКИ) из стационаров Московской области, ежегодная доля больных с ЛНГ составляет 1-3%. Как правило, диагноз ЛНГ устанавливается у детей с температурой тела выше 37,4°С, регистрируемой более 3 недель, при этом данные проведенного клинико-лабораторного обследования не позволяют уточнить нозологическую форму заболевания.
За последние годы отмечаются изменения возрастной и половой структуры ЛНГ: отмечается рост числа мальчиков с ЛНГ, а в возрастной структуре по сравнению с традиционным ранее преобладанием ЛНГ у подростков, зарегистрировано увеличение доли детей в возрасте до 5 лет и в препубертатном периоде. Выявленная динамика ЛНГ потребовала анализа этой нозологии для разработки новых подходов к уточнению этиологического фактора и коррекции схем терапии.
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Проанализировано 70 историй болезни детей с ЛНГ в возрасте от 1,5 до 15 лет, из них 33 мальчика и 37 девочек. Больные поступали на обследование с жалобами на субфебрильную температуру в течение длительного времени (от 3 месяцев до 1 года) недомогание, потерю массы тела, утомляемость, снижение аппетита.
Основная цель исследования состояла в выявлении очага хронической инфекции, диагностике нарушений гормонального и неврологического статуса, исключении онкологических болезней и диффузных заболеваний соединительной ткани.
План обследования включал комплекс лабораторных анализов (клинический и биохимический анализы крови, анализ на маркеры воспаления, общий анализ и функциональные пробы мочи, копрограмма, гормональный профиль, исследование методом ИФА на инфекции), инструментальные исследования (ЭКГ, ЭХО-КГ, ЭЭГ, УЗИ, по показаниям КТ или МРТ), консультации специалистов (невролог, отоларинголог, генетик).
Таблица 1. Структура этиологических факторов длительной лихорадки в зависимости от пола
| Основная причина | Всего, % | Соотношение мальчики : девочки |
| Вегетативно-сосудистая дистония | 36 | 2:3 |
| Очаг инфекции | 28 | 2:1 |
| Аллергический синдром | 23,4 | 3:2 |
| Тиреотоксикоз | 6,6 | все девочки |
| Заболевания соединительной ткани | 6 | 1:4 |
Нельзя обойти вниманием тот факт, что у половины (50%) детей с ЛНГ при осмотре были выявлены диагностически значимые (6-8 баллов) величины критериев Бейтса, позволяющие установить наличие недифференцированной дисплазии соединительной ткани. Необходим дальнейший анализ обнаруженного феномена, однако уже можно предположить, что данный фенотип является индикатором неврологических и эндокринных дисфункций.
Результаты собственных наблюдений не всегда согласуются с данными других исследований, соответственно которым чаще всего причиной ЛНГ являются инфекции верхних отделов дыхательных путей, болезни костей и суставов, пневмонии, кардиальные и интраабдоминальные инфекции [4,5]. По нашему мнению, в развитии лихорадки неясного генеза значительную роль играет сочетание соматической патологии с нейровегетативными дисфункциями, при котором ведущим фактором ЛНГ являются нарушения терморегуляции не воспалительной, а регуляторной этиологии.
В нашем исследовании диагноз нарушения терморегуляции центрального генеза подтверждался наличием минорных неврологических симптомов, нарушений на ЭЭГ. Применение комплекса нейротропных препаратов у этих больных сопровождалось нормализацией температуры.
ПАТОГЕНЕЗ ЛИХОРАДКИ
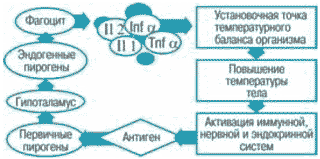
Рисунок 1. Схема патогенеза ЛНГ при наличии воспалительного процесса
Первичные пирогены инициируют лихорадку, стимулируя собственные клетки к выработке эндогенных пирогенов. Вторичные пирогены (ИЛ-1, 6, интерферон-а и пр.), синтезируемые лейкоцитами, воздействуют на рецепторы в гипоталамусе, в результате чего изменяется чувствительность нейронов центра терморегуляции к холодовым и тепловым сигналам.
Однако существуют и иные механизмы повышения температуры тела (рис. 2).
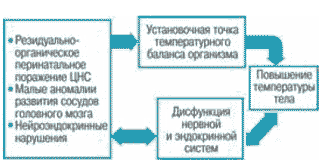
Рисунок 2. Схема патогенеза ЛНГ при нарушении терморегуляции центрального генеза
ПОИСК ПРИЧИНЫ
Для выполнения этой задачи используется проба с жаропонижающими препаратами, так как при этом достигается выключение из механизма повышения температуры фактора эндогенных пирогенов. Ранее проводились аспириновая или анальгиновая пробы. Согласно рекомендациям ВОЗ, широкое применение метамизола не рекомендуется в детской практике из-за наличия тяжелых осложнений (специальное письмо от 18.10.1991 г.). С недавнего времени в России также существует запрет на применение ацетилсалициловой кислоты у детей до 15 лет. Таким образом, возникла необходимость использования в пробе других жаропонижающих средств [1, 2, 3].
Проба с Анальгином была проведена 15 детям (возраст 11-15лет), из них 10 девочкам и 5 мальчикам. Проба с НУРОФЕНОМ ДЛЯ ДЕТЕЙ применена у 13 детей (возраст 6-15 лет), из них 5 девочек и 8 мальчиков. Таким образом, количество детей, возрастной, половой состав и нозология в группах существенно не отличались. Порядок проведения пробы оставался стандартным. Для мониторинга состояния к истории болезни подклеивался температурный лист.
Таблица 2. Переносимость нурофеновой пробы
| Переносимость | Хорошая | Удовлетворительная |
| мнение врача | 10 | 3 |
| мнение пациента | 11 | 2 |
Частота встречаемости побочных эффектов была сопоставлена в двух группах: дети, которым проводилась классическая анальгиновая проба, и больные, получавшие НУРОФЕН ДЛЯ ДЕТЕЙ (табл. 3).
Таблица 3. Частота побочных эффектов при сравнении анальгиновой и нурофеной проб
| Побочные эффекты | Анальгиновая проба | Нурофеновая проба |
| n = 1 | n = 7 | |
| тошнота | 3 | 1 |
| боль в животе | 1 | 0 |
| головная боль | 3 | 0 |
Таким образом, данное исследование показало необходимость учета фактора нарушения терморегуляции центрального генеза при дифференциальном диагнозе ЛНГ у детей. Использование диагностической пробы с НУРОФЕНОМ ДЛЯ ДЕТЕЙ (RECKITT BENCKISER) позволило получить убедительные доказательства дисфункциональных нарушений терморегуляции при хорошей переносимости препарата с минимальным количеством побочных эффектов.
Список использованной литературы находится в редакции.
Сведения об авторах:
Ацетилсалициловая кислота и астма: педиатрические аспекты
Ацетилсалициловая кислота была синтезирована F. Hoffmann в 1897 г. Вскоре после этого были описаны связанные с ее приемом случаи развития отека Квинке (Hirschberg, 1902), бронхоспазма (Barnett, 1905). Позже Widal
Ацетилсалициловая кислота была синтезирована F. Hoffmann в 1897 г. Вскоре после этого были описаны связанные с ее приемом случаи развития отека Квинке (Hirschberg, 1902), бронхоспазма (Barnett, 1905). Позже Widal и Lermayez (1922) ввели термин «аспириновая триада», подразумевающий сочетание бронхиальной астмы (БА), назальных полипов и непереносимости ацетилсалициловой кислоты. Сегодня в литературе этот феномен встречается под различными названиями: анальгетика-астма-синдром, аспириновая идиосинкразия, синдром Samter, аспирин-индуцированная астма, аспириновая астма и т. п.
Непереносимость НПВП — одна из наиболее распространенных причин лекарственной аллергии: у взрослых она составляет
36% и занимает второе место по частоте развития после антибиотиков [1]. Для некоторых больных БА непереносимость НПВП является фактором, провоцирующим тяжелое течение заболевания, развитие кортикозависимости и повышенную смертность. В последние годы в западной литературе широко обсуждается также вопрос о взаимосвязи между развитием БА и частотой приема парацетамола (ежедневно/еженедельно) взрослыми [2], беременными женщинами [3]. Так, наиболее высокий показатель продажи парацетамола в англоязычных странах за последнюю декаду положительно коррелировал с симптомами БА, экземы и аллергического ринита у подростков и взрослых [4].
Принято считать, что ацетилсалициловая кислота в редких случаях вызывает обострение БА у детей (GINA, 2002) [5]. В Национальной программе России по БА (1997) говорится о том, что у 12—28% детей с БА отмечается непереносимость НПВП [6]. Эти данные приводятся со ссылкой на работу G. Rachelefsky и соавт. и получены после проведения детям с БА провокационного теста ацетилсалициловой кислотой per os [7]. В отечественной литературе аспириновая астма у детей впервые описана проф. С. Ю. Кагановым и соавт. в 1988 г. [8].
Известно, что в диагностике непереносимости ацетилсалициловой кислоты и аспириновой астмы большую роль играет «проблемно-ориентированный анамнез» (фармакологический + аллергологический). Выводы относительно распространенности непереносимости НПВП среди детей с БА мы делали на основе собственного наблюдения: результатов ретроспективного анализа историй болезни 610 пациентов в возрасте 6—13 лет, наблюдавшихся амбулаторно в Респираторном центре г. Москвы [9]. Было установлено, что 3% детей с БА имели в анамнезе различные клинические проявления непереносимости анальгетиков (кожные, респираторные, гастроинтестинальные или смешанные). Классический симптомокомплекс аспириновой триады был выявлен у 0,3% обследованных детей. Почти во всех случаях имели место гиподиагностика непереносимости НПВП при отсутствии у врачей сведений относительно ее клинических проявлений, а также особенностей терапии больных аспириновой астмой [9]. Между тем аспириновая астма представляет собой очень важную проблему для клинической медицины: у большинства таких пациентов велик риск развития тяжелых, угрожающих жизни обострений; они чаще других нуждаются в длительной глюкокортикоидной терапии [5, 10, 11].
Учитывая выше сказанное, в настоящем обзоре мы суммируем сведения, касающиеся современных представлений о патогенезе, диагностике, лечении и профилактике аспириновой астмы у детей.
Эпидемиология
Точные эпидемиологические исследования, посвященные непереносимости анальгетиков у детей и взрослых, не проводились. Непереносимость НПВП рассматривается как причина обострений хронической крапивницы и отека Квинке у 21—30% детей и 8—89% взрослых [1, 11—13]. Считается, что чувствительность к ацетилсалициловой кислоте (другим НПВП) может не только стать причиной развития хронической крапивницы или ангиоотека, но и приводить к усилению уже существующей уртикарии у больного или действовать как кофактор реакции на пищу или физическую нагрузку, которые могут спровоцировать возникновение крапивницы [11]. Непереносимость НПВП отмечается примерно у 14—23% больных с назальным полипозом, но без БА [1]. Среди больных, страдающих БА в сочетании с полипозным риносинуситом, ацетилсалициловая кислота вызывала приступ удушья в 78% случаев [10, 15].
Показатели распространенности аспирин-индуцированного бронхоспазма у детей с БА могут широко варьировать. Так, R. Pearson [16] и J. Schull [17], исследовавшие влияние ацетилсалициловой кислоты, проводя провокационный тест у 32 и 90 больных БА детей в возрасте 1—9 лет, ни в одном случае не выявили бронхоспазма, вызванного ее приемом. Лишь у 1,9% из 1300 детей с БА в ходе другого исследования был выявлен положительный аспириновый тест [18]. Напротив, в ходе двойного, слепого исследования, в котором принимало участие 54 ребенка с БА, у 13% отмечалось аспирин-индуцированное снижение объема форсированного выдоха в 1 с (ОФВ1) [19]. По данным Т. Fischer, из 25 больных только у 6 (24%) был получен положительный провокационный тест с ацетилсалициловой кислотой и ацетаминофеном [20].
Следует выделить три наиболее важных момента, которые не были учтены в приведенных выше исследованиях:
Имеет значение также доза принимаемого препарата, в том числе и ацетаминофена. Показано, например, что у 12 из 42 взрослых больных БА побочный эффект наблюдался при приеме 1000 мг парацетамола, тогда как доза 500 мг не вызывала каких-либо нежелательных проявлений [21].
Аспириновой триадой страдают 3—10% взрослых больных БА [10, 11, 22], а среди стероидозависимых пациентов положительная реакция на провокацию ацетилсалициловой кислотой подтверждалась у 40% из них [11]. 25% больных, находившихся на искусственной вентиляции легких по поводу тяжелого обострения БА, имели непереносимость ацетилсалициловой кислоты, о которой во многих случаях не подозревали ни сами больные, ни врачи [10, 11].
Патогенез
Сегодня не существует общепринятой теории, объясняющей этиологию и патогенез аспириновой астмы, а также механизмы развития непереносимости анальгетиков.
Повышенный риск возникновения свистящего дыхания у детей раннего возраста, чьи мамы во время беременности часто применяли парацетамол, связывают с истощением глютатиона в легочной ткани и подавлением его антиоксидантных свойств [3].
У больных аспириновой астмой не найдены изменения в фармакологических свойствах или биотрансформации ацетилсалициловой кислоты [10, 25]. Как правило, астматические симптомы могут развиться и при приеме анальгетиков другой химической структуры.
Таким образом, хотя патогенез аспириновой астмы окончательно не выяснен, сегодня наиболее распространенной можно считать теорию ингибирования НПВП фермента циклооксигеназы с последующим накоплением в респираторном тракте сульфидопептидных лейкотриенов, вызывающих у больных формирование обструктивного синдрома [10, 11, 25].
Наследственный путь передачи аспириновой астмы не доказан [25]. А. Е. Богорад и соавт. описывают семейную форму аспириновой астмы у нескольких поколений больных [33].
Диагностика
Лабораторная диагностика непереносимости НПВП и самой аспириновой астмы по-прежнему достаточно сложна [11, 12, 17, 21, 31, 35]. «Золотым» стандартом признан провокационный пероральный тест ацетилсалициловой кислотой или ингаляционный тест лизин-ацетилсалициловой кислотой — с последующим исследованием функциональных показателей легких и определением уровня ЛтC4, ЛтE4 в моче и назальной лаважной жидкости [36]. Данные G. Rachelefsky о частоте распространенности непереносимости НПВП у детей с БА (14—28%), приводимые в рамках Национальной программы России, были получены в ходе 4-часового изучения воздействия 300 мг аспирина per os на бронхиальную проходимость у больных, принимавших ингаляционные кортикостероиды или кромоны [7]. Аспирин-индуцированный бронхоспазм диагностирован авторами на основании одного из следующих признаков: снижения после приема ацетилсалициловой кислоты ОФВ1 более чем на 30% и МОС25-75 на 20% по сравнению с базальным уровнем; снижения функциональных показателей легких, продолжавшегося на протяжении всего периода тестирования; вынужденного прекращения тестирования из-за острого бронхоспазма, развившегося у больного в ответ на прием ацетилсалициловой кислоты.
Однако провокационный тест ацетилсалициловой кислотой у ряда больных может вызвать парадоксальную реакцию в виде бронходилатации, которая в дальнейшем обычно заканчивается бронхоконстрикцией [35].
Тяжесть респираторных проявлений у больных БА, как правило, зависит от антициклооксигеназной активности НПВП, дозы и пути их введения [13, 14, 35].
При приеме комбинированных анальгетиков побочные реакции могут быть связаны с входящими в их состав эмульгаторами, витаминами, седативными и консервирующими веществами; играют также роль сопутствующие заболевания печени, желудочно-кишечного тракта, физические /психоэмоциональные стрессы у больного и т. д. [1, 12, 24].
Нередко непереносимость анальгетиков можно диагностировать только на основании данных положительного фармакологического анамнеза (побочные эффекты НПВП, развившиеся в разное время после их приема) [5].
Кожная проба на лизин-аспирин дает отрицательную реакцию [10]. Уровень общего IgЕ крови у детей и взрослых больных с аспириновой астмой ничем не отличался от этого показателя у контрольной группы больных БА с нормальной переносимостью анальгетиков, однако содержание IgG4 в крови было вдвое выше у лиц с аспириновой астмой [10, 11].
Болезнь начинается как вазомоторный круглогодичный ринит/риносинусит, который персистирует месяцами, иногда годами. Вначале в назальной жидкости у таких пациентов находят много эозинофилов (60—80%), позже (через несколько месяцев — три года) у них развиваются назальные полипы, при которых количество эозинофилов снижается примерно вдвое. В дальнейшем обычно присоединяются симптомы БА и непереносимости НПВП.
У детей клиническая симптоматика назального полипоза у детей и взрослых ничем не отличается [37]; однако у маленьких пациентов прежде всего следует исключить наличие муковисцидоза и синдрома неподвижности ресничек. По данным A. Szczeklik соавт., из 330 взрослых больных аспириновой астмой 77% имели симптомы ринита, которые появлялись в возрасте 20—40 лет [11]. При этом заложенность носа и насморк, а также снижение обоняния и чихание были наиболее типичными симптомами (89—92%), тогда как локальная синусная боль у больных отмечалась реже.
Первые симптомы непереносимости НПВП обычно возникают в возрасте 30—40 лет, чаще у женщин. Большинство таких больных (
60%) имеют в анамнезе хроническую крапивницу, у 70% находят повышенное количество эозинофилов в мокроте.
Непереносимость НПВП может проявиться в виде:
Как правило, у больных аспириновой астмой в течение первых 30 мин — 4 ч после приема НПВП возникают острый бронхоспазм, покраснение лица, глаз, ринорея, периорбитальный отек [5, 11, 14]. Приступы астмы учащаются, в дальнейшем в ответ на прием анальгетика могут возникать угрожающие жизни состояния (анафилактический шок, астматический статус, летальный исход). БА у аспирин-чувствительных больных приобретает прогрессирующее тяжелое течение, что довольно часто требует назначения системных глюкокортикостероидов [11].
Кожные и гастроинтестинальные симптомы в результате непереносимости НПВП обычно появляются позже — через 6—24 ч и даже один-два дня после их приема[1, 12].
Одновременный прием β2-агонистов, антигистаминных и метилксантиновых препаратов замедляет клинические проявления непереносимости НПВП у больных БА, а теофедрин оказывает двухстадийное действие: обычно больные сначала отмечают улучшение бронхиальной проходимости, затем у них наступает бронхоспазм [35].
Описаны случаи возникновения анафилактического шока после введения больным аспириновой астмой гидрокортизона сукцината [15, 38].
Считают, что соли бензойной кислоты, содержащиеся в большом количестве продуктов (консервы, кондитерские изделия и др.), являются причиной обострений болезни у 30—50% больных аспириновой астмой [14]. Тартразин не ингибирует активность циклооксигеназы и не дает перекрестной реакции с ацетилсалициловой кислотой [10, 14], тогда как возможность подобной связи между сульфитами и ацетилсалициловой кислотой не исключается [39].
Проявления непереносимости НПВП у больных могут исчезать спонтанно, однако такие случаи довольно редки, а аспириновой астмой пациенты страдают пожизненно [17, 25].
Прежде всего пациенты с непереносимостью анальгетиков и аспириновой астмой не должны принимать НПВП, а также продукты, содержащие природные салицилаты (грейпфрут, малина, яблоки, ревень и т. д.).
В качестве альтернативных средств рекомендуют использовать парацетамол и современные НПВП, селективно ингибирующие циклооксигеназу-2: нимесулид, целекоксиб, рофекоксиб (их разрешено назначать детям старше 12 лет), хотя в высоких дозах они также могут спровоцировать бронхоспазм у чувствительных лиц [40].
Изолированные или диффузные назальные полипы лечат в основном топическими стероидами и/или проводят эндоскопическую эндоназальную полисинусотомию. «Хотя доказано, что ни самая тщательная операция, ни кортикостероидная терапия не в состоянии излечить полипозный риносинусит, однако они дают возможность значительно улучшить качество жизни больных и удлинить промежутки между рецидивами. Группа ведущих ученых мира рекомендует следующую схему этапного лечения полипозного синусита: первая-вторая стадия — интраназальные кортикостероиды; третья стадия — короткий курс системной глюкокортикоидной терапии + назальные кортикостероиды; если терапия неэффективна — хирургическое лечение (Position statemet on nasal polyps, 1994). Короткий курс общей кортикостероидной терапии, называемый «медикаментозная полипотомия», широко применяется в лечении полипозного риносинусита, причем считается, что его эффективность не уступает эффекту инструментальной полипотомии (T. Lindhalt et al., 1988; K. Holmgren, G. Karksson, 1994). Эта позиция является общепринятой практически во всем мире, но пока с большим трудом завоевывает свое место в умах отоларингологов в России и бывших республиках СССР (цитируется по А. С. Лопатину) [41].
Следует помнить о том, что полипэктомия может стать причиной тяжелого обострения БА.
По данным A. Szczeklik соавт., взрослые больные аспириновой астмой, проживающие в Европе, имеют в анамнезе
2-3 полипэктомии [10]. Мы наблюдали двоих детей в возрасте 11 и 14 лет с диагнозом аспириновой астмы, перенесших 10 и 15 полипэктомий соответственно [42].
В лечении аспириновой астмы иногда используют кромоны [31].
Установлено, что блокаторы лейкотриеновых рецепторов способствуют улучшению не только клинических симптомов БА и показателей спирометрии, но и экстрапульмональных проявлений заболевания (назальные, гастроинтестинальные, кожные симптомы) [43, 44]. Однако следует помнить о том, что примерно у 1/3 пациентов чувствительность к антилейкотриеновым препаратам поначалу может не проявляться: обычно этот показатель оценивается к концу 3-4-й недели от начала их приема [46].
В литературе нет данных о терапевтической эффективности у больных аспириновой астмой сочетанного применения блокатора лейкотриеновых рецепторов и ингибитора фермента липооксигеназы, например зилеутона, зафирлукаста и монтелукаста.
У большей части больных с аспириновой триадой имеет место тяжелое течение БА, которое требует назначения гормональной терапии. Так, по данным A. Szczeklik и соавт., из 360 таких больных 80% принимали ингаляционные кортикостероиды, а 1/3 нуждались в их пероральном приеме; лечение иммуносупрессирующим препаратом циклоспорином А не способствовало снижению зависимости от стероидов [11].
Последние исследования подтверждают комплементарный эффект при сочетанном применении антилейкотриеновых и гормональных средств в терапии больных БА, в том числе и с аспириновым вариантом течения астмы [45—50].
У больных с аспириновой астмой, имеющих высокую сенсибилизацию к аэроаллергенам, при проведении специфической аллерговакцинации причинно-значимыми аллергенами может быть достигнут хороший клинический эффект [51].
При классическом симптомокомплексе (риносинусит + назальный полипоз + БА + эозинофилия) эффективна десенситизация аспирином. Регулярный прием определенных доз аспирина оказывает down-регулирующее влияние на уровень рецепторов цистеиновых лейкотриенов [10]. Этот метод лечения взрослых больных аспириновой астмой способствовал у 2/3 из них снижению проявлений риносинусита, а у 1/2 — клинической симптоматики заболевания. Особенно хороший эффект десенситизации достигается у больных аспириновой астмой, имеющих в анамнезе полипотомию. При анафилактической реакции на анальгетики десенситизация ацетилсалициловой кислотой противопоказана.
В литературе последних лет появились сообщения о том, что ацикловир — препарат, ингибирующий ДНК-полимеразу вируса герпеса, — помогает предотвратить развитие бронхоспазма и снизить уровень ЛтЕ4 в моче у больных аспириновой астмой. У таких пациентов предварительное вдыхание сальметерола оказывает мощный бронхопротективный эффект при проведении провокационного теста лизин-ацетилсалициловой кислотой.
Проведенный нами 8-недельный курс лечения рокситромицином у взрослых больных с аспириновой астмой позволил достоверно уменьшить симптоматику заболевания и снизить количество эозинофилов в крови и мокроте. Хотя влияния препарата на экскрецию ЛтЕ4 в моче при этом не отмечалось, воздействие на эозинофильную инфильтрацию респираторного тракта может представлять собой новый подход к терапии аспириновой астмы. Мизопростол — аналог простагландина Е2 — не улучшает клиническое течение аспириновой астмы и не влияет на метаболизм аспирина.
Распространенность аспириновой астмы в детском возрасте, особенности ее течения, а также многие неясные вопросы терапии этой очень сложной формы БА требуют дальнейших исследований, накопления и обобщения фактов.
По вопросам литературы обращайтесь в редакцию
Д. Ш. Мачарадзе, доктор медицинских наук
Детская городская поликлиника №102, Москва