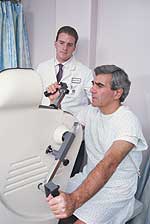
Установка электрокардиостимулятора

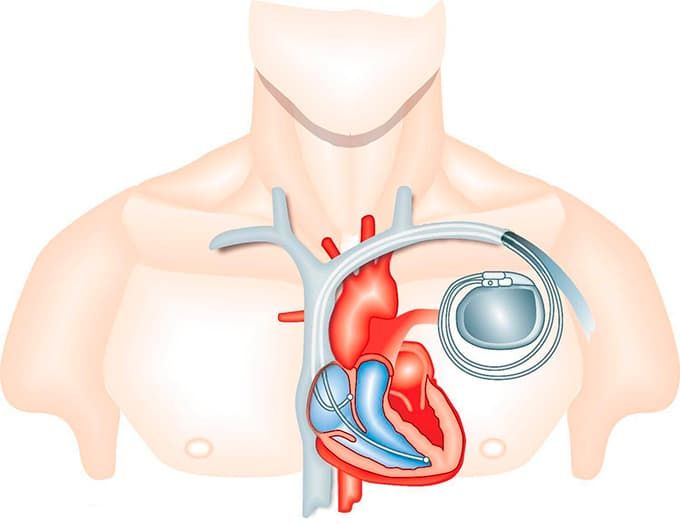
Электрокардиостимулятор, как правило, состоит из двух частей: металлический корпус, содержащий батарею, рассчитанную на 7-10 лет работы и микропроцессорный блок, который обеспечивает установку ЧСС и другие параметры; второй частью являются электроды, по которым происходит распространение электрических импульсов из ЭКС в камеры сердца. Кардиостимулятор являются лучшим средством для лечения брадиаритмий. Первый кардиостимулятор был имплантирован в 1958 году.
Существует три вида ЭКС (это зависит от места установки электродов):
Также ЭКС делят на временную (устанавливается наружный стимулятор на срок от нескольких часов до 2-ух недель) и постоянную (устанавливается вживляемый стимулятор).
Подготовка к лечению
Список обследований перед имплантацией ЭКС
Как проходит лечение
Возможные осложнения
Риски процедуры, как правило, составляет около 1%, включая кровотечение, пневмоторакс (попадание воздуха в плевральную полость), перфорацию сердца, риск нагноения и неисправность устройства.
Из возможных осложнений выделяют смещение и нарушения изоляции электродов, синдром ЭКС (головокружения и одышка при неправильной работе ЭКС) и инфекционные осложнения.
На самом деле подобные осложнения очень редки и несопоставимы с пользой установленного по показаниям электрокардиостимулятора.
 Прогноз и наблюдение после имплантации ЭКС
Прогноз и наблюдение после имплантации ЭКС
Имплантация кардиостимулятора может выполняться с минимальной болезненностью и практически без смертности. Пациент не испытывает каких то неприятных ощущений, связанных с деятельностью электрокардиостимулятора.
Сразу после имплантации аппарат начинает вырабатывать электрические импульсы при обнаружении долгой паузы в работе камер сердца, в другое время устройство находится в «ждущем режиме». Необходимо ежегодно проверять в клинике корректность работы и уровень заряда ЭКС.
Большинство пациентов выписываются из больницы в течение 24-48 часов после имплантации кардиостимулятора.
Пациенту необходимо будет носить идентификационную карту кардиостимулятора. Такие устройства, как противоугонные системы в магазинах, экранирующие устройства аэропорта и металлодетекторы, могут мешать работе устройства, хотя эти случаи встречаются редко.
Микроволновые печи и другие обычные бытовые приборы обычно не мешают функциям этих устройств. Однако мобильные телефоны должны быть размещены на расстоянии более 15 см от стимулятора, чтобы предотвратить возможное вмешательство.
Пациент с имплантированным кардиостимулятором должен всегда информировать врача перед тем, как пройти процедуру, которая использует медицинские или электронные устройства, опасаясь возможных помех.
Кардиолог регулярно проводит обследование пациента с установленным кардиостимулятором, чтобы оценить его функцию, настроить программы кардиостимуляции и оценить заряд батареи. Нельзя пренебрегать такими обследованиями, так как в случае остановки кардиостимулятора может остановиться и сердце.
Жизнь с кардиостимулятором
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Несмотря на то, что через 2-3 месяца после имплантации кардиостимулятора пациенты возвращаются к обычному образу жизни, существуют некоторые аспекты, которые необходимо знать пациентам с имплантированными устройствами.
Сразу после установки кардиостимулятора
Непосредственно после выписки из стационара в течение первой недели необходимо наблюдать за местом имплантации устройства. При появлении признаков воспаления, выделений из раны или расхождения швов, необходимо немедленно обратиться к врачу.
В первый месяц следует избегать подъема тяжестей, чрезмерной нагрузки на плечевой пояс и амплитудных движений руки на стороне имплантации. Через два месяца пациенты могут вернуться к обычной физической активности и возобновить занятия спортом, если они занимались спортом до имплантации стимулятора.
Не рекомендуются следующие виды физической активности:
Кардиостимулятор и электромагнитные приборы
Также имеются некоторые ограничения, связанные с возможным воздействием на устройство магнитных и электромагнитных полей. В настоящее время все устройства имеют достаточно надежную защиту от электромагнитных полей, и использование приборов и техники, окружающих нас в обычной жизни, не требует особых ограничений. Это касается компьютеров, микроволновых печей, мобильных телефонов. Не рекомендуется только носить мобильный телефон в нагрудном кармане.
Тем не менее, то или иное мощное воздействие может нарушить работу имплантированного устройства или причинить вред пациенту.
Запрещается:
1. Подвергаться воздействию мощных полей СВЧ, магнитных и электромагнитных полей, электрического тока (например, при использовании оборудования высокого напряжения, магнитов, используемых в промышленных зонах, радаров или других источников электромагнитного воздействия).
2. Выполнять магнитно-резонансную томографию (МРТ) в случаях, когда имплантируемое устройство не является МРТ-совместимым.
3. Использовать методы физиотерапии, связанные с магнитотерапией и электрическим воздействием.
4. Применять монополярную электрокоагуляцию при проведении хирургических вмешательств, в случаях, когда работа эндокардиального электрода запрограммирована в монополярном режиме
5. При проведении ультразвуковых исследований направлять луч непосредственно на корпус имплантированного устройства.
С осторожностью разрешается проводить следующие медицинские манипуляции и исследования:
2. МРТ: в случае МРТ-совместимого устройства необходимо запрограммировать устройство в МРТ режим.
3. Ультразвуковые исследования.
4. Дефибрилляцию и электрическую кардиоверсию.
6. Радиочастотные методы лечения.
7. Чрескожную электрическую нейростимуляцию.
Без каких-либо ограничений разрешается проводить стоматологические вмешательства и рентгенографические методы исследования.
Пациент должен наблюдаться специалистом, который будет с периодичностью 1-2 раза в год осуществлять проверку (программирование) имплантированного устройства с помощью специального оборудования-программатора. При появлении каких-либо симптомов (головокружение, предобморочные состояния, обмороки) следует незамедлительно обратиться к специалисту, который наблюдает пациента.
Рекомендации больным с имплантированным кардиостимулятором
Донецкая О.П, Дзвониская В.Н.
Кардиостимулятор – это медицинский прибор, который поддерживает ритм сердца в нормальном режиме. Операция по установке кардиостимулятора показана тем, у кого наблюдается слишком медленный ритм сердца или присутствует блокада между предсердиями и желудочками (антриовентикулярная блокада).
Операция по имплантации кардиостимулятора является малоинвазивной и может выполняться в условиях операционной, оснащенной рентгеновским аппаратом для мониторинга всех действий кардиохирурга. Для обезболивания применяется местная анестезия.
1. Врач пунктирует подключичную вену и закрепляет в ней интродьюсер, через который продвигает в просвет верхней полой вены электрод.
2. Далее под контролем рентгеноборудования электрод продвигается в правое предсердие или правый желудочек и закрепляется на стенке сердечной камеры. Если имплантируемый кардиостимулятор двух- или трехкамерный, то таким же образом выполняется и имплантация других электродов.
3. После фиксации электродов врач выполняет несколько проб для измерения порога возбудимости, на которые сердце отвечает сокращениями.
4. После получения хорошего графика ЭКГ, полученного с установленных электродов прибора, электроды фиксируются окончательно, и под кожей в подключичной области или под грудной мышцей выполняется «карман» для имплантации корпуса кардиостимулятора.
5. После введения прибора в «карман» и подключения к нему электродов ткани зашиваются.
В общей сложности такая методика операции по имплантации кардиостимулятора занимает не более одного часа.
Некоторое время после имплантации кардиостимулятора пациент может ощущать незначительное неудобство и болезненные ощущения в месте установки прибора. Также на месте введения прибора может образовываться гематома. У некоторых больных возможно повышение температуры тела. Все эти неприятные ощущения устраняются или самостоятельно, или при помощи симптоматической терапии. Как правило, больным после имплантации кардиостимулятора назначается профилактический курс приема антибиотиков. Уже в первый же день после операции большинство больных могут вставать с постели, а через неделю – возвращаются к привычному ритму жизни. Приступать к работе разрешается через 2 недели.
После установки кардиостимулятора больной в целом может вести привычный образ жизни. Большинство разнообразных приборов, оборудования и устройств, окружающих нас дома или на рабочем месте, не влияет на работу кардиостимулятора и может использоваться с минимальными мерами предосторожности или без них. Современные кардиостимуляторы достаточно хорошо защищены от внешних магнитных, электрических и электромагнитных воздействий, встречающихся в повседневной жизни.
Ограничений по питанию у пациентов с кардиостимуляторами нет. Необходимо следовать рекомендациям врача исходя из состояния здоровья и возможной диеты. Вождение транспорта также возможно без ограничений. Однако, необходимо соблюдать правила безопасности и не касаться высоковольтных проводов или проводов электрической системы автомобиля.
В первые три месяца после имплантации желательно ограничить движения рукой со стороны имплантации, избегая резких подъемов выше горизонтальной линии и резких отведений в сторону.
Пациенты с кардиостимуляторами могут заниматься любыми видами спорта, если нет ограничений по состоянию здоровья. Однако есть виды спорта, которых необходимо избегать:
• Стрельба из ружья или винтовки. Не стоит прикладывать приклад ружья в область плеча, где имплантирован кардиостимулятор. Отдача выстрела может привести к травме поверхностных тканей над кардиостимулятором.
• От подводного плавания, ныряния на любую глубину, дайвинга также желательно воздержаться. Разрешается заниматься обычным плаванием.
В любом случае, во время занятий физическими упражнениями необходимо ориентироваться на собственное самочувствие, и прекращать занятия сразу же, как возникнут тревожные симптомы или усталость.
Имплантируемый кардиостимулятор, как правило, не мешает обычной трудовой деятельности пациента. Можно работать по дому или на участке, использовать инструмент, в том числе электроинструмент, при условии его исправности (чтобы не было поражения электрическим током). Следует ограничить применение перфораторов и электродрелей, а также газонокосилок.
Существуют некоторые ограничения по использованию кардиостимуляторов и сотовых телефонов. Рекомендуется располагать телефон на расстоянии не менее 30 см от стимулятора и держать его у уха, противоположного стороне, на которой находится кардиостимулятор. На себе носить сотовый телефон не рекомендуется.
Кардиостимулятор не ограничивает человека в передвижении, и возможно планировать свои поездки на длительный период времени. Средства контроля в магазинах и аэропортах («рамки») испортить стимулятор не могут, однако желательно сократить пребывание в зоне их действия до минимума, так как магнитное поле оказывает влияние только непосредственно в момент прохода через «рамку». Необходимо будет предъявить свое удостоверение (карта пациента) на контрольно-пропускных пунктах в аэропортах, вокзалах, чтобы при необходимости выполнили ручной досмотр.
Однако во избежание сбоев в работе прибора следует соблюдать некоторые важные правила:
Проверка ЭКС
Первая проверка проводится через 1,5-3 месяца после операции. За это время формируется хронический порог стимуляции, то есть становится возможной окончательная регулировка энергетических параметров стимуляции и можно проводить коррекцию параметров частотной адаптации. В течение первого года желательно провести проверки через 6 и 12 месяцев после операции. Это позволит убедиться в правильности подбора параметров стимуляции и лечебных функций. Далее, при отсутствии жалоб, больной может проходить контрольные осмотры один или два раза в год.
По мере приближения к окончанию срока службы аппарата (7-8 лет), который определен временем разрядки батареи, интервалы между проверками должны укорачиваться, особенно в тех случаях, когда больной «стимуляторзависимый» (собственный ритм сокращений сердца менее 30 в минуту). Важно не пропустить время рекомендуемой замены ЭКС. Обычная проверка ЭКС в кабинете врача включает: регистрацию электрокардиограммы и определение параметров стимуляции с помощью специальных приборов. После проверки может потребоваться перепрограммирование ЭКС, для того чтобы стимуляционная терапия соответствовала состоянию пациента.
Досрочный визит к врачу должен состояться при появлении таких жалоб:
Таким образом, после установки кардиостимулятора больной в целом может вести привычный образ жизни, однако во избежание сбоев в работе прибора следует соблюдать некоторые правила и проходить регулярное медицинское обследование.
Статья добавлена 7 июня 2016 г.
Лечение нарушений ритма сердца
Почему терапия аритмий считается одним из самых сложных разделов кардиологии? Как классифицируются аритмии? Какие группы лекарственных препаратов используются при лечении аритмий? Нарушения ритма сердца (аритмии) представляют собой один из самы
Почему терапия аритмий считается одним из самых сложных разделов кардиологии?
Как классифицируются аритмии?
Какие группы лекарственных препаратов используются при лечении аритмий?
Нарушения ритма сердца (аритмии) представляют собой один из самых сложных разделов клинической кардиологии. Отчасти это объясняется тем, что для диагностики и лечения аритмий необходимо очень хорошее знание электрокардиографии, отчасти — огромным разнообразием аритмий и большим выбором способов лечения. Кроме того, при внезапных аритмиях нередко требуется проведение неотложных лечебных мероприятий.
Одним из основных факторов, повышающих риск возникновения аритмий, является возраст. Так, например, мерцательную аритмию выявляют у 0,4% людей, при этом большую часть пациентов составляют люди старше 60 лет [1, 2, 4]. Увеличение частоты развития нарушений ритма сердца с возрастом объясняется изменениями, возникающими в миокарде и проводящей системе сердца в процессе старения. Происходит замещение миоцитов фиброзной тканью, развиваются так называемые «склеродегенеративные» изменения. Кроме этого, с возрастом повышается частота сердечно-сосудистых и экстракардиальных заболеваний, что также увеличивает вероятность возникновения аритмий [17, 18].
Основные клинические формы нарушений ритма сердца
По характеру клинического течения нарушения ритма сердца могут быть острыми и хроническими, преходящими и постоянными. Для характеристики клинического течения тахиаритмий используют такие определения, как «пароксизмальные», «рецидивирующие», «непрерывно рецидивирующие» [2].
Лечение нарушений ритма сердца
Показаниями для лечения нарушений ритма являются выраженные нарушения гемодинамики или субъективная непереносимость аритмии. Безопасные, бессимптомные или малосимптомные легко переносящиеся аритмии не требуют назначения специального лечения. В этих случаях основным лечебным мероприятием является рациональная психотерапия. Во всех случаях прежде всего проводится лечение основного заболевания.
Антиаритмические препараты
Основным способом терапии аритмий является применение антиаритмических препаратов. Хотя антиаритмические препаты не могут «вылечить» от аритмии, они помогают уменьшить или подавить аритмическую активность и предотвратить рецидивирование аритмий.
Любое воздействие антиаритмическими препаратами может вызывать как антиаритмический, так и аритмогенный эффект (то есть, наоборот, способствовать возникновению или развитию аритмии). Вероятность проявления антиаритмического эффекта для большинства препаратов составляет в среднем 40–60% (и очень редко для некоторых препаратов при отдельных вариантах аритмии достигает 90%). Вероятность развития аритмогенного эффекта составляет в среднем примерно 10%, при этом могут возникать опасные для жизни аритмии. В ходе нескольких крупных клинических исследований было выявлено заметное повышение общей летальности и частоты случаев внезапной смерти (в 2 — 3 раза и более) среди больных с органическим поражением сердца (постинфарктный кардиосклероз, гипертрофия или дилатация сердца) на фоне приема антиаритмических препаратов класса I, несмотря на то что эти средства эффективно устраняли аритмии [7, 8, 9].
Согласно наиболее распространенной на сегодняшний день классификации антиаритмических препаратов Вогана Вильямса, все антиаритмические препараты подразделяются на 4 класса:
I класс — блокаторы натриевых каналов.
II класс — блокаторы бета-адренергических рецепторов.
III класс — препараты, увеличивающие продолжительность потенциала действия и рефрактерность миокарда.
IV класс — блокаторы кальциевых каналов.
Применение комбинаций антиаритмических препаратов в ряде случаев позволяет достичь существенного повышения эффективности антиаритмической терапии. Одновременно отмечается уменьшение частоты и выраженности побочных явлений вследствие того, что препараты при комбинированной терапии назначают в меньших дозах [3, 17].
Следует отметить, что показаний для назначения так называемых метаболических препаратов пациентам с нарушениями ритма не существует. Эффективность курсового лечения такими препаратами, как кокарбоксилаза, АТФ, инозие-Ф, рибоксин, неотон и т. п., и плацебо одинаковы. Исключение составляет милдронат, препарат цитопротективного действия, имеются данные об антиаритмическом эффекте милдроната при желудочковой экстрасистолии [3].
Особенности лечения основных клинических форм нарушений ритма
Экстрасистолия
Клиническое значение экстрасистолии практически целиком определяется характером основного заболевания, степенью органического поражения сердца и функциональным состоянием миокарда. У лиц без признаков поражения миокарда с нормальной сократительной функцией левого желудочка (фракция выброса больше 50%) наличие экстрасистолии не влияет на прогноз и не представляет опасности для жизни. У больных с органическим поражением миокарда, например с постинфарктным кардиосклерозом, экстрасистолия может рассматриваться в качестве дополнительного прогностически неблагоприятного признака. Однако независимое прогностическое значение экстрасистолии не определено. Экстрасистолию (в том числе экстрасистолию «высоких градаций») даже называют «косметической» аритмией, подчеркивая таким образом ее безопасность.
Как было уже отмечено, лечение экстрасистолии с помощью антиаритмических препаратов класса I C значительно увеличивает риск смерти. Поэтому при наличии показаний лечение начинают с назначения β-блокаторов [8, 17, 18]. В дальнейшем оценивают эффективность терапии амиодароном и соталолом. Возможно также применение седативных препаратов. Антиаритмические препараты класса I C используют только при очень частой экстрасистолии, в случае отсутствия эффекта от терапии β-блокаторами, а также амидороном и соталолом (табл. 3)
Тахиаритмии
В зависимости от локализации источника аритмии различают наджелудочковые и желудочковые тахиаритмии. По характеру клинического течения выделяют 2 крайних варианта тахиаритмий (постоянные и пароксизмальные. Промежуточное положение занимают преходящие или рецидивирующие тахиаритмии. Чаще всего наблюдается мерцательная аритмия. Частота выявления мерцательной аритмии резко увеличивается с возрастом больных [1, 17, 18].
Мерцательная аритмия
Пароксизмальная мерцательная аритмия. В течение первых суток у 50% больных с пароксизмальной мерцательной аритмией отмечается спонтанное восстановление синусового ритма. Однако произойдет ли восстановление синусового ритма в первые часы, остается неизвестным. Поэтому при раннем обращении больного, как правило, предпринимаются попытки восстановления синусового ритма с помощью антиаритмических препаратов. В последние годы алгоритм лечения мерцательной аритмии несколько усложнился. Если от начала приступа прошло более 2 суток, восстановление нормального ритма может быть опасным — повышен риск тромбоэмболии (чаще всего в сосуды мозга с развитием инсульта). При неревматической мерцательной аритмии риск тромбоэмболий составляет от 1 до 5% (в среднем около 2%). Поэтому, если мерцательная аритмия продолжается более 2 суток, надо прекратить попытки восстановления ритма и назначить больному непрямые антикоагулянты (варфарин или фенилин) на 3 недели в дозах, поддерживающих показатель международного нормализованного отношения (МНО) в пределах от 2 до 3 (протромбиновый индекс около 60%). Через 3 недели можно предпринять попытку восстановления синусового ритма с помощью медикаментозной или электрической кардиоверсии. После кардиоверсии больной должен продолжить прием антикоагулянтов еще в течение месяца.
Таким образом, попытки восстановления синусового ритма предпринимают в течение первых 2 суток после развития мерцательной аритмии или через 3 недели после начала приема антикоагулянтов. При тахисистолической форме сначала следует уменьшить ЧСС (перевести в нормосистолическую форму) с помощью препаратов, блокирующих проведение в атриовентрикулярном узле: верапамила, β-блокаторов или дигоксина.
Для восстановления синусового ритма наиболее эффективны следующие препараты:
Сегодня с целью восстановления синусового ритма при мерцательной аритмии все чаще назначают однократную дозу амиодарона или пропафенона перорально. Эти препараты отличаются высокой эффективностью, хорошей переносимостью и удобством приема. Среднее время восстановления синусового ритма после приема амиодарона (30 мг/кг) составляет 6 ч, после пропафенона (600 мг) — 2 ч [6, 8, 9].
При трепетании предсердий кроме медикаментозного лечения можно использовать чреспищеводную стимуляцию левого предсердия с частотой, превышающей частоту трепетания, — обычно около 350 импульсов в минуту, продолжительностью 15–30 с. Кроме того, при трепетании предсердий очень эффективным может быть проведение электрической кардиоверсии разрядом мощностью 25–75 Дж после в/в введения реланиума.
Постоянная форма мерцательной аритмии. Мерцание предсердий является наиболее часто встречающейся формой устойчивой аритмии. У 60% больных с постоянной формой мерцательной аритмии основным заболеванием являются артериальная гипертония или ИБС. В ходе специальных исследований было выявлено, что ИБС становится причиной развития мерцательной аритмии примерно у 5% больных. В России существует гипердиагностика ИБС у больных с мерцательной аритмией, особенно среди людей пожилого возраста. Для постановки диагноза ИБС всегда необходимо продемонстрировать наличие клинических проявлений ишемии миокарда: стенокардии, безболевой ишемии миокарда, постинфарктного кардиосклероза.
Мерцательная аритмия обычно сопровождается неприятными ощущениями в грудной клетке, могут отмечаться нарушения гемодинамики и, главное, повышается риск возникновения тромбоэмболий, прежде всего в сосуды мозга. Для снижения степени риска назначают антикоагулянты непрямого действия (варфарин, фенилин). Менее эффективно применение аспирина [1, 17, 18].
Основным показанием для восстановления синусового ритма при постоянной форме мерцательной аритмии является «желание больного и согласие врача».
Для восстановления синусового ритма используют антиаритмические препараты или электроимпульсную терапию.
Антикоагулянты назначают, если мерцательная аритмия наблюдается более 2 суток. Особенно высок риск развития тромбоэмболий при митральном пороке сердца, гипертрофической кардиомиопатии, недостаточности кровообращения и тромбоэмболиях в анамнезе. Антикоагулянты назначают в течение 3 недель до кардиоверсии и в течение 3 — 4 недель после восстановления синусового ритма. Без назначения антиаритмических препаратов после кардиоверсии синусовый ритм сохраняется в течение 1 года у 15 — 50% больных. Применение антиаритмических препаратов повышает вероятность сохранения синусового ритма. Наиболее эффективно назначение амиодарона (кордарона) — даже при рефрактерности к другим антиаритмическим препаратам синусовый ритм сохраняется у 30 — 85% больных [2, 12]. Кордарон нередко эффективен и при выраженном увеличении левого предсердия.
Кроме амиодарона для предупреждения повторного возникновения мерцательной аритмии с успехом используются соталол, пропафенон, этацизин и аллапинин, несколько менее эффективны хинидин и дизопирамид. При сохранении постоянной формы мерцательной аритмии больным с тахисистолией для снижения ЧСС назначают дигоксин, верапамил или β-блокаторы. При редко встречающемся брадисистолическом варианте мерцательной аритмии эффективным может быть назначение эуфиллина (теопек, теотард).
Проведенные исследования показали, что две основные стратегии ведения больных с мерцательной аритмией — попытки сохранения синусового ритма или нормализация ЧСС на фоне мерцательной аритмии в сочетании с приемом непрямых антикоагулянтов — обеспечивают примерно одинаковое качество и продолжительность жизни больных [17].
Пароксизмальные наджелудочковые тахикардии
Пароксизмальные наджелудочковые тахикардии, встречающиеся гораздо реже, чем мерцательная аритмия, не связаны с наличием органического поражения сердца. Частота их выявления с возрастом не увеличивается.
Купирование пароксизмальных наджелудочковых тахикардий начинают с применения вагусных приемов. Наиболее часто используют пробу Вальсальвы (натуживание на вдохе около 10 с) и массаж сонной артерии. Очень эффективным вагусным приемом является «рефлекс ныряния» (погружение лица в холодную воду) — восстановление синусового ритма отмечается у 90% больных. При отсутствии эффекта от вагусных воздействий назначают антиаритмические препараты. Наиболее эффективны в этом случае верапамил, АТФ или аденозин.
У больных с легко переносящимися и сравнительно редко возникающими приступами тахикардии практикуется самостоятельное пероральное купирование приступов. Если в/в введение верапамила оказывается эффективным, можно назначить его внутрь в дозе 160–240 мг однократно, в момент возникновения приступов. Если более эффективным признается в/в введение новокаинамида — показан прием 2 г новокаинамида. Можно иcпользовать 0,5 г хинидина, 600 мг пропафенона или 30 мг/кг амиодарона внутрь.
Желудочковые тахикардии
Желудочковые тахикардии в большинстве случаев возникают у больных с органическим поражением сердца, чаще всего при постинфарктном кардиосклерозе [13, 14].
Лечение желудочковой тахикардии. Для купирования желудочковой тахикардии можно использовать амиодарон, лидокаин, соталол или новокаинамид.
При тяжелых, рефрактерных к медикаментозной и электроимпульсной терапии, угрожающих жизни желудочковых тахиаритмиях применяют прием больших доз амиодарона: внутрь до 4 — 6 г в сутки перорально в течение 3 дней (то есть по 20 — 30 табл.), далее по 2,4 г в сутки в течение 2 дней (по 12 табл.) с последующим снижением дозы [6, 10, 15, 16].
Предупреждение рецидивирования тахиаритмий
При частых приступах тахиаритмий (например, 1 — 2 раза в неделю) последовательно назначают антиаритмические препараты и их комбинации до прекращения приступов. Наиболее эффективным является назначение амиодарона в качестве монотерапии или в комбинации с другими антиаритмическими препаратами, прежде всего с β-блокаторами.
При редко возникающих, но тяжелых приступах тахиаритмий подбор эффективной антиаритмической терапии удобно проводить с помощью чреспищеводной электростимуляции сердца — при наджелудочковых тахиаритмиях — и программированной эндокардиальной стимуляции желудочков (внутрисердечное электрофизиологическое исследование) — при желудочковых тахиаритмиях. С помощью электростимуляции в большинстве случаев удается индуцировать приступ тахикардии, идентичный тем, которые спонтанно возникают у данного больного. Невозможность индукции приступа при повторной электрокардиостимуляции на фоне приема препаратов обычно совпадает с их эффективностью при длительном приеме [17, 18]. Следует отметить, что некоторые проспективные исследования продемонстрировали преимущество «слепого» назначения амиодарона и соталола при желудочковых тахиаритмиях перед тестированием антиаритмических препаратов класса I с помощью программированной электростимуляции желудочков или мониторирования ЭКГ.
При тяжелом течении пароксизмальных тахиаритмий и рефрактерности к медикаментозной терапии применяют хирургические способы лечения аритмий, имплантацию кардиостимулятора и кардиовертера-дефибриллятора.
Подбор антиаритмической терапии у больных с рецидивирующимим аритмиями
С учетом безопасности антиаритмических препаратов оценку эффективности целесообразно начинать с β-блокаторов или амиодарона. При неэффективности монотерапии оценивают действенность назначения амиодарона в комбинации с β-блокаторами [17]. Если нет брадикардии или удлинения интервала РR, с амиодароном можно сочетать любой β-блокатор. У больных с брадикардией к амиодарону добавляют пиндолол (вискен). Показано, что совместный прием амиодарона и β-блокаторов способствует значительно большему снижению смертности пациентов с сердечно-сосудистыми заболеваниями, чем прием каждого из препаратов в отдельности. Некоторые специалисты даже рекомендуют имплантацию двухкамерного стимулятора (в режиме DDDR) для безопасной терапии амиодароном в сочетании с β-блокаторами. Антиаритмические препараты класса I применяют только при отсутствии эффекта от β-блокаторов и/или амиодарона. Препараты класса I C, как правило, назначают на фоне приема бета-блокатора или амиодарона. В настоящее время изучается эффективность и безопасность применения соталола (β-блокатора, обладающего свойствами препаратов класса III).
П. Х. Джанашия, доктор медицинских наук, профессор
Н. М. Шевченко, доктор медицинских наук, профессор
С. М. Сорокoлетов, доктор медицинских наук, профессор
РГМУ, Медицинский центр Банка России, Москва
 Прогноз и наблюдение после имплантации ЭКС
Прогноз и наблюдение после имплантации ЭКС