Антиэстроген
| Антиэстроген | |
|---|---|
| Класс препарата | |
 | |
| Идентификаторы класса | |
| Синонимы | Антагонисты эстрогенов; Блокаторы эстрогенов; Антагонисты эстрадиола |
| Использовать | Рак груди ; Бесплодие ; Мужской гипогонадизм ; Гинекомастия ; трансгендерные мужчины |
| Код УВД | L02BA |
| Биологическая мишень | Рецептор эстрогена |
| Химический класс | Стероидный ; Нестероидные ( трифенилэтилен и др.) |
| Внешние ссылки | |
| MeSH | D020847 |
| В Викиданных | |
Рецепторы эстрогена (ER), такие как ERα и ERβ, включают домен функции активации 1 (AF1) и домен функции активации 2 (AF2), в которых SERMS действуют как антагонисты для домена AF2, в то время как «чистые» антиэстрогены, такие как ICI 182,780 и ICI 164,384, являются антагонистами для домены AF1 и AF2. [9]
Хотя ингибиторы ароматазы и антигонадотропины могут считаться антиэстрогенами по некоторым определениям, их часто рассматривают как отдельные классы. [10] Ингибиторы ароматазы и антигонадотропины снижают выработку эстрогена, в то время как термин «антиэстроген» часто используется для обозначения агентов, снижающих реакцию на эстроген. [11]
Антиэстрогены используются для:
Антиэстрогенное действие что это
Рак молочной железы — серьезное заболевание, которое в том числе зависит от уровня эстрогенов. А еще часто говорят про метаболиты эстрогенов и их соотношение. Без медицинского образования разобраться в этом сложно. Мы попросили экспертов проекта «Новая жизнь» ответить на самые частые вопросы простым и понятным языком (насколько это вообще возможно). Прочитав эту статью, вы узнаете, что такое эстрогены и их метаболиты, как они связаны с женским здоровьем и многом другом не менее важном.
— Давайте для начала разберемся, что такое эстрогены и зачем они нужны.
Эстрогены — это половые гормоны. Их так называют, потому что они в основном действуют на репродуктивную систему женщины, то есть на те органы, которые нужны для беременности, рождения ребенка и кормления. Например, эстрогены помогают организовать менструальный цикл, чтобы женщина была готова к зачатию. У женщин эстрогенов намного больше, чем у мужчин. Собственно говоря, именно эстрогены делают женское тело женским.
У эстрогенов есть и другие функции. Например, они поддерживают здоровье костей, влияют на настроение, уровень холестерина, функцию сердца и сосудов и даже немного на состояние кожи. Каждый врач, который занимается женским здоровьем, должен хотя бы немного разбираться в эстрогенах. Чаще всего анализы на эстрогены назначают врачи-гинекологи. Грамотного врача интересует не сам гормон, а вся система, в которой он работает.
— Верно ли, что эстрогены бывают разные и что работают они в организме тоже по-разному?
Да, эстрогены — это собирательное название для нескольких гормонов. Три самых главных — это эстрон, эстрадиол и эстриол. Они отличаются друг от друга по строению и немножко по своей задаче. Эстрадиол — самый главный и самый известный. Он организует менструальный цикл и поддерживает женское здоровье вплоть до последней менструации. После этого главным становится эстрон, хотя его в организме меньше. Поэтому иногда врачи после 50 лет дают женщине небольшие дозы эстрадиола, чтобы она лучше себя чувствовала. Что касается эстриола, то он наиболее активен во время беременности.
— Что такое метаболиты эстрогенов и почему они важны?
В природе ничто не исчезает бесследно. После того как гормон пришел в клетку и сказал ей, что делать, его нужно куда-то деть. Иначе он продолжит давать сигналы, и клетка запутается. Поэтому в клетке есть специальная система, которая берет эстроген и меняет его структуру. Это процесс называется — метаболизм эстрогенов, а получившиеся новые молекулы — метаболиты эстрогенов. Они нужны для того, чтобы выводить использованные эстрогены из организма. Если бы их не было, то эстрогены накопились бы в организме, а это вредно.
— Говорят, что есть разные метаболиты. Чем они отличаются?
Сначала пару слов о том, как работает метаболизм эстрогенов. Это сложная цепочка химических реакций. Её можно сравнить с химической фабрикой. На входе — эстрогены, на выходе — метаболиты. И вот на этой фабрике есть три конвейера. В зависимости от того, на какой конвейер попадет эстроген, получится тот или иной метаболит. Чтобы не путаться, врачи и химики используют цифры — 2, 4 и 16. Можно сказать, что они обозначают, по какому конвейеру прошел эстроген. Например, 2-гидроксиэстрон и 2-гидроксиэстрадиол это разные молекулы, но обе получаются на одном конвейере. А вот 16-альфа-гидроксиэстрон или 4-гидроксиэстрадиол это уже продукты других конвейеров.
Это важно, потому что у метаболитов с разных конвейеров — разные химические свойства. Чтобы не путаться, скажем так: 2-метаболиты ослабляют сигнал эстрогенов, а 4-метаболиты и 16-метаболиты — дают такой же сигнал, как эстрогены или даже сильнее. Поэтому если у женщины есть факторы риска онкологических заболеваний, то 2-метаболиты для нее полезны, а 16-метаболиты — вредны. Поэтому врачей интересует соотношение 2-метаболитов и 16-метаболитов. Если 2-метаболитов больше, то эстрогенам будет сложнее заставить клетку расти. А если 16-метаболитов больше, то она будет расти сильнее. Что касается 4-метаболитов, то они действуют по-разному, и мы не будем в них подробно разбираться.
Врачи стараются подавить сигнал эстрогенов, чтобы клетки опухоли не росли. Например, для этого назначают тамоксифен — он не дает эстрогенам стимулировать рост клеток. Но у тамоксифена есть побочные эффекты, потому что он выключает все сигналы эстрогенов, и полезные, и вредные. Поэтому врачи придумали другие способы влиять на сигнал эстрогенов. Если сделать так, чтобы фабрика, про которую мы говорили, производила побольше безопасных 2-метаболитов и поменьше вредных 16-метаболитов, то организму будет проще бороться с опухолью или не давать ей возникнуть.
— Как же тогда понять, сколько и каких метаболитов производится?
Вот для этого как раз и нужен анализ на метаболиты эстрогенов. Обычно, когда мы делаем анализ, лаборатория нам выдает результаты с табличкой, в которой перечислены разные метаболиты и их уровни. Это выглядит примерно так:
| Метаболит | Название | Уровень | Норма |
| 2-OHE1 | 2-гидроксиэстрон | 2,69 | 0,24-11,1 |
| 2-OHE2 | 2-гидроксиэстрон | 6,32 | 0,35-10,77 |
| 16a-OHE1 | 6-альфагидроксиэстрон | 2,986 | 0,079-4,070 |
Когда мы получаем анализ, мы сразу смотрим, попадают ли наши уровни в нормальные значения. По этой табличке видно, что вроде бы все метаболиты в пределах нормы. Но радоваться рано, потому что нас интересуют не сами метаболиты, а их соотношение. Нам надо понять, каких метаболитов больше, а для это надо разделить хорошие на плохие. Обычно лаборатория это делает сама. Например, в бланке анализа может быть вот такая строчка:
(2-OHE1 + 2-OHE2) / 16a-OHE1 = 3,02
Разберемся, что есть что. В первой части, до знака деления у нас скобки. В этих скобках — два разных метаболита. По цифре «2» в названии мы понимаем, что это полезные 2-метаболиты. После знака деления у нас стоит опасный 16-метаболит. Все это значит, что в лаборатории посмотрели уровень каждого метаболита, а потом разделили 2-метаболиты на 16-метаболит. И получился результат — 3,05.
Чтобы было понятнее, давайте посмотрим, как это выглядит с цифрами:
2,69 + 6,32 / 2,986 = 3,02
Получается, что у этой женщины соотношение метаболитов — 3,02. Осталось понять, хорошо это или нет. У врачей для этого есть простое правило. Если соотношение больше 2, это значит, что хороших метаболитов в два раза больше, и это хорошо. Если соотношение меньше 2, то это не очень хорошо. В целом, чем соотношение выше, тем лучше. Чем ниже, тем хуже. Например, у другой женщины мы получаем такие результаты:
1,09 + 2,13 / 4,49 = 0,71
Результат 0,71 означает, что соотношение низкое, то есть что опасных 16-метаболитов намного больше. Это значит, что клетки получают сигнал для роста, и повышен риск различных заболеваний. Нужно что-то делать, и чуть позже мы поговорим об этом.
— Какой анализ лучше сдавать на метаболиты эстрогенов?
Метаболиты эстрогенов обычно смотрят в моче. Иногда в разовой порции, иногда — в суточной. Если есть возможность, то лучше делать в суточной, потому что тогда мы получаем более точную картину.
— Как подготовиться к исследованию?
Специальной подготовки не нужно. Если вы сдаете разовую мочу, то нужно утром собрать среднюю порцию в стерильный контейнер (вам его дадут в лаборатории или продадут в аптеке). Средняя порция означает, что надо начать мочиться в унитаз, потом подставить контейнер под струю и потом его убрать.
Если вы сдаете суточную мочу, то все чуть сложнее. В лаборатории вам дадут два контейнера — большой и маленький. В день, когда вы начинаете собирать мочу, утром вы мочитесь в унитаз, потому что первая суточная порция не учитывается. Далее в течение 24 часов вы мочитесь только в большой контейнер, даже если проснулись ночью. Хранить его надо в холодильнике на нижней полке (температура от 2 до 8 градусов, замораживать нельзя). На следующее утро вы также мочитесь в контейнер, а затем измеряете объем мочи (на контейнере есть мерные деления) и потом хорошенько перемешиваете мочу, отливаете 50-100 мл в маленький контейнер, и в течение часа относите в лабораторию. На маленьком контейнере нужно написать, сколько вы всего собрали мочи.
Есть еще несколько правил: во время сбора мочи вы пьете и едите как обычно, не принимаете алкоголь, стараетесь воздерживаться от физических нагрузок, не принимаете мочегонные препараты. Если все это выполнить, то анализ будет более точным.
— Кому это исследование показано?
Его можно делать любой женщине, у которой есть факторы риска онкологических заболеваний и некоторые другие проблемы. Самые частые из них — ожирение, нерегулярный менструальный цикл, разные виды дисфункции яичников. И конечно, любые проблемы с молочной железой. Анализ на соотношение метаболитов не заменяет собой другие анализы (например, на генетическую предрасположенность к онкологии). Но он помогает более эффективно планировать профилактику и смотреть, как она работает. — Что даст этот анализ, чему он поможет?
Давайте представим себе такую ситуацию. Есть женщина, которой 55 лет. Несколько лет назад у нее нашли рак молочной железы, сделали ей операцию и провели курс терапии. Сейчас ей вроде бы ничего не угрожает. Но врач решает проверить, насколько высок риск рецидива. Для этого женщина делает анализ на соотношение метаболитов, и оказывается, что оно очень низкое. Значит риск повышен. Врач дает ей рекомендации по профилактике и просит сдать анализ повторно через полгода. Женщина выполняет все рекомендации и на повторном анализе видит, что соотношение метаболитов выросло. Это значит, что риск снизился. Значит теперь она точно не заболеет?
К сожалению, риск есть всегда. Рак — это серьезное заболевание, и никто не может дать полной гарантии, что он не возникнет или что не будет рецидива. Но профилактика все равно нужна. Давайте посмотрим на это с другой стороны. Когда человек ездит на машине, всегда есть риск попасть в аварию и пострадать. Но этот риск бывает разным. Если водитель аккуратный и хорошо знает правила, машина — надежная и каждый год проходит техобслуживание, а дорога — чистая и безопасная, то риск очень низкий. А вот если водитель пьяный, машина дымит и скрипит, а на дороге — лед и туман, то риск очень высокий. Поэтому все, что мы можем сделать — это всеми силами снижать риск.
— Поговорим о профилактике.
Профилактика рака молочной железы бывает двух видов. Первый — это хемопрофилактика, то есть разные лекарственные средства, которые снижают активность сигнала эстрогенов. Их должен назначать врач. Второй — это здоровый образ жизни. Врачи рекомендуют не курить, больше двигаться, есть здоровую пищу. Это универсальные рекомендации, но для женщин они особенно важны. Дело в том, что правильное питание дает необходимые ресурсы для правильной работы нашей фабрики метаболитов. То есть, если женщина лучше питается, то у нее больше полезных метаболитов и меньше опасных.
— Какие продукты рекомендуется употреблять для улучшения процесса метаболизма эстрогенов?
Исследования последних лет показали, что лучше всего на эту роль подходят растения из семейства крестоцветных. Речь идет о брокколи, цветной капусте и кабачках. В процессе эволюции они научились синтезировать вещество, которое называется индол-3-карбинол. Оно помогает нашей внутренней фабрике работать лучше и производить больше полезных метаболитов. В результате соотношение метаболитов повышается, а риск снижается.
В крупном европейском исследовании сравнили людей, которые ели крестоцветные регулярно и тех, кто ел их редко или вообще не ел. Оказалось, что за счет крестоцветных можно снизить вероятность рака молочной железы на 17%. Это не очень много с точки зрения статистики, но для конкретных женщин, у которых не возникло рака молочной железы, это хороший результат.
— У многих сейчас возникнет вопрос, неужели теперь нужно каждый день есть брокколи или цветную капусту?
Можно, но, во-первых, не все любят брокколи, а во-вторых, часть полезных веществ погибает при термической обработке. Поэтому проще принимать биологически активную добавку к пище, которая уже содержит индол-3-карбинол. Например, в России есть БАД, который называется Промисан. В Промисане содержится необходимая для профилактики доза индол-3-карбинола, а также еще несколько полезных веществ — экстракт зеленого чая (помогает бороться с воспалительными процессами) и витамины. Промисан принимают два раза в сутки по две капсулы, одновременно с приемом пищи, в течение 3-6 месяцев. В сочетании с регулярной физической активностью и снижением веса это может дать хороший результат. И вот, чтобы его оценить, нам и нужны метаболиты эстрогенов.
Давайте разберем на примере. Допустим, есть женщина, которая хочет снизить риск рака молочной железы или рецидива. Она сдает анализы на метаболиты эстрогенов и начинает заниматься профилактикой: принимает индол-3-карбинол, старается больше двигаться, пробует бросить курить. Через полгода она сдает анализ и еще раз смотрит, что получилось. Если она все сделала правильно, то соотношение должно повыситься. Например, оно было 1.5, а стало 4.2. Это значит, что полезных 2-метаболитов стало больше, и поэтому риск снизился. Это хороший сценарий, а что может пойти не так? Да, в жизни бывает по-разному. Давайте посмотрим на другие сценарии.
— Можно ли Промисан сочетать с химиотерапией рака молочной железы?
Да, можно, он не мешает другим лекарствам (даунорубицин, паклитаксел, доксорубицин и другие). Но если вы наблюдаетесь у врача и получаете химиотерапию, то с врачом все равно нужно посоветоваться.
— Почему именно Промисан, а не другие препараты индол-3-карбинола, которые подешевле?
Потому что в отличие от большинства БАД, Промисан делают, соблюдая все необходимые технологические процедуры. Покупая Промисан, вы платите за две вещи: качественное сырье и правильную технологию производства. Если вам предлагают купить «то же самое, но дешевле», это значит, что производитель либо сэкономил на сырье, либо сэкономил на производстве. В результате это всегда экономия на вашем здоровье. Также хочется отметить, что Промисан клинически тестирован, что сложно найти у других БАД.
И помните, что лечение и профилактика — это разные вещи. Лечением занимается врач, для этого он может назначить лекарственное средство или сделать операцию. А вот профилактика — это задача пациента, врач здесь может только дать совет. Доктор может удалить опухоль, но не может за пациента каждый день есть полезную еду (или принимать БАД) или больше двигаться.
Антиэстрогенное действие что это
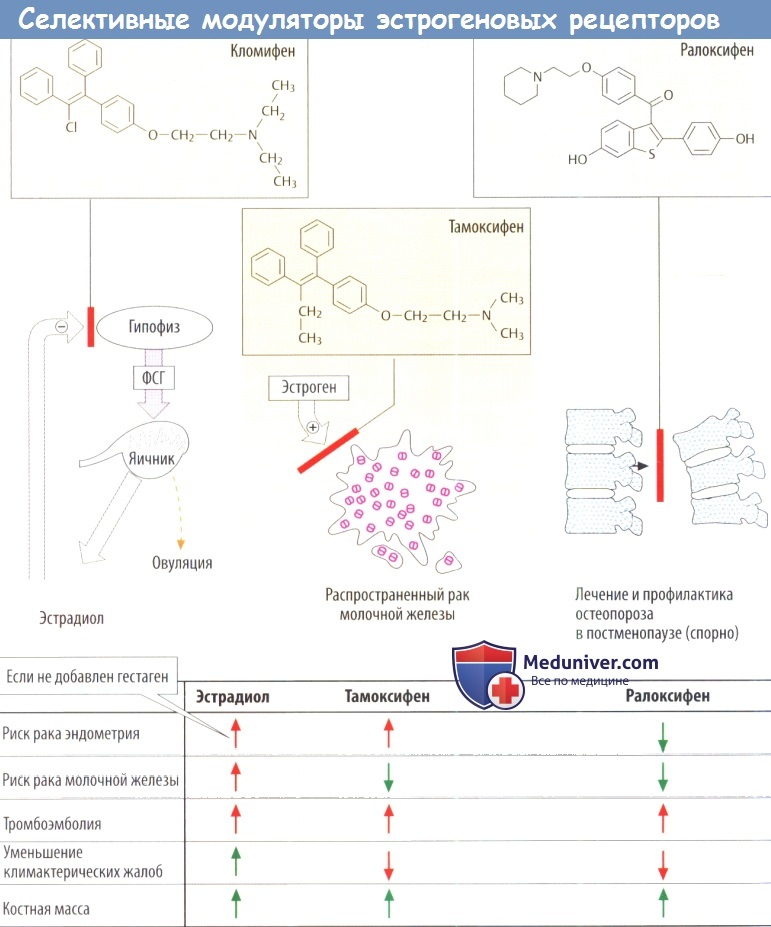
Селективные модуляторы эстрогеновых рецепторов (SERM). Эстрогеновые рецепторы принадлежат к группе рецепторов, регулирующих транскрипцию. Женский половой гормон эстрадиол является агонистом этих рецепторов. Существует несколько препаратов, которые являются антагонистами эстрогена.
Интересно, что их эффекты связаны с агонистами эстрогенов в определенных тканях. Вероятно, это объясняется тем, что каждый лиганд индуцирует специфическую конформацию эстрогенового рецептора. Комплексылиганд-эстрогеновый рецептор взаимодействуютс коактиваторами или репрессорами на определенной последовательности гена.
Корегуляторы отличаются в различных тканях, давая возможность каждому SERM формироватьтканеспецифическую активность. Терапевтически значимо то, что виды эстрогеновых и антиэстрогеновых эффектов отличаются по химической структуре вещества среди препаратов данного класса.
Полезно сравнивать профиль активности SERM с эстрадиолом, в частности, в отношении эффектов, которые наблюдаются в постменопаузе. При длительном введении эстрадиола риск рака эндометрия увеличивается. Одновременное введение гестагена предупреждает данный эффект. Рак молочной железы встречается чаще, так же как и тромбоэмболические заболевания.
Эстрадиол эффективно купирует климактерические приливы и потливость. После длительного лечения он снижает частоту переломов вследствие остеопороза заснет предупреждения потери эстрогензависимой части костной массы. Тем не менее эстрогены больше не рекомендуют использовать с этой целью из-за неблагоприятного соотношения пользы и риска.
а) Кломифен — производное стильбена, которое вводится внутрь при лечении женского бесплодия. Будучи антагонистом эстрогеновых рецепторов в аденогипофизе, он ослабляет подавление эстрадиолом секреции гонадотропина по принципу обратной связи. Итоговое повышение высвобождения ФСГ вызывает ускорение созревания фолликулов незрелой яйцеклетки.
Например, кломифен можно использовать при лечении расстройств желтой фазы, связанных с нарушением созревания фолликула или при лечении синдрома поликистоза яичников. Поскольку его можно применять только в определенные дни овариального цикла, необходим препарат, которые можно вводить длительно.
б) Тамоксифен — производное стильбена, которое используется при метастазирующем раке молочной железы для блокады эстрогенной стимуляции, вызывающей рост опухолевых клеток. Как смешанный антагонист/частичный агонист эстрогена тамоксифен скорее усиливает, а не ослабляет климактерические жалобы.
В то же время он проявляет агонистические свойства, которые интересны как потенциальный фактор риска,когда планируется использование препарата для профилактики рака молочной железы.
в) Ралоксифен одобрен для лечения и профилактики остеопороза. Как показано в таблице на рисунке ниже, он вызывает другие благоприятные, а также нежелательные реакции.
г) Антагонист эстрогеновых рецепторов фулвестрант — это резервный препарат для лечения гормонозависимого рака молочной железы.
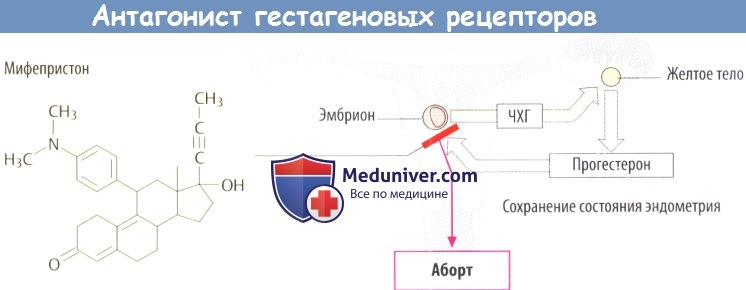
д) Антагонист гестагеновых рецепторов. Примерно через 1 нед. после оплодотворения эмбрион имплантируется в эндометрий в виде бластоцисты. За счет секреции человеческого хорионического гонадотропина (ЧХГ, в основном Л Г) трофобласт поддерживает желтое тело и секрецию прогестерона, что предотвращает менструальное кровотечение.
Мифепристон является антагонистом гестагеновых рецепторов и вызывает отслойку эндометрия. Следовательно, он действует как абортивный препарат в ранний период беременности. Его применение вызвало споры среди врачей (при сравнении побочных эффектов мифепристона с хирургическим вмешательством) и этически идеологические конфликты.
е) Ингибиторы ароматазы — дополнительный принцип антиэстрогенной терапии, который основан на подавлении синтеза эстрогена. Они используются в основном при лечении распространенного рака молочной железы в случае, когда опухоль теряет чувствительность к эстрогену, и у пациенток после менопаузы. Тем не менее один препарат в данном классе (анастрозол) разрешен к использованию при раннем раке молочной железы.
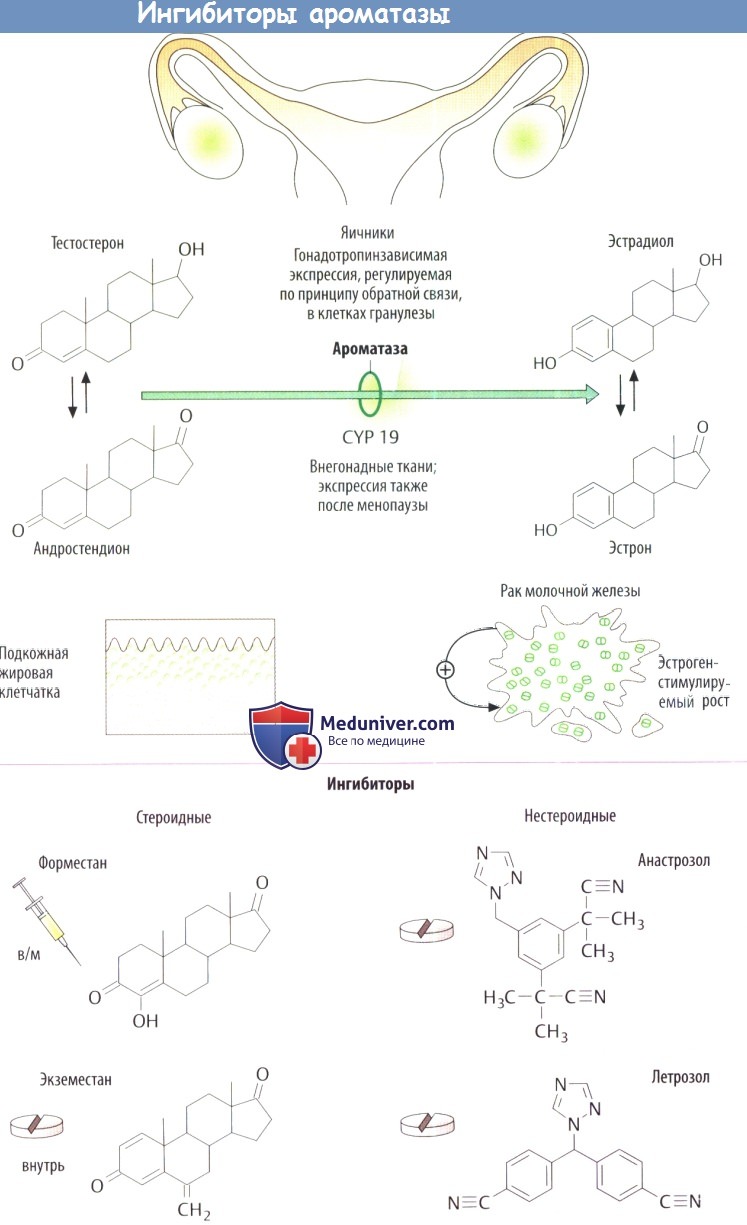
Ароматаза. Фермент превращает андрогены, например тестостерон и андростендион, в эстрогены (эстрадиол и эстрон). Эта реакция включает в себя отщепление метиловой группы на атоме C10 и ароматизацию кольца А. Ароматаза представляет собой изофермент CYP19.
У женщины во время репродуктивной фазы большая часть циркулирующих эстрогенов образуется в яичниках, где эстрадиол синтезируется в зернистых клетках созревающих третичных фолликулов. Оболочечные клетки, окружающие зернистые клетки, обеспечивают предшественниками андрогенов. ФСГ стимулирует образование эстрогенов, индуцируя синтез ароматазы в зернистых клетках. Изоформа 17β-гидроксистероиддегидрогеназа катализирует превращение андростендиона в тестостерон и эстрона в эстрадиол.
После менопаузы яичники не функционируют. Тем не менее эстрогены не исчезают полностью из крови, т. к. они продолжают поступать в кровоток из некоторых других тканей, в частности подкожной жировой ткани, которая продуцирует эстрон. Поэтому при гормонозависимом раке молочной железы ростопухоли стимулируется. Кроме того, раковые клетки молочной железы могут сами продуцировать эстрогены посредством ароматазы.
Следует отметить, что ароматаза имеет значение и у мужчин. В остеобластах она вызывает продукцию остеоанаболического эстрадиола из тестостерона.
Ингибиторы ароматазы служат для устранения экстраовариального синтеза эстрогенов у пациенток с раком молочной железы. Этого эффекта можно добиться только в постменопаузе, т. к., будучи ФСГ-зависимым ферментом, овариальная ароматаза подвергается регуляции женских половых гормонов по принципуобратной связи. Падение концентрации эстрадиола в крови приводит к повышению высвобождения ФСГ с компенсаторным повышением синтеза ароматазы и эстрогенов.
Две группы ингибиторов различают по химической структуре и механизму действия. Стероидные ингибиторы (форместан, экземестан) соединяются с участком связывания андрогена в ферменте и в виде промежуточных продуктов приводят к необратимому его подавлению. Нестероидные ингибиторы (анастрозол, летрозол) присоединяются к разным участкам связывания фермента. Посредством своего триазольного кольца они необратимо взаимодействуют с гемовым железом цитохрома Р450.
Среди побочных эффектов преобладают климактерические жалобы, отражающие снижение уровня эстрогена. В отличие от SERM (тамоксифена, который используется по такому же показанию) ингибиторы ароматазы не стимулируют рост эндометрия и не повышают риск тромбоэмболических осложнений.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Антиэстрогены
Содержание
Гормонные антагонисты и модуляторы (класс s 4) [ править | править код ]
Вещества с антиэстрогенной активностью нередко используют в профессиональном спорте с целью торможения преобразования тестостерона в женские половые гормоны (эстрогены), а также для увеличения мышечной массы.
Очень часто применение антиэстрогенов сочетается с приемом анаболических стероидов. Это обусловлено метаболизмом эндогенных и экзогенных анаболических стероидных гормонов в организме. Появление в организме вследствие поступления извне экзогенных стероидов и (или) накопление из-за сниженной функциональной способности печени чрезмерно высоких концентраций эндогенных анаболических стероидных гормонов, прежде всего, тестостерона, приводит к тому, что избыток тестостерона не успевает полностью метаболизироваться при прохождении физиологического пути. В этом случае часть анаболических стероидных гормонов проходит через обходной путь метаболизма — ароматизацию, при которой тестостерон превращается в эстроген с помощью фермента ароматазы. Именно для торможения преобразования тестостерона, который усиливает синтез белков и способствует тем самым гипертрофии скелетных мышц, а также для снижения содержания в организме эстрогенов и укорочения продолжительности их действия, недобросовестные спортсмены в погоне за результатом могут использовать вещества с антиэстрогенной активностью.
Классификация [ править | править код ]
Антиэстрогены в зависимости от механизмов своего влияния могут быть подразделены на три класса:
Существует и другая классификация антиэстрогенных препаратов (Baum, 2001). Согласно ей, они могут быть разделены также на три основных класса:
С нашей точки зрения, такая классификация не учитывает обратимости и необратимости действия препаратов на эстрогенные рецепторы и недостаточно полно учитывает генерацию препаратов и механизм их действия на рецепторы независимо от стероидной или нестероидной структуры лекарственного средства. Поэтому в дальнейшем описание классов и групп антиэстрогенных веществ будет основываться на первой классификации, которая в литературе распространена гораздо шире и намного более обоснована.
Все представители классов антиэстрогенных веществ являются запрещенными (Список запрещенных веществ и методов, 2008). Прием этих препаратов сопровождается рядом выраженных побочных эффектов, развитием многочисленных патологических состояний и может даже привести к летальному исходу.
Избирательные (селективные) модуляторы рецепторов эстрогена [ править | править код ]
Основными представителями избирательных (селективных) модуляторов рецепторов экстрогенов — ИМРЭ, или SERM (англ. Selective Estrogen-Receptor Modulators) — являются тамоксифен (синонимы — тамифен, нолвадекс, нолвадекс-форте, билем, интам, йеноксифен, цемид, валодекс, цито-зониум seu зитазониум), ралоксифен (Evista®, «Eli Lilly», Великобритания), торемифен (Фарестон®, «Orion Pharma», Финляндия), а также более поздние, пока мало исследованные аналоги тамоксифена (идоксифен, кеоксифен, дролоксифен). Все названные препараты класса ИМРЭ являются по своей структуре нестероидными веществами. К. стероидным представителям класса ИМРЭ относится фульвестрант (фазлодекс).
Тамоксифен [ править | править код ]
Первый антиэстроген из представителей класса ИМРЭ, тамоксифен, был синтезирован группой СоИе в 1971 г., и началось активное использование его как блокатора рецепторов эстрогенов. В последнее десятилетие создан высокоселективный «чистый» стероидный блокатор эстроген-рецепторов фульвестрант, который в настоящее время проходит III стадию клинических испытаний.
Наиболее часто используемым в фармакологии лекарственным препаратом класса ИМРЭ является тамоксифен, конкурентный ингибитор периферических эстрогеновых рецепторов. В настоящее время точка зрения, свидетельствующая, что тамоксифен не обладает эстрогеноподобным действием, опровергнута, поскольку доказано, что в определенной мере препарат проявляет и эстрогенную активность — соотношение его агонистической и антагонистической активности составляет 45/55.
Тамоксифен является производным трифенилэтилена; химическая структура 1-[p-(2-диметиламино)-этокси]-фенил-транс-1,2-ди-фенил-1-бутен, в виде цитрата. Форма выпуска: таблетки по 10, 20, и 40 мг. Тамоксифен хорошо усваивается в желудке; первый пик его концентрации в плазме крови регистрируется через 1—6 ч после введения, а второй — спустя 24—44 ч. Циркулирует препарат в крови довольно долго — максимально до 170 ч.
Выведение тамоксифена носит затяжной и двухфазный характер. Начальный период полувыведения препарата составляет 24—53 ч, а окончательное, в зависимости от дозы, от 3 до 18 сут. Выведение препарата происходит в основном через ЖКТ, причем с калом и желчью выделяется около 85—90 % метаболизированного препарата; незначительная его часть выводится из организма почками.
Тамоксифен выделяется из организма почти исключительно в виде метаболитов. Главные продукты биотрансформации представлены глюкуронидом и другими конъюгатами, а также неопределенными полярными метаболитами. Первичным этапом биотрансформации препарата является гидроксилирование ароматического кольца с образованием моногидроксипроизводного. В эксперименте именно этот промежуточный продукт оказался более активным антиэстрогеном, чем сам тамоксифен. Возможно, в клинических условиях именно этот продукт метаболизации тамоксифена способствует проявлению антиэстрогенного действия.
Более детально фармакокинетика и биотрансформация продуктов препаратов тамоксифенового ряда были изучены у женщин. После приема таблетированного препарата в лечебной дозе 0,3 мг-кг»1 массы тела максимальное содержание его в крови наблюдается в промежутке между 4—7 ч. Период полувыведения при использовании в такой дозе составляет 11 ч; через 2 нед содержание тамоксифена в сыворотке крови соответствует 0,013 мкг.
Начальная доза тамоксифена для лечебной практики составляет 20 мг (по одной таблетке 10 мг 2 раза в день), затем дозу повышают до 30 мг, а через 7—10 дней доводят до 40 мг в сутки. Лечение длительное — 2,5—3 мес, а иногда и более — до 5 лет. В течение многих лет лечение тамоксифеном было золотым стандартом терапии у женщин в постменопаузе, больных раком молочной железы, с эстроген-рецептор-позитивным статусом. В последние годы тамоксифен стали шире применять в лечении женщин детородного возраста, хотя некоторыми авторами обоснованность такого назначения вполне обосновано оспаривается (Endocrine. 2002; Молочная железа. 2006).
Побочные эффекты тамоксифена [ править | править код ]
Этот наиболее широко известный среди представителей класса ИМРЭ препарат обладает и самым широким спектром побочных явлений. Хотя, надо заметить, что негативные проявления той или иной выраженности наблюдаются после приема всех без исключения препаратов этого класса. Основные биологические эффекты тамоксифена выявляются в эндокринных органах. Препарат не проявляет ни андрогенного, ни антиандрогенного, ни гестагенного эффекта. У мужчин при приеме в высоких дозах может снижать массу яичек, семенных пузырьков и предстательной железы, что в дальнейшем приводит к бесплодию и импотенции. После многократного приема тамоксифена наблюдается нарушение функции печени. При этом прирост массы тела в конечном итоге отстает от такового у спортсменов, не принимающих подобного рода препараты. Тамоксифен может вызывать снижение уровня глюкозы и лейкоцитов в крови, главным образом за счет клеток лимфоцитарного ряда, незначительное, но часто дозозависимое уменьшение активности щелочной фосфатазы. Препарат угнетает антитоксическую функцию печени. При использовании высоких доз вызывает застой желчи (холестаз) и образование желчных камней. Его многократный прием также приводит к гиперплазии лимфоидной ткани селезенки и лимфоузлов, извращая естественную реакцию иммунной системы организма. Негативно влияет тамоксифен и на костную систему, существенно увеличивая риск развития остеопороза и переломов.
Хотя тамоксифен способствует уменьшению содержания холестерола в крови, его положительный эффект на частоту снижения кардиологической патологии не показан. Напротив, имеются! наблюдения, свидетельствующие об увеличении частоты развития ишемической болезни сердца, инфаркта миокарда и тромбоэмболий легочной артерии. У женщин-спортсменок прием тамоксифена в высоких дозах может препятствовать имплантации яйцеклетки в стенку матки. Использование этого антиэстрогена на ранних сроках беременности часто приводит к ее прерыванию путем прекращения роста матки, вызываемого эстрадиолом, и появлению уродств у плода (тератогенный эффект). При длительном применении тамоксифена наблюдается интенсивный рост опухолевых клеток. При этом в 4 (!) раза чаще чем у лиц, не принимавших данный препарат, регистрируется развитие рака печени и эндометрия, что обусловлено значительным и длительным увеличением уровня стероидных гормонов.
Лечебный эффект тамоксифена и синтезированного позднее препарата второго поколения селективных модуляторов эстрогеновых рецепторов — ралоксифена — выявляется в условиях повышенного уровня эстрадиола на фоне подавления секреции пролактина. Основное действие этих препаратов направлено непосредственно на опухолевую клетку-мишень, в которой антиэстрогены блокируют связывание эстрогенов на их специфических рецепторах. Наряду с прямым действием на клетки опухоли, антиэстрогены класса ИМРЭ приводят к торможению опухолевого роста посредством других механизмов, действуя на гипоталамо-гипофизарную систему и яичники.
Ралоксифен [ править | править код ]
Ралоксифен, как и тамоксифен, обычно применяется для лечения распространенного и прогрессирующего рака молочной железы, а также предупреждения метастазирования. Реже используется при химиотерапии рака тела матки и молочной железы у мужчин.
По сравнению с тамоксифеном ралоксифен оказывает менее выраженное влияние на деминерализацию костей, в меньшей степени влияет на изменение толщины эндометрия. Ралоксифен выпускается в виде таблеток, покрытых оболочкой, содержащих 60 мг активного вещества; его рекомендуется применять в дозе 60 мг-сут»1 до или во время приема пищи. Как агонист влияет на нерепродуктивные ткани, а как антагонист — на репродуктивные. Увеличивает концентрацию глобулинов, связывающих гормоны (в том числе половые, а также тироксин, кортикостероиды), с одновременным повышением их суммарного содержания в крови без увеличения уровня свободной фракции. Примерно 60 % препарата быстро всасывается после приема внутрь. До поступления в системный кровоток ралоксифен интенсивно метаболизируется с образованием глюкурони-дов. Абсолютная биодоступность составляет лишь 2 %. Время до достижения средней максимальной концентрации в плазме крови и биологическая доступность зависят от взаимопревращений ралоксифена в системном кровотоке и преобразований препарата и его глюкуронидных метаболитов в кишечнике и печени. Метаболизация происходит в основном в печени, поэтому нарушение ее функции является прямым противопоказанием для применения препарата. Ралоксифен широко распределяется в тканях организма, причем объем его распределения от дозы не зависит. Период полувыведения составляет 27,7 ч. Большая часть препарата и его метаболитов экскретируется в течение 5 дней и обнаруживается главным образом в фекалиях, а также в моче (6 %).
Побочные эффекты ралоксифена [ править | править код ]
Также как и тамоксифен ралоксифен способствует снижению уровня общего холестерола и холестерола ЛПНП, не влияя на содержание холестерола в ЛПВП. Однако по результатам крупномасштабного плацебо-контролируемого исследования RUTH компании «ЕИ Lilly», это не уменьшает риск развития ишемической болезни сердца и острого коронарного синдрома. Длительное применение препарата повышает риск возникновения тромбоэмболических осложнений, особенно в течение первых 4 мес. Прием ралоксифена может сопровождаться приливами, судорогами нижних конечностей, а также появлением периферических отеков. Учитывая вышеизложенное, а также тот факт, что препарат присутствует в Списке запрещенных веществ и методов (2008), применение его в практике спортивной подготовки является опасным для здоровья спортсмена и закономерно приведет к его дисквалификации.
К сожалению, в спорте, в частности бодибилдинге, эти антиэстрогены могут применяться атлетами при начинающихся явлениях феминизации и для ее профилактики. В комбинации с провироном (неароматизирующийся андроген местеролон) используются для придания мышцам жесткости и рельефности на этапе предконкурсной подготовки, а также для снижения активности эстрогеновых рецепторов в конце стероидного цикла.
Торемифен [ править | править код ]
С целью уменьшения побочных эффектов тамоксифена и ралоксифена в Финляндии был разработан новый препарат торемифен (Фарестон®, «Orion Pharma»), имеющий, согласно экспериментальным и клиническим данным, ряд преимуществ. Во-первых, в результате стабилизации структурной формулы тамоксифена за счет присоединения атома хлора достигается большая устойчивость молекулярной структуры препарата к метаболическим изменениям, в том числе гипероксидации, в организме. Во-вторых, онкогенный и гепатотоксический эффекты торемифена отмечаются гораздо реже. В то же время при длительном применении торемифена зафиксированы случаи развития злокачественных опухолей и их быстрое прогрессирование. У ряда лиц, принимавших препарат, возникает потеря определенных видов чувствительности.
Форма выпуска: таблетки по 20 и 60 мг. Торемифен быстро абсорбируется после приема внутрь. Максимальная концентрация в плазме крови в среднем достигается через 3 ч (от 2 до 5 ч). Динамика концентрации в плазме крови описывается биэкспоненциальной кривой. Период полувыведения в первой фазе (распределения) составляет 4 ч (от 2 до 12) ч. Во второй фазе (элиминации), длительность которой в среднем равняется 5 сут (от 2 до 10 сут), 99,5 % торемифена связывается с белками плазмы крови, главным образом альбуминами. Фармакокинетика препарата при приеме внутрь в дозах 11—680 мг-сут»1 имеет линейный характер. Равновесная концентрация торемифена при приеме в рекомендуемой дозе (60 мг-сут-1) в среднем составляет 0,9 (0,6—1,3) мкг-сут»1.
Побочные эффекты торемифена [ править | править код ]
Побочные эффекты от приема торемифена по сравнению с тамоксифеном менее выражены и продолжительны и опосредованы главным образом гормональным механизмом действия препарата. В клинических исследованиях наиболее частыми побочными эфектами являются приливы (более 20 %), потливость (14), тошнота (8), го- ловокружение (4), периферические отеки (3 %), а также рвота. Изредка могут возникать повышенная утомляемость, головные боли и боли в спине, увеличение массы тела, бессонница. Появление указанных симптомов, а также возникновение парезов, тремора в конечностях, анорексии, астении является важным для спортивной фармакологии.
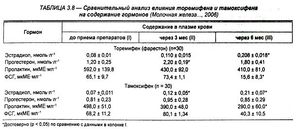
При клиническом использовании торемифена в онкологии, а также у спортсменок отмечается аналогичная действию тамоксифена направленность сдвигов содержания гормонов в сыворотке крови, но колебания их выражены в меньшей степени, кроме существенного (в 4 раза) снижения уровня фолликулостимулирующего гормона (ФСГ). При приеме торемифена также повышается уровень эстрадиола, но это примерно у 70 % спортсменок, принимавших препарат, сопровождается одновременным повышением содержания прогестерона.
Следует отметить, что отсутствие достоверных изменений содержания исследованных гормонов объясняется большими индивидуальными колебаниями, хотя вполне выразительная динамика относительно пролактина, прогестерона и ФСГ отчетливо прослеживается (табл. 3.8).
Как и другие препараты класса ИМРЭ, торемифен вызывает нарушения функции печени, о чем свидетельствует повышение активности печеночных трансаминаз в сыворотке крови. В начале приема торемифена возможно развитие гиперкальциемии с нарушением в последующем плотности костной ткани и возникновением остеопороза, хотя эти негативные проявления наблюдаются реже, чем при приеме тамоксифена. Остеопороз, обусловленный применением ингибиторов ароматазы, можно предотвращать и лечить путем перорального и внутривенного использования бифосфонатов (клодронат натрия, ксидифон, плеостат, бонефос, аредия, фосамакс, бондронат, ризедронат), которые предотвращают снижение плотности кости на фоне приема селективных блокаторов эстрогеновых рецепторов.
Для оценки механизмов действия и эффективности использования препаратов класса ИМРЭ следует учитывать не только их способность связываться с рецепторами, но и существенное влияние на гормональный гомеостаз спортсмена, что очень часто игнорируется в noгоне за результатом. Важно, что эти препараты в клинических условиях используются преимущественно у женщин в период постменопаузы, а так же у больных раком мужской молочной железы с заведомо измененным гормональным фоном. Поэтому прием антиэстрогенных препаратов класса ИМРЭ женщинами-спортсменками детородного возраста, а также мужчинами, может причинить непоправимый вред организму.
Фульвестрант [ править | править код ]
Новый антагонист эстрогенов фульвестрант (фазлодекс), недавно появившийся на фармацевтическом рынке и пока окончательно не изученный в клинических условиях, имеет стероидную структуру. В отличие от тамоксифена полностью блокирует трофическое действие эстрадиола и не обладает какой-либо эстрогенной активностью (потому и называется «чистым» антиэстрогеном). Первый «чистый» антиэстроген был синтезирован в 1987 г. Впоследствии наиболее активным его дериватом оказался фульвестрант («AstraZeneca», Великобритания), который был внедрен в клиническую практику в июне 2002 г.
Фульвестрант является новым типом антагонистов эстрогеновых рецепторов. Связываясь с рецепторами, он блокирует их, вызывает деградацию и снижает экспрессию прогестероновых рецепторов. Его сродство к рецепторам эстрогенов в 100 раз выше, чем у тамоксифена. Показаниями к применению фульвестранта является эстроген-рецептор-позитивный рак молочной железы у женщин в менопаузе, прогрессирующий после антиэстрогенной терапии тамоксифеном.
По фармакологическому действию фульвестрант заметно отличается от тамоксифена отсутствием свойств агониста и по выраженности блокирования эстрогеновых рецепторов. За счет стероидной структуры фульвестрант с гораздо большей аффинностью, чем тамоксифен, конкурентно связывается с эстрогеновыми рецепторами.
Результаты исследований, проведенных М. Berhens и сотрудниками в 2006 г., показали, что действие этого стероидного представителя класса ИРМЭ основано на деионизации рецепторов, что мешает их сгерической регуляции. В исследованиях in vitro и in vivo установлено, что фульвестрант обратимо увеличивает количество трансформаций генетического ядерного материала с параллельным снижением числа дефектных молекул эстроген-рецепторов в клетках-мишенях. Он также многогранно влияет на сигнальные пути этих рецепторов, блокируя димеризацию, ядерную локализацию эстрогенового рецептора и рецептор-зависимую транскрипцию, а также снижая количество рецептора в клетке.
По данным иммуногистохимических исследований, одна внутримышечная инъекция препарата оказывает дозозависимое снижение количества эстрогеновых и прогестероновых рецепторов и экспрессию рецептора гена Ki-67. Так, в дозе 250 мг фульвестрант уменьшает количество активних рецепторов в большей степени, чем тамоксифен.
В ходе III фазы клинических исследований было продемонстрировано наличие положительных свойств фульвестранта в эндокринной терапии рака молочной железы. У пациенток на фоне адьювантной (послеоперационной) терапии или первой линии эндокринной терапии эффективность фульвестранта наряду с хорошей переносимостью была сравнима с таковой анастрозола (см. второй класс антиэстрогенных препаратов).
Фульвестрант, «чистый» антиэстроген, в настоящее время проходит последнюю фазу клинических испытаний в качестве блокатора эстрогеновых рецепторов. В связи с недостаточным количеством исследований фульвестрант пока не зарегистрирован как «чистый» антиэстроген и описан как препарат, снижающий активность эстрогеновых рецепторов.
Применяется фульвестрант короткими курсами внутрь в дозе от 6 до 18 мг ежедневно или в виде внутримышечных инъекций один раз в неделю в дозе от 50 до 250 мг; по другим источникам — один раз в месяц у больных раком молочной железы в постменопаузе. Форма выпуска: таблетки по 6 мг; масляный раствор во флаконах по 250 мг/5 мл.
Применение препарата до операции уменьшает пролиферацию и(или) редукцию и исчезновение экспрессии эстрогеновых и прогестероновых рецепторов. Он снижает эстрогенную активность в большинстве неоперабельных случаев рака молочной железы и в этом отношении вдвое более активен, чем мегестрола ацетат — один из синтетических прогестинов, также обладающий антиэстрогенным действием, в основном за счет снижения синтеза эстрогенов (см. третий класс антиэстрогенных препаратов). Депрессия активности эстрогеновых рецепторов под влиянием фульвестранта имеет дозозависимый характер. Эффект влияния на гипофизарно-гипоталамическую дугу у препарата отсутствует. Таким образом, фульвестрант как препарат может применяться во второй линии антиэстрогенной терапии рака молочной железы.
Побочные эффекты фульвестранта [ править | править код ]
Побочные эффекты, возникающие после приема фульвестранта, однотипны для всех представителей класса ИМРЭ. Достаточно часто возникают тошнота, иногда рвота, запор, диарея, кожные высыпания, повышенная потливость, головная боль, боль в спине, брюшной полости. Изредка появляются гриппоподобный синдром, бессонница, депрессия, парестезии, фарингит, диспноэ, кашель. При приеме низких доз препарата побочные эффекты, такие, как нагрубание молочных желез или боли в ногах, возникают реже, чем при приеме в стандартных дозировках. На фоне низкодозовой терапии фульвестрантом приливы жара приходится купировать в 60—70 %, а на фоне стандартных дозировок — уже в 80—90 % случаев. То же относится и к сохранению плотности костной ткани. Процесс ее разрежения дозозависим: количество случаев остеопороза выше при приеме высоких доз препарата, чем при применении стандартных доз. Поэтому использование денситометрии и определение биохимических маркеров деструкции костной ткани рекомендуется пациенткам, принимающим фульвестрант даже в низких дозах без соответствующей терапии сопровождения. Частоту возникновения этого побочного эффекта можно снизить путем использования адекватных доз препаратов кальция и витамина D.
Фульвестрант по сравнению с тамоксифеном и мегестрола ацетатом более благоприятно влияет на изменения липидного профиля. При приеме стандартных доз препарата содержание ЛПНП и ЛПОНП на 12,3 и 14,2 % соответственно снижается, а уровень ЛПВП, напротив, повышается. При этом содержание общего холестерола и триацилглицеролов практически не изменяется.
По непонятным причинам, в разделе S4 Списка запрещенных веществ и методов (2006) этот; препарат отнесен к третьему классу «других антиэстрогенных субстанций». Однако в соответствии с механизмом действия фульвестрант как стероидный представитель ИМРЭ с полным основанием должен быть отнесен не к третьему, а к первому классу «веществ с антиэстрогенной активностью.
Однако в связи с незаконченностью III фазы клинических испытаний и достаточно обрывочными сведениями о его фармакодинамике и фармакокинетике, препарат пока не получил широкого распространения как селективный блокатор эстрогеновых рецепторов, несмотря на его выраженную физиологическую активность.
Следовательно, согласно Списку запрещенных веществ и методов (2008), все лекарственные средства антиэстрогеной направленности (независимо от класса) относятся к запрещенным препаратам, даже если индивидуально они пока не зарегистрированы в списке таковых. В клинических условиях в последние годы принято после приема препаратов класса ИМРЭ при необходимости переводить больных на терапию с помощью использования блокаторов ароматазы.
На 1 января 2016 года препарат разрешен к применению. и входит в список бесплатных препаратов для онкобольных.
Читайте также [ править | править код ]
Предупреждение [ править код ]