Диф. диагноз и особенности МРТ-картины при синдроме Сусака
Дифференциальный диагноз следует проводить с аутоиммунными демиелинизирующими заболеваниями, изолированным васкулитом ЦНС, поражением ЦНС при СКВ, болезнью Бехчета, болезнью Меньера, инфекционными энцефалитами, токсической лейкоэнцефалопатией, редким осложнением злоупотребления кокаином.
Синдром Сусака- ретинокохлеоцеребральная васкулопатия, впервые описанная в 1979 году группой авторов под руководством Джона Сусака.
Диагностика данного заболевания представляет серьёзную задачу для врача, т. к. клиническая картина синдрома может имитировать рассеянный склероз, острую, подострую или рекуррентную энцефалопатию, а также фокальный объёмный процесс.
Дифференциальный диагноз следует проводить с аутоиммунными демиелинизирующими заболеваниями ( рассеянным склерозом, о. рассеянным энцефаломиелитом), изолированным васкулитом ЦНС, поражением ЦНС при СКВ, болезнью Бехчета, болезнью Меньера, инфекционными энцефалитами, токсической лейкоэнцефалопатией, редким осложнением злоупотребления кокаином.
Вовлечение органов зрения и слуха с полиорганным характером поражения подразумевает проведение диф. диагностики с заболеваниями из группы системных васкулитов: гранулёматозом с полиангиитом Вегенера, с-мом Когана.
Для гранулёматоза с полиангиитом, в отличие от с-ма Сусака, характерно сочетание отита с поражением верхних дыхательных путей (некротический ринит, синусит).
Характерным признаком с-ма Когана является интерстициальный кератит, не встречающийся при синдроме Сусака.
Синдром Сусака также может маскироваться под случаи серонегативной системной красной волчанки.
Синдром также может напоминать паранеопластические синдромы, характерные для пациентов, получающих иммуносупрессорную терапию и таргетные противоопухолевые препараты.
МРТ головного мозга является одним из наиболее информативных исследований для постановки правильного диагноза.
К характерным для заболевания особенностям относятся небольшие множественные гиперинтенсивные Т2-очаги, а также очаги в сером и белом веществе мозжечка и подкорковых структурах, накапливающие контраст.
Очаги выявляются во внутренней капсуле, центральной части мозолистого тела (88-100%), перивентрикулярном глубоком белом веществе, мозжечке, стволе мозга, таламусе и базальных ганглиях, сером веществе (70%). Типично также появление линейных дефектов в центральной части мозолистого тела с контрастированием и поражением мозговых оболочек (33%).
При острой энцефалопатии диагностируются каллозальные поражения с центральной локализацией, напоминающие комья снега или снежные шары.
При обширном поражении лентикулостриарных артерий выявляются очаги наподобие «гигантских лакун».
На поздних стадиях возможно присоединение атрофии мозолистого тела.
К редким случаям относится вовлечение спинного мозга на уровне шейного отдела позвоночника.
Ангиит цнс что это
К.Е. Федоров (1), Т.А. Сергиенко (2), С.С. Голубев (3), Е.В. Атясова (4), Н.А. Назарова (2), С.В. Моисеев (5), П.И. Новиков (1)
(1) Ревматологическое отделение УКБ №3 ГБОУ ВПО Первый МГМУ им. И.М. Сеченова Минздрава РФ, Москва; (2) ФГБУ «Клиническая больница №1» Управления делами Президента РФ (Волынская), Москва; (3) Московская международная лаборатория патоморфологии LABORATOIRES DE GENIE, Москва; (4) Отделение лучевой диагностики МЦ «Петровские ворота», Москва; (5) Кафедра внутренних, профессиональных болезней и пульмонологии МПФ ГБОУ ВПО Первый МГМУ им. И.М. Сеченова Минздрава РФ
Васкулиты центральной нервной системы (ЦНС) – это тяжелые, потенциально инвалидизирующие заболевания, которые, как правило, развиваются в результате ревматических, инфекционных, лекарственных или онкологических заболеваний. К более редким формам церебрального васкулита относят изолированные, или первичные, васкулиты ЦНС [1]. В настоящее время морфологически выделяют гранулематозный (около 50%), лимфоцитарный (около 20%) и некротизирующий (около 20%) типы первичных васкулитов ЦНС. К гранулематозным ангиитам в свою очередь относят β-амилоид-ассоциированный васкулит (ABRA – Amyloid Beta Related Vasculitis), который занимает промежуточное положение между разновидностью церебральной амилоидной ангиопатии (ЦАА) и первичными васкулитами ЦНС. Также к этой промежуточной группе можно отнести ЦАА, ассоциированную с воспалением (CAA-RI – Cerebral Amyloid Angiopathy-Related Inflammation) [2].
Распространенность первичного васкулита ЦНС (PACNS – Primary Angiitis of the Central Nervous System) составляет 1 на 2,4 млн человек, в то время как заболеваемость ABRA – примерно 1 на 5 млн.
К основным проявлениям ABRA относятся рецидивирующие геморрагические и ишемические инсульты, эпилепсия и выраженные когнитивные нарушения. Гистологическая картина чаще всего включает гранулематозный ангиит с поражением сосудов среднего и малого калибров, разрывы стенок сосудов с кровоизлияниями, накопление β-амилоида в стенке сосудов в твердой, мягкой мозговых оболочках и веществе головного мозга [2].
В настоящее время нет единой классификации состояний, при которых происходит отложение β-амилоида в ЦНС. Спорадическая ЦАА характеризуется отложением β-амилоида в медии и адвентиции сосудов коры и мягкой мозговой оболочки [3–7]. Амилоид, который откладывается в сосудах, имеет такой же аминокислотный состав, как и предшественник белка амилоида (39–43 аминокислоты) в амилоидных бляшках при болезни Альцгеймера. Отложение β-амилоида в сосудах может приводить к повышенной ломкости сосудов, что ведет к разрыву сосудов и внутримозговым гематомам [3, 4]. Лобарные внутримозговые гематомы являются наиболее частыми проявлениями ЦАА, которая может сопровождаться воспалением сосудистой стенки. Это проявляется медленным снижением когнитивных функций, судорогами, головными болями и наличием гиперинтенсивных очагов в режиме T2 магнитно-резонансной томографии (МРТ), которые отвечают на лечение иммуносупрессивными препаратами [8–14]. Описано несколько разновидностей ЦАА: вариант с развитием периваскулярного воспаления без деструкции стенки сосуда, т.н. CAA-RI [11, 12], и вариант с трансмуральным, часто гранулематозным, ангиитом (ABRA) [13, 14]. Высказаны предположения, что ABRA является вариантом в большей степени первичного васкулита ЦНС, чем церебральной ангиопатии [13, 14]. В настоящее время также отсутствует единая классификация ABRA, поэтому прогноз заболевания и отдаленные последствия не изучены.
В результате одного из самых крупных ретроспективных исследований пациентов с первичными васкулитами ЦНС C. Salvarani была сделана попытка уточнить различные варианты ЦАА. Пациенты с ABRA по сравнению с больными ЦАА оказались моложе, реже имели снижение интеллекта, реже страдали от инсультов, в т.ч. геморрагических, и реже имели тяжелый неврологический дефицит. При МРТ накопление гадолиния в мягкой мозговой оболочке наблюдалось чаще у пациентов с ABRA, также у них отмечен лучший ответ на лечение и исход заболевания. Нельзя исключить, что такие результаты могут быть связаны с тем, что больных ЦАА лечили гораздо реже, чем больных ABRA. Тем не менее лучший ответ на лечение и исход при ABRA можно связать с наличием васкулита, который определяет проявления заболевания и поддается иммуносупрессивному лечению по сравнению с другими формами ЦАА, при которых отсутствует воспаление и состояние считается неизлечимым [2].
При сравнении ABRA и CAA-RI были обнаружены следующие различия. При ABRA чаще выявлялись изменения мягких мозговых оболочек в присутствии или без инфильтративных очагов в белом веществе, накапливающих контраст при МРТ. В то же время лобарные кровоизлияния и вазогенный отек в сочетании с масс-эффектом чаще обнаруживали при ЦАА. При сравнении ABRA и PACNS пациенты с ABRA были старше в момент установления диагноза, чаще страдали от снижения интеллекта и судорожных припадков при первом осмотре, реже имели гемипарезы и нарушения зрения. Уровень белка в ликворе был значительно выше у пациентов с ABRA. Ишемические инсульты встречались реже, а внутримозговые гематомы и накопление гадолиния в мягкой мозговой оболочке чаще в случае ABRA. Ответ на лечение, длительность лечения и исходы заболеваний были сопоставимыми.
Исследование С. Salvarani подтверждает результаты более ранних работ [13] о том, что ABRA и периваскулярная форма (CAA-RI) служат вариантами в большей степени PACNS, чем ЦАА, и имеют схожие механизмы развития. Необходимо также отметить, что, несмотря на отсутствие воспаления, клинические и радиологические проявления ЦАА у отдельных пациентов во многом схожи с ABRA и CAA-RI [15, 16]. Такое сходство заболеваний может объяснить ошибочную постановку диагноза СAA-RI вместо ABRA в случаях обнаружения лишь сегментарного поражения артерий головного мозга при биопсии.
У одного пациента с ABRA и у одного с CAA-RI описано выявление в ликворе интратекальных аутоантител к различным формам белка амилоида (1–40 и 1–42) [17, 18]. Снижение уровня этих антител было отмечено после трех месяцев стероидной терапии наряду с клиническим и радиологическим улучшением. Данные наблюдения могут свидетельствовать о том, что воспаление, связанное с ABRA и CAA-RI, может возникать в результате иммунного ответа на отложение амилоидного белка в церебральных сосудах. Эксперименты с лечением, направленным на активное или пассивное снижение уровня отложения амилоидного белка при болезни Альцгеймера, показали, что такое лечение приводило к менингоэнцефалиту или вазогенному отеку, вызывая клинические, рентгенологические и морфологические проявления, схожие с ABRA и CAA-RI [19, 20]. В исследовании C. Salvarani вазогенный отек, или масс-эффект, наблюдался у 22 (79%) из 28 пациентов с ABRA или CAA-RI [2]. При введении бапинезумаба (хуманизированное моноклональное антитело против амилоидного белка) также развивался вазогенный отек [20].
Клиническое наблюдение
Весной 2014 г. в клинику обратился мужчина 33 лет, армянин, работал менеджером. Причиной обращения были рецидивирующие геморрагические и ишемические инсульты головного мозга.
Из анамнеза известно, что заболеванию предшествовала закрытая черепно-мозговая травма. В 2010 г. выполнена правосторонняя орхидэктомия по поводу семиномы; химиотерапия и лучевая терапия не проводились в связи с полным удалением опухоли и отсутствием метастазов.
В 2012 г. лечение мерказолилом по поводу тиреотоксикоза.
Семейный анамнез без особенностей. Отмечена аллергия на новокаин в виде артериальной гипотензии.
Дебют настоящего заболевания состоялся осенью 2011 г., когда развился периферический парез лицевого нерва. При МРТ патологии не выявлено. Парез самостоятельно регрессировал в течение последующих трех недель. Дальнейшее ухудшение состояния пациента возникло в том же году после повторной закрытой черепно-мозговой травмы, когда появилась диффузная головная боль, двоение в глазах, нарушение походки. При обследовании обнаружены застойные диски зрительных нервов по данным МРТ головного мозга, множественные мелкие кровоизлияния в области моста, глубоких отделах правой височной доли. По данным компьютерной томографии (КТ) и магнитно-резонансной ангиографии сосудов мозга стенозы не выявлены. Проведено симптоматическое лечение с временным улучшением состояния и самочувствия. С мая 2012 г. вновь ухудшение состояния в виде появления сонливости, головокружения, тошноты, рвоты, субфебрилитета. Выявлено повышение уровня СРБ до 2 норм (рис. 1).
По данным МРТ, прогрессирование поражения головного мозга в виде увеличения количества мелких кровоизлияний.
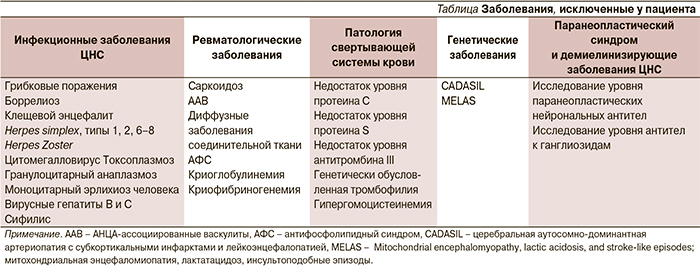
Дифференциальная диагностика проводилась между инфекционными заболеваниями, паранеопластическим синдромом с учетом семиномы в анамнезе, системных заболеваний соединительной ткани (см. таблицу). В анализах ликвора отсутствовали патологические изменения. Обсуждался постгерпетичекий геморрагический энцефалит Штрюмпеля–Ляйхтенштерна.
Лечение интерферонами было прекращено, начато введение дексаметазона с выраженным эффектом, пациент вернулся к повседневной жизни, нормализовались температура тела и уровень С-реактивного белка (СРБ). Через 2 месяца лечение дексаметазоном было прекращено. Следующее ухудшение – после длительного периода злоупотребления алкоголем в конце 2013 г., проявилось общей заторможенностью, нарушениями координации, психическими нарушениями в виде эпизодов неадекватности, агрессии, субфебрилитетом. По данным МРТ отмечено появление новых ишемических и геморрагических очагов в обоих полушариях головного мозга; данных о наличии интракраниальных стенозов не получено (рис. 3).
В марте 2014 г. после горячей ванны у пациента развивается крупное внутримозговое кровоизлияние в правой височной доле с признаками вклинения ствола головного мозга (рис. 4), была проведена хирургическая декомпрессия с эвакуацией гематомы.
Послеоперационный период протекал без осложнений. После кровоизлияния в марте 2014 г. у пациента отсутствовали грубые двигательные и чувствительные нарушения, однако больной был инвалидизирован в связи со стойким психоорганическим синдромом, который не позволял ему вести самостоятельный образ жизни и работать. В мае 2014 г. пациент обратился в Клинику им Е.М. Тареева. При осмотре выявили субфебрилитет, умеренные когнитивные нарушения (MMSE – Mini-Mental State Examination 20 баллов), психоорганический синдром, парциальные судорожные припадки (клонусы нижней челюсти и правой стопы), инвалидизация по модифицированной шкале Рэнкина 2 балла; в соматическом статусе без особенностей. По данным МРТ, отрицательная динамика в виде появления новых ишемических очагов в обоих полушариях головного мозга (рис. 5).
В анализах крови – стойкое повышение уровня СРБ до 2 норм.
Заподозрен первичный васкулит ЦНС. В пользу данного диагноза свидетельствовали множественные геморрагические и ишемические очаги в головном мозге, по данным МРТ, и признаки системного воспаления в виде субфебрилитета и стойкого длительного повышения уровня СРБ.
Дополнительно были исключены наследственная артериопатия (CADASIL) и митохондриальное наследственное заболевание (MELAS). С целью подтверждения диагноза больному выполнена биопсия головного мозга в условиях отделения нейрохирургии ФГБУ «Клиническая больница № 1» Управления делами Президента РФ (Волынская). Под эндотрахеальным наркозом произведен разрез по старому рубцу в правой височно-теменнозатылочной области. Кожный лоскут оттянут, костный лоскут удален. Твердая мозговая оболочка рубцово изменена, умеренно напряжена, слабо пульсирует. В проекции задних отделов нижней височной извилины выделен наиболее интактный участок твердой мозговой оболочки, иссечен на протяжении 5×5 мм, взят для исследования. После дополнительного лоскутного разреза твердой мозговой оболочки выделен интактный участок арахноидальной оболочки в малососудистой зоне, отсечен фрагмент 3×5 мм. Затем в проекции иссеченной арахноидальной оболочки острым путем иссечен фрагмент мозгового вещества 5×5 мм в глубину до 3 мм. Дефект твердой мозговой оболочки замещен фрагментом апоневроза. Костный лоскут уложен на место, фиксирован имевшимися на нем микровинтами. Рана ушита послойно.
При гистологическом исследовании твердой и мягкой мозговых оболочек выявлены признаки гранулематозного деструктивного васкулита в сочетании с массивным диффузным отложением амилоида в паренхиме вещества височной доли большого мозга и в сосудистой стенке (рис. 6).
Таким образом, наличие гранулематозного деструктивного васкулита в сочетании с отложением амилоида позволило диагностировать первичный β-амилоид-ассоциированный васкулит ЦНС.
На 4-е сутки после операции начато лечение. Проведены 3 внутривенные инфузии преднизолона по 1500 мг (из расчета 15 мг/кг массы тела) с последующим переходом на пероральный прием 75 мг/сут преднизолона. Начато лечение циклофосфамидом (ЦФ) в дозе 1400 мг внутривенно капельно 1 раз в 4 недели. В результате лечения через месяц отмечена нормализация уровня СРБ и температуры тела, отсутствие новых повреждений головного мозга.
Обсуждение
Наш клинический случай служит примером длительного течения ABRA, осложнившегося множественными ишемическими и геморрагическими инсультами, когнитивными расстройствами и эпилепсией. ABRA составляет примерно 30% всех PACNS.
К основным характеристикам ABRA по сравнению с другими подтипами PACNS относятся:
Необходимо отметить, что в дебюте заболевание проявлялось поражением периферической нервной системы в виде неврита лицевого нерва. В дальнейшем возникло поражение ЦНС в виде множественных ишемических и геморрагических очагов и отложения амилоида в головном мозге. Данная особенность не противоречит концепции заболевания, а по-видимому, является редким ее проявлением, т.к., с одной стороны, подобное поражение может быть проявлением гранулематозного воспаления, с другой – существуют описания сочетания поражений центральной и периферической нервной системы при PACNS [21].
К факторам риска развития васкулита у данного пациента можно отнести неоднократные травмы головы, лечение мерказолилом и злоупотребление алкоголем. Тщательное обследование пациента с исключением обширного спектра заболеваний позволило сузить круг предполагаемой патологии до PACNS, однако несвоевременно поздно выполненная биопсия не позволила начать адекватное лечение и предотвратить инвалидизацию. Стоит также отметить, что уже на ранних МРТ головного мозга можно было заподозрить отложение амилоида, тем не менее недостаточное качество исследований и неверная трактовка результатов значительно отдалили постановку диагноза. Более того, при хирургической декомпрессии головного мозга в марте 2014 г. по поводу крупного внутримозгового кровоизлияния у молодого больного с длительным анамнезом инсультов удаленный детрит не был исследован гистологически, что потребовало в дальнейшем повторной трепанации черепа для морфологической верификации диагноза.
В последние десятилетия ведутся разработки неинвазивных методов диагностики, таких как определение уровня β-амилоида в ликворе [18], позитронно-эмиссионная томография головного мозга и магнитно-резонансная спектроскопия с использованием высокопольных томографов. Следует отметить, что МРТ с применением специальных режимов остается чувствительным методом диагностики, позволяющим заподозрить PACNS на ранних стадиях; в отсутствие изменений на МРТ диагноз первичного церебрального ангиита маловероятен [21]. При анализе МРТ головного мозга нашего пациента, в особенности последних исследований с использованием режимов FLAIR (Fluid-Attenuated Inversion Recovery – режим с подавлением сигнала свободной воды) и SWI (Susceptibility – Weighted Imaging – изображения, взвешенные по неоднородности магнитного поля), отчетливо видны свежие ишемические очаги (FLAIR), располагающиеся вокруг мелких сосудов (SWI), отложение амилоида и гемосидерина (SWI). Совмещение изображений разных импульсных последовательностей может давать информацию о взаимоотношении очагов ишемии и сосудов головного мозга, состоянии стенок сосудов в очаге ишемии. Несмотря на развитие неинвазивных методик, биопсия остается единственным методом достоверной диагностики ABRA.
В большинстве случаев биопсия головного мозга и его оболочек – это безопасная рутинная операция. Для снижения риска осложнений операции используют стереотаксическую навигацию с учетом расположения сосудов и проводящих путей, а также функционального картирования головного мозга [22]. Существует несколько подходов к биопсии головного мозга. При диффузном поражении головного мозга или отсутствии возможности забора ткани из измененной области следует выполнять биопсию мягкой, твердой оболочек головного мозга, серого и белого вещества височной доли недоминантного полушария. При наличии крупного очага или кровоизлияния предпочтительно взятие материала из пораженной области и оболочки головного мозга, в частности при проведении хирургической декомпрессии по поводу внутримозгового кровоизлияния удаленный детрит должен быть рутинно исследован на наличие амилоида (окраска конго-красным) [21].
В описанном нами случае не использовалась стереотаксическая навигация, т.к. предполагалось поверхностное взятие материала из зоны уже перенесенного крупного кровоизлияния в височной доле недоминантного правого полушария. Обычно для исследования достаточно менее 1 см2 мягкой и твердой мозговых оболочек, объем фрагмента головного мозга определяется индивидуально. Фрагменты помещают в формалин, в перечень гистологических исследований обязательно должна входить окраска на амилоид [2]. При исследовании биоптата нашего пациента наиболее выраженные изменения были выявлены в твердой мозговой оболочке и веществе головного мозга. Именно сочетание таких признаков, как трансмуральный гранулематозный ангиит с разрывом стенок сосудов, кровоизлияния и массивное отложение β-амилоида в первую очередь в стенке сосудов, позволило отнести васкулит к ABRA.
В терапии ABRA используются те же подходы, что и при лечении жизнеугрожающих форм АНЦА-ассоциированных васкулитов: сочетание ГК и ЦФ, использование азатиоприна, препаратов микофеноловой кислоты, ритуксимаба, а также ингибиторов фактора некроза опухоли-α в отсутствие эффекта от стандартной терапии [23, 24]. Для поддержания ремиссии применяют обычно азатиоприн, микофенолат, метотрексат, ритуксимаб. Выраженный лечебный эффект достигается от монотерапии ГК или в сочетании с ЦФ [25, 26]. Уточнение типа PACNS играет важную роль в лечении, т.к. при ABRA не рекомендовано лечение антикоагулянтами и антиагрегантами в связи с очень высоким риском геморрагических инсультов [27].
Несмотря на редкость PACNS в популяции, инсульт в молодом возрасте, особенно сочетание геморрагических и ишемических очагов, эпилепсия, снижение когнитивных функций в сочетании со специфическими изменениями на МРТ всегда требуют проведения дифференциальной диагностики с PACNS. Нередко PACNS эффективно поддаются лечению, особенно на ранних стадиях, поэтому своевременная диагностика и адекватная терапия значительно снижают риск инвалидизации пациента. Решающую роль в диагностике PACNS с поражением артерий среднего и мелкого калибра играет биопсия, которая при правильном планировании и выполнении является безопасной процедурой и должна незамедлительно использоваться при подозрении на PACNS.
Васкулит – что это за болезнь? Симптомы, причины и лечение, запись на прием к специалисту клиники МЕДСИ
Оглавление
Васкулит – патология, поражающая крупные, средние и мелкие сосуды и характеризующаяся воспалением стенок артерий, вен, венол, артериал и мелких капилляров. Заболевание является не только неприятным для пациента, но и опасным. Точный диагноз может поставить лишь опытный ревматолог. Он же справится и с задачей непростого лечения васкулита.
Причины патологии
Точные причины заболевания неизвестны. Нередко патология возникает даже у абсолютно здорового человека.
Обычно васкулиты возникают на фоне:
К предрасполагающим факторам относят:
Васкулит может возникнуть и как осложнение реактивного артрита или красной волчанки.
Классификация
В зависимости от причин возникновения васкулиты делятся на:
В зависимости от локализации выделяют:
В некоторых случаях одновременно поражаются как мелкие и средние, так и крупные сосуды.
Симптомы васкулита
Основными признаками и симптомами васкулита, являющимися поводом для обращения к врачу и начала лечения, являются:
Симптомы васкулита у детей, после обнаружения которых следует обратиться к специалисту для лечения, являются таким же. Причем малыши страдают патологией чаще, чем взрослые. Наиболее подвержены недугу дети в возрасте от 4 до 12 лет. Как правило, развивается болезнь Кавасаки и другие системные васкулиты. У несовершеннолетних больных патология поражает мелкие сосуды эпидермиса, суставы, органы желудочно-кишечного тракта и почки.
Важно! Если своевременно не обратиться к врачу, не пройти диагностику и не начать лечение васкулита, заболевание перейдет в хроническую форму. Периодически пациент будет страдать от рецидивов патологического состояния.
Диагностика
Перед началом лечения всегда проводится диагностика васкулита. Она позволяет определить особенности течения заболевания и выявить его причину.
Лечение васкулита
Лечение васкулита направлено на:
В комплексной терапии применяются средства для:
Такое лечение включает:
Такое лечение васкулита проводится при наличии признаков тромбоза глубоких вен. Назначается оно только по строгим показаниям. Методики отбираются специалистами.
Профилактика
Васкулит на ногах и других частях тела часто не имеет не только ярко выраженных симптомов, но и причин, поэтому затрудняется не только его лечение, но и профилактика.
Тем не менее рационально:
В целях профилактики вторичной формы патологии следует:
Диета при васкулите
Основой питания при патологии является исключение аллергенов (цитрусовых, яиц, усилителей вкуса, меда, грибов, промышленных консервантов и др.).
Точную диету составит ваш лечащий врач. Он же даст и рекомендации, касающиеся образа жизни в целом. Это позволит как сократить симптомы заболевания, так и (в некоторых случаях) снизить дозировки принимаемых лекарственных препаратов.
Преимущества лечения васкулита в МЕДСИ
Если вы хотите записаться на прием к врачу и пройти лечение васкулита, позвоните нам