Простата и ее заболевания: преодолейте страх
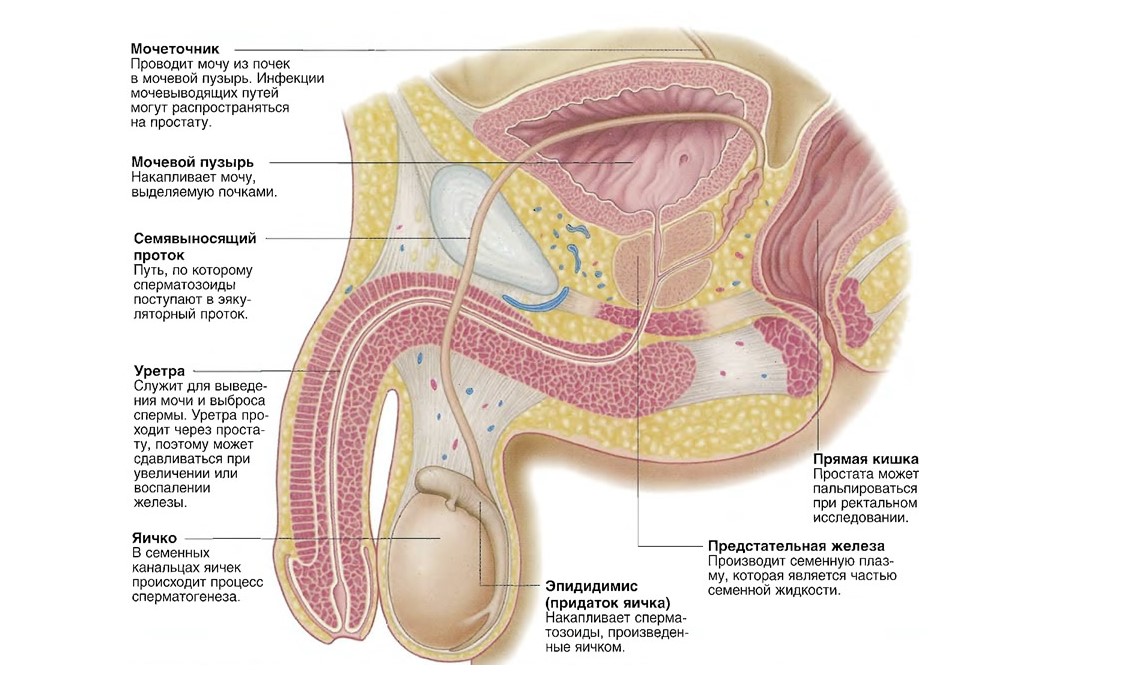
Простата – непарный железистый орган, размером с грецкий орех. Она расположена под мочевым пузырем и окружает мочеиспускательный канал.
Для чего нужна простата?
Основная функция простаты состоит в выработке секрета (сока), входящего в состав семенной жидкости, которая поддерживает процесс производства мужских половых клеток-сперматозоидов и обеспечивает их передвижение и семяизвержение (эякуляцию), а также участвует в формировании полового влечения (либидо) и оргазма.
Что такое аденома простаты?
К сожалению, по статистике, каждый второй мужчина старше 50 лет, сначала периодически, а потом все чаще и чаще страдает задержкой мочеиспускания. Это случается, потому что он становится жертвой аденомы – доброкачественного уголка, образующегося в простате и по мере увеличения, все больше сдавливающего мочеиспускательный канал.
Сначала мужчина испытывает какие-то непонятные ощущения «ниже пояса», дискомфорт и ощущение неопорожнения мочевого пузыря. Потом появляются легкие боли, затем постоянные, затрудненное мочеиспускание и даже кровь в моче. Эти неприятные симптомы могут сопровождаться бессонницей, ухудшением памяти и, конечно, разладом в сексуальной сфере. Как справиться с этой проблемой, куда обратиться? Конечно, есть такой врач, уролог-андролог, который помогает именно в таких непростых ситуациях.
Увеличение простаты может быть признаком онкозаболевания
Раковая опухоль простаты — самая распространенная онкологическая патология у мужчин, она занимает одно из ведущих мест среди причин смертности после рака кожи. На сегодняшний день заболевание достаточно легко диагностируется и успешно поддается лечению при своевременном обращении к врачу. Однако многие мужчины длительное время игнорируют первые признаки заболевания и поздно обращаются за медицинской помощью. Нередко именно это приводит к печальным последствиям. По словам специалистов турецко-американского Медицинского центра «Анадолу», один из основных симптомов, на который стоит обратить внимание — увеличение предстательной железы.
С чем связано увеличение простаты?
В целом, рост предстательной железы — это нормальный физиологический процесс. Простата начинает увеличиваться в период полового созревания под воздействием растущей концентрации мужских половых гормонов. Это увеличение железы продолжается до тех пор, пока в организме вырабатывается гормон тестостерон. Процесс может остановиться только если мужчина по какой-либо причине лишится яичек.
Каковы нормальные размеры простаты?
Предстательная железа — орган, который охватывает устье мочевого пузыря. В 18-20 лет, по завершению полового созревания, ее вес составляет 12-15 г, а в более зрелом возрасте может увеличиться до 60-100 г. В некоторых случаях вес может достигать 200 г.
Когда нужно обращаться к врачам?
У каждого мужчины структура простаты уникальна и зависит от анатомических особенностей тела и баланса мужских половых гормонов. Поэтому тревожным признаком является не столько ее размер, сколько появление сопутствующей симптоматики. Например, при патологическом увеличении предстательной железы происходит сдавливание мочевого пузыря и мочеиспускательного канала, что приводит к проблемам с мочеиспусканием. И вот это уже — повод для посещения уролога-андролога.
Какое лечение назначается в таких случаях?
Решение о методах лечения принимается на основе жалоб пациента, общего состояния его здоровья, возраста и имеющихся заболеваний. Обычно назначают медикаментозную терапию альфа-блокаторами, альфа-5 ингибиторами редуктазы, низкими дозами ингибиторов 5-фосфодиэстеразы (PDE5i) и их комбинациями.
Пациентам, которым не помогло медикаментозное лечение, может быть рекомендовано хирургическое вмешательство:
Является ли увеличение простаты признаком онкозаболевания?
Не всегда, но такой риск есть. Поэтому каждому пациенту с данной патологией необходимо проходить периодические обследования на наличие опухоли предстательной железы. В особенности это касается мужчин старше 40 лет, имеющих следующие симптомы:
Какие обследования проводятся для исключения рака?
В первую очередь — это мануальный осмотр предстательной железы и анализ уровня PSA (простатспецифического ракового антигена) в крови. Если в результате обследования у врача возникнет подозрение на наличие злокачественной опухоли простаты, может быть назначена биопсия.
Что такое MR-TRUS биопсия и почему она предпочтительнее, чем традиционная?
Во время традиционной биопсии образец ткани берут из стандартных участков железы под контролем трансректального ультразвукового исследования (ТРУЗИ). Однако врачам не всегда удается попасть именно в патологическую область и собрать достаточно материала. В связи с этим есть риск, что результаты исследования будут неточными или неполными.
MR-TRUS биопсия объединяет в себе магнитно-резонансную томографию и трансректальное ультразвуковое исследование. Благодаря этому врачи получают трехмерное изображение предстательной железы в режиме реального времени и могут взять образец ткани из подозрительного участка с максимальной точностью. Таким образом, если классическая биопсия позволяет диагностировать злокачественную опухоль в 70-75% случаев, то MR-TRUS биопсия — более чем в 95%.
Кроме того, при проведении MR-TRUS биопсии образец ткани берут очень точечно и непосредственно из пораженной области. Поэтому пациенты избавлены от сильного болевого синдрома, и риск развития осложнений в виде инфекции в этом случае снижен. Метод особенно информативен, когда по итогам нескольких биопсий онкопатологию не выявили, но уровень PSA продолжает расти.
Какие методы лечения при раке предстательной железы может предложить современная медицина?
Отличные результаты в лечении рака предстательной железы сегодня демонстрирует роботизированная хирургия. Традиционные вмешательства на простате проводят при помощи больших разрезов. Это приводит к развитию у пациента постоперационного болевого синдрома, увеличению срока госпитализации, появлению косметического дефекта и повышению риска развития инфекции.
Робот-ассистированная хирургия требует выполнения всего нескольких маленьких разрезов на животе, через которые в полностью стерильных условиях и производятся все манипуляции. Робот-хирург обладает высокой маневренностью и позволяет получить трехмерное изображение оперируемого участка с 12-кратным увеличением, поэтому опухоль удаляется с максимальной точностью. В результате эффективность операции в разы повышается, а пациент стремительно восстанавливается и может вернуться к обычной жизни максимально быстро.
Другим инновационным методом лечения рака простаты, который набирает все большую популярность, является радиационная терапия. Это безоперационный метод лечения опухоли при помощи ионизирующего излучения. Злокачественные ткани в буквальном смысле выжигаются мощным радиационным потоком — его очень точно направляют именно в пораженную область, минимально задевая здоровые ткани. Благодаря этому у пациентов снижается риск развития таких серьезных побочных эффектов, как недержание мочи и проблемы с потенцией, присущих традиционным хирургическим методам лечения. А кроме того, процедура избавляет и от проведения анестезии, и от появления хирургических разрезов, послеоперационного болевого синдрома и необходимости длительного восстановления.
Материал подготовлен по согласованию с врачом медицинского центра «Анадолу» доцентом Илкером Тинай.
Аденома предстательной железы
Нужна помощь?
+7 (495) 956-91-03
Аденома предстательной железы или доброкачественная гиперплазия
предстательной железы (ДГПЖ).
Что такое аденома предстательной железы (ДГПЖ)?
Аденома простаты или ДГПЖ – это не злокачественное разрастание ткани простаты. Этот процесс начинается обычно в возрасте около 40 лет и является очень распространенным. После 50 лет аденома простаты встречается практически у каждого мужчины. При аденоме предстательной железы ее внутренняя часть растет как семечко плода за счет активного роста клеток предстательной железы – фибробластов. Источником доброкачественной гиперплазии предстательной железы (ДГПЖ) являются парауретральные железы. Постепенно железа увеличивается в размерах, за счет разрастания клеток аденомы, и перекрывает выход из мочевого пузыря. Симптомы аденомы простаты не являются следствием нормального процесса старения, а представляет собой проявление заболевания, которое можно и нужно лечить! ДГПЖ не обязательно приводит к раку простаты, который также может быть выявлен у пожилых мужчин. Аденома простаты (ДГПЖ) и рак предстательной железы – это два разных заболевания. Однако аденома может привести к развитию осложнений, если лечиться не правильно.
Какие изменения в организме приводят к развитию аденомы?
При ДГПЖ можно выделить ряд патогенетических и клинических синдромов: гормональных нарушений (нарушение соотношения женских и мужских половых гормонов), гиперплазии, нарушения кровообращения (венозный застой в органах малого таза), воспалительный (различные варианты простатических изменений воспалительного характера), нарушений мочеиспускания (дизурический) и другие.
Чем опасна аденома для здоровья?
Увеличенная в размерах простата (предстательная железа), окружая мочеиспускательный канал, начинает на него давить, вызывая его сужение, которое приводит к нарушению оттока мочи из мочевого пузыря. На ранних стадиях аденомы мышца мочевого пузыря еще в состоянии протолкнуть мочу сквозь суженный мочеиспускательный канал. Однако если процесс сужения продолжается, мышца мочевого пузыря утолщается. Нарушается эластичность мочевого пузыря, и его стенки начинают сокращаться произвольно. В результате, возникают сильные внезапные позывы к мочеиспусканию, которые иногда заканчиваются недержанием мочи, и учащенное мочеиспускание в дневное и ночное время. При отсутствии лечения аденомы через некоторое время могут возникнуть следующие осложнения: недержание мочи, выделение крови с мочой (гематурия), образование камней в мочевом пузыре, инфекции мочевыводящих путей, задержка мочеиспускания, хроническая почечная недостаточность – необратимое поражение почек. Это самое грозное осложнение аденомы простаты, которое плохо поддается лечению!
Какие основные симптомы аденомы?
Основные симптомы аденомы простаты – это различные расстройства мочеиспускания: затрудненное и учащенное мочеиспускание (днем и особенно ночью), ослабление струи мочи, чувство неполного опорожнения мочевого пузыря после мочеиспускания, прерывистое мочеиспускание и другие. Аденома простаты может даже вызвать так называемую задержку мочи, когда мужчина вовсе не может самостоятельно помочиться. Если Вы отмечали у себя хотя бы один из этих симптомов, необходимо обратиться к урологу. В более молодом возрасте такие симптомы могут быть вызваны другими причинами (сужение уретры, нейрогенные расстройства мочеиспускания, воспалительные процессы, простатит).
Какие стадии болезни различают?
2 стадия характеризуется дистрофическими изменениями (истончение) стенок мочевого пузыря и появлением вследствие его недостаточной сократительной способности симптома остаточной мочи (более 50 мл). Наблюдается нарушение транспорта мочи на уровне мочеточников и почечных лоханок с последующим их расширением и снижением функции почек (компенсированная стадия почечной недостаточности). Сохраняется синдром дизурии (возникают частые позывы на мочеиспускание, учащение мочеиспускания или его задержка, может быть болевой синдром). Мочеиспускание учащено вначале только ночью, а затем и днем. Типично появление симптома повелительного (навязчивого) мочеиспускания, которое в отличие от цистита не сопровождается болезненностью и помутнением мочи, но интенсивность его бывает очень велика. Повелительный позыв может приводить к не удержанию мочи. Периодически дизурические явления могут исчезать на неопределенное время. Присоединяющаяся инфекция усиливает дизурию. Появляется затрудненное мочеиспускание после сна, продолжительного сидения, переполнения мочевого пузыря. Слабеет струя мочи, особенно в начале акта мочеиспускания (тонкая струя падает отвесно вниз), усиливается ночная поллакиурия (учащенное ночное мочеиспускание). Общее состояние больного в этой стадии вполне удовлетворительное. При значительной дизурии по ночам больные становятся нервными и раздражительными.
3 стадия характеризуется постепенным нарастанием количества остаточной мочи. Тонус детрузора падает, стенка пузыря постепенно истончается, появляются многочисленные мелкие ложные дивертикулы. Недостаточное опорожнение мочевого пузыря приводит к расширению мочеточников и почечной лоханки, почечная паренхима атрофируется, функции почек нарушаются. Вначале утрачивается их концентрационная функция, а затем — способность разведения. Течение заболевания постепенное, больной свыкается со своим состоянием, не замечая увеличивающегося количества остаточной мочи. Это объясняется также снижением чувствительности стенки мочевого пузыря. Постепенно пузырь растягивается, он может содержать до 2 л мочи, давление скопившейся в мочевом пузыре мочи преодолевает сопротивление сфинктеров, и моча начинает непроизвольно выделяться по каплям.
Со временем возрастает риск развития парадоксальной ишурии, «задержка мочи с недержанием». Характерны декомпенсация функции детрузора, расширение верхних мочевых путей, почечных лоханок и чашечек и прогрессирование почечной недостаточности до терминальной стадии с признаками уремии. Мочевой пузырь растянут и переполнен, на фоне хронической задержки мочи наблюдается ее непроизвольное выделение (ночное, а затем и дневное) в случае преодоления скопившейся мочой сопротивления пузырного сфинктера (парадоксальная ишурия).
Что Вас ожидает во время визита к урологу?
На консультации врач выяснит историю заболевания. Уролог должен, прежде всего, удостоверится, что возникшие у вас расстройства мочеиспускания действительно вызваны аденомой простаты.
Какие методы лечения аденомы?
Какая медикаментозная терапия лечения аденомы применяется?
Существует несколько типов лекарственных препаратов назначаемых при аденоме простаты. Широкое признание урологов всего Мира получили препараты из группы альфа-адреноблокаторов. Это препараты, расслабляющие простату с целью облегчения оттока мочи через простатический отдел мочеиспускательного канала (участка уретры, проходящего через предстательную железу). В гладкомышечных волокнах, окутывающих простату и простатическую часть уретры, были обнаружены рецепторы «альфа». При лекарственном воздействии на эти рецепторы, волокна расслабляются, что приводит к снижению давления ткани простаты на мочеиспускательный канал. В результате, мочеиспускание происходит более свободно. Но аналогичные рецепторы находятся в стенке кровеносных сосудов. Лекарство, воздействуя на них, приводит к расширению сосудов и снижению кровяного (артериального) давления. Это может быть хорошо для больных гипертонической болезнью, но в то же время и опасно для людей с нормальным или низким давлением. Данная группа препаратов обладает доказанной клинической эффективностью и рекомендована для симптоматического лечения аденомы простаты в качестве средств первого выбора. Все эти препараты, имея похожее химическое строение, улучшают мочеиспускание, уменьшают объем остаточной мочи, уменьшают количество ночных мочеиспусканий. Они достаточно эффективны в отношении симптомов, но не препятствуют росту простаты и дальнейшему прогрессированию заболевания, некоторые требуют подбора дозы. Нередко пациенту приходится «попробовать» два-три препарата, прежде чем будет выбран самый эффективный и безопасный. Каждый из препаратов этой группы имеет свои особенности химического строения и поэтому оказывает неодинаковое влияние на организм.
В последние годы уверенно набирает обороты метод гормонального лечения так называемыми ингибиторами 5 альфа-редуктазы. Это препараты, которые разными путями предотвращают воздействие мужского полового гормона — тестостерона на ткань предстательной железы, что приводит к уменьшению ее объема.
Сегодня почти каждый пациент интересуется мнением врача о возможности лечения препаратами на натуральной основе. Препараты растительного происхождения, в отличие от химиопрепаратов, не включают в себя синтезированные вещества, а построены из уже существующих в природе веществ, извлеченных различными способами из растений. Лечение препаратами из растений получило название фитотерапия. Сегодня известно, что в состав естественных препаратов входят такие вещества, как фитостероиды, растительные масла, жирные кислоты, фитоэстрогены. Точный механизм действия большинства препаратов неизвестен. По данным последних исследований, они оказывают противовоспалительный, антиандрогенный и эстрогенный эффекты. Кроме того, обнаружено воздействие некоторых веществ на рецепторы альфа, поддержание функции мочевого пузыря (механизм неизвестен) и, наконец, нельзя сбрасывать со счетов так называемый эффект плацебо — психологический эффект от самого факта приема препарата, который может достигать 40%.
Все эти препараты эффективны на ранних стадиях заболевания. При более выраженных стадиях они должны применяться в составе комбинированной терапии.
Какие методы хирургического лечения аденомы существуют?
Развитие, прежде всего медикаментозного метода привело к тому, что в США оперируется не более 20% больных аденомой простаты. Однако в некоторых случаях абсолютно показано хирургическое лечение. Радикальным является только хирургическое лечение (операция). Показания к операции: появление остаточной мочи, упорная инфекция мочевых путей, рецидивы острой задержки мочи, гематурия (примесь крови в моче), камни мочевого пузыря, резкое учащение ночного мочеиспускания. Ослабленным больным с плохой функцией почек показана двухэтапная чреспузырная аденомэктомия: первый этап — наложение надлобкового свища до улучшения почечной функции (установка мочевыводящей трубки в мочевой пузырь через низ живота в мочеприемник); второй этап — чреспузырная энуклеация аденомы (удаление аденоматозных узлов через мочевой пузырь). Одномоментная чреспузырная аденомэктомия отличается простотой подхода и относительно низкой летальностью (2%). Существует несколько способов оперативного и так называемого малоинвазивного (более щадящего) оперативного лечения среди них: трансуретральное эндохирургическое лечение (ТУР), трансуретральная электровапоризация, трансуретральная электроинцизия, методы эндоскопической лазерной хирургии (лазерная абляция, вапоризация, коагуляция) и криодеструкния предстательной железы. Аппаратные термальные методы лечения ДГПЖ используют с применением эндоурологических манипуляций на базе хирургических урологических отделений. Большинство аппаратов для термотерапии являются источником электромагнитного излучения в диапазоне дециметровых и сантиметровых волн, обеспечивают местное нагревание ткани до 45-85 °С и ее некротизацию (отмирание). Применяют как трансуретральные, так и трансректальные методики. Эти процедуры позволяют удалить гиперплазированную ткань простаты. Однако операция далеко не всегда позволяет избавиться от симптомов болезни. Поэтому оперативное удаление аденомы не означает автоматического излечения. Существуют противопоказания для проведения оперативного лечения аденомы. Любое оперативное вмешательство способно привести к развитию тяжелых послеоперационных осложнений.
Аневризма простаты что такое
Аневризмы висцеральных артерий (АВА) встречаются довольно редко и в большинстве наблюдений являются диагностической находкой при обследовании больного. По данным мировой литературы, частота АВА при аутопсиях составляет от 0,01 до 0,2% [8]. АВА классифицируются по происхождению: врожденные и приобретенные; по морфологии: истинные и ложные; по форме: мешотчатые и веретенообразные [1, 2]. Наиболее часто из АВА встречаются аневризмы селезеночной артерии (60-80%), затем следуют аневризмы печеночной артерии (20%), аневризмы гастродуоденальной, панкреатодуоденальной артерий, артерии поджелудочной железы (6%); реже наблюдаются аневризмы верхней брыжеечной артерии (5,5%), чревного ствола (4%); аневризмы артерий других локализаций встречаются менее чем в 4% наблюдений [2, 9]. Особняком стоит проблема диагностики и лечения аневризм почечных артерий, встречающихся гораздо чаще и занимающих второе место после аневризм селезеночной артерии [6].
Этиология АВА довольно широка. Причинами появления истинных АВА являются атеросклероз, фибромышечная дисплазия, нарушение в строении коллагеновых волокон и часто встречающееся разрушение медии сосудистой стенки, выражающееся в потере или фрагментации эластиновых нитей и уменьшении мышечных волокон. Однако, по данным литературы, атеросклеротические изменения сосудистой стенки рассматриваются как вторичные проявления. Псевдоаневризмы появляются вследствие травматического повреждения сосудистой стенки, вызванного в том числе ятрогенией, инфицированием, воспалением или васкулитами. Изменение структуры окружающих тканей также способствует развитию АВА. Наглядным примером является неблагоприятное воздействие ферментативной системы поджелудочной железы на окружающие ткани при развитии панкреатита [10].
Аневризмы селезеночной артерии (АСА)
АСА встречаются чаще всего. Для АСА характерна четкая связь с половой принадлежностью пациента, у женщин они встречаются в 4 раза чаще, чем у мужчин [11]. Данное соотношение объясняется агрессивным воздействием на сосудистую стенку селезеночной артерии повышенного уровня эстрогенов [9]. Среди женщин с АСА 40% являются повторнородящими [11] и у 10% выявляются деструктивные изменения печени с исходом в цирроз и развитием портальной гипертензии, приводящей к повышению давления в бассейне селезеночной артерии [11]. Фибродисплазия как основной фактор появления АСА отмечается в 2% наблюдений [11] в сочетании с изменениями в структуре почечных артерий. Псевдоаневризмы селезеночной артерии, как правило, возникают в результате развития панкреатита и панкреатических псевдокист. Как правило, АСА достигают 4 см в диаметре, мешковидные, протекают асимптомно и располагаются в средней или дистальной трети селезеночной артерии [10]. Гораздо реже встречаются веретенообразные АСА. Частота разрывов АСА зависит от размера аневризм и достигает 12% с летальностью 36% [5]. Разрывы АСА во время беременности, часто происходящие в III триместре, являются катастрофой и приводят к смерти плода и матери в 70-90% наблюдений [10].
Развернутая клиническая картина при АСА проявляется, как правило, при разрыве. Пациенты в момент разрыва АСА ощущают острую боль в области левого подреберья с иррадиацией в подлопаточную область, что сопровождается выраженной гипотонией. Начинающийся разрыв АСА происходит изнутри в толщу аневризматического мешка с последующим разрывом внешней оболочки и кровоизлиянием в брюшную полость; описанный процесс известен под названием «феномен двойного разрыва» [10].
В большинстве наблюдений АСА можно визуализировать при плановой рентгенографии органов грудной клетки как сосудистый кальцинат, имеющий вид круга [11]. Диагностика АСА дополняется применением мультиспиральной компьютерной томографии, а также селективной ангиографии.
Хирургическое лечение АСА сводится к резекции аневризматического мешка, перевязке селезеночной артерии и спленэктомии при больших размерах аневризматического мешка и расположении в воротах селезенки. После спленэктомии образовавшееся пространство заполняют большим сальником [11]. Дистальная панкреатотомия может быть выполнена при расположении аневризмы в паренхиме поджелудочной железы. Сохранение селезенки без реконструкции артериального сегмента может привести к инфаркту этого органа с развитием абсцесса. В случае возможности реконструкции производят резекцию аневризматического мешка с восстановлением структуры селезеночной артерии с помощью наложения анастомоза конец в конец или протезированием артерии аутовенозным трансплантатом.
Известны наблюдения эндоваскулярных вмешательств при АСА. Однако несмотря на малую травматичность применяемых методик, существуют ограничения в использовании эндоваскулярной хирургии. Для оптимального результата необходимо наличие широкой шейки АСА и расположения последней в проксимальной трети селезеночной артерии, что приведет к «выключению» аневризмы из кровотока и улучшению перфузии селезенки и снижению риска разрыва. Кроме того, применение стент-графта позволяет облегчить доступ к селезеночной артерии во время эмболизации селезенки при гиперспленизме. Однако естественный извитой ход селезеночной артерии, дистальное расположение аневризм существенно ограничивают проведение стента, поэтому открытое хирургическое вмешательство выходит на первый план [11].
Аневризмы печеночной артерии (АПА)
АПА занимают второе место по частоте среди аневризм непарных висцеральных ветвей брюшного отдела аорты, составляя 20%, половина из которых представлена ложными аневризмами. Расположение аневризм помогает в выявлении причины и определении дальнейшей тактики ведения больного. Внутрипеченочные аневризмы ветвей печеночной артерии часто образуются в результате травмы, ятрогенных повреждений после биопсии или оперативных вмешательств на печени, воздействия инфекционных агентов или вследствие васкулита. Внепеченочные аневризмы, как правило, наблюдаются после трансплантации печени, общехирургических манипуляций, чрескожных вмешательств на желчевыводящих путях, закрытой травмы живота, а также сопровождают гепатоцеллюлярный рак [10].
Как правило, АПА одиночные, веретенообразные или мешотчатые и в 80% наблюдений располагаются внепеченочно. Очень малая доля АПА протекает с определенной симптоматикой (дискомфорт в эпигастральной области вследствие расширения аневризматического мешка, болевой синдром, характерный для панкреатита) [11]. Иногда АПА могут вызывать желтуху или гемобилию. Описанные симптомы составляют триаду Квинке и отмечаются у 1 / 3 больных [10]. Чаще всего АПА диагностируют с помощью применения селективной ангиографии, компьютерной томографии, ультразвуковой диагностики или МРТ. Рентгенография малоинформативна ввиду низкой частоты атеросклеротического поражения артериальной стенки.
От 20 до 40% АПА осложняются разрывом, что приводит к летальному исходу в 35-40% наблюдений [10]. Велик риск разрыва неатеросклеротических АПА. Разрыв АПА чаще происходит в гепатобилиарное пространство, приводя к гемобилии, в желудочно-кишечный тракт, полость желчного пузыря, воротную вену, а также в брюшную полость [5].
Аневризмы гастродуоденальной, панкреатодуоденальной артерий и артерии поджелудочной железы
В большинстве наблюдений развитию аневризм указанных артерий способствуют панкреатит, язвенная болезнь желудка и двенадцатиперстной кишки, повышение артериального давления в соответствующих бассейнах при окклюзии чревного ствола, перенесенные оперативные вмешательства на поджелудочной железе. Большинство больных предъявляют жалобы на боль в эпигастральной области с иррадиацией в спину. Разрывы аневризм сопровождаются кровотечением в полость желудка, двенадцатиперстной кишки, реже через желчевыводящие пути и панкреатические протоки. F. Boudghene и соавт. сообщали об успешном лечении 32 аневризм панкреатодуоденальных артерий с применением транскатетерной эмболизации. Следует подчеркнуть, при использовании эндоваскулярного лечения очень важно произвести поиск «питающей» артерии, так как в перигастральной области имеется очень развитая сосудистая сеть. С целью контроля за эффективностью проведенного лечения необходим ангиографический контроль в динамике [4, 5, 10].
Аневризмы чревного ствола (АЧС)
АЧС встречаются в 4% всех аневризм висцеральных ветвей аорты и часто являются асимптомными. В 13% наблюдений отмечаются разрывы с летальностью более 50%. Клиническая картина при разрыве АЧС представлена кровотечением в брюшную полость или в желудочно-кишечный тракт. Часто АЧС бывает дегенеративными, сочетаются в 20% наблюдений с аневризмами аорты и в 40% наблюдений с аневризмами других висцеральных артерий. В большинстве наблюдений АЧС являются диагностическими находками. При лечении АЧС применяют традиционное хирургическое вмешательство в объеме резекции аневризмы с восстановлением проходимости чревного ствола путем анастомозирования конец в конец. Если это невозможно, то производят целиакоаортальное протезирование синтетическими протезами или аутовеной. Частое расположение аневризм в проксимальном отделе чревного ствола и отсутствие шейки ограничивают применение эндоваскулярного вмешательства [5, 10].
Аневризмы верхней брыжеечной артерии (АВБА)
АВБА составляют 5,5% всех аневризм висцеральных артерий, часто сопровождаются дискомфортом и болью в животе, варьирующей от тупой до нестерпимой и ассоциирующейся с «кишечной жабой». Они бывают мешотчатыми и веретенообразными, обычно располагаются в проксимальной части ВБА рядом с устьем панкреатодуоденальной артерии и средней толстокишечной артерии. Причинами развития АВБА являются грибковые поражения с вторичным присоединением бактериальной микрофлоры, связанные с бактериальным эндокардитом, наркоманией. Также имеются сведения о влиянии дегенерации медии, травмы и болезни Бекета. От 38 до 50% аневризм осложняются разрывами.
Выбор метода лечения зависит от состояния гемодинамики больного и операционного риска. Наиболее часто применяется традиционное хирургическое лечение. Варианты оперативных вмешательств включают резекцию, ушивание или перевязку аневризмы с выполнением артериальной реконструкции или без нее. Допускается перевязка ВБА и ЧС в связи с выраженным развитием коллатерального кровообращения. Однако реконструктивная хирургия с применением аутовенозного или синтетического трансплантата незаменима при высокой угрозе разрыва аневризмы или наличии признаков ишемии кишечника. Ввиду наиболее частого захвата аневризмой проксимального отдела ВБА, отсутствия зоны имплантации стента ограничивают применение эндоваскулярного лечения [3, 5, 10].
Аневризмы почечных артерий (АпА)
АпА часто рассматривают отдельно от остальных аневризм висцеральных ветвей ввиду отличной этиологии и значительно меньшего риска разрыва и низкой летальности. АпА тесно связаны с артериальной гипертензией. Частота истинных АпА составляет примерно 0,015-1%. Появлению АпА способствует дегенерация медии и фибродисплазия, а также фрагментация внутренней эластической пластинки, обнаруженная при гистологических исследованиях. В определенной степени развитию АпА способствуют артериальная гипертензия и атеросклероз. Редкими причинами являются нейрофиброматоз и неспецифический артериит. Большинство АпА мешотчатые и в 75% наблюдений они расположены в ветвях первого или второго порядка, менее чем в 10% наблюдений отмечается интрапаренхимальное расположение аневризм. Большинство АпА протекает асимптомно и лишь в 30% наблюдений имеют место злокачественная гипертензия, болевой синдром, гематурия, инфаркт почки и разрыв. Наиболее серьезным осложнением, встречающимся в 30% наблюдений, является разрыв АпА. Летальность достигает 10%. Однако имеются сведения о сочетании АпА с АСА у беременных, при разрыве во время беременности летальность достигает 80-90% [11].
АпА выявляются с помощью ультразвуковой диагностики, брюшной аортографии и мультиспиральной компьютерной томографии.
Лечение АпА заключается в применении как консервативных методов, так и хирургического лечения. Консервативный метод лечения используют при асимптомных АпА. Аневризмы диаметром до 2 см требуют динамического наблюдения. В случае злокачественной гипертензии, проявления урологических симптомов рекомендуют проведение диссекции, эмболизации, локальной компрессии путем эндоваскулярного вмешательства у женщин репродуктивного возраста или в периоде беременности. При хирургическом лечении производят резекцию аневризмы с последующей реконструкцией почечной артерии. При эндоваскулярном лечении в основном применяют стент-графты с учетом адекватного почечного кровотока. Однако при больших размерах аневризмы, распространении ее на паренхиму почки и при подозрении на разрыв производят резекцию почки или нефрэктомию с резекцией аневризмы и перевязкой пораженной почечной артерии. Оптимальным вариантом при хирургическом вмешательстве является забрюшинный доступ, обеспечивающий хорошую экспозицию почечной артерии и почки [6, 11]. В эпоху развития эндоваскулярной хирургии последнюю рассматривают как оптимальный вариант ввиду малой травматичности и хорошего отдаленного результата [7].
Таким образом, аневризмы висцеральных артерий являются редким сосудистым заболеванием и часто осложняются разрывом. Наиболее распространены аневризмы селезеночной, печеночной и почечных артерий. Клиническая картина крайне скудна и в основном проявляется в момент разрыва. Диагностический спектр включает ультразвуковое исследование, мультиспиральную компьютерную томографию с применением контрастных веществ; для оценки возможности применения эндоваскулярных методик используют селективную ангиографию. Выбор метода лечения зависит от тяжести состояния больного, клинических проявлений, а также локализации аневризмы и ее морфологии. Предпочтение отдают эндоваскулярным методикам, являющимся малотравматичными и обеспечивающими хороший долгосрочный результат. Однако в каждом конкретном наблюдении тактика ведения больного индивидуальна, выбор оптимального способа лечения аневризм висцеральных артерий основывается на данных всего спектра возможных диагностических манипуляций.