Амплификация в онкологии что это
Кроме транслокаций и других перестроек, при многих опухолях наблюдают другое цитогенетическое нарушение — амплификацию генов, ситуацию, когда в клетке появляется множество дополнительных копий сегмента генома. Амплификация генов часто встречается при многих опухолях, включая нейробластомы, сквамозноклеточный рак головы и шеи, колоректальные раки и злокачественные глиобластомы мозга.
Амплифицированные сегменты ДНК легко обнаружить при CGH, они проявляются как два типа цитогенетических изменений при обычном хромосомном анализе: двойные маркеры (очень небольшие дополнительные хромосомы) и гомогенно окрашивающиеся регионы, не имеющие нормальных бендов и содержащие многочисленные амплифицированные копии конкретного сегмента ДНК.
Как и почему появляются двойные маркеры и гомогенно окрашиваемые регионы, полного понимания нет, но известно, что амплифицированные регионы включают дополнительные копии протоонкогенов, такие как гены, кодирующие Мус, Ras, и рецептор эпителиального фактора роста, который стимулирует рост клеток или блокирует апоптоз, или и то другое сразу. Например, амплификация протоонкогена MYCN, кодирующего белок N-Myc — важный клинический прогностический показатель детской нейробластомы.
MYCN увеличивается более чем в 200 раз в 40% случаев на поздних стадиях развития нейробластом; несмотря на агрессивное лечение, только у 30% больных на поздней стадии выживаемость составляет более 3 лет. В отличие от этого, амплификацию MYCN обнаруживают только в 4% нейробластом на ранних стадиях, и 3-летняя выживаемость достигает 90%. Амплификация генов, кодирующих субстраты химиотерапевтических препаратов, также участвует в развитии резистентности к лекарствам у пациентов, ранее получавших химиотерапевтическое лечение.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в содержание раздела «генетика» на нашем сайте
Рак груди и HER 2
Прежде чем приступить к лекарственному лечению рака молочной железы, необходимо составить так называемый «биологический портрет опухоли». В этот комплекс входит определение рецепторного статуса опухоли, индекса пролиферативной активности ki-67 и статус HER 2.
Определение HER 2 статуса опухоли и FISH-тест
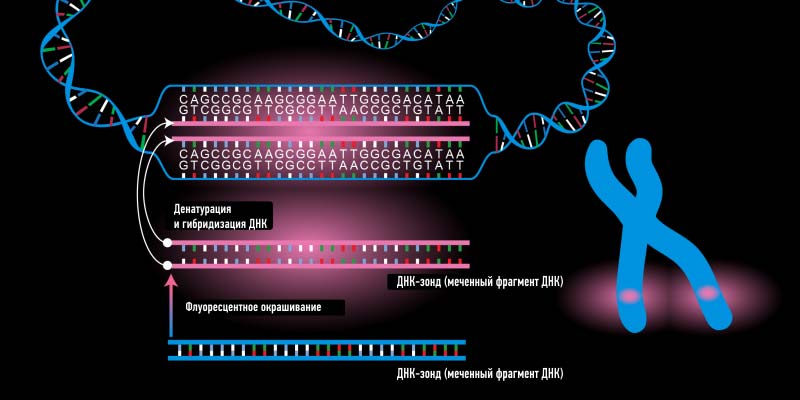
Дальше следует анализ опухоли на амплификацию гена. Он называется методом внутриклеточной флуоресцентной гибридизации или аббревиатурой FISH от английского fluorescence in situ hybridization. При FISH-тесте «рассматривают» в ядре опухолевой клетки саму ДНК, в которой флуоресцентные метки соединились с геном HER2. Светящиеся метки контактируют со всеми копиями гена, во флуоресцентный микроскоп видно, что копий гена больше, чем необходимо. Тест FISH выдаёт такие варианты ответа:
Механизм работы трастузумаба понятен не до конца. Предполагают, что он активирует Т-лимфоциты, поэтому при большом количестве Т-лимфоцитов в опухоли, трастузумаб не работает. Большое число Т-лимфоцитов, собравшихся вокруг клеток опухоли, как бы сигнализируют ему: «Место уже занято, борьба с опухолью идёт, больше тут делать нечего». А вот когда Т-лимфоциты не населяют опухоль, трастузумаб оказывается полезным.
В конечном итоге трастузумаб каким-то образом пресекает взаимодействие рецептора с фактором роста, поэтому опухолевая клетка не получает сигнала о делении, а чувствительность к гормональным препаратам и цитостатикам повышается.
Трастузумаб сопровождает цитостатическую и гормональную терапию, эффект от использования его в качестве единственного лекарства против рака молочной железы очень скромен.
Рекомендации обязывают использовать трастузумаб при наличии гена HER2 при любом противоопухолевом лечении пока только на протяжении года, но изучение результатов 6-месячной терапии продолжается. Препарат значимо удорожает лечение – 17 введений в течение года обходятся очень недёшево, поэтому исследователи стараются найти оптимальное соотношение длительности лечения и его эффективности.
Кардиотоксичность герцептина
Препарат герцептин обладает токсическим действием на миокард сердца, вызывая хроническую сердечную недостаточность и патологическое расширение желудочков сердца больше чем у трети больных. Женщинам с исходной сердечной патологией лечение проводят под контролем ЭХО-ЭКГ и в сокращённом режиме.
По большому счёту, каждая женщина, получающая химиотерапию с трастузумабом, должна иметь не только личного врача-химиотерапевта, но и личного врача-кардиолога, ориентированного в превратностях влияния противоопухолевых лекарств на сердечно-сосудистую систему.
Парадоксально, но в штатах государственных онкологических учреждений нет кардиологов, обычные кардиологи поликлиник и кардиологических диспансеров прекрасно разбираются в болезнях сердца, но не знают, какой противоопухолевый препарат какую патологию сердечно-сосудистой системы вызывает.
Кардиологи Юсуповской больницы не просто ориентированы, они специализируются на проблемах токсических повреждений миокарда, возникающих в процессе химиотерапии. Они всегда готовы оказать высококвалифицированную помощь и нацелены на профилактику патологии сердца.
Анти-HER2 терапия в лечении рака молочной железы
Анти-HER2 терапия в лечении рака молочной железы
Процессы роста и размножения всех клеток в организме находятся под жестким регулирующим контролем генов, которые способных запускать или останавливать их. В норме в организме поддерживается баланс между появлением новых клеток и гибелью старых. В опухолевых клетках процессы размножения клеток выходят из под контроля. Зачастую это происходит по причине возникновения «сбоев» в работе определенных генов, играющих наиболее важную роль в контроле над делением клеток.
HER2 (аббревиатура от английского human epidermal growth factor receptor 2 – рецептор фактора роста эпидермиса) является одним из таких генов. Этот ген может также обозначаться как «HER2-neu» или «ERBB2», эти названия являются синонимами. Его неправильная работа обнаруживается во многих случаях развития рака молочной железы и приводит к активной выработке в клетках одноименного белка (HER2), что заставляет клетки быстро делиться. Когда в клетке образуется избыточное количество белка HER2, говорят об амплификации этого гена. Амплификация HER2 обнаруживается примерно у 25% пациенток с диагнозом рака молочной железы. Её наличие приводит к повышению агрессивности опухолевых клеток. Вследствие высокой важности знания HER2-статуса опухоли, определение наличия амплификации HER2 является или избыточной выработки белка HER2 является одним из стандартных методов обследования, и проводится у всех пациенток с диагнозом рака молочной железы. Кроме того, в ряде исследований была продемонстрирована клиническая значимость выработки HER2 при раке желудка, по этой причине препараты, подавляющие активность этого белка также применяются для лечения рака желудка.
В чем особенности HER2-положительного рака молочной железы?
Изначально HER2-позитивный рак молочной железы был одним из наиболее агрессивных разновидностей этого заболевания, который характеризовался очень быстрым темпом роста опухоли, высоким риском развития рецидива болезни и появления отдаленных метастазов. Тем не менее, в настоящее время разработано множество препаратов, подавляющих активность этого белка (см. ниже). Они продемонстрировали высокую эффективность в лечении HER2-положительного рака молочной железы, превратив этот подтип рака в один из относительно благоприятных вариантов заболевания. Проведение целенаправленной («таргетной») терапии, блокирующей активность HER2, позволяет значительно повысить эффективность лечения и резко снизить риск развития рецидива рака молочной железы или добиться длительного контроля над болезнью в случае лечения её поздних стадий.
Кому назначаются препараты, блокирующие активность HER2?
Необходимо отметить, что применение препаратов, блокирующих активность HER2, целесообразно только в том случае, если в опухоли есть повышенная выработка этого белка вследствие наличия амплификации гена HER2. Если она отсутствует, раковые клетки не вырабатывают этот белок, следовательно, назначение препаратов, блокирующих активность этого белка не приведет к желаемому результату. По этой причине перед началом лечения всем пациенткам с диагнозом рака молочной железы перед началом лечения проводится специальное обследование, направленное на определение повышенной выработки HER2. Эта информация критически важна для правильного лечения рака молочной железы.
Как определяется HER2 статус опухоли?
В процессе диагностики рака молочной железы небольшой кусочек опухолевой ткани путем биопсии забирается для проведения иммуногистохимического исследования. Как правило, одновременно проводится определение наличия экспрессии (выработки) опухолевыми клетками рецепторов женских половых гормонов, HER2-статуса опухолевых клеток, а также темпов её роста (индекс Ki-67). При проведении этого исследования на опухолевые клетки наносятся специальные «красители», которые окрашивают HER2 в случаях, когда он содержится в клетках в большом количестве. Иммуногистохимическое исследование оценивает наличие гиперпродукции белка HER2 опухолевыми клетками.
По результатам иммуногистохимического определения HER2 статуса опухоли может быть получен один из следующих результатов:
0 баллов – в опухоли не отмечено признаков экспрессии HER2 (результат исследования отрицательный, назначение анти-HER2 препаратов нецелесообразно);
Если по результатам иммуногистохимического исследования была выявлена выраженная экспрессия HER2 (3+), пациентке показано назначение препаратов, блокирующих активность этого белка, так как опухолевые клетки активно вырабатывают этот белок и процессы их роста зависят от его функционирования. Если результат исследования отрицательный (0 или 1+) назначение такого лечения не приведет к желаемому результату.
Получение сомнительного результата (2+) означает, что по результатам иммуногистохимического исследования достоверно определить наличие экспрессии HER2 не удалось и необходимо проведение дополнительных методов исследования, например, т.н. «флюоресцентной гибридизации in situ» (FISH) или схожего с ней метода CISH. Эти методы позволяют напрямую оценить наличие амплификации HER2. По результатам проведения этих тестов может быть получен положительный или отрицательный ответ. Положительный ответ означает, что была выявлена амплификации HER2 и целесообразно назначение анти-HER2 терапии.
Какие существуют лекарственные препараты для лечения HER2-позитивного рака молочной железы?
На данный момент разработано и внедрено в клиническую практику 4 препарата, подавляющих активность HER2. Они несколько различаются по структуре и механизму действия, а также по показаниям к применению, эти лекарства могут назначаться как в комбинации с другими препаратами, например химиотерапевтическими агентами, так и самостоятельно (в монотерапии). В этом разделе представлено краткое описание этих препаратов.
Трастузумаб – лекарственный препарат, который представляет собой белок (моноклональное антитело), сконструированный таким образом, чтобы избирательно связываться с HER2 и «закрывать» его, не давая ему возможности нормально функционировать и провоцировать процессы роста и деления опухолевых клеток. Трастузумаб является препаратом, который наиболее часто назначается пациенткам с HER2-положительным раком молочной железы. Он применяется в сочетании с химиотерапией в качестве пред- или послеоперационной терапии данного заболевания, а также для первоначального лечения поздних его поздних стадий. Препарат выпускается как в виде раствора для внутривенных капельных введений, так и в виде раствора для подкожных введений. Трастузумаб-эмтанзин (T-DM1) – комбинированный препарат, который содержит молекулы трастузумаба, соединенные с противоопухолевым препаратом эмтанзином, который оказывает губительное действие на клетки. Препарат сконструирован таким образом, что молекулы трастузумаба связываются со своей мишенью на поверхности опухолевых клеток, после чего эмтанзин проникает в них и вызывает гибель раковых клеток. Помимо лечения рака молочной железы трастузумаб также применяется для лечения рака желудка в случае выявления в опухоли гиперэкспрессии HER2. Препарат вводится внутривенно капельно.
Пертузумаб – также как и трастузумаб, пертузумаб представляет собой моноклональное антитело к HER2, однако в отличие от трастузумаба он связывается с другим участком этого белка. Препарат назначается в комбинации с трастузумабом и позволяет повысить эффективность лечения. Препарат вводится внутривенно капельно.
Лапатиниб – препарат, блокирующий сигнальный путь, который проводит сигналы от HER2. Препарат применяется для лечения пациенток, у которых было отмечено прогрессирование на фоне применения режимов лечения с использованием трастузумаба, а также для лечения HER2-положительного гормонозависимого рака молочной железы, в этом случае лапатиниб применяется в комбинации с гормонотерапией. Препарат выпускается в виде таблеток и принимается внутрь.
Указанные препараты назначаются только пациенткам с HER2-положительными опухолями (экспрессия HER2 3+ при проведении иммуногистохимического исследования или выявленная амплификация гена при проведении FISH или схожего метода исследования).
Может ли HER2 статус изменяться в процессе проведения лечения?
Необходимо отметить, что HER2 статус опухоли может меняться в процессе проведения лечения как результат изменений, происходящих в раковых клетках. Клетки опухоли ищут способ выжить на фоне проводимой терапии и постоянно изменяются. Например, в случае, если произошел рецидив исходно HER2-положительной опухоли, во вновь выявленных опухолевых очагах может отмечаться исчезновение выработки этого белка и утрата зависимости опухолевых клеток от влияния этого гена. Возможно и обратное – появление гиперэкспрессии HER2 в опухолях, которые исходно не вырабатывали этот белок. По этой причине в случае развития рецидивов или появления метастазов врач может рекомендовать повторное проведение биопсии и проведение нового тестирования для определения HER2 статуса опухоли.
HER2: известные данные о роли рецептора фактора роста в онкогенезе и новые технологии направленной на него терапии
Одной из наиболее серьезных проблем онкологии настоящего времени является высокая распространенность рака молочной железы. Поверхностным маркером такой опухоли зачастую является HER2 — рецептор фактора роста, о котором и пойдет речь в данном материале.
HER2 (human epidermal growth factor receptor 2, человеческий рецептор эпидермального фактора роста 2 типа) представляет собой гликопротеиновый рецептор, ассоциированный с поверхностью мембран клеток эпителиального и мезенхимального происхождения. HER2 относится к семейству рецепторов тирозинкиназ, которое включает 4 подтипа белков: HER1 или EGFR, HER2, HER3 и HER4 [1]. Активация рецепторов этого семейства обычно протекает после связывания с соответствующими лигандами. Однако HER2 на поверхности клетки постоянно находится в активной конформации, образуя гомодимеры или гетеродимеры с другими рецепторами своего семейства [2].
Рисунок 1 ❘ Типичное строение мономерного HER2 с внеклеточным, трансмембранным и внутриклеточным доменами.
В норме HER2 необходим для нормального развития молочных желез, в большом количестве присутствует на поверхности недифференцированных клеток эмбриона. Кроме того, HER2 был обнаружен в тканях почек, сердца, органов желудочно-кишечного тракта. Основным физиологическим эффектом этого рецептора является запуск клеточной пролиферации и подавление апоптоза [3]. В негативных условиях именно это действие HER2 становится основой развития многих злокачественных новообразований.
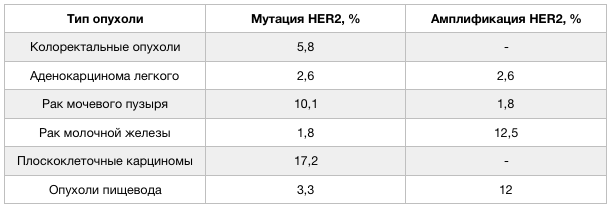
Структура HER2 кодируется протоонкогеном ERBB2, в структуре которого в случае развития опухоли зачастую обнаруживаются соматические мутации. Мутации могут влиять на строение как внеклеточного, так и трансмембранного участка HER2. При наличии таких измененных доменов сигнальные пути, поддерживающие опухолевый рост, функционируют даже в том случае, если в организме присутствуют нормальные копии гена данного рецептора [2]. Тип мутаций в гене ERBB2 определяет степень чувствительности опухоли к действию терапевтических агентов. Наибольшее число мутаций в гене HER2 обнаружено при нейроэндокринных опухолях предстательной железы, раке мочевого пузыря и плоскоклеточных карциномах. Кроме того, участие гена HER2 в онкогенезе доказано на примере его амплификации, обнаруживаемой при опухолях молочных желез и гастроэзофагеальных новообразованиях. Частота встречаемости мутаций и амплификаций ERBB2 в опухолях различного типа неодинакова.
Рисунок 2 ❘ Частота встречаемости мутаций и амплификаций гена HER2 при различных опухолях.
Прогностические данные в отношении опухолей, связанных с мутацией и амплификацией гена HER2, также различаются. При раке молочной железы отмечен меньший процент выживаемости пациентов, опухоль которых была вызвана мутацией гена. В случае немелкоклеточного рака легкого такой взаимосвязи выявлено не было. Для других распространенных опухолей подобная корреляция также не отмечалась, либо данные исследований неоднозначны [3].
Повышение выработки HER2 отмечается в 20 % случаев рака молочной железы и является негативным прогностическим фактором. Агрессивность роста и инвазии HER2-положительных опухолей связана с функционированием его как рецептора фактора роста, активирующего сигнальные пути, которые запускают рост и дифференцировку клеток, а также подавляют апоптоз. Кроме того, HER2-положительные опухоли часто являются малодифференцированными и имеют большую вероятность метастазирования в регионарные лимфоузлы и отдаленные органы [4].
Количество HER2 на поверхностях опухолевых клеток значительно, что позволяет достоверно отличать нормальные клетки от злокачественно измененных, используя методы иммуногистохимии и FISH. Кроме того, мутации в гене ERBB2 определяются современными методами генетических исследований, о чем было рассказано в материале про наследственные опухолевые синдромы (https://medach.pro/post/1858).
Современные технологии позволяют использовать для лечения HER2-позитивных опухолей высокоэффективные препараты таргетной терапии, внедрение которых существенно повлияло на общую выживаемость пациентов. Особенностью строения HER2 является крайняя стабильность эпитопов внеклеточных доменов, что позволяет эффективно исследовать и тестировать средства таргетной терапии. Такие препараты разрабатываются на основе моноклональных антител, ингибиторов малых молекул и препаратов-конъюгатов.
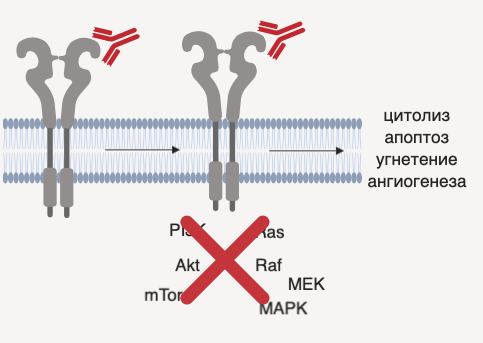
Наиболее распространены препараты моноклональных антител (например, трастузумаб), которые имеют двойной эффект: с одной стороны, они связываются с юкстамембранным и димеризационным доменами HER2, прекращая их активность, с другой стороны, обладают прямым цитотоксическим эффектом. Ингибиторы малых молекул (такие, как лапатиниб) снижают внутриклеточную каталитическую активность, прекращая таким образом функционирование сигнальных путей, ассоциированных с ростом опухолевой клетки. Препараты-конъюгаты имеют множественное действие в отношении опухолей и в настоящее время показывают более высокую эффективность в сравнении с изолированным применением препаратов моноклональных антител [5].
Рисунок 3 ❘ Принцип действия препаратов моноклональных антител, активных в отношении HER2.
Важным аспектом таргетной терапии HER2-позитивных новообразований является выработка резистентности опухолей к препаратам моноклональных антител. Снижение эффективности таких препаратов наблюдается у пациентов с крайне высокой концентрацией рецептора на поверхности опухолевых клеток. Резистентность к трастузумабу в настоящее время отмечается у 60 % пациентов и реализуется несколькими путями, например, путем снижения синтеза внеклеточных доменов HER2 в опухолевых клетках. В тканях подобных опухолей отмечается накопление карбоксилированных внутриклеточных доменов HER2, которые в будущем могут стать предикторами резистентности опухоли к трастузумабу [6]. Еще одним механизмом, связанным с формированием резистентности опухоли к препаратам таргетной терапии против HER2, является эпителиально-мезенхимальный переход [2]. Подобная тенденция требует поиска новых стратегий лечения. Так, показали себя эффективными комбинации HER2-направленных агентов и двойных блокаторов HER2. В сравнении с трастузумабом более эффективными оказываются препараты биспецифичных антител (например, эртумаксомаб) [7]. Несомненно, разработки в этой области должны продолжаться. Главной целью исследовательской работы в направлении изучения HER2 становится снижение смертности пациентов от рака молочной железы, опухолей легких и желудка, а также улучшение долгосрочных прогнозов при лечении таких новообразований.
Источники
Анализ дозы гена HER2/neu при раке молочной железы
Рецептор HER2 − один из наиболее значимых молекулярных маркеров при раке молочной железы (РМЖ). В нормальном состоянии рецептор HER2 располагается на поверхности многих клеток организма.
Примерно у каждой четвёртой женщины, больной РМЖ, количество этого белка в клетках опухоли повышено по сравнению с нормой.
В основе увеличенной экспрессии лежит амплификация гена HER2/neu. Избыточное количество этого рецептора на поверхности раковых клеток свидетельствует о высокоагрессивной форме РМЖ. Высокоагрессивная форма РМЖ − злокачественное новообразование в молочной железе с амплификацией и увеличенной экспрессией гена HER2/neu. Опухоль данного типа ведет себя крайне агрессивно и быстро метастазирует в другие органы.
Больные РМЖ с положительным HER2-статусом имеют плохой прогноз и низкую выживаемость (1-2 года с момента постановки диагноза). HER2-положительный статус опухоли выявляется у 25-30% всех пациентов с РМЖ (около 15 тыс. новых случаев в год). Заболеванию подвержены женщины в репродуктивном возрасте.
Показания к генетическому анализу:
 | Все женщины с выявленным РМЖ должны пройти проверку на определение HER2-статуса в клетках опухоли, поскольку этот статус крайне важен как для прогноза, так и для подбора адекватного лечения, так как опухоль с положительным HER2-статусом не реагирует на традиционные линии химиотерапии. |
 | Проверка HER2-статуса позволяет врачу с большей точностью определить, к какому из типов рака относится данная конкретная опухоль, уточнить диагноз и подобрать в индивидуальном порядке наиболее подходящее лечение. |
На сегодняшний день анализ дозы гена HER2/neu при метастатическом раке молочной железы рекомендован Европейским обществом медицинских онкологов как необходимый элемент обследования больного.
Положительный HER2-статус опухоли важен сразу с нескольких точек зрения:
 | позволяет врачу оценить склонность опухоли к прогрессированию; |
 | определить реакцию организма на предложенное лечение. |
Показано, что для пациентов с положительным HER2-статусом опухолей при химиотерапии:
 | использование метатрексата и тамоксифена неэффективно; |
 | использование антрациклинов и платиносодержащих препаратов более эффективно; |
 | использовани таксанов и ингибиторов ароматазы одинаково эффективно, вне зависимости от HER2-статуса опухоли. |
HER2-статус позволяет узнать, имеет ли смысл назначать лечение герцептином.
Герцептин (Roche, Швейцария) является ярким представителем класса таргетных препаратов на основе моноклональных антител, которые с высокой степенью избирательности связываются с внеклеточной частью рецептора HER2. Благодаря этому действию поражение раковых клеток становится более направленным, адресным, а лечение более щадящим по отношению к здоровым клеткам организма. После того как Герцептин блокирует HER2-рецепторы на поверхности раковой клетки, ее дальнейший рост прекращается и в ряде случаев наблюдается уменьшение опухоли. Кроме прямого антипролиферативного действия герцептин способен вызывать уничтожение опухолевых клеток за счет реакции антителозависимой клеточной цитотоксичности.
Использование герцептина позволяет:
 | увеличить время до прогрессирования и общую выживаемость больных с гиперэкспрессией HER2/neu; |
 | преодолеть резистентность опухоли к цитостатическим препаратам; |
 | уменьшить дозу химиотерапии, что дает шанс продлить отпущенные болезнью годы жизни. |
Установление статуса HER2
Для определения HER2-статуса опухоли проводится анализ дозы гена HER2/neu в клетках опухоли с помощью ПЦР в режиме реального времени. Данная технология имеет очень хорошую (более 95%) корреляцию с иммуногистохимическим методом диагностики HER2-статуса опухолей.
Кроме того, ПЦР в реальном времени является прекрасной альтернативой тест-системе на основе флуоресцентной гибридизации in situ (FISH), которая была рекомендована Управлением по контролю за качеством пищевых продуктов и лекарственных средств (США) как стандартный метод диагностики HER2-статуса опухолей при прогнозировании течения РМЖ.
Материал для исследования:
 | ДНК, выделенная из ткани опухоли РМЖ, полученной во время биопсии или операции; |
 | ДНК, выделенная из архивных образцов ткани опухоли РМЖ, заключённых в парафиновые блоки. |
Срок выполнения – 14 рабочих дней