Аммиак: чем опасен и как действовать при отравлении
Аммиак в переводе с греческого (hals ammoniakos) — амонова соль. Аммиак — бесцветный газ с резким запахом, температура плавления — 80° С, температура кипения — 36° С, хорошо растворяется в воде, спирте и ряде других органических растворителей. Синтезируют из азота и водорода. В природе образуется при разложении азотсодержащих органических соединений.
Чистый аммиак был получен английским химиком и философом Джозефом Пристли в 1774 году. Промышленную технологию получения аммиака разработали и осуществили в 1913 году немецкие химики Фриц Габер и Карл Бош, получившие за свои исследования Нобелевские премии.
Аммиак — один из самых важных продуктов химической промышленности. Большая часть получаемого в промышленности аммиака идёт на приготовление азотной кислоты, азотных удобрений, красителей. Применяется аммиак и для получения взрывчатых веществ. Широко используются водные растворы аммиака. Как слабое летучее основание, он применяются в химических лабораториях и производствах. С помощью аммиака получают пищевую соду.
В медицине 10% водный раствор аммиака известен как нашатырный спирт. Резкий запах аммиака раздражает специфические рецепторы слизистой оболочки носа и способствует возбуждению дыхательного и сосудодвигательного центров, поэтому при обморочных состояниях или алкогольном отравлении пострадавшему дают вдыхать пары нашатырного спирта.
При пайке металлов используют хлорид аммония — нашатырь — NH4Сl. При высокой температуре нашатырь разлагается с образованием аммиака, который очищает поверхности паяльника и спаиваемого изделия от оксидов металлов.
При испарении жидкого аммиака поглощается большое количество теплоты, поэтому его используют в холодильных установках.
Жидкий аммиак вызывает сильные ожоги кожи, поэтому его обычно перевозят в стальных баллонах (окрашены в желтый цвет, имеют надпись «Аммиак» черного цвета), железнодорожных и автомобильных цистернах, по воде — в специальных танкерах, транспортируют также по трубопроводам.
Смесь аммиака с воздухом взрывоопасна. Аммиак горит при наличии постоянного источника огня. Емкости могут взрываться при нагревании. Газообразный аммиак является токсичным соединением. При его концентрации в воздухе рабочей зоны около 350 мг/м3 (миллиграмм на кубический метр) и выше работа должна быть прекращена, а люди выведены за пределы опасной зоны. Предельно допустимая концентрация аммиака в воздухе рабочей зоны равна 20 мг/м3.
Первая медицинская помощь: промыть глаза и лицо водой, надеть противогаз или ватно-марлевую повязку, смоченную 5% раствором лимонной кислоты, открытые участки кожи обильно промыть водой, немедленно покинуть очаг заражения.
При попадании аммиака в желудок надо выпить несколько стаканов теплой воды с добавлением одной чайной ложки столового уксуса на стакан воды и вызвать рвоту.
Индивидуальная защита: изолирующий и фильтрующие противогазы марок М, КД, респиратор РПГ-67КД, при их отсутствии — ватно-марлевая повязка, смоченная 5% раствором лимонной кислоты, защитный костюм, резиновые сапоги, перчатки.
В зоне поражения необходимо держаться с наветренной стороны. Изолировать опасную зону и не допускать посторонних. В зону аварии входить только в полной защитной одежде. Соблюдать меры пожарной безопасности, не курить.
При утечке и разливе: устранить источники открытого огня. Устранить течь. Для осаждения газов использовать распыленную воду. Оповестить об опасности отравления местные органы власти. Эвакуировать людей из зоны, подвергшейся опасности заражения ядовитым газом. Не допускать попадания вещества в водоемы, тоннели, подвалы, канализацию.
При пожаре: убрать из зоны пожара, если это не представляет опасности, и дать возможность догореть. Не приближаться к горящим емкостям. Охлаждать емкости водой с максимального расстояния. Тушить распыленной водой, воздушно-механической пеной с максимального расстояния.
Материал подготовлен на основе информации открытых источников
15 запахов, которые могут говорить о присутствии опасного химического вещества
Нам повезло родиться в 21 веке, а не в конце 19 или начале 20, тем самым попав под раздачу Первой или Второй мировой войны. Это были самые страшные конфликты в истории, которые унесли жизни десятков миллионов человек.
1. Кислые фрукты
Запах кислых фруктов может свидетельствовать о наличии бромбензилцианида — боевого отравляющего маслянистого вещества тёмно-коричневого цвета, которое в больших дозах может вызвать отравление цианидом и летальный исход. С этим веществом вряд ли можно столкнуться в России, даже проникнув на заброшенное военное хранилище, так как оно использовалось в ходе Первой мировой войны западными странами, входящими в блок Антанта.
2. Черёмуха или цветущая яблоня
Если чувствуешь этот запах когда-то, кроме цветения черёмухи или яблони, а рядом проходит какая-нибудь незаконная акция, беги как можно дальше, ведь это может быть хлорацетофенон. Это боевое отравляющее вещество является слезоточивым газом, который может серьёзно повредить глаза и дыхательные пути. В отличие от предыдущего вещества, оно используется и сегодня, обычно в полицейских операциях для дезориентации людей и их лёгкого захвата.
3. Сладковатый резкий запах хлорки
Хлор — одно из самых популярных бытовых средств, которое встречается и в мирной жизни. Но хлор хлору рознь, и та низкая концентрация в обеззараживающих средствах для мытья сантехники не сравнится с тем, что хранится в заводских цехах для нужд промышленности. При утечке хлора можно почувствовать характерный запах хлорки, но более резкий и сладковатый. Этот зеленовато-жёлтый газ может вызвать серьёзные повреждения дыхательных путей.
4. Анисовый или мягкий горчичный запах
За эти ароматы отвечает хлорпикрин — вещество, которое используется в фумигантных смесях в сельском хозяйстве. То есть на него можно наткнуться даже в обычной жизни, если произойдёт утечка пестицидов в агрокомплексах. Это вещество раздражает кожу и слизистые, вызывает бронхит, отёк лёгких и неконтролируемые конвульсии мышц диафрагмы, а также слезотечение и рвоту.
5. Прелое сено
Если ты чувствуешь этот запах не в чистом поле, прогуливаясь рядом со стогами сена, а где-то в городе, особенно рядом с заводами, производящими поликарбонат или красители, у нас для тебя плохие новости — это фосген. Данное вещество обладает удушающим действием, которое повреждает дыхательную систему, приводит к отёку лёгких и смерти.
6. Запах загорающейся спички
Нормально чувствовать этот запах только когда кто-то рядом зажёг спичку. В других случаях это может говорить о наличии в воздухе оксида серы, который представляет собой бесцветный газ. В высоких концентрациях он токсичен и вызывает насморк, кашель, охриплость, першение в горле, а затем удушье, расстройство речи, рвоту, отёк лёгких и затруднение глотания. В городских условиях утечки этого вещества могут происходить рядом с овощехранилищами и складами, где им окуривают продукты для уничтожения микроорганизмов. Также его используют для отбеливания материалов, которые нельзя обрабатывать хлором.
7. Чеснок или горчица
Если не планируешь отправляться на машине времени на Первую мировую войну, вряд ли столкнёшься с ипритом, который имеет такой запах. Но так как снаряды с этим газом до сих пор лежат по всей Западной Европе, на это боевое отравляющее вещество можно наткнуться даже во время прогулки по лесу в путешествии за рубеж. Иприт не оказывает немедленного действия, и симптомы начинают проявляться только через 12-36 часов после попадания вещества на кожу и слизистые. Иприт поражает глаза, носоглотку и дыхательные пути, вызывает общее отравление организма и раздражение кожи с последующим образованием пузырей, которые позже лопаются и на их месте образуются язвы.
8. Герань
Нормально ощущать запах герани, если пришёл к своей бабушке, выращивающей эти цветы. В большинстве других случаев стоит как минимум напрячься, ведь этот запах может указывать на наличие в воздухе люзита — маслянистой тёмно-коричневой жидкости, имеющей кожно-нарывное действие. Наткнуться на люзит можно разве что, если стать диггером и бродить по бункерам времён Первой мировой войны, или оказаться там, где это вещество перерабатывают для получения мышьяка.
9. Миндаль или фрукты
Опять же опасность, как и в случае с люзитом, этот запах представляет для диггеров, которые ходят там, где не нужно, в данном случае, по бункерам времён Второй мировой войны. Так пахнет табун — боевое отравляющее вещество нервно-паралитического действия, которое, при попадании на кожу или слизистые, вызывает тревогу, сужение зрачков, насморк, чрезмерное слюноотделение, одышку, потливость, замедленное сердцебиение, судороги, потерю контроля над мочевым пузырём и кишечником, паралич и остановку дыхания.
10. Яблоки, камфора или скошенное сено
Эти запахи могут указывать на другое боевое отравляющее вещество нервно-паралитического действия — зоман. Поражает нервную систему и вызывает остановку дыхания. Симптомы схожи с воздействием табуна.
11. Лук или чеснок
От боевых отравляющих веществ перейдём к чему-то более мирному. Так пахнет акрилонитрил — вещество, используемое при производстве некоторых видов каучука, акрила и композитных материалов. Это ядовитое отравляющее канцерогенное вещество раздражает слизистые оболочки и кожу, и при вдыхании в больших концентрациях может приводить к раку лёгких, а также к летальному исходу.
12. Шпроты или запах испорченной рыбы
Если неподалёку упала отработанная ступень ракеты, и ты чувствуешь запах шпрот или испорченной рыбы — беги оттуда как можно скорее. Это может быть несимметричный диметилгидразин. Это вещество имеет канцерогенные свойства и обладает сильным токсическим и мутагенным действием. Симптомами отравления являются раздражение слизистых оболочек глаз и дыхательной системы, сильное возбуждение центральной нервной системы, тошнота и рвота.
13. Тухлые яйца
За этот запах отвечает сероводород. В больших концентрациях этот газ очень токсичен, вызывая головокружение, головную боль, тошноту, судороги, отёк лёгких, а также, при значительном превышении допустимой концентрации, приводит к коме и летальному исходу.
14. Уксус
Если живёшь рядом с промышленными объектами, где производят алюминий, полупроводники, сплавы металлов, синтетические масла, пластические массы или материалы из силикатов, и ощущаешь сильный запах уксуса, это может говорить о выбросе плавиковой кислоты. Это токсичное вещество вызывает острое отравление с раздражением кожи и слизистых, а также, при попадании в кровь, поражает кроветворные органы, органы пищеварения, и приводит к отёку лёгких.
15. Тухлая капуста
При разложении сераорганических соединений, например, при гниении белков, выделяется метантиол. Этот газ в небольших концентрациях содержится в кишечных газах, и именно он, вместе с другими тиолами, придаёт им неприятный запах. Также этот газ синтезируется в промышленности. В больших концентрациях метантиол является токсичным веществом, которое может поражать центральную нервную систему, вызывать головную боль, тошноту и раздражение дыхательной системы.
Аммиак – опасный, но важный газ!
Аммиак – опасный, но важный газ!
Химические реактивы, лабораторное оборудование и приборы – это главные 
Определение
Аммиак (в евр. языках – «аммониак») – это бесцветный газ, запах которого знаком каждому, даже тем, кто очень далек от химии. Он крайне острый, специфический, напоминающий запах нашатырного спирта, способный вызвать слезотечение. Аммиак очень ядовит, вдвое легче воздуха, смесь с которым взрывоопасна. Хорошо смешивается со спиртом и некоторыми другими органическими растворителями во всех соотношениях. При температуре 10 °C он сгущается в жидкость, кипящую при 33,7 °C. Этот химический реактив легко растворяется в воде с активным выделением тепла. Данный раствор называется аммиак водный или аммиачная вода. В пищевой промышленности – как добавка E527.
Раствор аммиака не совместим с:
— органическими кислотами;
— солями валентных металлов;
— крахмалом;
— солями ртути;
— йодом и др..
История открытия аммиака
В переводе с греческого он означает амонова соль, – так в древности называли нашатырь. Аммиак был открыт британским химиком Д. Пристлеем, который известен как первооткрыватель кислорода и углекислого газа. Именно он назвал этот газ «щелочным воздухом или летучей щелочью», так как водный раствор аммиака обладал всеми свойствами и признаками щелочи. Благодаря французскому химику Бертолле он получил официальный термин «нашатырь». Это определение употребляется во многих западноевропейских языках.
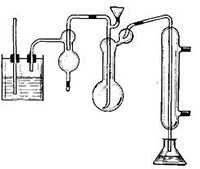
Аппарат для отгонки аммиака
Основной задачей данного лабораторного оборудования является дистилляция и отгонка аммиака с водяным паром, измерение массовой доли белка в пастеризованном, стерилизованном или сыром молоке, кисломолочных напитках.
Этот аппарат состоит из:
— конической колбы;
— воронки капельной с краном;
— переходника из лабораторного стекла;
— стеклянной колбы Кьельдаля;
— Т-образной, изогнутой соединительной и резиновых трубок;
— делительной воронки;
— холодильника шарового;
— каплеуловителя;
— стеклянных деталей (соединенных резиновыми трубками).
Применение аммиака
За последние несколько десятилетий производство аммиак на мировом рынке занимает одно из лидирующих мест, составляя приблизительно 100 миллионов т. Он может выпускаться как в жидкой форме, так и в виде аммиачной воды. Сфера применения его очень обширна, но главным образом это охватывает промышленность и медицину.
1. Промышленность:
— получение азотной кислоты для производства искусственных удобрений;
— изготовление солей аммония, уротропина, мочевины;
— для нейтрализации кислотных отходов;
— применение как дешевый хладагент при производстве холодильников;
— получение синтетических волокон (нейлона, капрона);
— при очистке и крашении шерсти, шелка и хлопка.
2. Медицина. Благодаря раздражающему действию аммиак в виде водного 
В хирургической практике раствор применяется в качестве средство для дезинфекции. Кроме того, примочки с раствором аммиака используются для нейтрализации токсинов при укусах насекомых и змей.
Меры предосторожности
Высококачественный аппарат для аммиака можно купить в специализированном online магазине химических реактивов Москва розница «Прайм Кемикалс Групп». Всегда в наличии имеется аммиак, лабораторная посуда, мешалка магнитная и весы электронные лабораторные для работы с ним.
Широкий ассортимент приборов, аппаратов, химреактивов, оборудования и лабораторной посуды купить в Москве также можно на нашем сайте. Весь товар сертифицирован и соответствуют нормам ГОСТ.
“Prime Chemicals Group” – с нами сотрудничать надежно и выгодно!
Источники аммиака
Аммиак естественным образом вырабатывается и используется всеми млекопитающими в их нормальном метаболизме. Аммиак вырабатывается в организме человека каждый день. Большая часть этого аммиака вырабатывается органами и тканями, но часть — бактериями, живущими в нашем кишечнике.
Аммиак встречается естественным образом в окружающей среде. Вы можете подвергаться воздействию аммиака, дыша воздухом, употребляя пищу или содержащую его питьевую воду, а также при контакте кожи с аммиаком или соединениями аммиака. Воздействие аммиака, находящегося в окружающей среде, чаще всего происходит при вдыхании аммиака, который выделяется в воздух.
Источники аммиака в воздухе
На открытом воздухе вы можете подвергнуться воздействию высоких концентраций аммиака в воздухе в результате утечек и разливов на производственных и складских объектах, а также из трубопроводов, автоцистерн, железнодорожных вагонов, кораблей и барж, перевозящих аммиак. Более высокие уровни аммиака в воздухе могут возникать при внесении удобрений с аммиаком или соединений аммиака на сельскохозяйственных полях. После внесения удобрений концентрация аммиака в почве может превышать 3 000 ppm, однако через несколько дней эти уровни быстро снижаются.
Внутри помещений Вы можете подвергаться воздействию аммиака при использовании бытовых продуктов, содержащих аммиак. Некоторые из этих продуктов — это растворы для мытья аммиака, средства для мытья окон, воск для пола и обонятельные соли.
Аммиак имеет очень сильный запах, который раздражает, и что Вы можете чувствовать запах, когда он находится в воздухе на уровне выше 5 ppm (частей на миллион). Поэтому Вы, вероятно, почувствуете запах аммиака до того, как подвергнетесь воздействию концентрации, которая может навредить Вам.
Уровни аммиака в воздухе, которые вызывают серьезные последствия у людей, намного выше, чем уровни, которые Вы обычно подвергаете себя дома или на работе. Однако низкие уровни аммиака могут навредить некоторым людям, страдающим астмой, и другим чувствительным людям.
Беспокоитесь о загрязнении воздуха производства аммиаком? Вас может заинтересовать измерение концентрации аммиака в воздухе.
Источники аммиака в воде
Вы можете ощутить аммиак в воде на уровне около 35 ppm. Более низкие уровни аммиака естественным образом проявляются в пищевых продуктах и воде. Проглатывание даже небольшого количества жидкого аммиака в чистящей жидкости может привести к ожогам во рту и горле. Несколько капель жидкого аммиака на коже или в глазах могут вызвать ожоги и открытые язвы, если их быстро не смыть. Воздействие больших количеств жидкого аммиака или ионов аммония в глазах вызывает сильные ожоги глаз и может привести к слепоте.
Бытовые и промышленные растворы для уборки могут содержать аммиак, и использование этих средств дома или на работе может привести к воздействию аммиака. Оба вида растворов для уборки аммиака производятся путем добавления в воду газа аммиака для образования жидкого аммиака.
Средства для очистки помещений обычно содержат более низкие уровни аммиака (от 5 до 10%) по сравнению с промышленными растворами для очистки, которые могут содержать более высокие уровни аммиака (до 25%).
Аммиак в фермерских хозяйствах
Фермеры могут подвергаться воздействию аммиака при работе с удобрениями, содержащими аммиак, или при внесении удобрений на полях. Фермеры, животноводы и люди, занимающиеся разведением других видов домашнего скота и/или птицы, могут подвергаться воздействию аммиака в результате разложения навоза. В некоторых производственных процессах также используется аммиак. В некоторых старых холодильных установках в качестве хладагента используется аммиак.
Во-вторых, представляем собственно заметку о трёх веществах, которые обыватели постоянно путают: нашатырь, нашатырный спирт и аммоний.
Зачем применяется нашатырный спирт? Во-первых, это нюхательная жидкость. Выделяющийся из неё аммиак обладает резким стимулирующим нервную систему действием, он сгоняет сонливость, опьянение, повышает кровяное давление. Во-вторых, это неплохое чистящее средство. В-третьих, его используют в садово-огородном деле для борьбы с некоторыми вредителями (главным образом слизнями).
Выглядит карбонат аммония, или гиршгорн (уж будем называть его именно так), как белый порошок или кристаллы с сильным запахом аммиака, таким же, как и у нашатырного спирта. У сухого гиршгорна амбрэ, однако, намного сильнее, чем у аптечного раствора аммиака. При нагревании он совершенно разлагается на углекислый газ, воду и аммиак; при конденсации этих паров образуется нашатырный спирт и очень небольшое количество карбоната аммония по сравнению с первоначальным, образующегося вновь из газов. Также, стоя просто на воздухе, он разлагается на аммиак и бикарбонат аммония (его тоже называли гиршгорном, и по свойствам он очень похож на карбонат, но более кислый и слабее пахнет).
Применяется «аммоний» в кулинарном деле вместо дрожжей: его способность разлагаться на газы при нагревании приходится очень кстати при выпекании разной пышной выпечки. Также его можно использовать для тех же медицинских целей, что и нашатырный спирт: как нюхательный стимулятор, снимающий сонливость и опьянение.