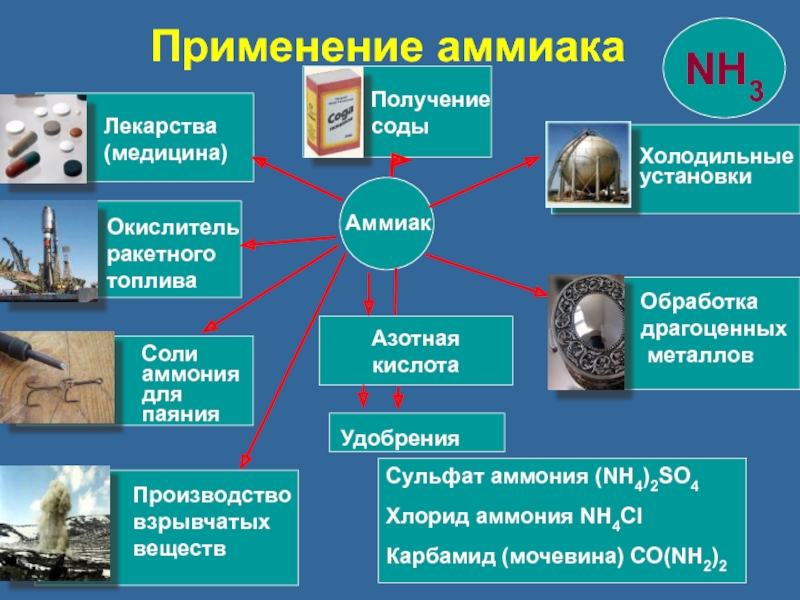
Применение аммиака
Аммиак — одно из наиболее часто применяемых в различных сферах человеческой деятельности химических веществ. Каждый год в мире производится огромное количество аммиака— больше 180 млн тонн.Из них порядка 15 млн тонн производит Россия, которая является одним из крупнейших экспортеров этого вещества. Для чего же человеку нужно такое количество этого продукта?
Об основных свойствах аммиака
Разнообразие сфер применения аммиака обусловлено его физическими и химическими свойствами. Аммиак (химическая формула NH3) —бесцветный газ с резким неприятным запахом. При длительном действии на организм человека аммиак вызывает поражение разных органов.
Аммиак вступает в химические реакции с другими элементами и соединениями с образованием новых веществ. Например, в результате реакции безводного аммиака с азотной кислотой получают аммиачную селитру, применяемую в производстве взрывчатых веществ и азотных удобрений.
Аммиак способен восстанавливать различные металлы из их оксидов.
Промышленное применение аммиака
Основная доля производимого технического аммиака используется в химической промышленности:
Применение аммиака в медицине
В медицине широко применяется 10%-й раствор аммиака, известный под названием — нашатырный спирт. Нашатырный спирт используют для приведения в чувство человека, потерявшего сознание. Применяют его и в качестве рвотного средства в очень слабом растворе и в малом количестве. Нашатырным спиртом обрабатывают укусы насекомых. Разведенным в воде нашатырным спиртом хирурги обрабатывают руки.
Важно! Использовать раствор аммиака следует с большой осторожностью и только по назначению. Передозировка его очень опасна!
Аммиак полезен и в быту
Вот только несколько возможных способов использования нашатырного спирта в доме.
И это только небольшая часть тех случаев, когда аммиак приходит на помощь человеку.
Сферы и области применения аммиака. Где применяется аммиак.
Одним из важнейших химических веществ, которое используют в разных сферах деятельности человека, является аммиак. Ежегодно это вещество производят в огромных количествах – больше 100 млн тонн. Только вдумайтесь в это число! Сразу же возникает вопрос: « Для чего производят такое количество аммиака?». В этой статье мы ответим на этот вопрос, а также выясним причину популярности аммиака.
Свойства аммиака
Физические и химические свойства аммиака обуславливают его применения в различных областях. Аммиак представляет собой газообразное вещество без цвета с очень резким и неприятным запахом. Вещество ядовито. При длительном воздействии на человеческий организм способен вызывать отёки и поражение различных органов.
Аммиак – это слабая кислота, он взаимодействует с кислотами, водой, а с металлами способен образовывать соли. Он способен вступать в различные химические реакции с другими химическими веществами. Например, реакция безводного аммиака с азотной кислотой на практике позволяет получить аммиачную селитру, которая применяется для производства удобрений.
Аммиак является восстановителем. Он способен восстанавливать разные металлы из их оксидов. Реакция взаимодействия аммиака с оксидом меди дает возможность получить азот.
Различные сферы использования аммиака
Несмотря на свою токсичность, аммиак используют в самых разных сферах. Основная часть производимого аммиака идет на изготовление разных продуктов химической промышленности. К таким продуктам относятся:
— сода. Существует аммиачный метод получения кальцинированной соды. Аммиак используется для насыщения солевого рассола. Данный метод активно используется для промышленного производства соды.
— азотная кислота. Для её производства используют синтетический аммиак. На данный момент промышленное производство данного вещества основано на явлении катализа синтетического аммиака.
— взрывчатые вещества. Нитрат аммония нейтрален к механическому воздействию, но при некоторых условиях характеризируется высокими взрывчатыми свойствами. Именно поэтому он используется для производства таких веществ. В результате получают аммониты – аммиачные взрывчатые вещества.
— растворитель. Аммиак, в жидком состоянии, может использоваться как растворитель различных органический и неорганических веществ.
— аммиачная – холодильная установка. Аммиак применяется в холодильной технике, в качестве холодильного агента. Аммиак не вызывает парниковый эффект, он экологически чистый и дешевле фреонов. Эти факторы обуславливают применения данного вещества в качестве хладагента.
— нашатырный спирт. Его применяют в медицине и в быту. Данное вещество отлично выводит пятна с одежды различного происхождения, а также нейтрализует кислоты.
Применение аммиака в медицине
Важно помнить, что передозировка аммиаком очень опасна. Возможны болевые ощущения в различных органах, их отеки и даже летальный исход. Этого можно избежать, если использовать данное вещество по назначению и с осторожностью!
Аммиак, нашатырь и нашатырный спирт — в быту их путают

На самом деле это разные вещества, которые отличаются друг от друга своим происхождением, агрегатным состоянием и химическими формулами. Роднит эти три разных вещества только резкий аммиачный запах.
Запах один, а вещества разные
Для того чтобы раз и навсегда разубедиться в том, что нашатырный спирт и аммиак — это одно и тоже, достаточно обратиться к истории их происхождения и посмотреть на их химические формулы.
Аммиак — нитрид водорода, газ с молярной массой 17 г/моль, химическая формула — NH3.
Нашатырный или аммиачный спирт — жидкость с химической формулой NH4OH.
Нашатырь — соль с химической формулой — NH4Cl.
Происхождение аммиака

По второй легенде, в северной Африке в районе оазиса Аммона находилось пересечение караванных путей. Там проходило огромное количество животных, дорога была усеяна их калом и обильно полита мочой, которые испарялись и выделяли газ, который называли «аммиак».
Что касается научного открытия газа с названием «аммиак», то оно датируется 1785 годом. Химическую формулу газа, NH3, определил французский ученый К. Л. Бертолле и назвал его «аммиак».
Но еще в 1774 году английский ученый Д. Пристли получил идентичный газ, которому дал название «щелочной воздух», но химического состава вывести не смог.
Получают аммиак двумя способами — промышленным и лабораторным. При лабораторном способе аммиак получается при нагревании щелочей и соли аммония:
В промышленных условиях аммиак сначала производится в газообразном виде, а затем его сжижают и доводят до 25%-го водного раствора, который называется аммиачная вода.

Промышленный способ синтеза аммиака был изобретен в 1909 году немецким химиком Фрицем Габером. В 1918 году за свое открытие в химии он получил Нобелевскую премию. Первый завод по производству аммиака был запущен в 1913 году в Германии, а в 1928 году производство аммиака было уже налажено в России.
Происхождение нашатыря
Нашатырь (Hammoniaci P. Sal) — это соль, химическая формула NH4Cl (хлорид аммония).
Нашатырь имеет вулканическое происхождение; встречается в горячих источниках, испарениях грунтовых вод, в залежах гуано и самородной серы; образуется при горении угольных пластов или скоплений мусора. Имеет вид натёков, землистых налётов, корочек или массивных скелетных кристаллических скоплений, гроздей и дендритов.
Чистый нашатырь бесцветный или белый, со стеклянным блеском. В зависимости от имеющихся в нем примесей, цвет может быть всех оттенков жёлтого, бурый, серый, разных оттенков красного, коричневый.
При нагревании из нашатыря выделяется аммиак, он хорошо растворяется в воде. Раствор на вкус жгучий едко — солёный, запах резкий аммиачный.
Нашатырь был известен людям с очень давних времен и использовался в ритуальных обрядах, при производстве и окраске тканей, а также алхимиками для пайки металлов и сплавления золота.
В Средние века научились получать искусственный нашатырь из рогов и копыт крупного рогатого скота, который называли «духом оленьего рога».
Происхождение нашатырного спирта

Это 10-процентный раствор аммиачной воды с химической формулой NH4OH; бесцветная прозрачная однородная смесь, способная испаряться; со специфическим запахом аммиака, который при замерзании сохраняется.
Упоминание о его использовании восточными алхимиками датируется еще VIII веком, а европейскими алхимиками 13 веком. До наших дней дошли их записи об используемых ими рецептурах.
В наши дни получают промышленным и простым бытовым способом:
Области применения
Область применения аммиака и аммиачного спирта широка, он используется практически во всех сферах жизнедеятельности человека, начиная от технологических процессов и заканчивая медициной и бытовыми нуждами.
Применение аммиака
Аммиак широко применяется в качестве хладагента в различном бытовом и промышленном оборудовании.
Он является одним из важнейших продуктов, используемых в химической промышленности. В частности, его используют в производстве:
Использование аммиачного спирта
Аммиачный спирт применяется в медицине и в быту.
Применение в медицине показано в следующих случаях:
Применение в быту заключается в обезжиривании и чистки различной домашней утвари.
Раствором спирта из расчета 2 ч. л. на 2 стакана воды и 1 ст. л. любого средства для мытья посуды можно отлично почистить столовое серебро, серебряные и золотые ювелирные украшения (изделия с жемчугом нашатырным спиртом чистить нельзя, он станет серым и мутным). Для этого надо поместить в раствор столовое серебро или ювелирные изделия, подержать от 1 до 2 часов, затем прополоскать в воде и насухо вытереть.
Он хорошо выводит пятна крови, мочи и пота с шерсти, шелка и лайкры. В качестве пятновыводителя используется 50% раствор. В концентрированном виде может удалить следы от карандаша на одежде.
С ковров, мебельной обивки и автомобильных чехлов можно удалить пятка раствором из 1 ст. л. чистого аммиака и 2 л горячей воды. Для этого надо прочистить загрязнение и дать просохнуть. Если будет необходимость, то можно повторно прочистить.
Оконные стекла, зеркала и фаянс тоже можно почистить раствором из 1 ст. л. чистого аммиака и 3 ст. воды. Поверхность будет чистая и хорошо блестеть.
Аммиачной водой 1 ст. л. в смеси с 4 л воды можно отчистить каменные налеты в ванне и умывальнике. Для этого надо их прочистить раствором, а потом промыть горячей водой.
Спирт может использоваться в садоводстве для борьбы с луковой мухой и тлей, а также в качестве удобрения, для огородных и комнатных растений в условиях кислой почвы.
Влияние на человека

При намерении использовать аммиак приобретать его надо исключительно в аптеках и внимательно знакомиться с прилагаемыми правилами пользования «Раствор аммиака. Инструкция по применению».
Превышение дозировок может вызвать отравление и серьезные проблемы со здоровьем, а также химические ожоги. Помещения, где он применяется, должны хорошо проветриваться.
Кроме ядовитости, пары аммиака взрывоопасные. Это происходит при смешении их с воздухом в определенной пропорции, поэтому при работе необходимо соблюдать особые правила техники безопасности при работе со взрывчатыми веществами.
Первыми симптомами отравления могут быть:
Дальнейшими признаками развития отравления являются:
При приеме внутрь аммиачной воды в превышающих дозах может возникнуть:
Если у человека имеется индивидуальная непереносимость к запаху аммиака, то даже незначительное его попадание через дыхательные пути или вовнутрь может сразу привести к самым неблагоприятным последствиям.
Если у человека на теле имеется нарушение кожных покровов в виде мокнущих язв, экзем или дерматитов, то применение примочек может привести к еще более обширной аллергической реакции и ожогам кожных покровов.
Первая помощь при отравлении
В случаях возникновения первых признаков отравления этими веществами необходимо срочно начать оказывать пострадавшему первую помощь.
К первой помощи можно отнести следующие меры:
В случае более тяжелых форм отравления необходимо срочно вызывать скорую помощь.
Аммиачный спирт обязателен в наборах медикаментов для первой помощи в аптечках и в нужный момент должен быть под рукой.
Сколько может стоить в аптеках? Ответ — совсем недорого. Приобретайте, пользуйтесь, но будьте предельно осторожны.
Аммиак – опасный, но важный газ!
Аммиак – опасный, но важный газ!
Химические реактивы, лабораторное оборудование и приборы – это главные 
Определение
Аммиак (в евр. языках – «аммониак») – это бесцветный газ, запах которого знаком каждому, даже тем, кто очень далек от химии. Он крайне острый, специфический, напоминающий запах нашатырного спирта, способный вызвать слезотечение. Аммиак очень ядовит, вдвое легче воздуха, смесь с которым взрывоопасна. Хорошо смешивается со спиртом и некоторыми другими органическими растворителями во всех соотношениях. При температуре 10 °C он сгущается в жидкость, кипящую при 33,7 °C. Этот химический реактив легко растворяется в воде с активным выделением тепла. Данный раствор называется аммиак водный или аммиачная вода. В пищевой промышленности – как добавка E527.
Раствор аммиака не совместим с:
— органическими кислотами;
— солями валентных металлов;
— крахмалом;
— солями ртути;
— йодом и др..
История открытия аммиака
В переводе с греческого он означает амонова соль, – так в древности называли нашатырь. Аммиак был открыт британским химиком Д. Пристлеем, который известен как первооткрыватель кислорода и углекислого газа. Именно он назвал этот газ «щелочным воздухом или летучей щелочью», так как водный раствор аммиака обладал всеми свойствами и признаками щелочи. Благодаря французскому химику Бертолле он получил официальный термин «нашатырь». Это определение употребляется во многих западноевропейских языках.
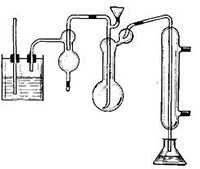
Аппарат для отгонки аммиака
Основной задачей данного лабораторного оборудования является дистилляция и отгонка аммиака с водяным паром, измерение массовой доли белка в пастеризованном, стерилизованном или сыром молоке, кисломолочных напитках.
Этот аппарат состоит из:
— конической колбы;
— воронки капельной с краном;
— переходника из лабораторного стекла;
— стеклянной колбы Кьельдаля;
— Т-образной, изогнутой соединительной и резиновых трубок;
— делительной воронки;
— холодильника шарового;
— каплеуловителя;
— стеклянных деталей (соединенных резиновыми трубками).
Применение аммиака
За последние несколько десятилетий производство аммиак на мировом рынке занимает одно из лидирующих мест, составляя приблизительно 100 миллионов т. Он может выпускаться как в жидкой форме, так и в виде аммиачной воды. Сфера применения его очень обширна, но главным образом это охватывает промышленность и медицину.
1. Промышленность:
— получение азотной кислоты для производства искусственных удобрений;
— изготовление солей аммония, уротропина, мочевины;
— для нейтрализации кислотных отходов;
— применение как дешевый хладагент при производстве холодильников;
— получение синтетических волокон (нейлона, капрона);
— при очистке и крашении шерсти, шелка и хлопка.
2. Медицина. Благодаря раздражающему действию аммиак в виде водного 
В хирургической практике раствор применяется в качестве средство для дезинфекции. Кроме того, примочки с раствором аммиака используются для нейтрализации токсинов при укусах насекомых и змей.
Меры предосторожности
Высококачественный аппарат для аммиака можно купить в специализированном online магазине химических реактивов Москва розница «Прайм Кемикалс Групп». Всегда в наличии имеется аммиак, лабораторная посуда, мешалка магнитная и весы электронные лабораторные для работы с ним.
Широкий ассортимент приборов, аппаратов, химреактивов, оборудования и лабораторной посуды купить в Москве также можно на нашем сайте. Весь товар сертифицирован и соответствуют нормам ГОСТ.
“Prime Chemicals Group” – с нами сотрудничать надежно и выгодно!
Аммиак – где используется, чем опасен, и что делать при утечке
Вещество аммиак один из часто используемых продуктов современной химии. Основная часть вещества NH3 используется для производства азотной кислоты, удобрений, различных красителей. Но есть и значительные определённые минусы. Аммиак опасное химическое вещество и требует особых условий при производстве, перевозке и хранении.
Как производят аммиак
Чистейший аммиак в 1774 году получил химик философ из Англии Джозеф Пристли. Но в промышленных масштабах аммиак производят с начала 20 века. Химики из Германии Карл Бош и Фриц Габер в 1913 году разработали промышленную технологию и запустили процесс производства. За данную разработку они были награждены Нобелевской премией.
Процесс получения NH3 очень энергоемкий, что является основным его недостатком. Из-за этого на протяжение долгих лет ученые ведут разработки по уменьшению затрат при производстве аммиака. В основе производства заложен принцип циркуляции. Все процессы должны идти непрерывно. Остатки исходных компонентов фильтруются от основного вещества и вновь уходят в процесс производства. Из-за чего синтез продукта цикличный и его нельзя резко останавливать.
В качестве сырья используют углеводород – природный газ. Прежде чем попасть в процесс производства NH3, газ несколько раз обрабатывают и выделяют водород. Далее водород подают в колонну синтеза под высоким давление совместно с азотом. Все процессы проходят при высоких температурах поэтому процесс получения аммиака является энергозатратным и очень опасным химическим производством.
Где используется вещество NH3
Аммиак – очень важное вещество в современной химической промышленности. Основная часть вещества используется для производства азотной кислоты, удобрений, красителей. Для получения взрывчатых веществ тоже используется аммиак. Водные растворы аммиака используются в ряде производственных процессов других веществ.
Из всем известных товаров, с помощью аммиака получают:
Чем опасен аммиак и что делают при утечке вещества
Для исключения разлива аммиака при транспортировке используют специальные стальные баллоны и цистерны. Также транспортируют в специальных танкерах. На производствах для транспортировки используют трубопроводы. Аммиак при контакте с воздухом превращается в взрывоопасную смесь. Воспламеняется при наличии источника огня. Емкости с аммиаком могут взорваться при перегреве из-за низкой температуры кипения вещества.
Газообразный аммиак очень ядовитое токсичное соединение. При концентрации аммиака в воздухе более 350 мг/м3 все работы должны быть прекращены. Люди должны выйти за пределы загазованной территории.
Аммиак при вдохе поражает дыхательные пути и так же влияет на зрение, при резкой высокой концентрации человек может погибнуть от отравления. Симптомы отравления:
При отравлении аммиаком необходимо срочно покинуть опасную зону и промыть глаза и открытые участки кожи водой, далее стоит обратиться к медикам.
В случае утечки, взрыва, пожара с наличием аммиака проводить ликвидацию аварии можно только в изолирующих химически защитных костюмах, например, изолирующие костюмы Стрелец.
В костюмах Стрелец АЖ ТАСК или Стрелец КИО ТАСК можно безопасно проводить работы в зонах распространения высококонцентрированного аммиака по устранению утечки и ликвидации последствий. Аммиак нейтрализуют большим количеством воды, которая распыляется под давлением в виде распыления с максимального расстояния от очага возгорания.
Учения по устранению утечки аммиака в костюмах Стрелец КИО