Использование продуктов на основе гидролизата молочного белка при пищевой аллергии у детей раннего возраста
Пищевые аллергены являются наиболее частыми этиологическими факторами в развитии атопии на первом году жизни. Одним из основных аллергенов, вызывающих развитие пищевой аллергии у детей грудного возраста, является белок коровьего молока (БКМ) [1]. Данный п
Пищевые аллергены являются наиболее частыми этиологическими факторами в развитии атопии на первом году жизни. Одним из основных аллергенов, вызывающих развитие пищевой аллергии у детей грудного возраста, является белок коровьего молока (БКМ) [1]. Данный продукт содержит более 20 антигенов, из которых наибольшими аллергенными свойствами обладают β-лактоглобулин, казеин, α-лактальбумин, бычий сывороточный альбумин. Ингредиенты коровьего молока (казеин, сывороточные белки) могут присутствовать во многих пищевых продуктах. Известно, что на первом году жизни аллергия к белкам коровьего молока встречается у 2–7% младенцев, находящихся на искусственном и 0,5–1,5% детей на естественном вскармливании. Среди больных атопическим дерматитом у 85–90% детей диагностируется аллергия к белкам коровьего молока. К другим распространенным клиническим проявлениям аллергии к БКМ относятся гастроинтестинальные нарушения, такие, как обильные срыгивания и рвота, колики, изменение характера стула — диарея или запоры. Реже встречается симптоматика со стороны органов дыхания — одышка, приступы удушья, апноэ.
Диагностика аллергии к БКМ основана на тщательном сборе аллергологического анамнеза и оценке всей клинической симптоматики. Для верификации диагноза в остром периоде заболевания проводится аллергологическое обследование — определение уровней специфических антител — IgE и IgG4 в сыворотке крови, реже — кожные пробы. Выявление тем или иным способом сенсибилизации к БКМ является показанием для полного исключения из питания ребенка продуктов, содержащих молочные протеины.
В случаях выявления пищевой аллергии у детей, находящихся на естественном вскармливании, учитывая уникальные свойства материнского молока, необходимо сохранить его в питании ребенка в максимальном объеме. Кормящей матери назначают гипоаллергенную диету, при этом степень пищевых ограничений и набор продуктов достаточно индивидуальны и зависят в первую очередь от тяжести клинических проявлений аллергии у младенца. При недостатке или отсутствии грудного молока в питании ребенка с аллергией к белку коровьего молока используются безмолочные лечебные смеси. Согласно современным рекомендациям, в период клинических проявлений аллергии (острый период атопического дерматита, желудочно-кишечные симптомы), безусловно, наиболее целесообразным является назначение смесей на основе высокогидролизованного молочного белка как продуктов, практически лишенных антигенных свойств [2, 3, 4, 5, 6]. Все продукты данной группы обогащены комплексом витаминов, макро- и микроэлементов и соответствуют требованиям ВОЗ по ингредиентному составу, биологической и пищевой ценности, влиянию на физическое и психомоторное развитие детей первого года жизни. Появление высокогидролизованных смесей значительно расширило возможности диетотерапии у детей раннего возраста с пищевой аллергией.
В зависимости от степени расщепления молочного белка выделяют смеси на основе его высокого (экстенсивного) или частичного (умеренного) гидролиза. Установлено, что чем ниже молекулярная масса пептидов гидролизата, тем ниже его иммуногенность и меньше риск развития аллергических реакций на данный продукт. Так, молекулярная масса нативного белка коровьего молока колеблется от 10 до 60 кDa. Молекулярный вес пептидов, ниже которого аллергенность белкового гидролизата становится минимальной, составляет 2,5–3 кDa. Однако и в составе данных продуктов возможно сохранение остаточных количеств белковых антигенов, способных вызвать аллергические реакции у больных с аллергией к белку коровьего молока. Аллергенные свойства частично гидролизованных белков снижены в 300–1000 раз по сравнению с БКМ.
По клиническому предназначению смеси на основе гидролизатов молочного белка можно подразделить на лечебные, лечебно-профилактические и профилактические. Включение смеси в ту или иную группу зависит от степени гидролиза белкового субстрата, а также от доказанной клинической эффективности продукта.
К лечебным относятся только специализированные смеси, созданные на основе высокогидролизованного молочного белка: «Альфаре», «Нутрилак пептиди СЦТ», «Нутрилон Пепти ТСЦ», «Прегестимил», «Нутрамиген», «Фрисопеп», «Фрисопеп АС» и др.
Такие гипоаллергенные смеси на основе частично гидролизованного молочного белка, как «НАН ГА 1», «НАН ГА 2», «Нутрилон ГА 1» и «Нутрилон ГА 2» должны применяться только для профилактики аллергических заболеваний у детей из групп высокого риска по развитию атопии, переводимых на смешанное и искусственное вскармливание.
Пептидный профиль ряда смесей, предназначенных для профилактики аллергии, — «Нутрилак ГА», «ХиПП ГА 1», «ХиПП ГА 2», «Хумана ГА 1» и «Хумана ГА 2» — свидетельствует о достаточно высокой степени гидролиза белкового субстрата, что позволяет говорить о возможности их использования не только в профилактических целях, но и для лечения легких форм аллергии к белкам коровьего молока, протекающих без участия IgE-опосредуемых механизмов.
Гипоаллергенные продукты на основе частично гидролизованного белка также могут применяться на втором этапе диетотерапии — этапе расширения рациона.
Кроме степени гидролиза белка, смеси отличаются по исходному субстрату, подвергаемому гидролизу: большинство продуктов создано на основе гидролиза сывороточных белков. Смеси «Прегестимил», «Нутрамиген», «Фрисопеп АС» — продукты на основе гидролизата казеина.
Имеются также определенные отличия в жировом и углеводном компонентах, по витаминному составу. Учет особенностей каждой смеси позволяет подобрать продукт в соответствии с индивидуальными особенностями клинической картины заболевания. В состав липидного компонента лечебных смесей «Альфаре», «Нутрилак пептиди СЦТ», «Нутрилон Пепти ТСЦ», «Прегестимил», предназначенных в первую очередь для детей с гастроинтестинальными проявлениями ПА и синдромом мальабсорбции, введены среднецепочечные триглицериды (до 50% общего количества липидов), которые легко всасываются в систему воротной вены, минуя лимфатические сосуды, не требуя эмульгирования и участия панкреатической липазы.
Необходимо также учитывать наличие или отсутствие лактозы в составе углеводного компонента смеси, поскольку аллергия к белку коровьего молока нередко сопровождается непереносимостью лактозы. В таких случаях целесообразно назначать смесь на основе высокогидролизованного белка, не содержащую лактозу [3].
Новым направлением детской нутрициологии является обогащение продуктов питания про- и пребиотиками. Среди гипоаллергенных продуктов следует отметить следующие смеси, обогащенные пребиотиками, — «Беби ГА», «Нутрилон ГА 1 и 2», «Нутрилон Комфорт 1 и 2», «Хумана ГА 2», а также единственный гипоаллергенный продукт, обогащенный бифидобактериями — «НАН ГА 2». Разработан и производится, но к настоящему времени не представлен на российском рынке продуктов детского питания «Нутрамиген LGG» — лечебный гидролизат с добавлением лактобактерий. Данные продукты наиболее показаны при наличии у детей дисбиотических отклонений в составе микрофлоры кишечника.
Несмотря на общепризнанную эффективность смесей на основе гидролизата молочного белка, поиск новых более гипоаллергенных субстратов для гидролиза продолжается. Так, появились первые сообщения о результатах исследования смеси, приготовленной на основе гидролизата белка риса. Исследование, проведенное в группе здоровых детей, показало хорошую усвояемость данной смеси. Был показан лечебный эффект данной смеси у детей с аллергией к БКМ [7, 8].
Еще одна группа продуктов, используемых в питании детей с аллергией к БКМ, это соевые смеси. В состав данных продуктов, помимо изолята соевого белка, входят растительные масла, декстрин-мальтоза, витаминно-минеральный комплекс в соответствии с физиологическими потребностями детей первого года жизни. Данные смеси содержат нативный белок и потенциально аллергенны [9, 10, 11], в связи с этим использование их у детей с пищевой аллергией в настоящее время ограничено. Следует избегать назначения соевых смесей детям младше 5–6 мес, в остром периоде заболевания, при наличии тяжелых, особенно гастроинтестинальных проявлений аллергии. Выполнение данных правил позволяет избежать развития сенсибилизации к соевому белку и появления аллергических реакций.
Алгоритм выбора лечебного продукта в зависимости от клинических проявлений аллергии и характера сенсибилизации представлен на рис. 1.
Сроки элиминации молочных смесей и продуктов из питания детей с пищевой аллергией индивидуальны. Минимальная длительность безмолочного питания у детей с аллергией к белкам коровьего молока составляет 4–6 мес, в отдельных случаях может продолжаться до одного года и более. Молочные продукты вводят в рационы детей, начиная со смесей на основе частично гидролизованного белка. Осуществляют это в период клинико-лабораторной ремиссии заболевания, постепенно, учитывая возможность развития повторных аллергических реакций.
Отметим, что в настоящее время нет окончательно сформированного общепринятого мнения в отношении возможности использования у детей с пищевой аллергией таких продуктов, как смеси на основе частично гидролизованного молочного белка, кисломолочных смесей, продуктов на основе козьего молока.
Кроме того, даже приведенный выше взвешенный диетологический подход — подбор продукта — заменителя грудного молока на основании всех имеющихся клинических данных и результатов специфической диагностики, с учетом индивидуальных особенностей больного позволяет выбрать лишь группу продуктов (лечебные, лечебно-профилактические, профилактические смеси), но не конкретный продукт детского питания. Вместе с тем клиническая практика показывает, что переносимость различных продуктов в пределах одной и той же группы у каждого конкретного ребенка может значительно отличаться. Различия индивидуальной переносимости продуктов в значительной мере связаны с разнообразием состава смесей, особенностей технологической обработки их белкового компонента, состава углеводных и жировых компонентов продукта, витаминного и минерального компонентов и других добавок.
С целью оптимизации диетотерапии и индивидуального подбора смеси для максимального снижения риска индивидуальной реакции непереносимости смесей нами был использован новый диагностический тест «Ифа-Лакттест» (далее «Лакттест»). Набор реагентов разработан в Медицинском научно-исследовательском центре «Медиан» (патент РФ 2006126792/15/029074/ от 24.07.06.). Он предназначен для полуколичественного определения в крови ребенка методом иммуноферментного анализа (ИФА) содержания антител классов IgG, IgG4 и IgЕ, иммунореактивных в отношении белково-пептидных антигенов, содержащихся в продуктах детского питания различных типов. Набор позволяет также определять концентрацию специфических антител к белковым компонентам грудного, коровьего и козьего молока, сои, овса, глютена пшеницы, а также к фракциям белка коровьего молока (бычий сывороточный альбумин, казеин, β-лактоглобулин) и яйца (овальбумин).
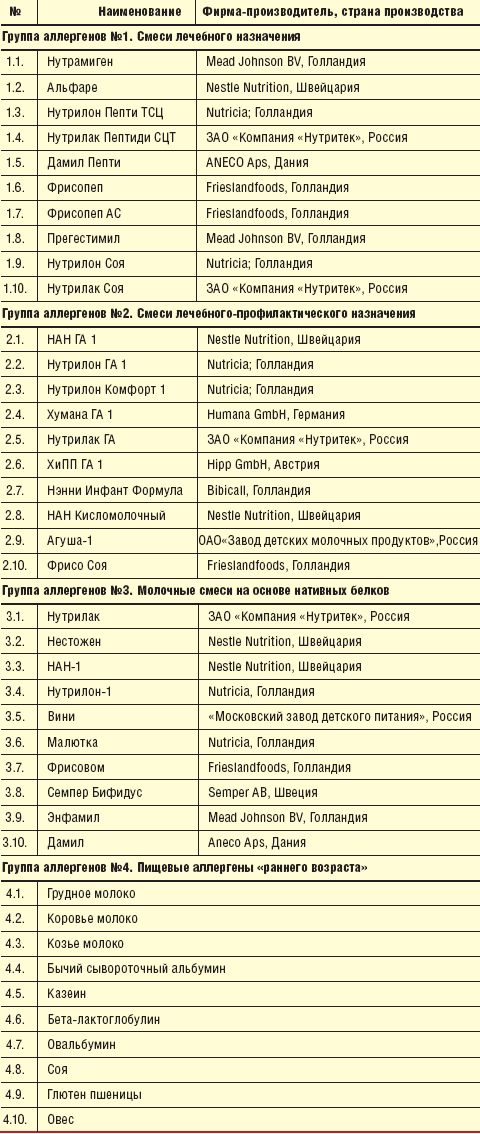
Используемые в наборе аллергены разделены на 4 группы (табл. 1), каждая из которых представлена на отдельном иммунологическом планшете (панели): 1-я группа включает суммарные белково-пептидные аллергены смесей лечебного назначения, 2-я — аллергены смесей профилактического назначения, 3-я — аллергены молочных смесей на основе нативных белков, 4-я — пищевые аллергены «раннего возраста». Данный набор аллергенов позволяет: во-первых, верифицировать диагноз аллергии к белку коровьего молока, поскольку включает аллерген белка коровьего молока и наиболее аллергенных его фракций (бычий сывороточный альбумин, β-лактоглобулин, казеин); во-вторых, наличие аллергена козьего молока позволяет выявить случаи перекрестной аллергии к козьему молоку; в-третьих, наличие в панели наиболее часто встречающихся пищевых аллергенов первого года жизни — сои, глютена, овальбумина — позволяет контролированно подбирать блюда прикорма; и наконец благодаря включению в состав панели грудного молока возможно оценить переносимость грудного молока детьми, находящимися на естественном вскармливании, и выявлять редко встречающиеся случаи непереносимости грудного молока. 1-я, 2-я и 3-я панели предназначены для индивидуального подбора специализированных смесей — заменителей грудного молока.
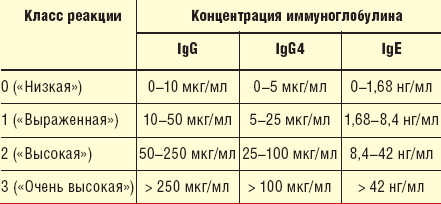
Содержание специфических антител оценивали полуколичественно в классах реакции. Каждый класс соответствует определенному диапазону концентраций иммуноглобулина (табл. 2).
У здоровых детей содержание специфических иммуноглобулинов характеризуется классом реакции 0. Повышение содержания антител к пищевым аллергенам (класс реакции 1 и выше) рассматривали как свидетельство сенсибилизации к данным аллергенам.
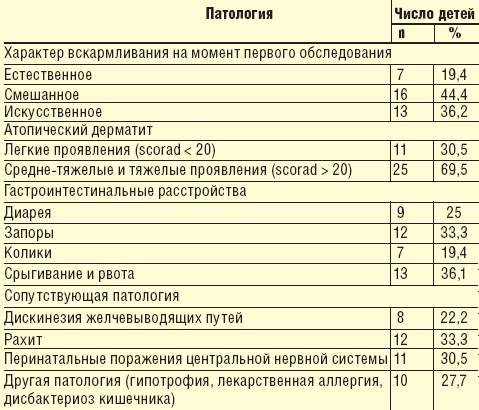
Оценка эффективности применения данного теста при назначении диетотерапии у детей с атопическим дерматитом первого года жизни нами была проведена у 36 детей, 58% из которых — мальчики, 15% — девочки в возрасте от 4 до 12 мес, находившихся на обследовании и лечении в Консультативно-диагностическом центре и отделении питания здорового и больного ребенка НЦЗД РАМН (табл. 3).
Длительность заболевания колебалась от 3 нед до 6 мес. Клиническое обследование детей проводилось по общепринятому плану и включало сбор анамнеза; оценку нутритивного статуса, клинических проявлений заболевания; инструментальные и лабораторные исследования (УЗИ органов брюшной полости, по показаниям — копрологическое исследование, определение экскреции углеводов с калом, исследование кишечной микрофлоры), аллергологическое обследование — определения методом ИФА специфических IgG4 к пищевым продуктам (анализ проводили в лаборатории клинической биохимии НЦЗД РАМН).
Выраженность проявлений атопического дерматита оценивали на момент обследования по индексу scorad. У 21 ребенка кожные проявления аллергии сопровождались симптоматикой со стороны желудочно-кишечного тракта, с помощью УЗИ в 8 случаях выявлены признаки дискинезии желчных путей, у 17 детей — реактивное увеличение поджелудочной железы.
Тщательный сбор аллергологического анамнеза позволил выявить четкие указания на аллергию к БКМ у 25 детей. Так, у 22 детей начало заболевания было связано с введением в питание детских смесей на основе нативных БКМ, в 9 случаях отмечалась отчетливая реакция в виде кожных высыпаний или гастроинтестинальной симптоматики при приеме продуктов, содержащих молочные протеины. У детей, находящихся на исключительно грудном вскармливании, во всех случаях имел место докорм молочной смесью в роддоме, употребление матерью значительного количества молочных продуктов во время кормления грудью.
Использование панели №4 (пищевые аллергены раннего возраста) благодаря возможности определять одновременно три класса антител — IgG, IgG4 и IgЕ позволило получить более полную информацию о характере пищевой сенсибилизации у каждого ребенка (табл. 4).
Благодаря комплексному обследованию с помощью «ЛАКТТЕСТ» сенсибилизация к БКМ была установлена у 86,1% обследованных детей, что превышает частоту выявления существующими методами. IgE опосредованная аллергия к БКМ диагностирована у 22 детей (55,9%), а IgE не опосредованная — у 9 (24,3%).
Сенсибилизация к белку козьего молока по данным «Лакттест» была выявлена у 24 детей (66,7%). При этом сенсибилизация к данному белку отмечалась у детей как получавших (7 детей), так и не получавших (17 детей) продукты на основе козьего молока. Сенсибилизация к козьему молоку всегда сочеталась с сенсибилизацией к БКМ, что указывает на наличие перекрестной аллергической реакции. Аллергия к белку сои выявлена у 3 детей, при этом 2 больных ранее не получали соевых смесей, аллергия к овальбумину — у 3 детей, к глютену пшеницы — у 2 детей.
У всех детей с сенсибилизацией к БКМ была обнаружена повышенная иммунореактивность иммуноглобулинов одного или нескольких классов в отношении всех смесей на основе нативных белков коровьего молока (панель №3), однако выраженность реакции с аллергенами разных смесей у каждого ребенка была неодинакова и варьировалась в пределах от 1 до 3 класса реакции.
Наиболее интересные результаты были получены при анализе данных панели №1 (смеси лечебного назначения) и панели №2 (смеси лечебно-профилактического и профилактического назначения). Данные об индивидуальной переносимости смесей сопоставлялись с характером выявленной сенсибилизации, полученным при использовании панели №4. В первую очередь следует отметить, что индивидуальная переносимость смесей значительно отличалась даже для, казалось бы, аналогичных продуктов. Непереносимость смесей на основе частично гидролизованного молочного белка «НАН ГА 1», «Нутрилон ГА 1», «Нутрилон Комфорт 1», «Хумана ГА 1», «Нутрилак ГА», «ХиПП ГА 1» отмечалась у детей с подтвержденной аллергией к БКМ и имела значительные индивидуальные различия. Выявление непереносимости той или иной смеси не зависело от того, получал ли ее ребенок до начала обследования.
Непереносимость смеси «Нэнни», произведенной на основе козьего молока установлена у 24 больных (обнаружение сенсибилизации к белку козьего молока). Однако у 2 детей с выявленным диагностически значимым уровнем IgЕ антител к козьему молоку переносимость смеси «Нэнни» можно было расценивать как хорошую, что подтверждалось анамнезом — дети получали данную смесь с удовлетворительным результатом.
Выявление диагностического уровня антител к смесям на основе гидролизата белка высокой степени гидролиза, относящихся к группе лечебных смесей, отмечалось довольно редко. Однако в 6 (!) случаях все же была установлена индивидуальная непереносимость смесей из данной группы, что составляет 16,7% (!) всех наблюдений. Это подтверждает несомненный практический интерес использования данной диагностической системы. В одном случае непереносимость смеси была подтверждена клинически в процессе данного исследования и иллюстрируется клиническим примером.
Кроме того, в пределах диагностического уровня значения содержания антител к лечебным смесям также имели значительные индивидуальные различия, и представляется целесообразным учет этих данных для наиболее оптимального подбора продукта.
Алгоритм индивидуального подбора продуктов для диетотерапии детей с пищевой аллергией с учетом результатов «Лакттест» представлен на рис. 2.
Использование данного подхода позволило получить положительный результат от проводимого лечения у всех обследованных детей. За 1,5 мес наблюдения полная клиническая ремиссия была достигнута в 12 случаях, в 20 случаях отмечалась частичная ремиссия, у 4 детей можно было говорить о выраженном клиническом улучшении. Через 3 мес от начала наблюдения полная или частичная ремиссия была достигнута у всех детей. Реакций на назначаемые специализированные продукты-заменители грудного молока не отмечалось.
Проведенное исследование показало, что применение нового диагностикума — набора реагентов «Ифа-Лакттест» при обследовании детей раннего возраста с пищевой аллергией позволяет повысить эффективность аллергологического обследования, диагностировать in vitro индивидуальную переносимость конкретных продуктов детского питания и на основе этого в каждом отдельном случае индивидуально решить вопрос о возможности назначения того или иного продукта на всех этапах диетотерапии; избежать эмпирического подбора продукта из определенной группы, то есть нежелательной для ребенка смены продуктов в случае их индивидуальной непереносимости. Применение данного теста может облегчить назначение лечебного питания, например, при встречающихся в клинической практике случаях упорного отказа ребенка употреблять продукты на основе высокогидролизованного молочного белка вследствие горького вкуса. При резко негативном отношении матери к продуктам данной группы может быть подобран продукт из другой группы с учетом индивидуальной переносимости. Кроме того, тест представляет возможность врачу дать максимально точные рекомендации по подбору гипоаллергенной смеси детям с атопическим дерматитом, находящимся на грудном вскармливании в случае необходимости назначения докорма.
Использование всех вышеизложенных принципов позволяет максимально индивидуализировать побор специализированного продукта для диетотерапии детей первого года с пищевой аллергией.
По вопросам литературы обращайтесь в редакцию.
С. Г. Макарова, кандидат медицинских наук
Т. Э. Боровик, доктор медицинских наук, профессор
С. Н. Шихов, кандидат медицинских наук
Л. В. Шумилина
И. М. Гусева
А. П. Чеканникова
НЦЗД РАМН, Москва,
Медицинский научно-исследовательский центр «Медиан», Электросталь
Лечебные смеси в питании грудных детей
Лечебное питание является мощным терапевтическим фактором, при котором правильно составленная диета становится ключевым механизмом, позволяющим воздействовать на нарушенные звенья метаболизма, нормализовать функции пищеварительной системы, активизировать
Лечебное питание является мощным терапевтическим фактором, при котором правильно составленная диета становится ключевым механизмом, позволяющим воздействовать на нарушенные звенья метаболизма, нормализовать функции пищеварительной системы, активизировать защитные силы организма, что во многом определяет течение и исход болезни. При отдельных видах патологии лечебное питание является единственным средством лечения.
Для организации лечебного питания больного ребенка первого года жизни важен правильный выбор продукта со специальным заданным составом, отвечающим особенностям заболевания и характеру нарушенных при этом обменных процессов.
В настоящее время в нашей стране существует широкий спектр специализированных продуктов лечебного и профилактического предназначения отечественного и зарубежного производства для диетологической коррекции различных заболеваний у грудных детей.
Специализированные смеси для детей с функциональными нарушениями желудочно-кишечного тракта
В последние годы в питании грудных детей со срыгиваниями, рвотами, запорами широко используются антирефлюксные молочные смеси [1, 2]. В зависимости от вида загустителя они подразделяются на две группы: смеси, содержащие камедь из плодов рожкового дерева («Нутрилак АР», «Нутрилон АР», «Фрисовом», «Хумана АР») или крахмал («Сэмпер Лемолак», «Энфамил АР», «Нутрилон Комфорт») (табл. 1).
В белковом компоненте большинства перечисленных антирефлюксных продуктов преобладают сывороточные белки, которые легко перевариваются и относительно быстро выводятся из желудка. Единственной казеинпредоминантной смесью является «Нутрилон АР». Казеин образует в желудке более плотный сгусток, что может препятствовать срыгиваниям и усиливает эффект камеди. Кроме того, в данной смеси умеренно снижено содержание жира (3,1 г/100 мл), что способствует более быстрой эвакуации пищи из желудка.
Камедь рожкового дерева представляет собой растворимые полисахариды, не содержащие крахмал, которые набухают в желудке ребенка, тем самым препятствуют срыгиваниям. Углеводы, входящие в состав камеди, являются пищевыми волокнами — неперевариваемыми полисахаридами, которые не подвергаются расщеплению в верхних отделах гастроинтестинального тракта, а ферментируются микроорганизмами толстой кишки, способствуя селективному росту индигенной микрофлоры.
Максимально допустимое содержание камеди в продукте составляет 1 г в 100 мл. В антирефлюксных смесях содержание камеди колеблется от 0,34 до 0,5 г в 100 мл. Пищевая камедь подразделяется на инстантную (быстрорастворимую) и натуральную (требующую разведения горячей водой для набухания), получаемую из семян среднеземноморской акации и содержащую 85% углеводов, 5% белка, 10% влаги.
В зависимости от вида добавленной в продукт камеди температура воды для разведения антирефлюксных смесей различна и составляет: для продуктов, содержащих инстантную камедь, 40–50°С («Хумана АР», «Нутрилак АР», «Нутрилон АР»); для продуктов с натуральной камедью значительно выше 70–80°С («Фрисовом 1» и «Фрисовом 2»).
Антирефлюксные продукты, содержащие камедь, вводятся в рацион ребенка постепенно, в каждое кормление. Возможно их добавление в бутылочку со стандартной молочной смесью, которую получает ребенок, но более эффективным является самостоятельное применение в начале кормления. Объем лечебного продукта подбирается индивидуально до прекращения срыгиваний.
Вторую группу антирефлюксных продуктов составляют смеси, в качестве загустителя содержащие рисовый, кукурузный или картофельный крахмал, богатые амилопектином («Сэмпер Лемолак», «Энфамил АР», «Нутрилон Комфорт 1» и «Нутрилон Комфорт 2»). Амилопектин представляет собой высокомолекулярное соединение — разветвленный полимер глюкозы, переваривание которого замедленно. Его расщепление происходит преимущественно в тонкой кишке под действием гликоамилазы. Амилопектин не обладает пребиотическими свойствами.
Антирефлюксные молочные смеси в первую очередь используются при регургитации (срыгиваниях) у детей грудного возраста. Срыгивания — обратный заброс пищевого химуса после проглатывания съеденной пищей. Нередко срыгивания обусловлены неадекватно проводимым вскармливанием (быстрое сосание, аэрофагия, перекорм, нарушения режима кормлений, неадекватный выбор смесей), а также перинатальными поражениями центральной нервной системы, пилороспазмом и др. Поэтому назначению антирефлюксных смесей должно предшествовать выявление причин, вызывающих срыгивания [3].
Смеси, содержащие камедь, могут также применяться в питании детей с функциональными запорами: хронической задержкой опорожнения кишечника более чем на 36 ч, увеличением интервалов между актами дефекации по сравнению с физиологической нормой, затруднением акта дефекации, отхождением малого количества кала повышенной плотности. Известно, что камедь обладает свойствами пищевых волокон: удерживает дополнительное количество воды и способствует мягкой стимуляции перистальтики кишечника, что приводит к устранению запоров. Наиболее эффективными из этой группы продуктов являются смеси с преобладанием сывороточной фракции в белковом компоненте, поскольку казеины обладают закрепляющим воздействием. При лечении запоров молочные смеси с камедью могут вводиться не в каждое кормление, а самостоятельно в качестве отдельного кормления — 2–3 раза в сутки [3].
Помимо смесей, в состав которых входит камедь, в питании детей с запорами хорошо себя зарекомендовала смесь «Сэмпер Бифидус», содержащая лактулозу (табл. 2). Лактулоза — дисахарид, состоящий из галактозы и фруктозы, полученный синтетическим путем. Он, подобно пищевым волокнам, не переваривается ферментами гастроинтестинального тракта, доходит в неизмененном виде до толстой кишки, где подвергается ферментации лакто- и бифидобактериями, служит субстратом для их роста. В процессе ферментации происходит образование короткоцепочечных жирных кислот, снижается рН кишечного содержимого и повышается осмотическое давление, в результате чего в просвет кишечника поступает жидкость, усиливается перистальтика и устраняется запор [4].
В настоящее время выпускается «Детское молоко Агуша с лактулозой» (ОАО «Завод детских молочных продуктов», Россия), которое рекомендуется к использованию в питании детей с функциональными нарушениями желудочно-кишечного тракта.
Помимо детских молочных продуктов лактулоза введена в состав детских инстантных каш «Нутрилак. Кукуруза с лактулозой», «Нутрилак. Овсянка с лактулозой» (Нутритек, Россия). Эти продукты эффективны в питании больных детей с нарушениями моторной функции кишечника (запоры, неустойчивый стул).
Образованию более мягкого стула способствуют также пищевые волокна — олигосахариды, которые являются линейными полимерами глюкозы и других моносахаров (галактозы, фруктозы). В женском молоке галактоолигосахариды составляют 12–14% от общего количества углеводов. Они оказывают пребиотический эффект, обеспечивая рост бифидобактерий в кишечнике ребенка. Подобными свойствами обладает пребиотическая добавка, содержащая 90% короткоцепочечных галактоолигосахаридов и 10% длинноцепочечных фруктоолигосахаридов, входящая в состав смесей «Нутрилон Комфорт 1» и «Нутрилон Комфорт 2» [5].
Низколактозные и безлактозные смеси
К низко- и безлактозным детским смесям относят продукты, созданные на основе белков коровьего молока и предназначенные для вскармливания детей первого года жизни с лактазной недостаточностью.
В безлактозных смесях количество лактозы (молочного сахара) практически приближается к нулю. Основным углеводным компонентом таких смесей является декстрин-мальтоза. В низколактозных смесях количество лактозы составляет приблизительно 1 г на 100 мл (от 0,9 до 1,33 г), для сравнения — в женском молоке и стандартных молочных смесях содержится 6–7 г лактозы на 100 мл.
Как правило, в низко- и безлактозных смесях соотношение сывороточных белков к казеину составляет 60:40 или 50:50, а жировой компонент представлен композицией растительных масел, что характерно для адаптированных детских молочных смесей и позволяет рекомендовать их к использованию с первых дней жизни ребенка. К преимущественно «казеиновым» формулам относятся смеси «Хумана-ЛП» с пребиотиками: галактоолигосахаридамии, пищевыми волокнами и «Хумана-ЛП+СЦТ» (соотношение казеина к сывороточной фракции 80:20). Содержание пребиотиков (галактоолигосахариды, клетчатка) в сочетании с низким содержанием жира дают основание к нахначению этих смесей для коррекции диарейного синдрома при лактазной недостаточности (табл. 3) [6].
Гиполактазии или алактазия — заболевания, возникающие в результате недостаточной активности или полного отсутствия фермента пристеночного пищеварения — лактазы, расщепляющей молочный сахар (лактозу), которые проявляются осмотической («бродильной») диареей после приема лактозосодержащих молочных продуктов [7].
Диетотерапия является основным методом лечения лактазной недостаточности. Она направлена на «обход» метаболического блока. Использование низко- и безлактозных смесей в питании детей с лактазной недостаточностью позволяет обеспечить патогенетический подход к лечению данной патологии.
При первичной (конституциональной) лактазной недостаточности низколактозная (безлактозная) диета назначается пожизненно. При вторичной лактазной недостаточности основное внимание уделяется лечению патологии, приведшей к данному состоянию, а ограничение лактозы в рационе является временным, однако необходимым мероприятием.
При искусственном вскармливании следует подбирать смесь с максимальным количеством лактозы, которое переносит пациент, не допуская появления клинической симптоматики и повышения экскреции углеводов с калом. Это связано с тем, что лактоза является единственным источником галактозы, которая образуется при ее расщеплении. Галактоза используется для синтеза галактолипидов, включая цереброзиды, которые необходимы для формирования центральной нервной системы и миелинизации нервных волокон. Кроме того, считается что ежедневное употребление малых количеств лактозы необходимо для адаптации к ней кишечной микрофлоры и поддержания нормального микробиоценоза кишечника. Безлактозные продукты назначаются только при тяжелых формах лактазной недостаточности, когда использование низколактозных смесей неэффективно.
В отдельных случаях безлактозные продукты могут временно вводиться и при грудном вскармливании, когда назначение фермента лактазы неэффективно и необходимо ограничение лактозы. Назначение безлактозных смесей (в отличие от низколактозных продуктов) позволяет сохранить использование материнского молока в максимально возможном объеме.
Диетическая коррекция при лактазной недостаточности заключается в постепенной замене детской молочной смеси низколактозным или безлактозным продуктом, который вводится в каждое кормление. Необходимый объем лечебной смеси определяется клинической симптоматикой: в случае, если удается добиться устранения диареи и колик комбинацией низколактозной или безлактозной смеси со стандартной молочной смесью, последнюю полностью отменять не следует [8].
Кисломолочные смеси и продукты
Кисломолочные продукты занимают важное место в лечебном питании детей первого года жизни, так как они благоприятно влияют на секреторную деятельность пищеварительного тракта, перистальтику кишечника, оказывают ингибирующее действие на патогенные микроорганизмы, стимулируют рост индигенной микрофлоры, способствуют улучшению всасывания кальция, фосфора, магния и железа, оказывают иммуномодулирующее действие и повышают защитные силы организма [2, 6, 9].
Ингибирование роста патогенных микроорганизмов при использовании кисломолочных смесей происходит за счет продукции антимикробных субстанций, конкуренции за питательные вещества, препятствия адгезии патогенной флоры на рецепторы энтероцитов. Иммуномодулирующий эффект данных продуктов заключается в усилении фагоцитоза, активизации пролиферации лимфоцитов, препятствии деградации секреторного иммуноглобулина А, стимуляции выработки интерферона, лизоцима, пропердина, влиянии на цитокиновую систему, регуляции выработки интерлейкинов.
Если кисломолочные продукты содержат живые микроорганизмы (бифидо- и лактобактерии) — представители нормальной микрофлоры кишечника человека, то их называют продуктами-пробиотиками. Они обладают двойным функциональным эффектом, обусловленным присутствием пробиотических штаммов микроорганизмов и продуцируемой ими молочной кислоты.
При разработке продуктов пробиотического действия используются различные виды микроорганизмов, преимущественно бифидобактерии и лактобактерии, к которым, как и к продуктам, созданным на их основе, предъявляются строгие требования, касающиеся безопасности, функциональной эффективности, технологичности [10].
Основные требования к безопасности продукта и входящих в него компонентов сформулированы в документах санитарного законодательства Российской Федерации, а также в международных рекомендациях ФАО/ВОЗ и заключаются в использовании штаммов микроорганизмов, выделенных от человека; отсутствии патогенности, токсичности и побочных реакций, антибиотикоустойчивости, высоких адгезивных свойствах к эпителию слизистой кишечника, стабильности генетического кода [11, 12].
Каждый штамм бифидобактерий имеет свои характеристики и диапазон действия. Так, Bifidobacterium (B.) bifidum и B. infantis превалируют в кишечнике у детей, находящихся на грудном вскармливании, а B. adolescentis — при искусственном вскармливании. В последнее время для получения кисломолочных смесей с пробиотическими свойствами широко используются штаммы B. lactis (Bв 12), обладающие выраженной функциональной активностью и хорошей устойчивостью в желудочно-кишечном тракте ребенка.
Лактобактерии чаще используются в комбинированных заквасках при создании кисломолочных продуктов. Известно, что лактобактерии Lactobacillus (L.) acidofilus, L. rhamnosus (LGG), L. casei обладают хорошей сохранностью в продукте, устойчивостью к внешним воздействиям, высоким пробиотическим эффектом (табл. 4).
Кисломолочные продукты могут быть жидкими и сухими, они также подразделяются на адаптированные и неадаптированные (табл. 5).
Жидкие адаптированные кисломолочные смеси «Агуша 1» и «Агуша 2» (ОАО «Завод детских молочных продуктов», Россия) предназначены для использования в питании детей первого года жизни. Продукт «Бифилин» и ацидофильная смесь «Малютка» относятся к частично адаптированным кисломолочным смесям. Содержание белка в них составляет 1,7 г в 100 мл жидкого продукта, а соотношение альбуминовой и казеиновой фракций — 20:80, как и в коровьем молоке.
К неадаптированным жидким молочным продуктам относятся «Тема. Кисломолочный напиток с Вв12» (ОАО «ЮНИМИЛК», Россия), а также «Наринэ», «Биолакт», «Биокефир», «Бифидокефир», «Бифидок», которые выпускаются на детских молочных кухнях или в цехах детского питания. Их используют в питании детей с 8 мес [13].
На российском потребительском рынке также имеются жидкие кисломолочные продукты-пробиотики «Активиа» и «Актимель» (Данон, Франция), предназначенные для детей старше 3 лет.
Новым в детской диетологии является создание сухих адаптированных кисломолочных смесей (табл. 6).
При использовании кисломолочных продуктов у детей первого года жизни отмечается уменьшение выраженности функциональных нарушений процессов пищеварения, таких как колики, склонность к запорам, диспепсические проявления, сниженный аппетит, а также улучшение состава микрофлоры кишечника. Указанные продукты нашли применение у грудных детей из группы риска по развитию алиментарно-зависимых заболеваний, а также страдающих рахитом, анемией, гипотрофией. При этом отмечены более высокая усвояемость железа и повышение уровня гемоглобина у детей с анемией, улучшение процессов остеогенеза у детей с рахитом и более выраженное увеличение массы тела у детей с гипотрофией, что обусловлено высокой усвояемостью из них белка, кальция и железа [3, 4, 13].
Гипоаллергенные продукты, созданные на основе гидролизатов молочного белка
Появление смесей, созданных на основе гидролизатов молочного протеина, знаменует собой начало новой эры в профилактике и лечении пищевой аллергии, а также ряде тяжелых заболеваний, сопровождающихся синдромом нарушенного кишечного всасывания, снижением нутритивного статуса ребенка [14].
В зависимости от степени расщепления молочного белка, выделяют смеси на основе его полного (высокого) или частичного (умеренного) гидролиза. Гидролизу могут подвергаться как казеиновая, так и сывороточная фракции молочных протеинов.
К казеиновым смесям на основе гидролизатов молочного белка (в зависимости от исходного молочного сырья) относятся «Нутрамиген», «Прегестимил», «Фрисопеп АС». К сывороточным относятся «Дамил Пепти», «Нутрилак ГА», «Нутрилак пептиди СЦТ», «Нутрилон Пепти ТСЦ», «Нутрилон ГА 1» и «Нутрилон ГА 2», «Альфаре», «НАН ГА 1» и «НАН ГА 2», «Фрисопеп», «ХиПП ГА 1» и «ХиПП ГА 2», «Хумана ГА 1» и «Хумана ГА 2».
Установлено, что чем выше молекулярная масса пептидов гидролизата, тем больше риск развития аллергических реакций. По сравнению с белком коровьего молока аллергенность белкового компонента продуктов, созданных на основе высоко гидролизованного белка, снижена в 10 000–100 000 раз, частично гидролизованного — в 300–1000 раз. Молекулярная масса пептидов, при которых аллергенность гидролизата становится минимальной, составляет 1,5 кDа, пептиды с молекулярной массой 3–3,5 кDа в отдельных случаях могут вызывать аллергические реакции.
Все смеси данного класса обогащены комплексом витаминов и минеральных веществ в соответствии с физиологическими потребностями детей первого года жизни и соответствуют требованиям ВОЗ по ингредиентному составу, биологической и пищевой ценности, влиянию на физическое и психомоторное развитие детей первого года жизни [15].
В соответствии с клиническим предназначением смеси на основе гидролизатов молочного белка подразделяются на лечебные, лечебно-профилактические и профилактические (табл. 7).
К лечебным относятся только смеси, полученные в результате глубокого гидролиза молочного белка, которые, как правило, являются полуэлементными, так как помимо модифицированного белкового компонента содержат среднецепочечные жирные кислоты, моносахариды, полимеры глюкозы и полностью лишены лактозы. Указанные продукты предназначены для детей с тяжелыми проявлениями пищевой аллергией, обусловленной гиперчувствительностью к белкам коровьего молока и другим пищевым протеинам, а также больных с синдромом мальдигестии и мальабсорбции на фоне целиакии, панкреатической недостаточности, дистрофии слизистой кишечника, после резекций участков тонкой кишки и пр.
Знание особенностей липидного и углеводного состава различных лечебных смесей, созданных на основе высоко гидролизованного молочного белка, позволяет подобрать оптимальный продукт в зависимости от клинических проявлений в каждом конкретном случае. В состав липидного компонента смесей «Альфаре», «Нутрилак пептиди СЦТ», «Нутрилон Пепти ТСЦ», «Прегестимил» введены среднецепочечные триглицериды (до 50% общего количества липидов), которые легко расщепляются, не требуют эмульгирования желчью и участия панкреатической липазы, всасываются в систему воротной вены, минуя лимфатические сосуды. Указанные продукты показаны пациентам с тяжелыми гастроинтестинальными проявлениями пищевой аллергии и синдромом мальабсорбции.
При использовании лечебных гидролизатов белка удается достичь существенного улучшения со стороны кожных и желудочно-кишечных проявлений через 2–3 нед от начала их применения, а клинической ремиссии — спустя еще 2–3 мес. При этом у детей с дефицитом массы тела происходит нормализация нутритивного статуса. Продолжительность применения указанных продуктов индивидуальна, в среднем она составляет 3–4 и более месяцев.
При выборе специализированного продукта на основе гидролизата белка необходимо также учитывать наличие или отсутствие лактозы в составе его углеводного компонента, так как вторичная лактазная недостаточность часто сопутствует пищевой гиперчувствительности, в таких случаях целесообразно применять лечебные смеси, не содержащие лактозу («Нутрамиген», «Фрисопеп АС»).
Гипоаллергенные смеси с частично (умеренно) гидролизованным молочным белком («НАН ГА 1» и «НАН ГА 2», «Нутрилон ГА 1» и «Нутрилон ГА 2») предназначены только для профилактики аллергических заболеваний у детей из групп высокого риска по развитию атопии, переводимых на смешанное или искусственное вскармливание.
Пептидный профиль и низкая остаточная аллергенность таких смесей, как «Дамил Пепти», «Нутрилак ГА», «ХиПП ГА 1» и «ХиПП ГА 2», «Хумана ГА 1» и «Хумана ГА 2», позволяют использовать их не только в профилактических целях, но и для лечения нетяжелых форм аллергии к белкам коровьего молока, протекающих без участия иммуноглобулин E-опосредуемых механизмов [16].
Все продукты, созданные на основе гидролизатов молочного белка, имеют горьковатый вкус и специфический запах, при их назначении в период адаптации возможен несколько разжиженный и учащенный стул, зеленоватого или коричневого цвета, что не должно служить причиной для отмены продукта.
Смеси на основе изолята соевого белка
Современные соевые смеси разработаны на основе изолята соевого белка, в котором содержание протеинов составляет более 90%, а нежелательные компоненты (неперевариваемые углеводы, ингибитор трипсина, лектины и сапонины) удаляются в процессе технологического производства. При производстве соевых смесей для детского питания не используется генетически модифицированная соя.
Биологическая ценность изолята соевого белка повышена за счет дополнительного введения L-метионина и других аминокислот и сопоставима с молочным казеином. Жировой состав соевых смесей представлен смесью растительных жиров, а углеводы состоят из декстрин-мальтозы, кукурузного крахмала (табл. 8). Таким образом, все соевые смеси являются безмолочными и безлактозными.
Смеси на основе изолята соевого белка обогащены витаминно-минеральным комплексом, а применение современных технологий позволяет повысить усвоение кальция, фосфора и железа.
Смеси на основе изолята соевого белка можно достаточно эффективно использовать при лечении пищевой аллергии, индуцированной белками коровьего молока. Однако клинические наблюдения показывают, что у 20–25% детей первого года жизни они могут быть причиной возникновения или обострения атопического дерматита или гастроинтестинальных проявлений аллергии. Наши исследования свидетельствуют о том, что наиболее часто аллергические реакции развиваются при быстром (в течение 1–2 дней) введении соевых смесей, раннем их назначении (детям первых месяцев жизни), отягощенном аллергоанамнезе [14, 17].
Для предотвращения развития нежелательного эффекта при использовании соевых смесей у детей необходимо соблюдать определенные условия: у ближайших родственников должна отсутствовать аллергия к сое и бобовым, возраст ребенка — не менее 5–6 мес (особенно при кожно-гастроинтестинальной или гастроинтестинальной формах пищевой аллергии), постепенное (в течение 5–7 дней) введение продукта в рацион ребенка. Следует также учитывать индивидуальную переносимость смеси, применять ее нужно не менее 3 мес [16].
Кроме того, эти соевые смеси могут использоваться для лечебного питания у детей с галактоземией (при данной патологии они являются первыми продуктами выбора), лактазной недостаточностью, целиакией в качестве альтернативы молочным продуктам и смесям. Признавая в целом нутритивную адекватность промышленных соевых смесей, не следует рекомендовать их недоношенным детям.
Таким образом, использование в педиатрической практике детских специализированных смесей, полученных с применением самых современных технологий, позволяет в максимально короткие сроки организовать патогенетически обоснованное лечебное питание, обеспечить потребности больного ребенка в макро- и микронутриентах, облегчить течение патологического процесса, улучшить нутритивный статус и ускорить достижение клинической ремиссии заболевания или выздоровление.
Литература
Т. Э. Боровик, доктор медицинских наук, профессор
В. А. Скворцова, доктор медицинских наук
К. С. Ладодо, доктор медицинских наук, профессор
Е. А. Рославцева, кандидат медицинских наук
Н. Н. Семенова, кандидат медицинских наук
Т. Н. Степанова, кандидат медицинских наук
НЦЗД РАМН, Москва