Памятка для пациентов с непереносимостью нестероидных противовоспалительных средств
Противопоказан прием лекарственных средств следующих групп:
а) производные пиразолона (анальгин, антипирин, пропифеназон), а также содержащие в своем составе производных пиразолона (андипал, анапирин, темпалгин, баралгин, максиган, спазмалгон, триган, саридон и др.).
б) парацетомол (ацетоминафен, калпол, тайленол, эффералгин, панадол и др.) и комбинированные средства, содержащие парацетомол (колдрекс, солпадеин, панадеин, панадол-экстра, саридон, цитрамон седалгин Н, томапирин и др.);
в) кетеролак (долак, кетанов, кеторал, торадол и др.).
Нестероидные противовоспалительные средства:
а) салицилаты —ацеитисалициловая кислота (аспирин, аспирин Кардио, тромбо АСС, анопирин, джасприн и др.);
б) средства, содержащие в своем составе аспирин (цитрамон П, асфен, аскофен, кофецил, седалгин Н, аспро С форте, алко-зельтцер, алко-прим, томапирин и др.);
в) бутадион (фенилбутазон, буталан, бутазолидин и др.);
г) другие нестероидные противовоспалительные препараты: индометацин (метиндол, индоцид и др.); ибупрофен (бруфен, солпафлекс и др.); ортофен (дифлофенак, вольтарен и др.); пироксикам (роксикам, пирокс, пирокам и др.); напроксен (апрол, наксен, проксен и др.); сулиндак (юлинорил и др.); кетопрофен (кетанал, остофен, кетопласт и др.); менафамовая кислота (понстел и др.); нимфулоновая кислота (нимфлюран и др.);
Не назначаются отвары и настои растений (ива белая, первоцвет, мята, лабазник, тысячелистник, плоды мелиссы, смородины), содержащие природные салицилаты.
Возможно применение с целью обезболивания трамала.
Показано исключить из пищи все продукты, содержащие природные и синтетические салицилаты (элиминационная диета):
а) фрукты: яблоки, абрикосы, грейфруты, виноград, лимоны, дыни, апельсины, сливы, персики, нектарин;
б) ягоды: красная и черная смородина, вишня, ежевика, крыжовник, малина, земляника, клубника, клюква;
в) овощи: огурцы, перец, помидоры, картофель;
г) смешанная труппа; МИНдШIЬНЫЙ орех, изюм, вино и винный уксус, сидр и яблочный уксус, мятные конфты, напитки из корнеплодов, газированные напитки.
Исключаются продукты, окрашенные тертразином или содержащие консерванты, применяемые в пищевой промышленности и подобные по действию аспирину: желе, икра, маргарин, сливочное масло, мороженное, пудинги, сыры, окрашенные мучные изделия; все консервы, в том числе фруктовые, все гастрономические изделия (колбасы, ветчина, буженина), торты и пирожные с кремами желтого цвета, фруктовые воды, конфеты-карамель, мармелад и драже.
Прием и консультация врача-аллерголога проводится на платной основе по предварительной записи по телефону +375 17 377-09-37 (г. Минск, ул. Уральская,5).
Задавайте вопросы врачу-специалиегу по e-mail: Этот адрес электронной почты защищён от спам-ботов. У вас должен быть включен JavaScript для просмотра.
Существуют ли различия между нестероидными противовоспалительными препаратами? В центре внимания нимесулид
В данной работе представлены различия нестероидных противовоспалительных препаратов, применяемых для лечения заболеваний, сопровождающихся острой болью.
This paper describes different non-steroid anti-inflammatory preparations used for treatment of diseases accompanied with acute pain.
Распространенность заболеваний, сопровождающихся острой болью и требующих применения обезболивающих препаратов, в современном мире постоянно растет. К ним относятся, в частности, ревматические болезни, воспалительные и дегенеративные заболевания опорно-двигательного аппарата, головная боль. Примерно 40% визитов к врачу общей практики обусловлены слабой и умеренной острой болью, а более 70% посещений отделений неотложной помощи происходит из-за наличия у пациента интенсивной острой боли [1]. В структуре общей заболеваемости населения Российской Федерации болезни костно-мышечной системы и соединительной ткани (БКМС) занимают 3-е место после болезней системы кровообращения и органов дыхания [2]. Агентство National Health Interview Survey демонстрирует следующие данные: в 2011 г. 28,4% взрослых американцев сообщали о боли в нижней части спины (БНС) в течение предыдущих опросу 3 месяцев [3].
Эффективность нестероидных противовоспалительных препаратов (НПВП) при острой боли не подвергается сомнению. НПВП обладают противовоспалительной, обезболивающей и жаропонижающей активностью. Входящие в состав НПВП вещества относятся к различным химическим классам, поэтому обладают разными фармакокинетическими и фармакодинамическими свойствами.
Обзор клинической эффективности НПВП показывает, что различные препараты данной группы обладают примерно схожей терапевтической активностью. В данной работе будут представлены различия НПВП и особое внимание будет уделено представителю НПВП нимесулиду.
Фармакологические свойства НПВП
Ингибирование синтеза простагландинов
В начале 70-х годов Vane высказал предположение, что в основе противовоспалительного действия Аспирина и аналогичных ему препаратов лежит способность ингибировать биосинтез простагладинов, путем ингибирования ответственного за их синтез фермента циклооксигеназы (ЦОГ). Лишь 20 лет спустя эта гипотеза получила свое подтверждение, и стало известно, что за синтез простагландинов отвечают две изоформы ЦОГ (ЦОГ-1 и ЦОГ-2), а НПВП можно разделять с учетом селективности в отношении разных изоформ ЦОГ.
ЦОГ-1 отвечает в основном за синтез простагландинов, участвующих в процессах гомеостаза в жизненно важных органах. Именно с ингибированием ЦОГ-1 связывают хорошо известные желудочно-кишечные побочные эффекты традиционных неселективных НПВП.
Ингибирование ЦОГ-2 обеспечивает противовоспалительный эффект НПВП, так как она участвует в синтезе воспалительных простагландинов.
Неселективные НПВП ингибируют обратимо или необратимо как ЦОГ-1, так и ЦОГ-2. Большинство токсических эффектов этих препаратов связано с их способностью блокировать синтез физиологических простагландинов, необходимых для обеспечения гомеостаза в почках, желудке и тромбоцитах за счет ингибирования ЦОГ-1.
Появление на рынке в конце 90-х годов селективных ингибиторов ЦОГ-2 (коксибов) давало клиницистам надежду на то, что эта группа НПВП обеспечит высокую фармакологическую эффективность при более низком уровне желудочно-кишечных осложнений. Однако ожидания были оправданы не в полной мере, в частности, получены доказательства того, что применение коксибов сопровождается увеличением частоты тромбоэмболических осложнений, что привело к выводу с рынка во всем мире таких препаратов, как рпсиофекоксиб и валдекоксиб. Кроме того, применение валдекоксиба связывают с частым развитием нежелательных кожных реакций. Кардиотоксичность коксибов объясняют блокированием синтеза простациклинов, опосредованного ЦОГ-2, что нивелирует их защитные эффекты в отношении тромбогенеза, гипертензии и атерогенеза in vivo.
НПВП классифицируют по степени селективности в отношении изоформ ЦОГ (рис. 1). Селективность в отношении ЦОГ определяется химической структурой НПВП. Аминокислотная структура ЦОГ-1 и ЦОГ-2 является достаточно стабильной, однако рентгеновские кристаллографические исследования ЦОГ показали, что активная область связывания с НПВП у ЦОГ-2 позволяет связываться с большим количеством субстратов, чем центр связывания у ЦОГ-1. Этот активный канал является гидрофобным, у ЦОГ-2 возможно открытие бокового гидрофильного кармана, который у ЦОГ-1 закрыт изолейцином.
Так, флурбипрофен, который относят к неселективным НПВП, взаимодействует с ЦОГ-1 посредством связывания фенильной группы с гидрофобным каналом и карбоксильной группы с аргинином в 120-м положении. Взаимодействие флурбипрофена с ЦОГ-2 сходно с вышеописанным, однако, связываясь с аргинином в 120-м положении, карбоксильная группа блокирует активный центр ЦОГ-2, не позволяя ему взаимодействовать с субстратом. Напротив, селективные ингибиторы ЦОГ-2 не могут войти в активный канал ЦОГ-1 и не имеют карбоксильной группы для связывания с аргинином в 120-м положении.
Нимесулид — единственный представитель класса сульфонанилидов, преимущественно ингибирующим ЦОГ-2. Активность нимесулида в отношении ЦОГ-2 в 5–50 раз превосходит активность в отношении ЦОГ-1. В исследованиях in vivo использование нимесулида в терапевтической дозе (100 мг 2 раза в сутки) продемонстрировало значительное снижение концентрации простагландина E2 в плазме крови. Нимесулид не оказывает влияния на агрегацию тромбоцитов, что было доказано при оценке индуцированной активности ЦОГ-1, и не влияет на образование в желудке простагландина E2 и простагландина I2, а также ЦОГ-1 зависимых эффектов.
Фармакокинетический профиль
На основании периода полувыведения НПВП могут быть разделены на две большие группы: с коротким периодом полувыведения (менее 6 часов) и с длительным периодом полувыведения (более 10 часов). Группа НПВП с коротким периодом полувыведения включает Аспирин, диклофенак, ибупрофен, флурбипрофен, индометацин, лумиракоксиб* и нимесулид. Группа препаратов с длительным периодом полувыведения включает целекоксиб, напроксен, сулиндак, рофекоксиб, оксапрозин*, пироксикам. Достижение равновесной концентрации препарата в плазме крови происходит после его применения в течение периода, превосходящего период полувыведения в 3–5 раз, поэтому достижение пиковой концентрации в плазме крови и максимального клинического эффекта НПВП с коротким периодом полувыведения происходит быстрее, чем препаратов с длительным периодом полувыведения.
Нимесулид: фармакологический профиль
Нимесулид оказывает быстрое обезболивающее действие, что подтверждают следующие исследования. Применение нимесулида у пациентов с острым артритом характеризуется быстрым началом действия и ранним ингибированием образования простагландина E2 (маркера активности ЦОГ-2). В клинических исследованиях у пациентов с остеоартритом коленных суставов были получены доказательства быстрого начала действия нимесулида. У данной категории больных нимесулид вызывал достоверно более значимое облегчение боли, связанной с ходьбой, и эффект наступал быстрее, чем при применении целекоксиба и рофекоксиба. Начало обезболивающего действия нимесулида фиксировалось уже через 15 минут после приема. Согласно недавним исследованиям, эффективные концентрации нимесулида в плазме крови и синовиальной жидкости обнаруживаются уже через 30 минут после его приема.
НПВП могут обладать противовоспалительными свойствами, которые не зависят от ЦОГ. Было показано, что нимесулид, помимо периферического ингибирующего воздействия на ЦОГ, может ингибировать высвобождение фактора некроза опухолей (ФНО), гистамина, образования активных форм кислорода (АФК), высвобождения матриксных металлопротеаз (ММП) и гибели хондроцитов (рис. 2).
 Влияние нимесулида на медиаторы воспаления
Влияние нимесулида на медиаторы воспаления
ФНО-α играет ведущую роль в воспалительном процессе, что делает его идеальной целью при терапии ревматоидного артрита. В исследованиях на крысах, которым вводили липополисахариды для увеличения уровня ФНО-α, нимесулид эффективно ингибировал его высвобождение.
Выработка фагоцитами супероксида и высвобождение лактоферрина из нейтрофилов были исследованы у восьми добровольцев до и после приема нимесулида внутрь. В качестве активирующих стимулов были использованы фактор хемотаксиса N-формил-метионил-лейцил-фенилаланин и частицы опсонизированного зимозана. Нимесулид значимо ингибировал образование АФК N-формил-метионил-лейцил-фенилаланином и активированными за счет воздействия опсонизированных частиц зимозана фагоцитами (ингибирование до 67,6% и 36,8% соответственно) (рис. 3). Он не оказывал влияния на высвобождение лактоферрина нейтрофилами, что позволило авторам предположить, что нимесулид не оказывает влияния на механизмы, происходящие при экзоцитозе специфичных гранул.
В ходе воспалительной реакции для предупреждения повреждения тканей требуется поддержание баланса между протеиназами (преимущественно эластазами, выделяемыми мигрировавшими в очаг нейтрофилами) и антипротеазами (в основном эластаз-специфическим альфа-1-ингибитором протеиназ; A1PI). Нейтрофильные клетки способны инактивировать A1PI с помощью серии окислительных реакций с участием хлорноватистой кислоты, что позволяет эластазе свободно разрушать соединительную ткань. Возможным способом регулирования активности нейтрофильной эластазы является фармакологическая защита A1PI от окислительной инактивации под действием хлорноватистой кислоты нейтрофилов. В доклинических исследованиях было показано, что нимесулид предотвращал инактивацию A1PI под действием выделяемой нейтрофилами хлорноватистой кислоты, что позволяет осуществлять опосредованный A1PI контроль гистотоксической функции эластазы. Полученные данные позволяют предполагать, что защитное влияние нимесулида на A1PI может иметь значение в реализации его противовоспалительного действия.
В другом исследовании морским свинкам предварительно вводили нимесулид или индометацин, после чего ацетальдегидом провоцировали выброс гистамина и бронхоспазм (рис. 4). В контрольной группе, получавшей только ацетальдегид, концентрация гистамина в крови была равна 195 ± 12 мг/л, в группе, получавшей нимесулид, при использовании дозы 0,1 мг/кг она была равна 154 ± 10 мг/л (p
О. В. Котова, кандидат медицинских наук
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
Нимесулид (Nimesulid) инструкция по применению
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Нимесулид
Фармакологическое действие
Фармакокинетика
Показания препарата Нимесулид
Препарат предназначен для симптоматической терапии, уменьшая боль и воспаление на момент использования, на прогрессирование заболевания не влияет.
Открыть список кодов МКБ-10
| Код МКБ-10 | Показание |
| K08.8 | Другие уточненные изменения зубов и их опорного аппарата (в т.ч. зубная боль) |
| M05 | Серопозитивный ревматоидный артрит |
| M13 | Другие артриты |
| M15 | Полиартроз |
| M25.5 | Боль в суставе |
| M65 | Синовиты и теносиновиты |
| M70 | Болезни мягких тканей, связанные с нагрузкой, перегрузкой и давлением |
| M71 | Другие бурсопатии |
| M79.1 | Миалгия |
| N94.4 | Первичная дисменорея |
| N94.5 | Вторичная дисменорея |
| R51 | Головная боль |
| R52.0 | Острая боль |
| R52.2 | Другая постоянная боль (хроническая) |
| T14.3 | Вывих, растяжение и перенапряжение капсульно-связочного аппарата сустава неуточненной области тела |
Режим дозирования
Пациентам с хронической почечной недостаточностью требуется снижение суточной дозы до 100 мг.
Минимально эффективная доза должна назначаться на протяжении как можно более короткого периода времени с тем, чтобы минимизировать риск развития побочных реакций. Максимальная продолжительность приема препарата не должна превышать 15 дней.
Побочное действие
Аллергические реакции: реакции гиперчувствительности, анафилактоидные реакции.
Со стороны ЦНС: головокружение, ощущение страха, нервозность, кошмарные сновидения, головная боль, сонливость, энцефалопатия (синдром Рейе).
Со стороны кожных покровов: зуд, кожная сыпь, усиление потоотделения, эритема, дерматит, крапивница, ангионевротический отек, отечность лица, многоформная экссудативная эритема, в т.ч. синдром Стивенса-Джонсона, токсический эпидермальный некролиз (синдром Лайелла).
Со стороны мочевыделительной системы: отеки, дизурия, гематурия, задержка мочи, гиперкалиемия, почечная недостаточность, олигурия, интерстициальный нефрит.
Со стороны пищеварительной системы: диарея, тошнота, рвота, запор, метеоризм, гастрит, боли в животе, стоматит, дегтеобразный стул, желудочно-кишечное кровотечение, язва и/или перфорация желудка или двенадцатиперстной кишки.
Со стороны печени и желчевыводящей системы: повышение печеночных трансаминаз, гепатит, молниеносный гепатит, желтуха, холестаз.
Со стороны системы кроветворения: анемия, эозинофилия, тромбоцитопения, панцитопения, пурпура, удлинение времени кровотечения.
Со стороны дыхательной системы: одышка, обострение бронхиальной астмы, бронхоспазм.
Со стороны органов чувств: нечеткость зрения.
Со стороны сердечно-сосудистой системы: артериальная гипертензия, тахикардия, геморрагии, приливы.
Прочие: общая слабость, гипотермия.
Противопоказания к применению
С осторожностью: ИБС, цереброваскулярные заболевания, ХСН, дислипидемия/гиперлилидемия, сахарный диабет, заболевания периферических артерий, курение, почечная недостаточность (КК менее 30-60 мл/мин), анамнестические данные о развитии язвенного поражения ЖКТ, наличие инфекции Helicobacter pylori, пожилой возраст, длительное использование НПВП, тяжелые соматические заболевания, одновременный прием антикоагулянтов (в т.ч. варфарин), антиагрегантов (в т.ч. АСК, клопидогрел), пероральных ГКС, селективных ингибиторов обратного захвата серотонина (в т.ч. циталопрам, флуоксетин, пароксетин, сертралин).
Применение при беременности и кормлении грудью
Применение при нарушениях функции печени
Противопоказан при печеночной недостаточности или любом активном заболевании печени.
При появлении у больных, принимающих Нимесулид, симптомов, указывающих на повреждение печени (например, анорексия, тошнота, рвота, боль в животе, повышенная утомляемость, темная моча), или повышения уровня печеночных трансаминаз, препарат следует отменить. Таким больным не рекомендуется назначать Нимесулид и в дальнейшем.
Применение при нарушениях функции почек
Противопоказан при выраженной хронической почечноой недостаточности (ХПН) (КК менее 30 мл/мин); при прогрессирующих заболеваниях почек.
С осторожностью: почечная недостаточность (КК менее 30-60 мл/мин).
Пациентам с хронической почечной недостаточностью требуется снижение суточной дозы до 100 мг.
В случае ухудшения функции почек препарат следует отменить.
Применение у детей
Применение у пожилых пациентов
Применять с осторожностью у пациентов пожилого возраста.
У больных пожилого возраста наиболее часто развиваются побочные эффекты при приеме препарата, в том числе желудочно-кишечные кровотечения, перфорации, нарушение функции сердца, почек и печени. Поэтому рекомендуется регулярный клинический контроль состояния больного.
Особые указания
Для снижения риска развития побочных эффектов необходимо применять препарат в минимальной эффективной дозе с наименьшей продолжительностью. Если состояние больного не улучшается, лечение необходимо прекратить.
Необходимо прекратить прием препарата в случае повышения температуры или развития на фоне его приема гриппоподобных симптомов.
При появлении у больных, принимающих Нимесулид, симптомов, указывающих на повреждение печени (например, анорексия, тошнота, рвота, боль в животе, повышенная утомляемость, темная моча), или повышения уровня печеночных трансаминаз, препарат следует отменить. Таким больным не рекомендуется назначать Нимесулид и в дальнейшем.
Желудочно-кишечное кровотечение или язва/перфорация желудка или двенадцатиперстной кишки могут развиться в любой момент при применении препарата, которые могут не сопровождаться клинически выраженными симптомами (в т.ч. болевой синдром). При возникновении желудочно-кишечного кровотечения или язвы препарат следует отменить.
В случае ухудшения функции почек препарат следует отменить.
В случае использования препарата более 2-х недель необходим контроль показателей функции печени.
У больных циррозом печени или с почечной недостаточностью с гипоальбуминемией или гипербилирубинемией связывание нимесулида снижается.
У больных пожилого возраста наиболее часто развиваются побочные эффекты при приеме препарата, в том числе желудочно-кишечные кровотечения, перфорации, нарушение функции сердца, почек и печени. Поэтому рекомендуется регулярный клинический контроль состояния больного.
Применение нимесулида может отрицательно влиять на женскую фертильность и не рекомендуется женщинам, планирующим беременность.
Влияние на способность к управлению транспортными средствами и механизмами
В случае, если при использовании препарата возникают нежелательные явления со стороны ЦНС и органов чувств необходимо воздержаться от вождения автотранспортом и занятий видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Передозировка
Симптомы: тошнота, рвота, сонливость, апатия, желудочно-кишечное кровотечение, повышение АД, острая почечная недостаточность, угнетение дыхания;
Лекарственное взаимодействие
Имеются данные о том, что нимесулид может снижать биодоступность фуросемида, выступать конкурентом по связыванию белков плазмы с фенофибратом, салициловой кислотой, толбутамидом.
Нимелид может замещать салициловую кислоту и фуросемид (но не варфарин) в плазменных белках.
Он не оказывает никакого влияния на препараты, воздействующие на концентрацию глюкозы крови и толерантность к глюкозе у больных сахарным диабетом, леченных различными препаратами, содержащими производные сульфонилмочевины.
Не рекомендуется прием нимесулида одновременно с мочегонными, оказывающими повреждающий эффект на почечную гемодинамику.
Физиологические концентрации ненасыщенных жирных кислот не влияют на связывание нимесулида с сывороточным альбумином.
В терапевтических концентрациях на связывание нимесулида не влияли варфарин, фуросемид, глибенкламид, дигитоксин.
В присутствии нимесулида могут значительно возрасти свободные фракции метотрексата.
Прием нимесулида в терапевтических дозах внутрь в течение короткого периода не изменяет сывороточный профиль дигоксина у больных со слабо выраженной сердечной недостаточностью.
Концентрация лития в плазме повышается при одновременном приеме препаратов лития и нимесулида. Нимесулид может усиливать действие циклоспорина на почки.
Использование с ГКС, ингибиторами обратного захвата серотонина увеличивает риск развития желудочно-кишечных кровотечений.
Условия хранения препарата Нимесулид
Препарат хранить в сухом, защищенном от света месте, при температуре не выше 25°С. Хранить в недоступном для детей месте.
Разумный выбор НПВП при сочетанной патологии: заболеваниях суставов и гипертонической болезни
Нестероидные противовоспалительные препараты (НПВП) являются одной из основных групп лекарственных средств, применяемых при лечении ревматоидного артрита (РА). Противовоспалительный и анальгетический эффект данной группы препаратов связан с подавлением а
Нестероидные противовоспалительные препараты (НПВП) являются одной из основных групп лекарственных средств, применяемых при лечении ревматоидного артрита (РА). Противовоспалительный и анальгетический эффект данной группы препаратов связан с подавлением активности циклооксигеназы-2 (ЦОГ-2) в очаге воспаления — ключевого фермента синтеза простагландинов провоспалительной активности, а подавление изоформы ЦОГ-1 приводит к нарушению физиологических реакций: в частности, к нарушению синтеза простагландинов класса Е в слизистой оболочке желудка и развитию НПВП-гастропатии.
Большинство «стандартных» НПВП способно подавлять активность обеих изоформ ЦОГ, поэтому их применение часто ограничено из-за развития побочных эффектов, в первую очередь — со стороны желудочно-кишечного тракта (ЖКТ). Субъективные симптомы со стороны ЖКТ встречаются примерно у трети больных, а в 5% случаев представляют серьезную угрозу жизни пациентов. Именно поэтому в последние годы особо пристальное внимание привлекает проблема безопасного применения НПВП. Полагают, что препараты более селективные в отношении ЦОГ-2 реже вызывают развитие НПВП-гастропатии. Изучение механизмов действия НПВП послужило толчком к созданию новых препаратов, обладающих всеми положительными свойствами стандартных НПВП, но менее токсичных, — это специфические ингибиторы ЦОГ-2 [3, 4, 13].
В последние годы особую актуальность приобрела проблема взаимодействия НПВП и гипотензивных препаратов, а также связи между применением НПВП и развитием гипертонической болезни (ГБ). Неселективные НПВП могут привести к повышению АД (преимущественно диастолического) не только у больных артериальной гипертензией (АГ), но и у лиц с нормальным АД за счет ингибиции системного и локального, внутрипочечного синтеза простагландинов. Известно, что постоянный прием НПВП вызывает у пациентов увеличение АД в среднем на 5,0 мм рт. ст. Характерным свойством НПВП является также взаимодействие с гипотензивными препаратами, в основе гипотензивного действия которых лежат преимущественно простагландин-зависимые механизмы. Назначение НПВП пациентам, получающим по поводу АГ β-адреноблокаторы, ингибиторы АПФ и диуретики, приводит к снижению гипотензивного эффекта [8, 9].
Нимесулид был разработан еще в 1985 г. и является одним из первых НПВП, при изучении которого продемонстрирована более высокая селективность в отношении ЦОГ-2 и накоплен большой клинический опыт. В многочисленных исследованиях in vitro и in vivo было показано, что нимесулид примерно в 5–20 раз более селективно ингибирует ЦОГ-2, чем ЦОГ-1. Большой интерес представляет и тот факт, что нимесулид обладает широким спектром ЦОГ-независимых эффектов, которые могут определять его противовоспалительную, анальгетическую и хондропротективную активность [1, 2, 5, 7, 11, 12].
Нимесулид хорошо переносится больными и редко вызывает развитие серьезных побочных эффектов, требующих отмены препарата. По результатам ряда исследований, частота побочных эффектов, развивающихся на фоне приема нимесулида, достоверно не отличается от плацебо или ниже, чем при приеме других НПВП. Например, по данным мета-анализа, у больных, получавших нимесулид, общая частота побочных реакций со стороны ЖКТ была значительно ниже (8,7%), чем при назначении других НПВП (16,8%). Низкую частоту поражения ЖКТ на фоне лечения нимесулидом связывают не только с ЦОГ-2-селективностью препарата, но и с антигистаминным действием, приводящим к снижению секреции соляной кислоты в желудке [6, 10, 13].
Таким образом, нимесулид относится к селективным ингибиторам ЦОГ-2, сравним по эффективности с «классическими» НПВП, но отличается более благоприятным профилем токсичности. Фармакоэкономический анализ свидетельствует о преимуществах нимесулида по сравнению с диклофенаком, в первую очередь в связи с более низкой частотой поражения ЖКТ.
Целью нашего исследования явилось изучение эффективности и переносимости найза (нимесулида) у больных РА в сравнении с ортофеном (диклофенаком).
Материалы и методы
Оба НПВП назначались случайным способом 40 больным с момента первого установления диагноза РА, согласно критериям Американской коллегии ревматологов. Найз применялся в виде таблеток по 100 мг дважды в день, ортофен — в виде таблеток по 25 мг в суточной дозе 150 мг. Одновременно всем больным проводилась базисная терапия, преимущественно метотрексатом или сульфасалазином. Эффективность и переносимость НПВП оценивались через 3 нед. от начала лечения, т. е. в те сроки, когда эффект базисных препаратов еще не имел клинической значимости.
В I группе из 20 пациентов, получавших найз, было 14 женщин и 6 мужчин, средний возраст пациентов составил 55,1 года, длительность суставного синдрома к моменту установления диагноза — от 3 до 14 мес., в среднем — 7,25 мес. Во II группе из 20 больных, получавших ортофен, было 18 женщин и 2 мужчин, средний возраст больных — 42,75 года, длительность суставного синдрома — от 2 до 14 мес., в среднем — 5,65 мес. Клиническая характеристика обеих групп представлена в таблице 1.
Результаты лечения оценивались по динамике показателей суставного синдрома (суставной индекс Ричи (СИ), счет болезненных суставов (СБС), счет припухших суставов (СПС), продолжительность утренней скованности (мин), выраженность боли по визуально-аналоговой шкале (ВАШ)) и на основании общей оценки эффективности лечения, по мнению врача и больного. Кроме того, у всех больных оценивалась динамика АД на фоне лечения НПВП.
Результаты
В I группе на фоне лечения найзом в суточной дозе 200 мг за 3 нед. лечения достигнута достоверная динамика показателей суставного синдрома. При этом эффективность терапии оценена 17 пациентами (85%) как хорошая и 3 (15%) — как удовлетворительная. По мнению врача, в 16 случаях (80%) наблюдалась хорошая эффективность препарата, в 4 случаях (20%) — удовлетворительная (рис. 1). Переносимость найза у 85% была хорошей, только у 2 больных (10%) отмечались изжога и гастралгии, у 1 больного (5%) — чувство тяжести в эпигастральной области. Однако при фиброгастроскопии у этих пациентов не выявлено эрозивного повреждения слизистой оболочки желудка. В группе больных, принимавших найз, не потребовалось отмены препарата ни у одного больного.
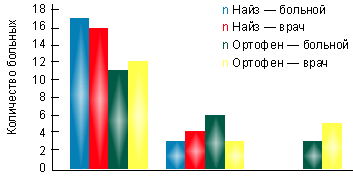 |
| Рисунок. Оценка эффективности препаратов на основании мнения больного и врача |
Во II группе на фоне терапии ортофеном в суточной дозе 150 мг через 3 нед. также отмечена существенная динамика показателей суставного синдрома. Однако оценка эффективности терапии показала, что только 11 пациентов (55%) оценили эффективность препарата как хорошую, 6 (30%) — как удовлетворительную и трое больных (15%) признали ее неудовлетворительной. По мнению лечащего врача, достаточная эффективность ортофена, соответствующая градации «хорошая», отмечалась в 12 случаях (60%), удовлетворительная — в 3 (15%) и неудовлетворительная — в 5 (25%) случаях (рис.).
Переносимость препарата ортофен была хуже, чем у найза: у 9 пациентов (45%) отмечались симптоматические побочные эффекты, причем у 3 больных (15%) потребовалась отмена препарата через 2 нед. от начала лечения в связи с выявленным при ФГДС эрозивным поражением слизистой оболочки антрального отдела желудка. В целом из побочных эффектов чаще отмечались изжога — у 7 (35%) пациентов, гастралгии — у 8 (40%), тошнота — у 4 (20%) и диарея — у 2 (10%) больных.
Особый интерес представляет влияние исследуемых НПВП на уровень АД, так как из 40 больных у 15 имелась сопутствующая ГБ, по поводу которой проводилась гипотензивная терапия. Динамика уровня АД в обеих группах на фоне лечения найзом и ортофеном представлена в таблице 2. Следует отметить, что терапия найзом не требовала усиления проводимой гипотензивной терапии (β-блокаторами, ингибиторами АПФ, диуретиками) и не вызывала повышения АД у ранее нормотензивных пациентов. В то же время лечение ортофеном потребовало коррекции доз гипотензивных препаратов у 4 (66,7%) из 6 больных ГБ и вызвало повышение АД у 5 (25%) женщин в постменопаузе с исходно высоконормальным АД. Данный эффект неселективного НПВП — ортофена — следует считать предсказуемым, особенно с учетом характера проводимой гипотензивной терапии. Все больные ГБ получали в разных комбинациях β-адреноблокаторы, ингибиторы АПФ и диуретики; при этом ни одному пациенту не был назначен дигидропиридиновый антагонист Са — амлодипин, который является препаратом выбора для лечения АГ в условиях терапии НПВП.
Таким образом, результаты открытого клинического исследования показали, что препарат найз у больных РА проявляет выраженную противовоспалительную активность, превосходящую диклофенак. При этом найз характеризуется хорошей переносимостью, малым числом симптоматических побочных эффектов и превосходит с этой точки зрения наиболее широко применяемый в клинической практике ортофен. Дополнительным преимуществом препарата найз можно считать менее выраженное влияние на уровень АД. При назначении найза не требовалось увеличения дозы гипотензивных препаратов. С учетом высокой распространенности эссенциальной гипертензии в популяции, взаимодействие НПВП с наиболее часто используемыми гипотензивными средствами представляется актуальной проблемой. Ревматические заболевания, требующие постоянной терапии НПВП, часто сочетаются с АГ. При этом у большинства больных ГБ коррекция АД может достигаться только благодаря комбинированной антигипертензивной терапии, а монотерапия дигидропиридиновыми антагонистами Са признается недостаточно эффективной. Следовательно, в большинстве случаев при лечении воспалительных ревматических заболеваний у лиц, страдающих ГБ, невозможно полностью нивелировать отрицательное взаимодействие «стандартных» НПВП с основными кардиологическими препаратами — β-адреноблокаторами, ингибиторами АПФ и диуретиками. В такой ситуации представляется рациональным выбор для проведения противовоспалительной терапии специфических ингибиторов ЦОГ-2, представителем которых является найз.
Литература
И. М. Марусенко, кандидат медицинских наук
Н. Н. Везикова, кандидат медицинских наук, доцент
В. К. Игнатьев, доктор медицинских наук, профессор
Петрозаводский университет, кафедра госпитальной терапии
.gif)
.gif)
.gif) Влияние нимесулида на медиаторы воспаления
Влияние нимесулида на медиаторы воспаления