Аллергия на кордарон чем заменить
Качественная Клиническая Практика
Рекомендации по безопасному применению Кордарона (амиодарона гидрохлорида)
Кордарон (амиодарон) был синтезирован в 1960 году в Бельгии. Первоначально он предназначался в качестве коронарного вазодилататора для лечения стенокардии. При клинических исследованиях было установленно, что Кордарон обладает достаточно высокой антиангинальной эффективностью. Вместе с тем оказалось, что переносимость препарата при его длительном применении оказалась хуже, чем у b–адреноблокаторов и антагонистов кальция, поэтому Кордарон не получил широкого применения в качестве антиангинального препарата.
Спустя некоторое время R. Charlier и соавт. в опытах на животных выявили антиаритмическое действие Кордарона. В 70–е годы в многочисленных экспериментальных и клинических исследованиях были изучены механизмы антиаритмического (и антифибрилляторного) действия Кордарона, а также доказана его эффективность при различных формах нарушений ритма сердца. В результате Кордарон стал широко использоваться в разных странах для профилактики и лечения различных видов аритмий.
Во многом широкому использованию Кордарон способствовали его свойства, выделяющие его среди всех антиаритмических средств(в частности, хинидина, прокаинамида, дизопирамида, лидокаина, b–адреноблокаторов), что дало основание E.M. Vaughan Williams отнести его к особому, третьему классу антиаритмических препаратов.
Однако, как показала практика, с применением Кордарона с целью коррекции нарушений ритма сердца связано развитие многих неблагоприятных побочных реакций (НПР), в том числе и серьезных, со стороны различных органов и систем организма человека.
С целью профилактики их развития, ЦЭБЛС счел целесообразным информировать медицинскую общественность, а также потребителей, о мерах предотвращения возможных негативных последствий, связанных с применением Кордарона, которые представлены ниже в виде рекомендаций.
Врачам, назначающим Кордарон для лечения и профилактики нарушений ритма сердца, а так же пациентам, целесообразно ознакомиться с данными рекомендациями.
Информация, предоставляемая в этих рекомендациях, не заменяет пациенту консультацию врача по вопросам, связанным с лечением данным препаратом.
I. Что такое Кордарон?
II. Противопоказания и предостережения при приеме Кордарона.
III. Возможные побочные эффекты Кордарона.
IV. Что должны знать врачи и пациенты перед началом приема Кордарона?
V. Взаимодействие Кордарона с другими лекарственными средствами.
VI. Как следует принимать Кордарон?
VII. Как следует хранить Кордарон?
I. Что такое Кордарон?
Кордарон- антиаритмический препарат III класса (ингибитор реполяризации). Обладает также антиангинальным, коронародилатирующим, альфа- и бета-адреноблокирующим и гипотензивным действием. Этот препарат применяется у взрослых для лечения и профилактики рецидивов нарушений ритма сердца, угрожающих жизни, при непереносимости или неэффективности других препаратов для лечения аритмий.
Показания к назначению Кордарона :
ü Купирование приступов пароксизмальной тахикардии:
§ желудочковой пароксизмальной тахикардии;
§ наджелудочковой пароксизмальной тахикардии с высокой частотой сокращений желудочков, в особенности на фоне WPW-синдрома;
§ Купирование пароксизмальной и устойчивой формы мерцательной аритмии (фибрилляции предсердий) и трепетания предсердий.
ü Профилактика рецидивов:
§ желудочковых аритмий и фибрилляции желудочков сердца, угрожающих жизни (лечение должно быть начато в стационаре при тщательном кардиомониторном контроле);
§ наджелудочковых пароксизмальных тахикардий (документированных приступов рецидивирующей устойчивой наджелудочковой пароксизмальной тахикардии у больных с органическими заболеваниями сердца; документированных приступов рецидивирующей устойчивой наджелудочковой пароксизмальной тахикардии у больных без органических заболеваний сердца, когда антиаритмические препараты других классов не эффективны или имеются противопоказания к их применению; документированных приступов рецидивирующей устойчивой наджелудочковой пароксизмальной тахикардии у больных с WPW-синдромом);
§ мерцательной аритмии (фибрилляции предсердий) и трепетания предсердий.
Прием Кордарона противопоказан при:
ü повышенной чувствительности к йоду и/или амиодарону;
ü синдроме слабости синусового узла (синусовая брадикардия, синоатриальная блокада), за исключением случаев коррекции искусственным водителем ритма (опасность «остановки» синусового узла);
ü нарушениях AV и внутрижелудочковой проводимости (AV блокада II–III степени, блокада ножек пучка Гиса) при отсутствии искусственного водителя ритма (кардиостимулятора);
ü врожденном или приобретенном удлинении интервала Q-T;
ü одновременном приеме препаратов, удлиняющих интервал Q-T и способных вызвать полиморфную желудочковую тахикардию типа «пируэт» (torsade de pointes);
ü дисфункции щитовидной железы (гипотиреоз, гипертиреоз);
ü гипокалиемии, гипомагниемии;
ü сердечной недостаточности (в стадии декомпенсации);
ü беременности, периоде лактации;
ü одновременном приеме ингибиторов МАО;
ü интерстициальной болезни легких;
ü кардиогенном шоке;
ü выраженной артериальной гипотензии.
Кордарон противопоказан для применения у лиц до 18 лет (эффективность и безопасность не установлены).
Кордарон следует применять с осторожностью при:
ü хронической сердечной недостаточности (III-IV ФК по классификации NYHA);
ü печеночной недостаточности;
ü бронхиальной астме;
ü в пожилом возрасте (высокий риск развития выраженной брадикардии).
Кордарон может вызвать серьезные неблагоприятные побочные реакции:
ü Со стороны сердечно-сосудистой системы:
§ нарушения проводимости (синоатриальная блокада, AV блокада различных степеней, внутрижелудочковая блокада)
§ остановка синусового узла (у пациентов с дисфункцией синусового узла и пожилых пациентов)
§ прогрессирование ХСН (при длительном применении),
ü Со стороны дыхательной системы:
§ интерстициальный или альвеолярный пневмонит
§ плеврит, облитерирующий бронхиолит с пневмонией, иногда заканчивающиеся летальным исходом
§ бронхоспазм у пациентов с тяжелой дыхательной недостаточностью (особенно у пациентов с бронхиальной астмой)
§ острый респираторный дистресс-синдром взрослых, с возможным летальным исходом, чаще всего сразу после хирургического вмешательства
ü Со стороны печени:
§ в начале курса лечения возможно повышение уровня трансаминаз в сыворотке крови, которое обычно бывает умеренным (в 1,5–3 раза выше нормальных значений). Повышенный уровень трансаминаз снижается при уменьшении дозы препарата или даже спонтанно;
§ острые нарушения функции печени (острый токсический гепатит) с повышенным уровнем печеночных трансаминаз в сыворотке и/или с желтухой, включая развитие печеночной недостаточности (возможен летальный исход). В таких случаях лечение следует прекратить;
§ развитие хронической печеночной недостаточности (жировой гепатоз, псевдоалкогольный гепатит, цирроз). Клинические симптомы и изменения лабораторных показателей включают гепатомегалию, повышение уровеня печеночных трансаминаз до 1,5–5 раз по сравнению с нормальными показателями, в связи с чем, в ходе лечения рекомендуется проводить регулярный контроль функций печени.
ü Со стороны обмена веществ:
§ повышение уровня T3 в сыворотке крови, при этом уровень T4 остается нормальным или слегка пониженным. В таких случаях, при отсутствии клинических признаков дисфункции щитовидной железы, отмены препарата не требуется;
§ гипотиреоз- увеличение массы тела, пониженная активность, брадикардия, повышение уровня ТТГ сыворотки крови. Нормализация функции щитовидной железы обычно наблюдается в течение 1–3 мес после прекращения лечения. В ситуациях, связанных с опасностью для жизни, лечение Кордароном может быть продолжено с одновременным дополнительным приемом левотироксина;
ü Со стороны органов зрения:
§ микродепозиты в роговице глаза, возникающие на фоне приема препарата, вызывают нарушения зрения в виде появления окрашенного ореола при ярком освещении или ощущения тумана (обратимы после отмены препарата);
§ повышенная чувствительность глаз к свету;
§ развитие нейропатии или неврита зрительного нерва, которые могут приводить к постоянной слепоте.
ü Со стороны нервной системы:
§ сенсомоторные периферические нейропатии и/или миопатии (обратимые после отмены препарата);
§ доброкачественная внутричерепная гипертензия (псевдоопухоль мозга), головная боль;
§ нарушение сна, кошмарные сновидения.
ü Со стороны кожных покровов:
§ фотосенсибилизация. По этой причине в ходе лечения следует избегать солнечного света (и УФ лучей);
§ эритема при проведении радиотерапии;
§ при продолжительном применении препарата в высоких суточных дозах может наблюдаться сероватая или голубоватая пигментация кожи; после прекращения лечения эта пигментация медленно исчезает.
Другие возможные неблагоприятные побочные реакции Кордарона:
ü нарушения пищеварения (тошнота, рвота, нарушения вкуса);
ü снижение аппетита;
ü притупление или потеря вкусовых ощущений;
ü ощущение тяжести в эпигастрии;
ü реакции повышенной чувствительности;
ü поражение почек с повышением уровня креатинина;
ü синдром нарушения секреции АДГ;
ü эксфолиативный дерматит;
ü гемолитическая и апластическая анемия.
Ø Перед началом терапии необходимо провести рентгенологическое исследование легких, оценить функцию щитовидной железы (концентрация гормонов), печени (активность трансаминаз) и концентрацию электролитов плазмы.
Ø В период лечения периодически (каждые 3 месяца) контролировать электрокардиограмму (ширина комплекса QRS и длительность интервала Q-T), содержание трансаминаз (при повышении в 3 раза или удвоении при исходно повышенной их активности дозу Кордарона следует уменьшить, вплоть до полного прекращения терапии).
Ø При возникновении AV блокады I ст. необходимо усилить наблюдение за пациентом. При развитии AV блокады II-III ст., SA блокады или двухпучковой внутрижелудочковой блокады, лечение должно быть прекращено.
Ø Рекомендуется ежегодное рентгенологическое исследование легких, 1 раз в полгода — исследование функции внешнего дыхания.
Ø Рекомендуется 1 раз в полгода контролировать содержание гормонов Т3 и Т4 в плазме крови. При отсутствии клинических признаков дисфункции щитовидной железы лечение прекращать не следует.
Ø Необходимо периодическое наблюдение окулиста (выявление значительных отложений в роговице и нарушений зрения требует отмены Кордарона).
Ø Парентеральное введение должно проводиться только в стационаре под контролем артериального давления, частоты сердечных сокращений, электрокардиограммы.
Ø Применение при беременности и лактации возможно только при угрожающих жизни нарушениях ритма при неэффективности др. антиаритмической терапии (вызывает у новорожденных гипотиреоз, зоб, брадикардию и задержку умственного развития).
Ø Безопасность и эффективность препарата у детей не изучена, начало и продолжительность эффекта у них могут быть иной, чем у взрослых.
Ø После отмены препарата фармакодинамический эффект сохраняется в течение 10-30 дней.
Ø Перед проведением хирургическиого вмешательства необходимо поставить в известность анестезиолога о приеме больным препарата (риск усиления гемодинамического эффекта общих и местных анестетиков, возможность развития острого респираторного дистресс-синдрома у взрослых непосредственно после хирургического вмешательства).
Кроме того, врачу необходимо знать обо всех лекарствах, которые пациент принимает, включая рецептурные и безрецептурные препараты, витамины и биологически активные добавки.
Ø Не употреблять грейпфрутовый сок одновременно с приемом Кордарона. Грейпфрутовый сок влияет на метаболизм препарата и повышает его концентрацию в плазме крови.
Ø Кордарон делает кожу чувствительной к солнечным лучам (фоточувствительность), к свету от лампы для загара и солярию. Поэтому следует избегать ламп для загара, солярия и ограничить время нахождения на солнце. Можно получить тяжелые солнечные ожоги, волдыри или припухлость кожи. Следует использовать солнцезащитный крем и носить закрывающую кожу одежду и шляпу при нахождении под прямыми солнечными лучами.
Ø Не принимать Кордарон при беременности без консультации с врачом. Кордарон может нанести вред плоду.
Ø Не рекомендуется кормление грудью во время приема Кордарона. Кордарон проникает в молоко и может нанести вред ребенку. Кордарон может оставаться в организме в течение нескольких месяцев после прекращения лечения, поэтому не следует кормить грудью во время приема препарата и несколько месяцев после его отмены.
Ø В период лечения необходимо соблюдать осторожность при вождении автотранспорта и занятии другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Ø Необходимо сообщить врачу о появлении любых неблагоприятных побочных эффектов.
Врачу необходимо знать обо всех заболеваниях и особых состояниях у пациентов, включающих:
ü заболевания легких;
ü нарушение дыхательных функций;
ü заболевания печени;
ü заболевания щитовидной железой в настоящий момент или в индивидуальном или семейном анамнезе;
ü заболевания сердца;
ü нарушения артериального давления;
ü беременность или ее планирование;
ü грудное вскармливание.
Кордарон может вызывать различные побочные реакции, в том числе и серьезные, при взаимодействии с другими лекарственными средствами:
ü Противопоказано совместное применение с препаратами, которые могут вызывать полиморфную пароксизмальную желудочковую тахикардию типа «пируэт» (torsade de pointes) :
§ антиаритмические средства, включая препараты класса IA (хинидин, гидрохинидин, дизопирамид, прокаинамид), III класса (дофетилид, ибутилид, бретилия тозилат), бепридил, соталол;
§ препараты, не обладающие антиаритмической активностью, включая винкамин, фенотиазины (хлорпромазин, циамемазин, левомепромазин, тиоридазин, трифлуоперазин, флуфеназин), бензамиды (амисульприд, сультоприд, сульпирид, тиаприд, вералиприд), бутирофеноны (дроперидол, галоперидол), сертиндол, пимозид; трициклические антидепрессанты, цизаприд, макролиды (эритромицин в/в, спирамицин), азолы, противомалярийные ЛС (хинин, хлорохин, мефлохин, галофантрин, лумефантрин); пентамидин (парентерально), дифеманила метилсульфат, мизоластин, терфенадин, фторхинолоны (в т.ч. моксифлоксацин), т.к. имеется риск возникновения пароксизмальной тахикардии с возможностью летального исхода.
ü Не рекомендуется комбинированная терапия со следующими препаратами:
§ бета-адреноблокаторы и некоторые блокаторы Са-каналов (верапамил, дилтиазем), т.к. возможно нарушение сердечного автоматизма (выраженная брадикардия) и проводимости;
§ слабительные, стимулирующие моторику кишечника, т.к. они могут вызывать гипокалиемию и тем самым повышать риск пароксизмальной тахикардии, поэтому следует назначить другой тип слабительного.
ü С осторожностью следует назначать в комбинации с Кордароном следующие препараты:
§ пероральные антикоагулянты (усиление эффекта пероральных антикоагулянтов с повышенным риском кровотечения). Необходим частый контроль уровня протромбина в крови и коррекции доз антикоагулянтов в период лечения Кордароном и после отмены препарата;
§ сердечные гликозиды — могут возникнуть нарушения автоматизма (выраженная брадикардия) и предсердно-желудочковой проводимости (синергизм действия). Кроме того, возможно увеличение концентрации дигоксина в плазме крови (из-за снижения клиренса дигоксина). В случае их совместного применения необходимо осуществлять клинический, электрокардиографический и лабораторный контроль (включая, при возможности, определение уровня дигоксина в плазме крови), может возникнуть необходимость в изменении доз сердечных гликозидов;
§ фенитоин, т.к. возможно увеличение уровня фенитоина в плазме крови, с последующим риском развития неврологических нарушений. Необходимы клинический мониторинг и снижение дозы фенитоина при появлении признаков передозировки, определение уровня фенитоина в плазме;
§ ЛС, метаболизирующиеся с участием изофермента CYP3A4 (циклоспорин, фентанил, лидокаин, такролимус, силденафил, мидазолам, триазолам, дигидроэрготамин, эрготамин, статины, в т.ч. симвастатин). Кордарон повышает их концентрацию, поэтому возникает риск развития их токсичности и/или усиления фармакодинамических эффектов. Следует изменить дозировку этих препаратов на фоне терапии Кордароном;
§ флекаинид, т.к. возможно увеличение уровня флекаинида в плазме крови. В связи с этим, на фоне терапии Кордароном рекомендуется проводить корректировку доз флекаинида;
§ орлистат, т.к. он снижает концентрацию Кордарона и его активного метаболита;
§ клонидин, гуанфацин, ингибиторы холинэстеразы (донепезил, галантамин, ривастигмин, такрин, амбенония хлорид, пиридостигмин, неостигмин), пилокарпин в связи с тем, что они увеличивают риск развития выраженной брадикардии;
§ радиоактивный йод, т.к. Кордарон (содержит в своем составе йод) может нарушать поглощение радиоактивного йода, что может искажать результаты радиоизотопного исследования щитовидной железы;
§ рифампицин и препараты зверобоя продырявленного (мощные индукторы изофермента CYP3A4), снижающие концентрацию Кордарона в плазме;
§ ингибиторы протеазы ВИЧ (ингибиторы изофермента CYP3A4) могут повышать плазменные концентрации Кордарона;
ü Принимать Кордарон точно как предписано. Врач может изменить дозу в ходе лечения соответсвенно возникающим эффектам препарата.
ü Не следует прекращать прием препарата самостоятельно, без рекомендаций врача.
ü Принимать Кордарон можно во время приема пищи или вне его.
ü Принимать Кордарон следует каждый день в одно и то же время.
ü Кордарон в таблетированной форме следует проглатывать, запивая водой. Не запивать грейпфрутовым соком, это повлияет на всасывание препарата в желудке.
ü При пропуске очередной дозы Кордарона не следует принимать двойную дозу, чтобы компенсировать пропущенную дозу. Следует дождаться следующего очередного приема препарата.
ü Не использовать Кордарон для лечения заболеваний, для которых использование препарата не предусмотрено.
В случае передозировки пациентам следует незамедлительно обратиться за медицинской помощью. Передозировка препаратом может проявиться в виде различных неблагоприятных побочных эффектов (см. «Возможные побочные эффекты Кордарона»)
· Хранить Кордарон при комнатной температуре, в сухом месте, вдали от источников тепла и солнечного света.
· Держать в плотно закрытом контейнере. Не использовать препарат с истекшим сроком годности.
· Хранить Кордарон и все лекарства в недоступном для детей месте.
Fang M. C. et al. National trends in antiarrhythmics and antithrombotic medications use in atrial fibrillation. Arch. Intern. Med., 2004; 164: 55–60.
Состояния, вызванные приемом амиодарона, в практике кардиолога и эндокринолога
В клинической практике врачам разных специальностей нередко приходится сталкиваться с проблемой назначения препаратов, обладающих не только высокой эффективностью, но и большим спектром побочных действий, которые могут осложнять течение основного заболев
В клинической практике врачам разных специальностей нередко приходится сталкиваться с проблемой назначения препаратов, обладающих не только высокой эффективностью, но и большим спектром побочных действий, которые могут осложнять течение основного заболевания. К таким препаратам относится амиодарон, занимающий ведущее место в лечении потенциально злокачественных и злокачественных форм желудочковых аритмий, но имеющий широкий спектр воздействия на щитовидную железу.
Амиодарон — антиаритмический препарат III класса, был открыт Tondeur и Binon в 1960 г. и с тех пор широко используется в кардиологической практике. Частота его применения достигает 24,1% от общего числа назначений антиаритмических препаратов.
В основном препарат используют для лечения злокачественных форм желудочковых и наджелудочковых аритмий, пароксизмальной суправентрикулярной тахикардии, фибрилляции предсердий, которые рефрактерны к терапии другими антиаритмическими препаратами и сопровождаются высоким риском внезапной сердечной смерти.
Мета-анализ 13 многоцентровых исследований, посвященных первичной профилактике внезапной смерти у пациентов, перенесших инфаркт миокарда или имеющих хроническую недостаточность кровообращения, продемонстрировал способность амиодарона снижать показатели не только аритмической, но и общей летальности.
Так как амиодарон не оказывает выраженного отрицательного инотропного действия на миокард, показано его применение при нарушениях сердечного ритма у больных с застойной сердечной недостаточностью. Он также является средством выбора при лечении и профилактике аритмий у больных с синдромом Вольффа-Паркинсона-Уайта.
Помимо антиаритмического действия у ряда больных препарат оказывает влияние на функцию щитовидной железы, вызывая тиреотоксикоз или гипотиреоз. В течение ряда лет эти изменения являлись одной из причин отмены или отказа от применения амиодарона несмотря на то, что препарат назначался по жизненным показаниям. Продолжающиеся исследования в данном направлении позволили изменить взгляд на проблему и разработать новые подходы к диагностике и лечению указанных нарушений.
Механизм действия амиодарона
Препарат представляет собой йодированную жирорастворимую производную бензофурана, которая по структуре имеет близкое сходство с тироксином. Препарат состоит на 37,5% из йода, приблизительно 10% молекул подвергается дейодированию ежедневно. Высокое содержание йода в амиодароне считается одной из причин возникновения тиреоидной дисфункции. У пациентов, принимающих амиодарон, уровень неорганического йода в моче и плазме увеличивается в 40 раз. Препарат проникает во многие органы и ткани: в печень, легкие, щитовидную железу, миокард, но более всего накапливается в жировой ткани. Период полувыведения амиодарона составляет от 30 дней до 5 месяцев.
Механизм воздействия амиодарона на щитовидную железу
Установлено, что у 1/3 пациентов в процессе лечения амиодароном наблюдается повышение уровня общего и свободного тироксина (Т4), реверсивного (неактивного) трийодтиронина (ТЗ), уменьшение уровня ТЗ. Это обусловлено подавлением активности 5-дейодиназы I типа, нарушающего конверсию Т4 в Т3 в периферических тканях, особенно в печени. Подавление активности 5-дейодиназы может сохраняться на протяжении нескольких месяцев и после отмены препарата. Кроме того, препарат снижает проникновение тиреоидных гормонов в клетки периферических тканей. В конечном итоге оба механизма способствуют развитию доброкачественной формы эутиреоидной гипертироксинемии, с повышенным уровнем общего и свободного Т4, рТЗ, нормальным или субнормальным ТЗ. Не-смотря на повышенный уровень св Т4 [14,7;23,2], у пациентов не отмечается признаков тиреотоксикоза (рис. 1).
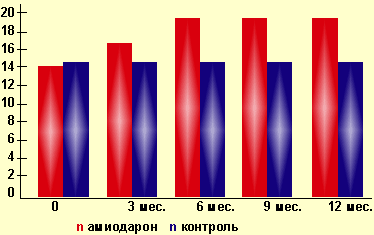 |
| Рисунок 1. Динамика показателей свТ4 у пациентов, принимающих амиодарон (контроль — пациенты с ИБС, не принимающие амиодарон) |
Эутиреоидная гипертироксинемия не требует медикаментозной коррекции, а диагноз тиреотоксикоза не должен основываться на одном только обнаружении повышенного уровня тироксина у больных, получающих амиодарон. По нашим данным, развитие эутиреоидной гипертироксинемии не приводит к утрате амиодароном антиаритмической эффективности и рецидивам предшествующих нарушений сердечного ритма. Пациенты должны оставаться под динамическим наблюдением с периодическим мониторированием функционального состояния щитовидной железы.
В процессе лечения амиодароном у ряда больных может произойти изменение уровня ТТГ в сыворотке крови без клинических проявлений нарушения функции щитовидной железы. Повышение концентрации ТТГ у клинически эутиреоидных пациентов зависит как от дозы, так и от длительности приема препарата. Так, при ежедневном приеме 200–400 мг амиодарона уровень ТТГ обычно находится в пределах нормы. При более высокой дозе препарата увеличение концентрации ТТГ может произойти в первые месяцы приема, с последующим возвращением к норме (табл. 1).
Амиодарон снижает чувствительность клеток, особенно кардиомиоцитов, к тиреоидным гормонам, приводя к «местному», тканевому гипотиреозу. Развитию этого состояния способствуют взаимодействие амиодарона с рецепторами тиреоидных гормонов, сокращение числа катехоламиновых рецепторов и снижение эффекта ТЗ на кардиомиоциты.
На клеточном уровне амиодарон действует как антагонист тиреоидных гормонов. Наиболее активный метаболит амиодарона, диэтиламиодарон (ДЭА), действует как конкурентный ингибитор присоединения трийодтиронина к α-1-ТЗ-рецептору и как неконкурентный ингибитор β-1-ТЗ-рецептора. Действие ДЭА зависит от его концентрации в различных тканях. При низкой концентрации ДЭА может выступать как агонист действия ТЗ и только при больших концентрациях — как антагонист ТЗ. Известно, что α-1-ТЗ-рецепторы находятся в основном в сердечной и скелетной мускулатуре, тогда как в печени, почках и мозге преобладают β-1-ТЗ-рецепторы. Следовательно, при достаточной концентрации амиодарон действует как конкурентный ингибитор Т3, обусловливая развитие «местного» гипотиреоза в сердечной мышце. Кроме того, исследования последних лет показали, что амиодарон вызывает мутацию гена ядерного рецептора Т3.
Снижение проникновения Т3 в кардиомиоциты оказывает антиаритмический эффект за счет изменения экспрессии генов ионных каналов и других функциональных белков. Амиодарон непосредственно влияет на ионные каналы, вне зависимости от его воздействия на тиреоидные гормоны. Экспериментально доказано, что амиодарон способен ингибировать Nа-К-АТФ-азу. Препарат блокирует несколько ионных токов на мембране кардиомиоцита: выход ионов К во время фаз реполяризации, а также вход ионов Na и Ca.
Кроме вышеописанных эффектов амиодарон и его метаболит ДЭА оказывают цитотокическое действие на щитовидную железу.
Экспериментальными исследованиями установлено, что амиодарон и его метаболит вызывают лизис клеток линии человеческих тиреоцитов, а также нетиреоидной ткани. Амиодарон оказывает самостоятельный, токсический эффект, усиливаемый содержанием йода в молекуле, при этом его активный метаболит ДЭА обладает большей цитотоксичностью и его интратиреоидная концентрация выше, чем у самого препарата.
В литературе широко обсуждается вопрос о влиянии амиодарона на течение аутоиммунных процессов в щитовидной железе. Предполагается, что избыток йода, высвобождаемый из амиодарона, может приводить к индукции или манифестации аутоиммунных изменений в щитовидной железе. Классическими маркерами аутоиммунного процесса являются антитела к тиреоглобулину (ТГ) и пероксидазе (ТПО). У ряда пациентов антитела к пероксидазе регистрируются как на ранних этапах лечения, так и в течение 6 мес. после отмены препарата. По мнению ряда исследователей, этот феномен объясняется ранним токсическим эффектом амиодарона на щитовидную железу, приводящим к высвобождению аутоантигенов и последующему запуску иммунных реакций. С другой стороны, у большинства лиц, получающих амиодарон, не отмечается увеличения частоты встречаемости тиреоидных антител.
Амиодарон-ассоциированная дисфункция щитовидной железы
У большинства больных, принимающих амиодарон, сохраняется эутиреоз. Тем не менее у некоторых пациентов могут развиться нарушения функции щитовидной железы.
Возникновение гипотиреоза объясняется длительным блоком органификации йода и нарушением синтеза тиреоидных гормонов (эффект Вольфф-Чайкова). В развитие этого состояния вносит вклад и ингибирование тиреоидных рецепторов в тканях.
По современным представлениям, в основе патогенеза другой дисфункции щитовидной железы — тиреотоксикоза, развивающегося на фоне приема амиодарона, — лежат 2 основных механизма, приводящих к формированию 2 вариантов амиодарон-ассоциированного тиреотоксикоза (АмАТ):
Клинические особенности и лечение нарушений функции щитовидной железы на фоне приема амиодарона
Амиодарон-ассоциированный гипотиреоз. Распространенность гипотиреоза на фоне приема амиодарона варьирует от 6% в странах с низким потреблением йода до 13% с высоким потреблением йода.
Наиболее часто гипотиреоз встречается у пожилых людей и женщин, которые наиболее подвержены развитию гипотиреоза (отношение полов 1,5:1).
По данным нашего исследования, среди пациентов с амиодарон-ассоциированным гипотиреозом органическая патология щитовидной железы выявлена в 70,8% случаев (в основном аутоиммунный тиреоидит) (рис. 2).
 |
| Рисунок 2. Структура патологии щитовидной железы у лиц с гипотиреозом, развившимся на фоне приема амиодарона (%) |
В клинической картине отмечаются классические признаки гипотиреоза: утомляемость, сухость кожи, зябкость, запоры, сонливость, ухудшение внимания, отечный синдром, брадиаритмии и др. Субклинический вариант протекает бессимптомно, но возможно нарушение липидного обмена (повышение ЛПНП, коэффициентов обХс/ЛПВП, ЛПНП/ЛПВП и снижение ЛПВП), ухудшение памяти, депрессия.
Диагностика этого состояния основана на определении сниженного уровня свободного Т4 и повышенного ТТГ (обычно > 10mU/l) или нормального уровня свободного Т4 при повышенном уровне ТТГ при субклиническом варианте течения. Уровень Т3 не является надежным индикатором, так как при гипотиреозе он может быть в пределах нормы или даже несколько повышен в результате компенсаторного дейодирования Т4 в биологически более активный Т3.
Лечение амиодарон-ассоциированного гипотиреоза. С амиодарон-индуцированным гипотиреозом можно бороться 2 способами: либо отменить амиодарон, либо подобрать заместительную терапию тиреоидными гормонами. После отмены амиодарона эутиреоз обычно восстанавливается, но на это могут потребоваться месяцы в связи с длительным периодом выведения лекарства. Часто на практике отмена амиодарона невозможна, так как препарат применяется по жизненным показаниям, особенно для лечения тяжелых желудочковых тахиаритмий. В таких случаях лечение амиодароном продолжают. Пациентам назначается L-тироксин. Уровень ТТГ снижается обычно до верхней границы нормы. Рекомендуется начинать заместительную терапию тиреоидными гормонами с минимальных доз 12,5–25 мкг/сут с постепенным повышением ее под контролем ТТГ с интервалом в 4–6 нед. до достижения эффекта, не допуская при этом декомпенсации кардиальной патологии или развития аритмии. При субклиническом течении гипотиреоза вопрос о заместительной терапии решается индивидуально. Назначение L-тироксина может быть показано при сопутствующем нарушении липидного профиля, депрессии, повышении уровня ТТГ более чем на 10 МЕ/л, причем подбирается минимально эффективная доза для коррекции выявленных нарушений. Пациент должен оставаться под наблюдением с целью оценки динамики состояния на фоне лечения первые 6 нед., а затем каждые 3 мес. При отсутствии изменений в лабораторных показателях липидного спектра и клинической симптоматике препарат отменяют.
Амиодарон-ассоциированный тиреотоксикоз. По статистике АмАТ развивается в 2–12 % случаях при постоянном приеме препарата. Некоторые исследования показали, что распространенность варьирует в зависимости от потребления йода с пищей. В популяции АмАТ превалирует в районах с низким потреблением йода (например, Центральная Европа) и редко встречается в районах, где пища насыщена йодом (например, Северная Америка, Великобритания).
По нашим данным, среди пациентов с АмАТ, проживающих в районе легкого и умеренного йодного дефицита (Москва и Московская область), преобладали лица с измененной щитовидной железой (61%), в основном с узловыми зобами и аутоиммунным поражением щитовидной железы (рис. 3).
 |
| Рисунок 3. Структура патологии щитовидной железы у лиц с тиреотоксикозом, развившимся на фоне приема амиодарона |
Частота тиреотоксикоза не зависит от суточной и кумулятивной дозы амиодарона. Необходимо отметить, что между началом приема препарата и развитием тиреотоксикоза может проходить достаточно долгое время (до 3 лет). Более того, описаны случаи возникновения этого состояния через несколько месяцев после отмены амиодарона.
Клинические особенности АмАТ определяются тем, что это состояние преимущественно развивается у лиц пожилого возраста. Обычные симптомы тиреотоксикоза — зоб, похудание, потливость, тремор пальцев рук — могут быть выражены незначительно или вовсе отсутствовать. В клинической картине доминируют сердечно-сосудистые и психические расстройства. Серьезную опасность представляют именно кардиальные эффекты избытка тиреоидных гормонов, такие, как ухудшение течения сопутствующих форм аритмий, учащение приступов ИБС. Повышенная чувствительность к адренергической стимуляции при тиреотоксикозе может увеличивать частоту желудочковых аритмий, особенно у больных с предшествовавшей сердечной патологией.
Токсическое действие тиреоидных гормонов на центральную нервную систему приводит к развитию тиреотоксической энцефалопатии, которая проявляется нервной возбудимостью, эмоциональной лабильностью, нарушением сна. Однако у больных пожилого возраста, как правило, доминируют противоположные признаки: психическая заторможенность, апатия, отсутствие аппетита, слабость, адинамия, депрессия, что может затруднять диагностику АмАТ.
Дифференциальная диагностика АмАТ I и АмАТ II типов
Для клинициста важно дифференцировать 2 формы АмАТ для выбора правильной тактики ведения пациентов.
Как было сказано выше, АмАТ I типа развивается на фоне существующих или предшествующих заболеваний щитовидной железы. Помимо изменений гормонального спектра и определения повышенного титра антитиреоидных антител (в случаях манифестации диффузного токсического зоба), АмАТ I типа характеризуется нормальным или, гораздо реже, сниженным захватом радиофармпрепарата, при УЗИ отмечаются признаки узлового зоба или аутоиммунного зоба с нормальным или повышенным кровотоком.
АмАТ II типа развивается на фоне интактной железы. Главная клиническая особенность этих форм — внезапное развитие и тяжесть тиреотоксикоза, в том числе развитие болевых форм, клинически похожих на подострый тиреоидит. При исследовании с радиоактивным йодом отмечается снижение накопления препарата в железе. В биоптате щитовидной железы, полученном при тонкоигольной биопсии или после хирургического вмешательства, отмечается большое количество коллоида, инфильтрация макрофагами, деструкция тиреоцитов. Часто наблюдается отсутствие или снижение кровотока в щитовидной железе, определяемое при УЗИ с доплерографией.
Обсуждается роль повышенной концентрации ИЛ-6 как маркера этого состояния, однако в нашем исследовании мы не обнаружили существенных различий в уровне ИЛ-6 и косвенного показателя активности ИЛ-6 — С-реактивного белка у лиц с АмАТ I и II типов и пациентов с аутоиммунным тиреотоксикозом.
Кроме этих 2 форм в практике клинициста могут встречаться смешанные варианты течения этого осложнения с чертами АмАТ I и II типов.
У пациентов с деструктивным тиреотоксикозом из-за действия амиодарона позже может развиться гипотиреоз. Сводные данные об отличии двух форм представлены в таблице 2.
Основным и наиболее ранним проявлением амиодарон-ассоциированного тиреотоксикоза в наших исследованиях стала потеря антиаритмической эффективности амиодарона во всех случаях. У пациентов с пароксизмами желудочковой тахикардии мерцательной аритмии отмечалось рецидивирование нарушений ритма сердца. У больных с желудочковой экстрасистолией по результатам суточного мониторирования ЭКГ наблюдалось увеличение общего количества парных желудочковых экстрасистол и пробежек желудочковой тахикардии на 61,7, 83,5 и 85% соответственно, по сравнению с показателями, регистрировавшимися до развития тиреотоксикоза.
Лечение амиодарон-ассоциированного тиреотоксикоза. В отличие от гипотиреоза, который сравнительно легко лечится заместительной терапией тиреоидными гормонами, компенсация тиреотоксикоза сопряжена со многими трудностями и требует индивидуального подхода в каждом случае.
У пациентов с легким тиреотоксикозом, исходно неизмененной щитовидной железой и небольшим зобом тиреотоксикоз устраняется после отмены препарата. Наоборот, у пациентов с предшествующими заболеваниями щитовидной железы тиреотоксикоз, как правило, не проходит без лечения даже спустя несколько месяцев после окончания терапии амиодароном.
Отмена амиодарона возможна только в тех случаях, когда нарушения сердечного ритма не опасны для жизни и могут быть нивелированы альтернативными антиаритмическими препаратами.
Для лечения тиреотоксикоза применяют тионамиды, пропилтиоурацил, высокие дозы глюкокортикоидов, плазмаферез, оперативное лечение. За рубежом используют конкурентный ингибитор захвата йода щитовидной железой — перхлорат калия.
Для компенсации тиреотоксикоза требуются большие дозы антитиреоидных препаратов (например, метизола 40–60 мг или пропицила 300—600 мг) для ингибирования синтеза гормонов. Для нормализации уровня свободного Т4 может потребоваться 6–12 нед. и более. Длительная терапия высокими дозами тиреостатиков обычно необходима пациентам, которые продолжают получать амиодарон по жизненным показаниям. Некоторые исследователи предпочитают продолжать терапию поддерживающими дозами тиреостатиков, с тем чтобы сохранить полный или частичный блок синтеза тиреоидных гормонов в течение всего периода терапии амиодароном. В случае развития гипотиреоза к лечению добавляется L-тироксин.
Одним из главных фактов патогенеза АмАТ II типа, особенно возникшего у лиц без предшествующих изменений щитовидной железы, служит развитие деструктивного тиреоидита и выход ранее синтезированных гормонов в кровоток. В такой ситуации предлагается использовать глюкокортикоиды. Преднизолон назначается в дозе 30–40 мг/сут. Курс лечения может продолжаться до 3 мес., так как описаны случаи возвращения симптомов тиреотоксикоза при попытке снизить дозу препарата.
В случае развития гипотиреоза у пациентов, перенесших АмАТ II типа, к лечению добавляется L-тироксин. По показаниям к проводимой терапии добавляются пропранолол и другие симптоматические средства.
При тяжелом течении амиодарон-ассоциированного тиреотоксикоза (обычно при сочетании 2 форм) используют комбинацию тионамида и глюкокортикоида. У некоторых пациентов комбинированная лекарственная терапия может быть неэффективной, что требует хирургического вмешательства. Оперативное лечение, как правило, проводится в случае невозможности достижения компенсации заболевания после длительного (около 6 мес.) курса медикаментозной терапии или при сочетании амиодарон-ассоциированного тиреотоксикоза с узловым зобом. Несмотря на риск тиреотоксического криза во время анестезии и хирургического вмешательства, в мире накоплен опыт лечения таких больных, показавший, что субтотальная резекция щитовидной железы позволяет быстро добиться ремиссии тиреотоксикоза и продолжить антиаритмическую терапию. При крайне тяжелом состоянии используют плазмаферез.
Радиоактивный йод обычно не эффективен в лечении пациентов с АмАТ, так как большая концентрация йода предотвращает достаточное поглощение щитовидной железой радиоизотопа. Кроме того, это может привести к усилению тиреотоксикоза в результате высвобождения гормонов. Однако в районах с пограничным уровнем йодного дефицита пациенты с диффузным или узловым зобом, у которых наблюдается нормальное или повышенное поглощение радиоизотопа, несмотря на прием амиодарона, могут отвечать на терапию радиоактивным йодом.
Как было отмечено выше, амиодарон назначается при тяжелых, жизнеугрожающих аритмиях, часто рефрактерных к другой терапии. Отмена препарата в такой ситуации может быть недопустима по жизненным показаниям. Поэтому в лечебной практике в случае невозможности прекращения приема антиаритмика компенсацию тиреотоксикоза проводят на фоне продолжающейся терапии амиодароном. Более того, поскольку препарат и его метаболит ДЭA вызывают развитие «местного гипотиреоза», это, как ни парадоксально, защищает сердце от действия избытка тиреоидных гормонов, поэтому отмена препарата может усилить токсическое действие тиреоидных гормонов на сердце. В литературе описаны случаи успешного ведения пациентов с тиреотоксикозом без отмены амиодарона, поэтому в каждом конкретном случае решение о смене антиаритмического препарата должно приниматься индивидуально, совместно кардиологом и эндокринологом. Ряд авторов предполагают, что даже в тех случаях, когда планируется отмена препарата, пациенты должны принимать амиодарон, пока тиреотоксикоз не будет полностью компенсирован.
Мониторинг тиреоидной функции
Всем пациентам, которым планируется назначение амиодарона, необходимо провести исследование функционального состояния щитовидной железы и ее структуры. Это позволяет не только выявить наличие тиреоидной патологии, но и прогнозировать возможное развитие тиреотоксикоза или гипотиреоза после начала терапии.
План обследования щитовидной железы до назначения препарата включает: определение ТТГ; определение свободного Т4 при измененном уровне ТТГ; УЗИ щитовидной железы; определение уровня антител к ТПО; сцинтиграфию щитовидной железы — при подозрении на автономию (снижение уровня ТТГ, наличие узлового/многоузлового зоба); пункционную биопсию щитовидной железы (при наличии узлов, подозрении на новообразование).
Присутствие антител к ТПО увеличивает риск развития амиодарон-ассоциированного гипотиреоза у пациентов с аутоиммунным тиреоидитом, особенно во время первого года лечения.
Повторное определение уровня свТ4, ТТГ можно повторить через 3 мес. от начала терапии, а затем через каждые 6 мес. При нормальных показателях мониторинг осуществляется по уровню ТТГ 1-2 раза в год, особенно у пациентов с измененной щитовидной железой.
В случае наличия патологии щитовидной железы до лечения или развития ее на фоне приема препарата проводится лечение по вышеуказанным рекомендациям.
Напомним, что появление рефрактерности к антиаритмической терапии может быть ранним признаком манифестации амиодарон-ассоциированного тиреотоксикоза.
Амиодарон на сегодняшний день является наиболее эффективным и широко используемым препаратом для лечения и профилактики угрожающих жизни желудочковых нарушений сердечного ритма и различных других форм сердечных аритмий. Однако, как и любой фармакологический препарат, он может вызывать нежелательные эффекты со стороны различных органов и тканей, что осложняет его использование. Одним из самых распространенных таких эффектов является нарушение функционального состояния щитовидной железы, что обусловлено фармакологическими особенностями препарата — высоким содержанием йода в его молекуле.
Среди пациентов старшей возрастной группы, получающих амиодарон, наиболее часто встречается субклинический гипотиреоз и тиреотоксикоз. Наличие сопутствующей патологии щитовидной железы является безусловным фактором риска нарушения ее функции. Развитие тиреотоксикоза может сопровождаться утратой антиаритмической активности амиодарона и приводить к рецидивированию нарушений ритма сердца. Ухудшение течения предшествующей аритмии, частичная утрата антиаритмической активности препарата должны насторожить кардиолога и направить его поиск на выяснение возможной эндокринной причины неэффективности лечения.
Развитие субклинического гипотиреоза на фоне приема амиодарона протекает без утраты антиаритмической активности препарата, но может сопровождаться дислипидемией с повышением показателей общего холестерина и ЛПНП. В таких случаях проведение заместительной терапии L-тироксином позволяет улучшить показатели липидного спектра.
Для предупреждения и прогнозирования возможных осложнений со стороны щитовидной железы пациенты, которым планируется лечение амиодароном, должны быть направлены к эндокринологу с целью уточнения функционального состояния щитовидной железы и наличия сопутствующей тиреоидной патологии. В дальнейшем на фоне приема препарата необходимо исследовать функцию щитовидной железы не реже 1 раза в 6 мес. и всегда при ухудшении течения аритмии согласно предложенному алгоритму. Выявление тиреотоксикоза является показанием к назначению тиреостатической терапии. При неэффективности монотерапии тиреостатиками к лечению добавляют глюкоамиотикоиды. Рекомендуется проводить лечение тиреотоксикоза в течение не менее 2 лет. В случаях, когда медикаментозное лечение невозможно, необходимо рассмотреть вопрос об оперативном лечении.
В случае развития явного гипотиреоза назначается прием L-тироксина под контролем уровня ТТГ. У лиц старшей возрастной группы при субклиническом гипотиреозе рекомендуется проведение заместительной терапии L-тироксином, если уровень ТТГ выше 10 МЕ/л. Если уровень ТТГ не превышает 10 МЕ/л, относительным показанием к назначению L-тироксина с использованием минимально эффективных доз и хорошей переносимости препарата является наличие зоба и дислипидемии. В остальных случаях проводится динамическое наблюдение с определением ТТГ 1 раз в 6 мес. и УЗИ щитовидной железы 1 раз в год.
В тех случаях, когда амиодарон назначается для первичной или вторичной профилактики фатальных желудочковых нарушений ритма сердца или когда отмена препарата невозможна по иным причинам, компенсацию тиреотоксикоза и заместительную терапию при гипотиреозе проводят на фоне продолжения приема амиодарона. Вопрос об отмене или продолжении лечения амиодароном должен решаться индивидуально для каждого пациента совместно кардиологом и эндокринологом. Клинический опыт показывает, что в большинстве случаев выбор делается в пользу продолжения лечения.
Н. Ю. Свириденко, доктор медицинских наук
Н. М. Платонова, кандидат медицинских наук
Н. В. Молашенко
С. П. Голицин, доктор медицинских наук, профессор
С. А. Бокалов, кандидат медицинских наук
С. Е. Сердюк
Эндокринологический научный центр РАМН, Москва
Институт клинической кардиологии им. А. Л. Мясникова, Москва