Видео
Гиперальдостеронизм кошек: действительно ли болезнь настолько редка, что не заслуживает нашего внимания?
Ключевые слова: гиперальдостеронизм, электролитные нарушения, гипокалиемия, гипертензия
Key words: hyperaldosteronism, electrolyte imbalance, hypopotassemia, hypertension
Гиперальдостеронизм до недавнего времени считался достаточно редкой патологией эндокринной системы. В 1983 г. появились первые сообщения о многочисленных зарегистрированных случаях первичного гиперальдостеронизма, или болезни Конна, давая доказательства того, что эта болезнь может быть более частой, чем ее оценивали в прошлом [18]. В последние годы появляется все большее количество сообщений о выявлении данной болезни у кошек. Это обусловлено и тем, что все больше внимания уделяется диагностике вторичной патологии (вторичного гиперальдостеронизма), и тем, что развивается диагностика первичной патологии. Но до сих пор эту эндокринную болезнь (как первичную, так и вторичную) нельзя назвать широко распространенной. Гиперальдостеронизм – это заболевание, при котором патофизиологические механизмы обусловлены высокой концентрацией циркулирующего в крови альдостерона. В данном случае название болезни говорит само за себя. В ходе изучения этой болезни следует вернуться к азам физиологии и рассмотреть компоненты и механизмы работы РААС. Эти основы крайне важны для правильного понимания патогенеза гиперальдостеронизма, а соответственно, и для понимания правильного диагностического и лечебного подхода к пациенту.
(0,9% раствор хлорида натрия)
объем циркулирующей крови
ингибиторы ангиотензинпревращающего фактора
нестероидные противовоспалительные средства
общий клинический анализ крови
хроническая болезнь почек
каудальная полая вена
Альдостерон и РААС
Альдостерон – это минералокортикоидный стероидный гормон, синтезирующийся в клубочковой зоне коры надпочечников из холестерола через ряд промежуточных метаболитов. На долю альдостерона приходится 95% всех гормонов, вырабатываемых клубочковой зоной коры надпочечников [8].
Важно понимать, что регуляция синтеза альдостерона в коре надпочечников обусловлена двумя ведущими механизма. Первый механизм – это влияние РААС. При этом альдостерон следует рассматривать не как отдельно существующий гормон, а как неотъемлемый компонент этой сложноорганизованной системы. РААС активируется в ответ на снижение объема циркулирующей крови и почечного кровотока. Это приводит к снижению доставки натрия и хлорида к клеткам дистальных канальцев почек и стимулирует секрецию ренина в клетках юкстагломерулярного комплекса. Именно поэтому сниженное кровяное давление, которое воспринимается сначала клетками почек, индуцирует биосинтез и секрецию ренина. Ренин, в свою очередь, расщепляет ангиотензин до ангиотензина I, который затем гидролизуется с образованием ангиотензина II в легких с помощью АПФ и выполняет роль вазоконстриктора. АПФ имеется также в подавляющем большинстве других тканей и в крови. Но наиболее его активность выражена именно в легких. Непосредственно ангиотензин II, образовавшийся в конце этой цепочки, стимулирует секрецию аль-достерона. Образующийся альдостерон поступает в кровь и вызывает экскрецию калия и задержку натрия, чем косвенно способствует накоплению воды и повышению кровяного давления. Такой, казалось бы на первый взгляд, сложный механизм, схематически можно проиллюстрировать достаточно короткой последовательностью реакций (Схема 1).
Таким образом, гиперальдостеронизм в случае вторичной патологии станет последним звеном в цепи реакций РААС.
Кроме снижения кровяного давления в афферентных артериолах на фоне снижения ОЦК и почечного кровотока, пусковыми механизмами для синтеза ренина являются:
• снижение концентрации натрия в плазме крови;
• уменьшение осмотического давления в дистальных извитых канальцах;
• стимуляция симпатических нервных волокон, иннервирующих афферентные артериолы [8].
С тех пор как было показано, что снижение перфузии почек провоцирует секрецию ренина и, как результат, повышение кровяного давления, ренин считается одним из патогенетических факторов гипертензии [4].
Второй, не менее важный механизм регуляции синтеза альдостерона в коре надпочечников – это прямая регуляция через ионы калия, циркулирующие в плазме крови. Увеличение калия в сыворотке крови стимулирует выработку альдостерона корой надпочечников, поскольку этот гормон осуществляет его экскрецию с мочой.
Для чего необходим альдостерон?
Главная физиологическая функция альдостерона – это регуляция гомеостаза натрия и калия в сыворотке крови и поддержание нормального внутрисосудистого объема жидкости. Циркулирующий в крови альдостерон оказывает свое основное физиологическое влияние на почки. Это приводит к реабсорбции натрия, в результате чего задерживается вода, но экскретируются ионы калия и водорода. По мере экскреции калия в моче концентрация калия в плазме снижается. Вследствие этого объемы плазмы и экстраклеточной жидкости увеличиваются совместно с общим периферическим сопротивлением из-за вазоконстрикции, вызванной ангиотензином II, что приводит к повышению кровяного давления. Увеличение объема экстраклеточной жидкости приводит к усилению кровотока в почках, за счет чего снижается секреция ренина.
Как и в первый раз, данная цепочка на первый взгляд может показаться сложным физиологическим механизмом. Поэтому схематическое упрощение реакций может помочь воспринять каскад реакций (Схема 2).
На основании приведенных данных о физиологическом действии альдостерона можно прийти к выводу о том, какие ведущие клинические последствия будут сопровождать повышенные концентрации альдостерона. Избыточное высвобождение альдостерона из клубочковой зоны приведет к различной степени электролитных, жидкостных и метаболических расстройств. Основными клиническими последствиями избыточной продукции альдостерона становятся, таким образом, усиленная задержка натрия и воды, вызывающая системную артериальную гипертензию, и повышенная экскреция калия почками, приводящая к гипокалиемии.
Далее в тексте неоднократно будет идти речь об артериальной гипертензии кошек. В статье использованы категории артериальной гипертензии по классификации IRIS (Табл. 1).
Гиперальдостеронизм дифференцируется на первичный и вторичный. Первичный гиперальдостеронизм также носит название болезни или синдрома Конна. Он характеризуется автономной повышенной продукцией альдостерона патологически измененной клубочковой зоной при одновременном наличии низкой концентрации ренина в плазме. Для животных, страдающих первичным гиперальдостеронизмом, характерно неадекватное увеличение секреции альдостерона, независимое от РААС и концентрации ионов калия в сыворотке крови. Избыток альдостерона в этом случае приводит к угнетению РААС. Увеличение количества внеклеточной жидкости и плазмы воспринимается рецепторами растяжения юкстагломерулярного аппарата, а задержка натрия в сыворотке крови – так называемым «плотным пятном», что приводит в итоге при первичной патологии к снижению биосинтеза и продукции ренина. Подавление активности рениновой системы служит маркером первичности патологии.
Первичный гиперальдостеронизм ассоциирован с новообразованием/ ями коры надпочечников, продуцирующим альдостерон. Новообразование может быть представлено унилатеральной (что наиболее часто характерно для кошек) или билатеральной аденомой или аденокарциномой. В некоторых случаях к болезни приводит билатеральная гиперплазия клубочковой зоны коры надпочечников. «Унилатеральная адренокортикальная неоплазия является наиболее часто описываемой причиной первичного гиперальдостеронизма у кошек, причем аденомы и карциномы у них возникают с примерно одинаковой частотой» [2].
Гистопатологические результаты исследования коры надпочечников при первичном гиперальдостеронизме у кошек могут соответствовать следующим диагнозам:
• унилатеральные или билатеральные адренокортикальные аденокарциномы;
• унилатеральные или билатеральные аденомы;
• идиопатическая билатеральная нодулярная гиперплазия надпочечников.
При вторичном гиперальдостеронизме клетки коры надпочечников не изменены, но обладают повышенной биосинтетической активностью. Вторичный гиперальдостеронизм встречается относительно чаще, и основной его отличительной особенностью является постоянная активация РААС, которая и становится стимулом коры надпочечников для повышенной продукции альдостерона. Предполагать эту болезнь можно у пациентов с развитием, например, сердечной недостаточности, заболеваниями почек, тяжелой гепатоцеллюлярной дисфункцией, которые сопровождаются генерализованным отеком или активацией юкстагломерулярного аппарата. Также одной из причин патологии способно стать низкое содержание натрия в рационе [1]. Эти группы первичных патологий приводят к гиповолемии, снижению ОЦК, что становится непосредственной причиной для синтеза ренина и активации всех звеньев РААС. Следовательно, вторичный гиперальдостеронизм можно встретить также и при многих других заболеваниях, сопровождающихся дегидратацией, гипотензией, сниженной перфузией почек или дефицитом натрия. И в этом случае повышение уровня циркулирующего альдостерона будет напрямую коррелировать с активностью ренина.
Болеют гиперальдостеронизмом обычно кошки среднего-пожилого возраста. Половая и породная предрасположенность к болезни при этом не отмечена. Как упоминалось выше, основными клиническими последствиями избыточной продукции альдостерона становятся усиленная задержка натрия и воды, вызывающая системную артериальную гипертензию, и повышенная экскреция калия почками, приводящая к гипокалиемии. Гиперальдостеронизм, как первичный, так и вторичный, является достаточно ярким примером болезни-причины клинически значимой гипокалиемии умеренно-тяжелого характера, развивающейся по причине потери ионов калия с мочой. Гипокалиемия сопровождается не только снижением концентрации циркулирующих ионов калия, но и приводит также к снижению запасов калия с потерей общего калия организма. Перемещение ионов калия из внутриклеточного пространства во внеклеточную жидкость, в свою очередь, приводит к внутриклеточному движению водородных ионов, повышенной экскреции ионов водорода и развитию метаболического алкалоза. Тяжелый метаболический алкалоз, в свою очередь, способен привести к гипокальциемии и, как следствие, к депрессии сердечно-сосудистой системы, вялости, тетании и судорогам. Неспецифические симптомы, связанные с метаболическим алкалозом, представлены слабостью и дегидратацией.
Физиологический эффект гипокалиемии – это гиперполяризация мембранного потенциала отдыхающей клетки. При гипокалиемии повышается клеточный мембранный потенциал покоя, приводя к увеличенной разнице между потенциалом покоя и пороговым потенциалом, необходимым для потенциала действия и мышечного сокращения. Это вызывает неспособность мышц нормально сокращаться, следовательно, ведущим клиническим признаком является так называемая миопатия, выражающаяся в слабости гладкой и поперечно-полосатой мускулатуры. Проявляться слабость поперечно-полосатой мускулатуры будет эпизодическими или постоянными симптомами, в том числе цервикальной вентрофлексией (Рис. 1), «стопохождением», слабостью тазовых конечностей. Владельцы нередко интерпретируют последнюю проблему как нарушение поведения, так как видят неспособность или нежелание кошки запрыгнуть на те поверхности, которые ранее были для нее легко доступными. Сильная гипокалиемия ( №3–2021 
Гиперальдостеронизм или синдром Конна как причина cтопохождения у кошек
Основной функцией альдостерона является регуляция калия и натрия в сыворотке крови и, соответственно, поддержание необходимого объёма циркулирующей крови за счёт осмотического давления, создаваемого данным гормоном.
Избыток же продукции альдостерона приводит к задержке натрия и воды, что в свою очередь приводит к артериальной гипертензии и к повышению выработки калия почками, приводящая к гипокалиемии.
Гиперальдостеронизм дифференцируется на первичный и вторичный.
Первичный носит название синдром Конна, характеризующийся постоянно повышенной продукцией альдостерона.
Наиболее частая причина синдрома Конна – это новообразования коры надпочечников, продуцирующие альдостерон. Новообразование регистрируется как унилатерально, так и билатерально (с двух сторон), чаще как аденокарцинома или аденома. В некоторых случаях к данному состоянию приводит билатеральная гиперплазия клубочковый зоны коры надпочечников. Подтверждается данный диагноз исключительно гистологическим путём.
Чаще данное заболевание обнаруживается у кошки среднего или пожилого возраста, и основными последствиями избыточного гормона, альдостерона, становится усиленная задержка натрия и воды и к дальнейшей гипокалиемии, далее это приводит к неспособности мышц нормально сокращаться, и основным клиническим признаком становится миопатия, слабость гладкой и поперчено-полосатой мускулатуры что проявляется в виде цервикальной вентрофлексии – стопохождение.
Сопутствующие клинические признаки:
• Илеус
• Атония мочевого пузыря
• Вялость
• Угнетение центральной нервной системы
• Снижение зрения/слепота
• Мидриаз
Гиперальдостеронизм кошек: действительно ли болезнь настолько редка, что не заслуживает нашего внимания?
Список сокращений: ПУ/ПД – полидипсия, полиурия, ГК – глюкоза крови, ЕД – единица действия, ЖКТ – желудочно-кишечный тракт, АПФ – ангиотензинпревращающий фактор, ГКМП – гипертрофическая кардиомиопатия, ОКА – общий клинический анализ крови, Т4о – общий тироксин, СД – сахарный диабет, РААС – ренин-ангиотензин-альдостероновая система, ОЦК – объем циркулирующей крови, МВП – мочевыводящие пути, НО – новообразования, ХБП – хроническая болезнь почек, КПВ – каудальная полая вена.
Аннотация:
Гиперальдостеронизм до недавнего времени считался достаточно редкой патологией эндокринной системы. В 1983 году появились первые сообщения о многочисленных зарегистрированных случаях первичного гиперальдостеронизма или болезни Конна, где приводились доказательства того, что эта болезнь может быть более распространенной, чем ее оценивали в прошлом [16]. В последние годы регистрируется все большее количество сообщений о выявлении данной болезни у кошек. Это также обусловлено тем, что все больше внимания уделяется диагностике вторичной патологии (вторичного гиперальдостеронизма) и тем, что развивается диагностика первичной патологии. Однако до сих пор эту эндокринную болезнь (как первичную, так и вторичную) нельзя назвать широко распространенной. Гиперальдостеронизм – это заболевание, при котором патофизиологические механизмы обусловлены высокой концентрацией циркулирующего в крови альдостерона. В данном случае название болезни говорит само за себя. В ходе изучения этого заболевания следует вернуться к азам физиологии и рассмотреть компоненты и механизмы работы РААС. Эти основы крайне важны для правильного понимания патогенеза гиперальдостеронизма, а следовательно, верного диагностического и лечебного подхода к пациенту.
Альдостерон и РААС
Альдостерон – это минералокортикоидный стероидный гормон, синтезирующийся в клубочковой зоне коры надпочечников из холестерола через ряд промежуточных метаболитов. На долю альдостерона приходится 95% всех гормонов, вырабатываемых клубочковой зоной коры надпочечников [8].
Важно понимать, что регуляция синтеза альдостерона в коре надпочечников обусловлена двумя ведущими механизмами. Первый механизм – это влияние РААС. При этом альдостерон следует рассматривать не как отдельно существующий гормон, а как неотъемлемый компонент этой сложноорганизованной системы. РААС активируется в ответ на снижение объема циркулирующей крови и почечного кровотока. Это приводит к снижению доставки натрия и хлорида к клеткам дистальных канальцев почек и стимулирует секрецию ренина в клетках юкстагломерулярного комплекса. Именно поэтому сниженное кровяное давление, которое воспринимается сначала клетками почек, индуцирует биосинтез и секрецию ренина. Ренин, в свою очередь, расщепляет ангиотензин до ангиотензина I, который затем гидролизуется с образованием ангиотензина II в легких с помощью АПФ и выполняет роль вазоконстриктора. АПФ имеется также в подавляющем большинстве других тканей и в крови, но наибольшая его активность выражена именно в легких. Непосредственно ангиотензин II, образовавшийся в конце этой цепочки, стимулирует секрецию альдостерона. Образующийся альдостерон поступает в кровь и вызывает экскрецию калия и задержку натрия, чем косвенно способствует накоплению воды и повышению кровяного давления. Такой, казалось бы на первый взгляд, сложный механизм схематически можно проиллюстрировать достаточно короткой последовательностью реакций (схема 1).
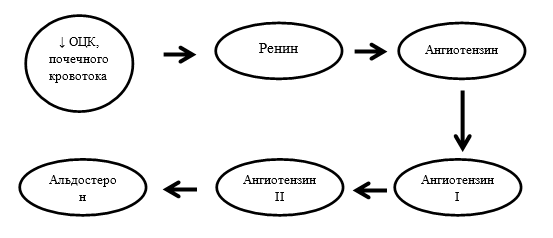
Таким образом, гиперальдостеронизм в случае вторичной патологии станет последним звеном в цепи реакций РААС.
Кроме снижения кровяного давления в афферентных артериолах на фоне снижения ОЦК и почечного кровотока, пусковыми механизмами для синтеза ренина являются:
– снижение концентрации натрия в плазме крови;
– уменьшение осмотического давления в дистальных извитых канальцах;
– стимуляция симпатических нервных волокон, иннервирующих
афферентные артериолы [8].
С тех пор как было показано, что снижение перфузии почек провоцирует секрецию ренина и, как результат, повышение кровяного давления, ренин считается одним из патогенетических факторов гипертензии [4].
Второй, не менее важный механизм регуляции синтеза альдостерона в коре надпочечников – это прямая регуляция через ионы калия, циркулирующие в плазме крови. Увеличение калия в сыворотке крови стимулирует выработку альдостерона корой надпочечников, поскольку этот гормон осуществляет его экскрецию с мочой.
Для чего необходим альдостерон?
Главная физиологическая функция альдостерона – это регуляция гомеостаза натрия и калия в сыворотке крови и поддержание нормального внутрисосудистого объема жидкости. Циркулирующий в крови альдостерон оказывает свое основное физиологическое влияние на почки. Это приводит к реабсорбции натрия, в результате чего задерживается вода, но экскретируются ионы калия и водорода. По мере экскреции калия в моче концентрация калия в плазме снижается. Вследствие этого объемы плазмы и экстраклеточной жидкости увеличиваются совместно с общим периферическим сопротивлением из-за вазоконстрикции, вызванной ангиотензином II, что приводит к повышению кровяного давления. Увеличение объема экстраклеточной жидкости усиливает кровоток в почках, за счет чего снижается секреция ренина.
Как и в предыдущем случае, данная цепочка может показаться сложным физиологическим механизмом, поэтому схематическое упрощение реакций может помочь воспринять каскад реакций (схема 2).
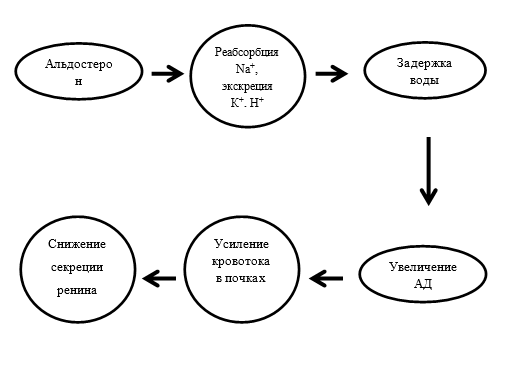
На основании приведенных данных о физиологическом действии альдостерона можно прийти к выводу о том, какие ведущие клинические последствия будут сопровождать повышенные концентрации альдостерона. Избыточное высвобождение альдостерона из клубочковой зоны приведет к различной степени электролитных, жидкостных и метаболических расстройств. Таким образом, основными клиническими последствиями избыточной продукции альдостерона становятся усиленная задержка натрия и воды, вызывающая системную артериальную гипертензию, и повышенная экскреция калия почками, приводящая к гипокалиемии.
Далее в тексте неоднократно будет идти речь об артериальной гипертензии кошек. В статье использованы категории артериальной гипертензии по классификации IRIS (см. табл. 1).
Артериальное давление
Категория гипертензии
Диастолическое
Систолическое
Клинические признаки
Болеют гиперальдостеронизмом обычно кошки среднего и пожилого возраста. Половая и породная предрасположенность к болезни при этом не отмечена. Как упоминалось выше, основными клиническими последствиями избыточной продукции альдостерона становятся усиленная задержка натрия и воды, вызывающая системную артериальную гипертензию, и повышенная экскреция калия почками, приводящая к гипокалиемии. Гиперальдостеронизм, как первичный, так и вторичный, является достаточно ярким примером причины клинически значимой гипокалиемии умеренного и тяжелого характера, развивающейся вследствие потери ионов калия с мочой. Гипокалиемия сопровождается не только снижением концентрации циркулирующих ионов калия, но и приводит также к снижению запасов калия с потерей общего калия организма. Перемещение ионов калия из внутриклеточного пространства во внеклеточную жидкость, в свою очередь, вызывает внутриклеточное движение водородных ионов, повышенную экскрецию ионов водорода и развитие метаболического алкалоза. Тяжелый метаболический алкалоз способен привести к гипокальциемии и, как следствие, к депрессии сердечно-сосудистой системы, вялости, тетании и судорогам. Неспецифические симптомы, связанные с метаболическим алкалозом, представлены слабостью и дегидратацией.
Физиологический эффект гипокалиемии – это гиперполяризация мембранного потенциала отдыхающей клетки. При гипокалиемии повышается клеточный мембранный потенциал покоя, приводя к увеличенной разнице между потенциалом покоя и пороговым потенциалом, необходимым для потенциала действия и мышечного сокращения. Это вызывает неспособность мышц нормально сокращаться, следовательно, ведущим клиническим признаком является так называя миопатия, выражающаяся в слабости гладкой и поперечно-полосатой мускулатуры. Проявляться слабость поперечно-полосатой мускулатуры будет эпизодическими или постоянными симптомами, в том числе цервикальной вентрофлексией (рис. 1), стопохождением, слабостью тазовых конечностей. Владельцы нередко интерпретируют последнюю проблему как нарушение поведения, так как видят неспособность или нежелание кошки запрыгнуть на те поверхности, которые ранее были для нее легкодоступными. Сильная гипокалиемия (
Давление крови у больных кошек может варьироваться от нормального до очень высокого. Симптомы артериальной гипертензии менее специфичны, и их сложнее интерпретировать у наших пациентов, нежели в гуманной медицине. Относительно часто встречается субклиническая гипертензия. Также нередко последствия артериальной гипертензии выражаются в офтальмологических патологиях, которые владельцы кошек способны отметить невооруженным взглядом.
В этом случае заметными для владельцев могут стать:
– снижение зрения (однако при этом стоит учитывать, что владелец, как правило, не в состоянии заметить незначительные нарушения зрения у кошки);
– внезапная слепота, развивающаяся в результате внутриглазных кровотечений или отслоения сетчатки;
– кровоизлияния, видимые невооруженным глазом (рис. 3);
– изменение цвета рефлекса глазного дна.
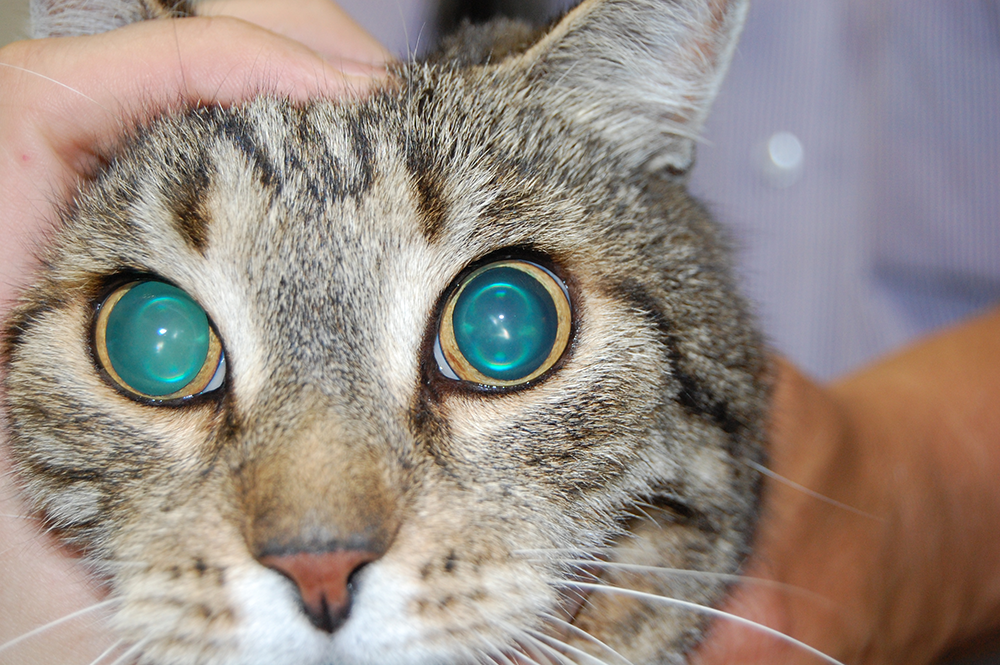
Рис. 2. Мидриаз. Зрачок не реагирует на свет или реагирует вяло. Реакция на ослепляющий свет может отсутствовать или присутствовать. Зрение может отсутствовать или быть сниженным.
Гораздо реже владельцы больных гиперальдостеронизмом кошек отмечают полиурию, полидипсию, снижение массы тела, полифагию. Данные симптомы являются неспецифичными и нередко регистрируются также при других болезнях пожилых кошек.
Поскольку у данной возрастной категории пациентов возможен комплекс сразу нескольких заболеваний, нам могут потребоваться знания о распространенности основных симптомов, специфичных для наиболее часто встречаемых эндокринных патологий. В статье не рассматриваются подробно такие болезни, как СД и гипертиреоз. Но, поскольку эти болезни относятся к разряду более распространенных, чем гиперальдостеронизм, автор статьи привела данные патологии для сравнения основных специфических и неспецифических клинических признаков (табл. 2).
