Акинезия при паркинсонизме что это
Нарушения эмоционального тонуса в той или иной степени были характерны для всех больных, выражаясь в тревоге за свое соматическое состояние, пониженном настроении, не достигая, однако, степени глубокой депрессии или апатии. Создается впечатление, что внешний моторный облик больных несколько гиперболизирует эти черты.
При этом у больных, не имевших выраженной акинезии, можно было обнаружить даже высокую эмоциональную реактивность (гиперэмотивность). Им часто свойственна повышенная внушаемость, которая клинически иногда коррелировала с тревожным состоянием.
Больные же с выраженной акинезией были нередко аспонтанны, эмоционально уплощены и менее внушаемы. Часто выявлялось снижение либидо и потенции. Некоторые больные оценивали себя как педантичных, скрупулезных, сдержанных и в то же время чувствительных и обидчивых.
Реже можно было говорить о явных психастенических проявлениях. В одном наблюдении отмечались обсессивно-компульсивные феномены. Круг интересов соответствовал образованию и воспитанию.
В целом по группе усредненный профиль личности, по данным методики многостороннего исследования личности, имеет характерный код «1—8», обе вершины которого примерно в одинаковой степени выходят за пределы нормальных колебаний, приближаясь к 75 баллам (в Т-нормах). Формальная характеристика такого профиля сводится к констатации особого модуса мышления и поведения личности с затяжными, стабилизированными ипохондрическими тенденциями.
Очень существенным моментом в профиле личности этих больных является высокий уровень на шкале депрессии (в среднем более 70 баллов) при самой низкой точке профиля на 9-й шкале, отражающей степень активности личности. «Паркинсоническая пятерка» также чрезвычайно характерна, но все-таки не патогномонична для паркинсонизма.
Следовательно, кроме приведенной выше характеристики поведение таких лиц отличается низким уровнем активности и интерперсональных отношений. Профиль отражает замкнутость, необщительность, тенденцию к ограничению и уклонению от социальных контактов, недостаточность побуждений, безразличие. Часто это неудовлетворенные, эгоцентрические личности с пессимистическим отношением к своим проблемам и перспективам.
Они чувствуют себя отчужденными и не включенными в общую социальную среду. Эти лица испытывают затруднения в межличностных отношениях.
Обнаружена определенная динамика в структуре личности в зависимости от выраженности акинезии. По нашим данным, у больных с незначительно выраженной гипокинезией профиль личности имеет усредненный код «1—7», при котором поведение заметно определяется тревогой за собственное соматическое состояние.
В группе больных с выраженной акинезией левые и правые шкалы остаются без динамики, за исключением 7-й шкалы, которая уже не является ведущим пиком профиля, а резко опускается, образуя характерный провал между 6-й и 8-й шкалами. Такая динамика в профиле личности говорит о том, что по мере утяжеления акинезии формируется прочный патологический стереотип мышления и поведения. Чем глубже провал на 7-й шкале, тем более ригидна личность, тем меньше она мотивирована к изменению.
Акинезия при паркинсонизме что это
Дополнительные методы исследования используют не только для диагностики заболеваний у лиц, обратившихся за помощью, но и для раннего распознавания стертых и субклинических форм, выявления скрытых носителей патологического гена, изучения распространенности и риска заболевания, наследственной предрасположенности в семьях больных, различных группах населения.
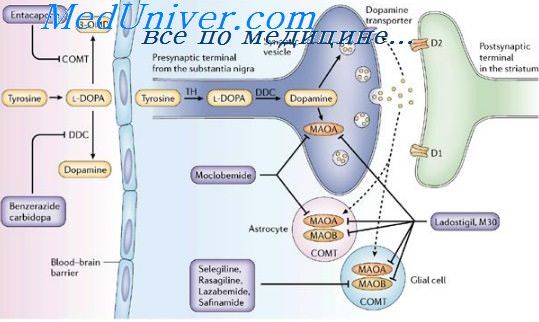
Биохимические методы. Скрининг-тесты исследования мочи и крови позволяют быстро «отсеять» для дообследования лиц с подозрением на искомые метаболические нарушения. В генетике применяются обычные лабораторные способы определения углеводов, липидов и других веществ, индикаторные бумажки (для выявления в моче новорожденных недоокисленных аминокислот и др ), колориметрия, хроматография, электрофорез и другие методы. Исследования способствуют диагностике болезни Вильсона — Коновалова (церулоплазмин в крови, медь в моче), миопатий (мышечные ферменты, аминокислоты), болезни Паркинсона (катехоламины), пароксизмальной миоплегии (калий) и др. Иммунологические методы позволяют распознать иммунодефицитные состояния, антигенную несовместимость плода и матери.
Цитологические, гистохимические и цитогенетические методы используют в диагностике наследственных болезней крови (микроскопия лейкоцитов и эритроцитов), прогрессивных мышечных дистрофий (гистохимия и электронная микроскопия). При изучении полового хроматина в клетках эпителия или нейтрофилах устанавливают аномалии половых хромосом Подсчетом и идентификацией хромосом в культуре лейкоцитов или клеток эпидермиса диагностируют хромосомные болезни.
Электрофизиологические методы применяют для уточнения диагноза эпилепсии и хореи Гентингтона и выявления в семье субклинических форм и предрасположения (ЭЭГ), при миопатий, миотонии, миастении (ЭМГ, исследование электровозбудимости).
Другие методы. Изучение узора кожи пальцев, складок и борозд ладоней (дерматоглифика)—вспомогательный метод диагностики хромосомных болезней. В диагностике нарушений обмена аминокислот и углеводов используется микробиологический метод — свойство некоторых бактерий к росту только при наличии определенных веществ. Для пренатальной диагностики применяют ультразвуковое сканирование и осмотр плода (выявление некоторых уродств), биохимическое и цитогенетическое исследование околоплодной жидкости и крови из пупочных сосудов (установление нарушений обмена и хромосомных аномалий). Ценные результаты дают сочетания клинико-генеалогических, статистических и перечисленных дополнительных методов исследования.
Гипокинезия и акинезия при паркинсонизме
Гипокинезия (акинезия) относится к группе основных симптомов паркинсонизма. Нейрофизиологические механизмы, лежащие в основе гипокинезии, изучены в меньшей степени, а ее клиническое значение часто недооценивается по сравнению с такими симптомами, как тремор и ригидность. Не существует и общепринятого определения акинезии. При описании клинических проявлений паркинсонизма мы уже указывали, что даже по своей феноменологии гипокинезия при этом заболевании представляет собой очень сложный синдром, выражающийся в обеднении, замедлении и уменьшении спонтанной моторной активности.
Следует заметить, что акинетический синдром занимает особое место не только в клинической семиотике паркинсонизма, но в неврологической синдромологии вообще. Клинические прояв-ения акинезии сами по себе не содержат достаточно четких неврологических критериев, которые позволили бы расценивать это нарушение движений как заведомо органическое. Даже при выраженной акинезии невропатолог констатирует достаточно хорошую точность движений, отсутствие истинных паретических явлений, а иногда и отсутствие существенных изменений мышечного тонуса. Ранее некоторые авторы рассматривали акинезию как следствие повышения мышечного тонуса.
При жалобах больного на «скованность» обычно в первую очередь замечается повышение мышечного тонуса, а сопутствующая ему гипокинезия, особенно если последняя слабо выражена, нуждается в специальной объективизации и может остаться незамеченной.
Этот симптом по своей сущности не является демонстративным, напротив — он «скрадывает выразительность» всякого движения и действия. В настоящее время общепризнанной является точка зрения, согласно которой акинез представляет собой совершенно самостоятельное явление, непосредственно не связанное с повышением мышечного тонуса. Акинезия плохо поддается хирургическому лечению, она может даже прогрессировать после ликвидации тремора и ригидности. При тяжелом течении паркинсонизма, особенно в IV стадии заболевания, акинезия является основным фактором, определяющим тяжесть состояния больного.
Еще в 1923 г. описан постэнцефалитический «синдром акинезии без гипертонии». Мы также наблюдали больных паркинсонизмом с тяжелой акинезией при нормальном или минимально измененном мышечном тонусе. Однако гораздо чаще акинезия сочетается с другими симптомами паркинсонизма, причем, в отличие от тремора, она чаще обнаруживает параллельную динамику с мышечной ригидностью (так называемый акинетико-ригидный синдром).
Недостаточная эффективность экспериментального изучения акинезии связана в основном с методическими трудностями, в частности с трудностями количественной оценки гипокинезии, а также с невозможностью дифференцированного выделения психологических и неврологических компонентов в этом едином психомоторном синдроме.
Акинезия при паркинсонизме что это
Одним из самых важных клинических проявлений паркинсонизма любой этиологии является гипокинезия или акинезия, которая в большей степени, чем другие двигательные нарушения при этом заболевании, ограничивает функциональные возможности больного. Как будет показано ниже, гипокинезия коррелирует с наибольшим функциональным дефектом не только в моторных, но и в вегетативных, эмоциональных и сомнических системах мозга больных.
Акинезия является более сильным инвалидизирующим фактором по сравнению с дрожанием или мышечной ригидностью, она в значительной степени определяет общие двигательные возможности больного, в том числе его трудоспособность и способность к самообслуживанию, и, следовательно, степень тяжести всего заболевания.
Поэтому хирургическая ликвидация тремора или ригидности у больных с выраженной акинезией часто не приводит к заметному улучшению их самочувствия или трудоспособности. Акинезия длительное время хуже остальных симптомов поддавалась лечению, и в настоящее время проблема лечения акинезии еще не решена окончательно.
До сих пор существуют трудности количественной оценки гипокинезии. Для решения этой задачи в условиях неврологической клиники мы использовали набор двигательных тестов.
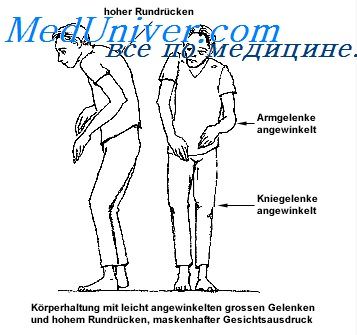
Происходит постепенное обеднение двигательных возможностей больного. Вначале оно проявляется в наиболее сложноорганизованных формах двигательного поведения, уменьшаются и постепенно выпадают те микродвижения, которые придают пластичность и грациозность двигательному акту; движения теряют индивидуальную выразительность; двигательный образ, в норме свойственный каждому человеку (походка и почерк являются его элементами), постепенно распадается за счет его упрощения и оскудения, моторное поведение в целом начинает приобретать черты, свойственные движениям «робота».
Клинические проявления гипокинезии свидетельствуют, по нашему мнению, о том, что больной теряет возможность использовать то бесчисленное множество двигательных программ, с помощью которых в норме достигается инвариантный результат. В норме каждая двигательная задача имеет большое число потенциально возможных способов ее решения. При гипокинезии для больного становится доступной лишь небольшая часть возможных движений.
Сложные движения, требующие одновременного и дифференцированного участия многих мышечных групп (например, естественная пантомимика), выполняются лишь частично; невербальное общение как наиболее сложная форма моторного поведения, по существу, страдает в первую очередь.
Всякое движение можно рассматривать как достаточно сложный двигательный образ, несущий в себе, помимо биомеханической картины, определенное психологическое содержание. Это положение касается не только выразительных телодвижений, специально предназначенных для эмоциональной экспрессии. Достаточно напомнить такой постоянно осуществляемый и автоматизированный моторный акт, как походка, двигательный рисунок которой зависит не только от условий поверхности, по которой идет человек, но и от особенностей актуального психического состояния, темперамента, воспитания, профессии и т. д.
Все движения человека, даже относительно элементарные, являются по своему характеру психомоторными актами.
Неотложные состояния при болезни Паркинсона
Болезнь Паркинсона (БП) – хроническое прогрессирующее заболевание головного мозга, преимущественно связанное с дегенерацией дофаминергических нейронов черной субстанции с накоплением в них белка α-синуклеина и образованием особых внутриклеточных включений (телец Леви), которое проявляется сочетанием гипокинезии с ригидностью, тремором покоя и постуральной неустойчивостью, а также широким спектром немоторных проявлений (психических, вегетативных, сенсорных и др.) [1, 2].
Хроническое медленно прогрессирующее течение процесса при этом заболевании может меняться с развитием острой декомпенсации БП – внезапного нарастания симптомов паркинсонизма, сопровождающегося
существенным ограничением функциональных возможностей пациента и сохраняющегося более 24 часов, несмотря на продолжение или возобновление привычной для пациента противопаркинсонической терапии [3]. Данное расстройство развивается у 0,3-1% больных БП ежегодно, а в 10% случаев приводит к летальному исходу.
— акинетический криз (АК);
— акинетико-гипертермический (злокачественный) синдром (АГС);
— злокачественный нейролептический синдром (ЗНС);
— тяжелые инвалидизирующие дискинезии с гипертермией;
— психоз;
— серотониновый синдром (СС).
Неотложные состояния при БП, в зависимости от состояния и степени вовлеченности дофаминергической системы, условно можно разделить на две группы:
1. Неотложные состояния, возникающие в результате дофаминергического дисбаланса:
А – развивающиеся в период «OFF» или гипофункции дофаминергической системы: синдром паркинсонизм – гиперпирексия или акинетический криз;
Б – развивающиеся в период «ON» или избыточной активности дофаминергической системы: психоз, тяжелая дискинезия с гиперпирексией и т.п.;
2. Неотложные состояния, не связанные напрямую с состоянием дофаминергической системы (серотониновый синдром, электролитные нарушения и т.п.)
Акинетический криз и акинетико-гипертермический (злокачественный) синдром
Акинетический криз – резкое нарастание гипокинезии и ригидности с развитием обездвиженности, спутанности сознания, анартрии, нарушения глотания и вегетативными расстройствами (тахикардия, артериальная
гипотензия, недержание мочи, потоотделение). Для акинетико-гипертермического синдрома характерны симптомы акинетического криза, а также гипертермия (гиперпирексия), вызванная дисфункцией гипоталамуса.
К основным причинам развития АК и АГС относятся:
— изменение дофаминергической терапии;
— блокада дофаминергических рецепторов;
— интеркуррентные состояния;
— нарушение работы системы глубокой электростимуляции (при наличии таковой у пациента).
Точная частота развития АК и АГС не известна. Наиболее цитируемой работой, в которой обсуждается частота встречаемости данных расстройств, является статья M.Serrano-Duenas [4]. Согласно его данным, у 3,6% (11 пациентов из 305) регулярно наблюдаемых им пациентов с БП в течение 9 лет развилось данное расстройство. Среди всех осмотренных за 9 лет пациентов с БП данный процент составил 0,04%. Во всех случаях причиной развития АГС являлась самостоятельная отмена препаратов леводопы без согласования с лечащим врачом. С другой стороны, в исследовании ELLDOPA [5], в которое были включены пациенты с ранней стадией заболевания, в результате двухнедельной отмены леводопы ни у одного из 361 пациента не развился АГС. Данный факт указывает на значение выраженности дегенерации нигростриатного пути, отражающего стадию заболевания в развитииакинетического криза.
Патофизиология акинетического криза окончательно не ясна, однако очевидно, что в основе его развития лежит не только отмена препарата. Особенностью АК является низкая эффективность возобновленной терапии
леводопой, при этом срок начала ответа может достигать 11 дней. Таким образом, во время акинетического криза, по-видимому, развивается временная блокировка ответа на привычную для пациента терапию. В 2014 г. была опубликована работа [6], в которой при помощи SPECT с лигандом [123I] FP-CIT, проведенной до, в период и после акинетического криза, было показано, что в острый период происходит значимое снижение накопления лиганда в пресинаптических терминалях стриатума и его дальнейшее медленное восстановление.
Впервые АГС был описан в 80-е годы ХХ в. у пациентов во время прекращения дофаминергической терапии в рамках проведения «лекарственных каникул». В настоящее время, в связи с пониманием всей опасности «лекарственных каникул», наиболее частой причиной развития АК и АГС называют изменение схемы ранее назначенной терапии (резкое снижение дозы, непропорциональная замена дофаминергического препарата). Прием препаратов, блокирующих дофаминовые рецепторы, таких как типичные нейролептики, метоклопромид, циннаризин, резерпин и др., также может приводить к развитию декомпенсации БП. Более того, существуют сообщения о развитии АК на фоне приема препаратов из группы атипичных нейролептиков. Нельзя забывать и о возможности влияния интеркуррентных заболеваний на течение БП. АГС может развиваться у пациентов с патологией желудочно-кишечного тракта в связи со снижением всасывания дофаминергических препаратов и развития состояния, эквивалентного отмене терапии. К таким состояниям относятся опухоли, резекция кишечника, тяжелые гастроэнтериты, непроходимость. Некоторые сопутствующие заболевания, несмотря на отсутствие прямого влияния на всасывание препаратов, также способны приводить к АК/АГС (инфекции, дегидратация, электролитные расстройства). Основными электролитными расстройствами, способными привести к развитию острой декомпенсации, являются гипо- и даже гипернатриемия, а неадекватная коррекция данных состояний способна вызвать понтинный или экстрапонтинный миелинолиз, усугубив течение АГС. Описаны случаи развития декомпенсации, связанные с менструальным циклом – вероятно за счет отрицательного влияния высокого уровня прогестерона на дофаминергическую систему. В связи с активным внедрением глубокой электростимуляции головного мозга, нельзя забывать о возможности развития декомпенсации у пациентов, перенесших данное оперативное лечение. Акинетический криз может развиться в случае прекращения стимуляции, некорректного программирования стимулятора, разрядки батареи, и даже непреднамеренного отключения стимуляции самим пациентом. При этом описаны случаи развития АГС в результате снижения дозы дофаминергической терапии даже на фоне эффективной глубокой электростимуляции.
Акинетический криз и акинетико-гипертермический синдром – неотложные состояния, требующие срочной госпитализации пациента в отделение интенсивной терапии. При развитии данной патологии в кратчайшие сроки должна быть проведена диагностика возможных интеркуррентных заболеваний (в первую очередь инфекционных), проведен комплекс лабораторных обследований (в первую очередь для исключения водно-электролитного и кислотно-щелочного расстройства). Акинетический криз требует тесного взаимодействия реаниматолога и невролога.
Клиническая картина АГС характеризуется следующими симптомами:
— сроки развития от 18 часов до 7 суток (с момента изменения/прекращения дофаминергической терапии или развития состояния, которое могло спровоцировать декомпенсацию);
— выраженная ригидность/акинезия;
— вегетативные расстройства (тахикардия, тахипноэ, лабильность АД, нарушение мочеиспускания, цианоз, потоотделение);
— через 72-96 часов (в некоторых случаях одновременно с дебютом акинезии) развивается гипертермия (до 41 °С);
— нарушение сознания (от возбуждения до оглушения и комы);
— возможно развитие генерализованных тонико-клонических судорог, миоклоний;
— изменение лабораторных показателей: лейкоцитоз, повышение уровня креатинкиназы (260-50000 Ед/л);
Основными осложнениями АК и АГС являются:
— тромбоз глубоких вен;
— эмболия легочной артерии;
— аспирационная пневмония;
— почечная недостаточность.
Мероприятия, проведение которых необходимо при поступлении больного с акинетическим кризом:
— интубация, проведение ИВЛ (при выраженной дыхательной недостаточности);
— постановка назогастрального зонда, мочевого катетера;
— антибиотикотерапия (в случае выявления инфекционного процесса);
— назначение антипиретиков;
— адекватная инфузионная терапия (коррекция электролитных расстройств);
— гемодиализ (при выявлении почечной недостаточности);
— гепаринотерапия, компрессионный трикотаж (профилактика тромбоза глубоких вен голеней и эмболии легочной артерии);
— позиционирование в кровати (профилактика пролежней).
Основой терапии акинетического криза является восстановление приема дофаминергической терапии в случае ее отмены. Особенности ответа на возобновленную терапию требуют учета следующих аспектов:
— раннее возобновление дофаминергической терапии;
— увеличение исходной дозы дофаминергических препаратов;
— продолжение терапии вне зависимости от наличия ответа (должный ответ может развиться лишь спустя 11 суток);
— невозможность ограничения терапии акинетического криза только дофаминергическими препаратами.
Важным дополнением к терапии является введение раствора амантадина сульфата как препарата, способного снизить активность глутаматной системы, возможно лежащей в основе АГС. Следует придерживаться следующей схемы назначения препарата:
— 500 мл раствора (200 мг амантадина сульфата) 2-3 раза в день в течение 10-14 дней;
— после завершения курса инфузионной терапии обязателен перевод на пероральную форму в таблетках (300-600 мг/сут).
Также в качестве дополнительной терапии рассматриваются апоморфин, дантролен и метилпреднизолон. К сожалению, первые два препарата не зарегистрированы в нашей стране. Метилпреднизолон назначается в дозе 1000 мг/сут в течение 3-5 дней. Терапия метилпреднизолоном существенно улучшает исходы и сокращает сроки акинетического криза. Окончательный механизм действия метилпреднизолона при акинетическом кризе не ясен. В экспериментальной модели на крысах было показано наличие глюкокортикоидных рецепторов на дофаминергических нейронах в вентральной области покрышки, за счет стимуляции которых возможно и развивается эффект метилпреднизолона. Имеется сообщение о применении ротиготина в виде трансдермальной терапевтической системы при акинетическом кризе [7].
Злокачественный нейролептический синдром Злокачественный нейролептический синдром – это ятрогенная, потенциально фатальная патология, которая может развиться на фоне приема любых препаратов, блокирующих дофаминергическую передачу. Чаще всего данный синдром развивается в ответ на прием типичных нейролептиков, однако описаны случаи развития ЗНС и при терапии атипичными нейролептиками. Патогенез ЗНС связан с блокадой дофаминергических структур в базальных ганглиях и гипоталамусе, иммунологическими нарушениями и повышением проницаемости гематоэнцефалического барьера, которые приводят к нейросенсибилизации организма с последующим аутоиммунным поражением ЦНС и висцеральных органов. В патогенезе ЗНС важную роль играет симпатоадреналовая и серотониновая гиперактивность.
Частота встречаемости ЗНС составляет 0,1–1% среди больных, получающих нейролептики. В данную группу попадают и пациенты с БП, течение которой осложнилось психотическими расстройствами. Чаще всего ЗНС развивается в первые дни после начала приема препарата, либо резкого увеличения его дозы. ЗНС может проявиться в любом возрасте, но чаще наблюдается у молодых мужчин. Факторами риска при ЗНС являются интеркуррентная инфекция, физическое истощение, нарушения водно-электролитного баланса (в первую очередь дегидратация), также, как и при АГС.
Клиническая картина ЗНС во многом схожа с АГС: характерно быстрое прогрессирование симптоматики с пиком в течение 72 часов, длительностью 7-14 дней. В случае ЗНС возможно купирование симптоматики без дополнительной терапии.
В 1985 г. Levenson J.L. впервые предложил критерии диагностики данной патологии [8], позже, в 1994 г., новые критерии были предложены в рамках DSM-IV:
Для ЗНС характерны изменения лабораторных показателей:
— повышение креатинкиназы (>90%);
— полиморфонуклеарный лейкоцитоз (75%);
Levenson J.L., 1985
DSM-IV, 1994
Стандарты лечения болезни Паркинсона
Лечение при появлении моторных флуктуаций и/или дискинезий
Уменьшение длительности действия средств, содержащих леводопу. При усилении симптомов паркинсонизма к концу действия очередной дозы средства, содержащего леводопу, прибегают к одной из следующих мер:
Если выбранная мера оказалась неэффективной, следует применить комбинацию препаратов (уровень С).
Замедленное наступление или отсутствие эффекта разовой дозы средства, содержащего леводопу. Если отдельные дозы препарата леводопы, принятые в течение дня, оказываются неэффективными, рекомендуют:
Непредсказуемые колебания эффекта разовой дозы средств, содержащих леводопу, в течение дня (синдром «включения-выключения»). При появлении эпизодов внезапного усиления симптомов паркинсонизма на фоне действия очередной дозы леводопы следует предпринять следующее:
Кроме того, показаны меры, аналогичные рекомендуемым, при замедленном наступлении или отсутствии эффекта разовой дозы средства, содержащего леводопу.
Насильственные движения на высоте действия разовой дозы средства, содержащего леводопу (дискинезия пика дозы). Если на высоте действия препарата леводопы появляются насильственные движения, ограничивающие жизнедеятельность пациента, нужно предпринять следующие действия:
Насильственные движения в начале и конце действия разовой дозы средства, содержащего леводопу (двухфазные дискинезии). При двухфазных дискинезиях нужно предпринять следующие меры:
Дистония, вызванная прекращением действия очередной дозы средства, содержащего леводопу. При болезненных дистониях, вызываемых прекращением действия очередной дозы средства, содержащего леводопу, необходимы следующие меры:
Если, несмотря на коррекцию схемы приема противопаркинсонических средств, сохраняются непроизвольные движения или нестабильность эффекта средств, содержащих леводопу, которые существенно ограничивают жизнедеятельность пациента (снижают трудоспособность или возможность самообслуживания), показана консультация нейрохирурга, специализирующегося в стереотаксической нейрохирургии, для решения вопроса о целесообразности нейрохирургического вмешательства.
Лечение нарушений сна
При пробуждениях, вызванных усилением симптомов паркинсонизма в ночное время (ночная акинезия), прибегают к одной из следующих мер:
При ночной акатизии уменьшают вечернюю дозу средства, содержащего леводопу (уровень С), а если эта мера оказывается недостаточной, то на ночь назначают клоназепам (уровень С). При неэффективности указанных мер дополнительно назначают золпидем, 10–20 мг на ночь (уровень С), антидепрессант с седативным действием (тразодон — 75–150 мг, амитриптилин — 25–50 мг или миртазапин — 15–30 мг) (уровень С).
Лечение больных БП с нарушением познавательных функций
Ухудшение познавательных функций требует в первую очередь оптимизации противопаркинсонической терапии с обеспечением адекватного уровня двигательных функций. Основным противопаркинсоническим средством у больных с выраженными познавательными нарушениями должны быть препараты, содержащие леводопу, которые у этой категории больных реже вызывают побочные эффекты (уровень С). Назначение антихолинергических средств противопоказано в связи с высоким риском ухудшения психических функций и развития психотических расстройств (уровень В).
Кроме того, при ухудшении познавательных функций необходимы:
Для улучшения познавательных функций у больных БП с деменцией могут применяться:
Консультация психиатра и наблюдение за больными с психическими нарушениями показаны при развитии тяжелых психотических расстройств (депрессии, психопатоподобные нарушения, галлюциноз, параноидный синдром, делирий).
При зрительных галлюцинациях на фоне ясного сознания, сохранности ориентации и критики проводится плановая коррекция противопаркинсонической терапии (уровень В). В первую очередь снижают дозу или отменяют недавно назначенное или наименее эффективное средство (уровень В), часто в следующем порядке: холинолитик — селегилин — амантадин — агонист дофаминовых рецепторов — ингибитор КОМТ (уровень С).
При сохранении галлюцинаций следует снизить дозу средства, содержащего леводопу, до минимального эффективного уровня, обеспечивающего необходимый уровень двигательной активности (уровень В). При неэффективности этой меры или невозможности снизить дозу средства, содержащего леводопу, из-за нарастания двигательного дефекта назначается клозапин в дозе от 6,25 до 50 мг на ночь (уровень В); после регресса галлюциноза препарат постепенно отменяют в течение 2–3 нед (уровень С). В течение всего срока лечения клозапином необходимо 1 раз в неделю исследовать содержание лейкоцитов в крови. При снижении их уровня ниже 3 тыс./мкл препарат должен быть отменен.
При неэффективности или непереносимости клозапина вместо него может быть назначен кветиапин, 25–200 мг/сут (уровень С), ингибитор холинэстеразы (уровень С).
При сочетании зрительных галлюцинаций с бредовыми нарушениями или при их возникновении на фоне спутанности сознания с развитием делирия необходимо, помимо указанных выше мер, следующее:
Следует избегать назначения на ночь бензодиазепинов с длительным действием (диазепам, хлордиазепоксид и т. д.), способных спровоцировать спутанность сознания.
Лечение акинетического криза
Акинетический криз — внезапное стойкое усиление гипокинезии и ригидности с развитием обездвиженности и нарушения бульбарных функций (дизартрии и дисфагии), возникающее спонтанно или связанное с прекращением приема, снижением дозы средств, содержащих леводопу, нарушением их всасывания в желудочно-кишечном тракте, развитием интеркуррентной инфекции.
Лечение осуществляется в условиях стационара. Проводится исследование причин акинетического криза (прекращение приема или снижение дозы противопаркинсонических средств, заболевание желудочно-кишечного тракта, вызывающее нарушение всасывания препаратов леводопы, интеркуррентная инфекция, цереброваскулярное заболевание, декомпенсация соматического заболевания).
Лекарственная терапия назначается индивидуально на основании данных анамнеза и ежедневного осмотра пациента. При дисфагии необходимо введение назогастрального зонда для кормления и введения лекарств. Показан комплекс мер по предупреждению пролежней, прежде всего повороты в постели каждые 2 ч, регулярная обработка мест костных выступов камфорным спиртом, использование противопролежневых матрасов.
Если акинетический криз возник в результате внезапного прекращения приема средства, содержащего леводопу, то его следует назначить вновь в более низкой дозе (50–100 мг 3–4 раза в сутки), затем постепенно увеличивать дозу каждые 3 дня до получения эффекта (но не более чем до 700–800 мг леводопы в сутки) (уровень С).
Если акинетический криз возник вследствие снижения дозы, то ее следует увеличить на 100 мг каждые 3 сут до достижения эффекта (но не более чем до 700–800 мг леводопы в сутки) (уровень С).
При дисфагии (но при нормальной функции желудочно-кишечного тракта) препараты леводопы вводят в растворенном виде через зонд.
В качестве дополнительного средства, особенно при нарушении глотания и всасывания препаратов в желудочно-кишечном тракте, назначают амантадина сульфат — 200 мг/500 мл в/в капельно со скоростью 60 капель в 1 мин 1–2 раза в сутки в течение 5–10 дней (уровень С) с последующим обязательным переходом на прием амантадина внутрь (100–200 мг 3 раза в день).
При дегидратации с целью достижения эуволемии вводят физиологический раствор, раствор Рингера, 0,45% раствор хлорида натрия и 5% раствор глюкозы, раствор альбумина, Реополиглюкин (уровень С).
Для профилактики тромбоза глубоких вен голени и тромбоэмболических осложнений показано назначение прямых антикоагулянтов (Гепарин, 2,5–5 тыс. единиц подкожно 2 раза в день или Фраксипарин 0,3 мл подкожно 2 раза в сутки) до разрешения акинетического криза (уровень С).
До восстановления глотания питание проводится через назогастральный зонд. При нарушении функции желудочно-кишечного тракта проводится парентеральное питание.
При появлении дыхательной недостаточности, острой сердечной недостаточности и тяжелой дисфагии, создающей угрозу аспирации, больной переводится в отделение интенсивной терапии, где проводится интубация, а при необходимости и искусственная вентиляция легких. Реабилитация, включающая лечебную гимнастику и массаж, осуществляется после купирования криза и стабилизации состояния.
По вопросам литературы обращайтесь в редакцию.
О. С. Левин, доктор медицинских наук, профессор
РМАПО, Центр экстрапирамидных заболеваний, Москва