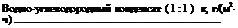Агрессивные физико-химические воздействия
К химически агрессивным веществам по отношению к металлам и древесине можно отнести прежде всего газы-окислители и так называемые окисляющие кислоты и перекиси. Они способны окислять металлы, а при содействии других факторов вызывать горение и гниение древесины.
Окислительные процессы обусловливают ежегодное уничтожение (по всем странам) более 100 млн. г стали и около 300 млн. м 3 древесины только от гниения.
На второе место по объему вызываемых разрушений, преимуществено камней и бетонов, можно поставить действие кислот. Кислоты являются веществами, легко отдающими в раствор ионы водорода (Н), а щелочи — их принимающими.
Способность к отщеплению ионов водорода (протонов) или гидроксилов обусловлена природой элементов, точнее, состоянием поверхностных (валентных) зон электронных оболочек их атомов, что определяется положением атома в периодической системе элементов Д. И. Менделеева.
Высокая активность кислот по отношению к сооружениям объясняется тем, что большинство используемых в строительной технике материалов — цементные бетоны, известковые и цементные растворы, краски — являются слабо щелочными. Металлы в кислых средах разрушаются также много быстрее, чем в щелочных.
Вероятность протекания в жидкой фазе химического взаимодействия между составляющими материала и среды определяется наличием реагирующих ионов, образующих после взаимодействия малорастворимые или малодиссоциированные соединения, выходящие из сферы реакции.
Весьма распространенным частным случаем взаимодействия этого типа будет реакция нейтрализации водородных и гидроксильных ионов с образованием слабодиссоциированного соединения воды:
Известно, что вода или любой химический раствор характеризуется наличием диссоциированных в них ионов водорода и гидроксила, излишек которых определяет кислотность или щелочность воды. Последнюю принято обозначать величиной водородного показателя рН, являющегося логарифмом концентрации водородных ионов с отрицательным знаком:
Значения рН меньше. 7 характеризуют кислые воды, больше 7 — щелочные.
В общем случае наличие в воде-среде ионов, одноименных с теми, которые могут выделяться материалом даже при слабом растворении его водой, как правило, действуют стабилизирующим образом. В частности, растворимость материала в воде понижается и тем значительнее, чем больше концентрация стабилизирующих ионов в растворе (в воде-среде). При этом предполагается,что одноименные ионы не реагируют с другими разнозначными ионами материала по типу нейтрализации или замещения.
Кислоты и кислые газы являются наиболее агрессивными по отношению к металлам, обычным бетонам на щелочной основе, силикатному кирпичу и к осадочным горным породам известнякам, доломитам и т. п.) Керамические изделия, глиняный кирпич и бетоны на жидком стекле хорошо противодействуют кислотам и относительно быстро разрушаются щелочами.
Агрессивность кислот определяется их природой, концентрацией, рН водных растворов, наличием окислительных свойств и температурой среды. Разрушительное действие кислот и кислых газов: определяется также стойкостью (растворимостью) образуемых продуктов коррозии при взаимодействии кислот с металлами или с бетонами.
Действие растворов щелочей во многом прямо противоположно действию кислот. Концентрированные растворы щелочей, особенно при нагреве, разрушающе действуют на некоторые металлы, камни и бетоны. Разрушение камней и бетонов объясняется тем, что в состав некоторых горных пород входят «кислые» включения в виде кремнезема, особенно аморфной формы, или даже рыхлых низкоосновных силикатов; разложение их щелочами приводит к образованию трещин и потере прочности камнем или бетоном с применением такой породы в качестве заполнителя. Механизм разрушения металлов щелочами более сложен.
Действие на металлы, бетоны, керамику и органические материалы (в частности, пластмассы) различных солей менее aгрессивно, чем кислот.
Повышенная скорость коррозии металлов в растворах солей по сравнению с водой объясняется усилением протекания электрохимических процессов и увеличением растворимости продуктов коррозии.
Классификация солей на кислые, нейтральные и основные позволяет в каждом отдельном случае развить представление о существе их агрессивного действия на те или иные материалы. Разрушающее действие растворов солей во многих случаях определяется их способностью взаимодействовать с водой (подвергаться гидролизу) с образованием водородных («кислых») или гидроксильных («щелочных») ионов; при этом в последующем разрушение материала идет так же, как при действии кислот или щелочей.
Действие органических жидкостей — сахаров, масел и растворителей — на отдельные материалы своеобразно. К агрессивным в отношении цементных бетонов следует отнести глюкозиды, т. е. растворы сахара, патоку, фруктовые соки и т. п. При взаимодействии глюкозидов с известью цементного камня могут образоваться растворимые сахараты кальция, что и приводит к довольно интенсивному поверхностному разрушению бетонов. Наиболее агрессивно растворы сахара действуют при брожении, когда в них образуются слабые органические кислоты.
Действие масел на цементные бетоны изучено относительно мало. Известно, что на некоторых производствах, и прежде всего в текстильной промышленности, при систематических проливах смазочных масел наблюдаются сквозные пропитки ими железобетонных перекрытий. При эхом отмечается значительное разрыхление и размягчение бетона иногда до полного его разрушения. Весьма агрессивны по отношению к бетону растительные окисляющиеся и прогорклые масла. По-видимому, здесь имеет место сложное воздействие на бетон имеющихся или образующихся в маслах кислот наряду с физическим процессом размягчения материала.
Органические неполярные жидкости действуют преимущественно на битумы и синтетические продукты, растворяя их.
Лако-красочные материалы — производство
Технологии и оборудование для изготовления красок, ЛКМ
АГРЕССИВНЫЕ СВОЙСТВА СРЕД, ВСТРЕЧАЮЩИХСЯ. ПРИ ДОБЫЧЕ НЕФТИ И ГАЗА
Агрессивные свойства сред при добыче нефти обусловлены наличием в них большого количества минерализованной воды, а также сероводорода и двуокиси углерода. Особенно страдает от коррозии оборудование старых месторождений, в которых с целью увеличения добычи нефти в пласт закачивают высокоминерализованную, а иногда и морскую воду, а также применяют кислотную обработку. Закачивание такой воды в пласт создает благоприятные условия для протекания микробиологических процессов, способствующих жизнедеятельности восстанавливающих сульфат бактерий и появлению в системе сероводорода.
Содержание сероводорода в продуктах старых скважин из года в год растет. Если учесть, что во многих нефтяных скважинах соотношение между пластовой водой и нефтью может возрасти до 100: 1, а содержание сероводорода достигнуть 300—600 мг/л, становится ясным, с какими коррозионно-активным средами приходится иметь дело в нефтяной промышленности. Пластовая вода и нефть образуют часто стойкие эмульсии, которые из-за неравномерного подвода коррозионно-активного электролита (пластовой воды) к поверхности металла способствуют развитию местной коррозии.
Нефть сама по себе, как правило, «е обладает агрессивными свойствами, более того, она часто ингибирует процесс коррозии, образуя тонкие пленки на по-
верхности труб. Однако при больших скоростях движения смеси воды с нефтью ( > 2 м/с) такие пленки смываются. Их защитные свойства можно повысить, если вводить в систему поверхностно-активные вещества, увеличивающие смачивание металла нефтью.
Не менее серьезные коррозионные проблемы возникают и в технологических процессах по переработке нефти. Хотя при первичной подготовке нефти применяются меры к глубокому ее обессоливанию и обезвоживанию, вода и хлориды все же попадают в нефть. При дальнейшей переработке нефти вследствие гидролиза хлоридов магния и кальция, попадающих в нефть из пластовой воды, в системе появляется хлористый водород, отличающийся сильными агрессивными свойствами.
Другим источником хлористого водорода в системе, по данным Лялина [182], являются имеющиеся в некоторых нефтях органические соединения хлора. Поэтому снижение содержания неорганических хлоридов в перерабатываемых нефтях до 20—30 мг/л не исключает агрессивность при последующем нагреве. Серьезные трудности возникают и при защите теплообменной аппаратуры в установках термического крекинга, трубопроводах по перекачке нефти и в особенности воды, нагнетаемой в пласт.
Очень серьезные и трудные для решения проблемы возникают и в газовой промышленности при добыче газа, подготовке его к транспортировке и переработке. Особую остроту эта проблема приобрела за последние годы в связи с открытием в Средней Азии, Оренбургской области и других районах газовых месторождений, в газе которых высокая концентрация сероводорода и двуокиси углерода, что можно видеть из табл. 9,1 [183].
Такой газ является исключительно агрессивным, вызывающим сильную коррозию оборудования газовых месторождений, а также аппаратуры сероочистки и подготовки его к транспортировке и т. д. Транспортировка газа с повышенным содержанием сероводорода по трубопроводам приводит к коррозионному растрескиванию трубопроводов. Такой газ следует предварительно освобождать от сероводорода и воды.
Другим коррозионно-активным агентом при добыче природных газов является двуокись углерода, встречающаяся в некоторых газовых месторождениях. Двуокись углерода, растворяясь в конденсирующейся на поверхности трубопроводов и оборудования воде,
Таблица 9,1- Химический состав газа месторождений Средней Азии
а также конденсате, содержащем низкомолекулярные кислоты, вызывает сильную коррозию.
Углекислотная коррозия характеризуется обычно язвенными разрушениями, а сероводородная — охрупчиванием металла и коррозионным растрескиванием. Сама по себе сероводородная коррозия, с нашей точки зрения, не представляла бы серьезной опасности (сероводород увеличивает коррозию в 2—8 раз), если бы она не сопровождалась охрупчиванием металла.
Установить в настоящее время предельно допустимое содержание сероводорода в газе с позиций коррозионной опасности еще нельзя из-за отсутствия достаточного числа экспериментальных данных. Что же касается углекислого газа, то согласно [166] коррозионно-опасными считаются газы, в которых парциальное давление С02 превышает 2 МПа, коррозионно-неактивными — в которых парциальное давление С02 ниже 5-Ю4 Па. Когда парциальное давление С02 находится между 5 и 2-Ю4 Па, считают, что коррозия может возникнуть. Степень воздействия двуокиси углерода зависит от минерального состава воды, а также наличия низкомолекулярных кислот, в присутствии которых коррозия наступает при меньшем давлении двуокиси углерода. О составе водных конденсатов некоторых месторождений Краснодарского края можно судить по данным табл. 9,2 [184]. Как видно, суммарное содержание агрессивных компонентов превышает 200 мг/л, а среда является слабокислой, при которой и наблюдается рост коррозии.
От коррозии сильно страдают также нефтехранилища, хранилища топлив, баки летательных аппаратов. Наиболее сильная коррозия наблюдается в нижней части хранилища или бака горючего, вследствие попадания в систему воды. Глубокие коррозионные поражения наблюдаются на границе раздела двух несмешивающихся фаз электролит — углеводород. Сильной коррозии подвергается также верхняя часть хранилища в поясах так называемой воздушной подушки. В этой части хранилища коррозия протекает в тонкой пленке электролита, конденсирующейся на поверхности металла в результате температурных перепадов.
В баках для горючего у летательных аппаратов коррозия возникает в результате конденсации влаги на стенах баков при их охлаждении и постепенного стекания воды в нижнюю часть. Иногда воду и соли вносят с недостаточно обезвоженным топливом. Из
Таблица 9,2. Состав водных конденсатов газовых месторождений
Таблица 9,3. Содержание воды и сероводорода в некоторых нефтяных скважинах
баков часто сливают по нескольку литров электролита. Разрушение бензобаков автомобилей в результате накопления в нижней части воды хорошо знакомо автомобилистам.
В рамках данной монографии, к сожалению, невозможно рассмотреть все коррозионные проблемы, с которыми встречаются в нефтяной и газовой промышленности. Мы коснемся лишь тех вопросов, которые имеют непосредственное отношение к проблеме ингибирования. При этом рассмотрим механизм коррозии в двух несмешивающихся жидкостях электролит — углеводород, коррозию в эмульсионных системах углеводород — электролит, а также механизм сероводородной и углекислотной коррозии и методы ингибирования подобных систем.
Интересные данные о коррозионной активности сред в нефтяных скважинах собрала Аракелова [185]. По ее данным (табл. 9,3) большинство старых скважин сильно обводнено и содержит относительно большую концентрацию сероводорода в воде. Такая агрессивная среда естественно должна вызывать сильную коррозию оборудования, что и наблюдается на практике.
Из-за коррозионной усталости часто наблюдаются обрывы глу- биннонасооных штанг, сквозной коррозии подвергаются насоснокомпрессорные трубы, выходят из строя насосы, разрушаются штанговые муфты (табл. 9,4).
Таблица 9,4. Срок службы оборудования в некоторых нефтяных
Число ремонтов В ГОД
Средний срок службы оборудования, мес.
Межремонтный период, сут.
Таблица 9,5. Срок службы оборудования в некоторых нефтяных скважинах [186]
Число обследованных скважин
Число ремонтов скважин в год по причинам
ная, не содержащая H2S Сероводородная
Не менее поучительные данные приведены в работе Негреева [186] (табл. 9,5).
Коррозионные поражения зависят от содержания воды, сероводорода, а также их соотношения. Чем больше в скважине нефти, тем меньше коррозии. В сильно обводненных скважинах применение ингибиторов коррозии может оказаться очень полезным, что видно из опыта применения на некоторых скважинах катапина, И-1-В и ИКНХП [186]. Ингибиторы подавались в скважину путем непрерывной и периодической закачки, а также закачки в призабойную зону скважин. Ингибирующий эффект был довольно высок, обрывы штанг и коррозионные разрушения труб уменьшились в среднем в 2 раза (табл. 9,6).
Можно надеяться, что при испытании ингибиторов на новом оборудовании ингибирующий эффект будет еще более высоким. На это указывают, в частности, высокие защитные свойства, обнару-
Таблица 9,6. Влияние ингибиторов на продолжительность работы подземного оборудования нефтяных скважин [186]
Число обрывов штанг за 1 месяц
Числ ремонтов из-за коррозии труб
Межремонтный период, сут.
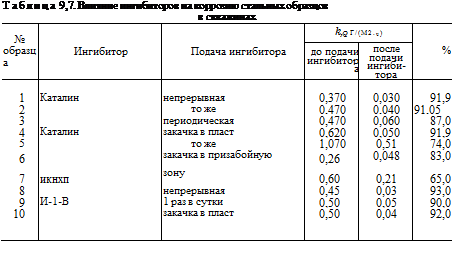 |
женные этими же ингибиторами на образцах свидетелей, которые были помещены в скважины (табл. 9,7).
Как видно, защитный эффект в большинстве скважин достигал 90%, что соответствует 10—15-кратному уменьшению коррозии.
§ 2. УГЛЕКИСЛОТНАЯ КОРРОЗИЯ
Двуокись углерода обычно заметно усиливает коррозию стали, что видно из данных, приведенных ниже:
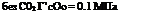
Механизм действия двуокиси углерода еще не совсем ясен. Обычно его связывают с подкислением среды. Однако разрушения, наблюдающиеся в промысловых условиях, намного превосходят те значения, которые следует ожидать, исходя из одного эффекта подкисления.
Скорость коррозии стали на некоторых месторождениях Краснодарского края в начальный период их эксплуатации достигала
В связи с этим нельзя не вспомнить гипотезу, высказанную Луневым [187], о возможности участия двуокиси углерода в процессе катодной деполяризации с восстановлением двуокиси углерода до метана. Справедливость этой гипотезы недавно была доказана для рассолов Фокиным с сотр.
Не исключено, что при высоких давлениях и температурах двуокись углерода выступает в качестве катодного деполяризатора, усиливая этим коррозию. Кроме того, имеют значения и конструктивные особенности аппаратуры: при неудачном конструировании (щели, зазоры, застойные места) коррозия усиливается. Определенное значение имеют в связи с большими скоростями движения
газового потока и эрозионные разрушения. Всеми этими факторами объясняют, почему в реальных условиях в начальный период эксплуатации газоконденсатных месторождений, содержащих двуокись углерода, наблюдались катастрофические разрушения промыслового оборудования. Об агрессивных свойствах электролитов газоконденсатных месторождений, содержащих двуокись углерода, можно судить по данным, которые сообщают Кузнецов, Кутовая, Легезин, Обухова и др. [184—190]. Углекислотная коррозия сопровождалась эрозионными разрушениями, вызванными большими скоростями движения газожидкого потока. Сильно корродируют те элементы оборудования, где скапливается вода. Исследование [188] опытных образцов стали марки Д, установленных в устье газоконденсатных и газовых скважин показало, что при скоростях потока 7—25 м/с, температурах 60—100 °С и содержании в жидкой фазе 20% (об.) углеводородного конденсата скорость коррозии стали в жидкой фазе сильно возрастает по мере повышения парциального давления двуокиси углерода и достигает 3,6 мм/год при Рсо2 =0,3 МПа. При дальнейшем увеличении парциального давления С02 скорость коррозии продолжает расти, однако не в такой сильной степени (при 1,2 МПа — 5,7 мм/год).
Скорости коррозии различных видов арматуры на Некрасовском и Березовском месторождениях составляли от 1 до 5,8 мм/год [188].
С увеличением скорости движения потока в скважине от 2 до 8—10 м/с скорость коррозии возрастает в 1,5—2 раза. Затем наблюдается небольшой спад и дальнейшее увеличение скорости коррозии при больших скоростях потока >20 м/с. Чем выше парциальное давление С02, тем при меньшей скорости ‘Потока наблюдается максимальная коррозия. С уменьшением парциального давления С02 максимальные значения скорости коррозии наблюдаются при больших скоростях потока. По мере обводнения углеводородного конденсата скорость коррозии возрастает. Заметные разрушения начинаются уже при содержании 20% воды. Из пластовых вод, встречающихся в месторождениях Северного Кавказа, наиболее агрессивными являются хлоридкальциевые, насыщенные двуокисью углерода. Менее агрессивными являются натрийгидрокарбонатные.
Сильная коррозия насосно-компрессорных труб некоторых месторождений была связана с поступлением в скважины большого объема высокоминерализованных пластовых вод кислого характера.
По данным Обуховой [189], существенное влияние на углекислотную коррозию подземного оборудования газоконденсатных месторождений оказывают низкомолекулярные карбоновые кислоты — муравьиная, уксусная, нропионовая, масляная, концентрация которых в конденсационных водах может достигать 500 мг/л (от 50 до 90% составляет уксусная кислота). Высокие температуры (80—90 °С) и низкие значения pH (3—5) способствуют развитию сильной коррозии. Уже небольшого количества уксусной кислоты (15—20 мг/л) достаточно, чтобы углекислотная коррозия увеличилась в 1,5—2 раза.
О концентрациях карбоновых кислот, парциальном давлении двуокиси углерода, температуре и скоростях коррозии в газоконденсатных скважинах можно судить по данным, представленным в табл. 9,8.
К счастью, углекислотная коррозия не сопровождается водородным охрупчиванием (двуокись углерода в отличие от сероводорода не замедляет процесс молизации водорода), поэтому приходится думать лишь об уменьшении общей или локальной коррозии. Анализ показывает, что основным коррозионно-активным агентом является двуокись углерода. Карбоновые кислоты, хотя и усиливают коррозию, однако не так сильно, как можно было ожидать, исходя из чисто лабораторных экспериментов. В реальных газоконденсатах, по-видимому, содержатся азотистые соединения, которые обладают, как было выше показано, ингибирующими свойствами.
Таблица 9,8. Скорости коррозии, парциальные давления углекислого газа, температуры и содержание карбоновых кислот в некоторых скважинах
Аммиак
Используется при производстве азотной кислоты, соды, синильной кислоты и многих других неорганических соединений; удобрений; в органическом синтезе; при крашении тканей; в качестве хладагента в холодильниках. 10%-й раствор аммиака известен под названием �нашатырный спирт�. 18-20%-й раствор аммиака называется аммиачной водой и используется в качестве удобрения.
Сжиженный аммиак при испарении охлаждается, и при соприкосновении с кожей возникает отморожение различной степени, а также возможны ожог и изъязвления.
Водород цианистый (синильная кислота)
Отравление кислотой возможно при вдыхании паров и при попадании внутрь организма. В зависимости от концентрации паров и времени их действия различают поражения легкой, средней и тяжелой степени, а также молниеносную форму.
Через кожу проникает как газообразная, так и жидкая фаза синильной кислоты. Поэтому при длительном пребывании в атмосфере с высокой (более 0,5 г/м 3 ) концентрацией кислоты в противогазе, но без средств защиты кожи, появляются признаки отравления.
Соляная кислота (концентрированная)
Концентрированный рас-твор хлористого водорода в воде с максимальной его концентрацией 38-39%. Кипит при 110 0 С. Негорючая агрессивная жидкость, реагирует с металлами с выделением водорода.
Широко применяется в промышленности. По масштабам использования из АХОВ после аммиака и хлора занимает прочное третье место. Обладает высокими токсическими свойствами, при проливах возможно образование очагов химического поражения на значительных территориях.
При контактном воздействии на коже появляются волдыри, пораженные участки имеют серо-белесоватый цвет. На слизистых оболочках глаз возникают воспалительные явления, наблюдается помутнение роговицы. При вдыхании паров наблюдается охриплость, кашель, одышка, боли в груди.
Применяется в производстве хлоридов металлов, синтетических смол, каучуков, органических красителей, гидролизного спирта, сахара, желатина, клея, для дубления и окраски кожи, при производстве активированного (активного) угля, крашения тканей, травления металлов, в металлургии и нефтедобыче.
Отравление происходит обычно не хлористым водородом, а туманом соляной кислоты, образующейся при взаимодействии газа с водяными парами воздуха. Пары действуют на организм как через органы дыхания, так и через кожу.
Для защиты кожи используют костюмы из кислотостойкой ткани, сапоги, рукавицы, перчатки из кислотостойкой резины.
Находит широкое применение в промышленности, в том числе для отбеливания тканей и бумажной массы, в производстве пластмасс, каучуков, инсектицидов, растворителей, в цветной металлургии, а также в коммунально-бытовом хозяйстве для обеззараживания питьевой воды. Ежегодное потребление хлора в мире исчисляется десятками миллионов тонн.
Защиту органов дыхания на месте аварии и на удалении от места разлива или источника заражения до 500 м должны использоваться изолирующие противогазы и дыхательные аппараты.
Фосген
Используются при получении красителей трифенилметанового ряда, поликарбонатных полимеров, полиуретанов; в производстве мочевины и других химических продуктов.
В ряде стран фосген находился на вооружении в качестве запасно-табельного отравляющего вещества.
Используется главным образом для борьбы с вредителями сельского хозяйства, а также в качестве учебного опасного химического вещества при подгонке средств индивидуальной защиты органов дыхания.
В капельно-жидком состоянии может привести к тяжелым поражениям кожи.
Формальдегид
Используется для получения феноло-формальдегидных смол, изопрена, красителей, взрывчатых веществ, лекарств, а также как дубящее, антисептическое и дезодорирующее средство.
При ингаляционном попадании наблюдаются резкий кашель и одышка, которые сопровождаются �давлением в груди�. На фоне нарушения координации движения присутствует двигательное возбуждении, присутствуют тошнота и рвота. Как следствие возникают судороги и нарушение сознания.
При воздействии на кожу наблюдаются дерматиты с образование пузырей. При ингаляционном поражениях возможны тошнота, рвота, �чувство тяжести� в брюшной полости и диарея. В большинстве случаев не наблюдается раздражение верхних дыхательных путей и слизистых оболочек глаз.
В промышленности его получают как побочный продукт при очистке нефти, природного и коксового газа. Применяется в производстве серной кислоты, серы, сульфидов, сероорганических соединений.
Применяется в качестве растворителя жиров, масел, смол, каучука и парафинов.
Используется в производстве серной кислоты, серного ангидрида, солей серной и серноватистой кислот. Применяется в бумажном и текстильном производстве, а также для дезинфекции помещений. Жидкий с ернистый ангидрид может использоваться как хладагент и растворитель.
Особо опасен при вдыхании, возможно поражение слизистых оболочек.
Наиболее частой причиной поражения организма является ингаляционное поступление, однако известны случаи крайне тяжелых и даже смертельных отравлений при кожно-резорбтивном способе попадании газа в организм человека.
При ликвидации проливов необходимо использование средств защиты кожи.
При концентрации 0,4 г/м 3 возникает опасность острого отравления.
Используется в производстве ускорителей вулканизации, средств защиты растений (инсектициды и фунгициды), лекарств, растворителей и красителей, поверхностно-активных веществ.
Опасен при вдыхании, а также в случаях попадания на кожу.
Применяется в синтезе ускорителей для каучуков, как ингибитор кислотной коррозии металлов, при производстве мыла.
Пары газа действуют раздражающе на слизистые оболочки и кожу.
Вызывает сильное раздражение верхних дыхательных путей, при попадании на кожу приводит к возникновению пузырьковых дерматитов.
При ликвидации проливов фтористого водорода обязательно использование изолирующих средств защиты кожи.