Иммунотропные препараты и адаптогены
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Ключевые слова: иммунитет, цитокины, иммуномодуляторы, бактериальные лизаты, адаптогены, антиоксиданты, Трекрезан.
Для цитирования: Маркова Т.П. Иммунотропные препараты и адаптогены. РМЖ. 2019;8(I):60-64.
Immunotropic drugs and adaptogens
Federal Research Clinical Center of the Russian Medical Biological Agency, Moscow
Immunotropic drugs are medications which affect immune system (e.g., stimulate synthesis of immunoglobulins, cytokines etc.). This class includes bacteria- and plant-derived medicines, bee products, hormones, cytokines, mediators etc. Adaptogens are drugs which improve the resistance to various chemical, physical, and biological effects. Adaptogens (which include ginseng, Siberian ginseng, magnolia vine and other plant-derived medicines) stimulate antioxidant protection, reduce metabolic acidosis, prevent accumulation of oxidation products, improve tissue and organ hemodynamics. Mechanisms of action of most adaptogens including their effects on immune parameters still remain elusive. Adaptogens with immunomodulating properties are of special interest. Among these agents, Trekrezan ® is a well-studied drug which provides antioxidant, reparative, anti-inflammatory, antitoxic, and energy-stabilizing (anti-asthenic) effects. Trekrezan ® is a low-toxicity drug. Its efficacy was demonstrated in various preclinical and clinical trials. Further studies on Trekrezan ® from the viewpoint of evidence-based medicine will elucidate its mechanisms of action in various immune disorders.
Keywords: immunity, cytokines, immunomodulators, bacterial lysates, adaptogens, antioxidants, Trekrezan.
For citation: Markova T.P. Immunotropic drugs and adaptogens. RMJ. 2019;8(I):60–64.
Статья посвящена возможностям применения иммунотропных препаратов и адаптогенов.
Иммунотропные препараты
Иммунотропные препараты относят к лекарственным средствам c доказанным воздействием на различные звенья иммунной системы или выработку цитокинов, антител. Первым официальным препаратом с доказанным in vitro и in vivo эффектом у животных и человека был левамизол, его изучение началось в 1960-х гг. За 60 последующих лет появились новые препараты, в фармакологических справочниках была выделена фармакотерапевтическая группа иммунотропных препаратов.
В 1995 г. в реестр медицинских специальностей была введена специальность «аллергология и иммунология» (приказ Минздравмедпрома РФ от 16.02.1995 г. с утверждением прав и обязанностей врача аллерголога-иммунолога). В приказе Минздрава России от 20.12.2012 г. № 1183Н «Об утверждении номенклатуры должностей медицинских работников» был уточнен порядок подготовки кадров по этой специальности. В права и обязанности врача аллерголога-иммунолога входит диагностика, лечение и реабилитация больных с аллергическими и/или иммунодефицитными заболеваниями. Аллерголог-иммунолог направляет и оценивает результаты иммунологического обследования пациента (включая иммунограмму) и может назначать иммунотропные препараты в комплексном лечении.
Многочисленные исследования подтверждают эффекты иммунотропных препаратов, которые могут назначаться в острый период заболевания вместе с этиотропной терапией либо после ее окончания. Предпочтительно курсовое назначение препаратов, длительность курса определяется на основании утвержденной инструкции и результатов иммунологического обследования пациента. С целью профилактики иммунотропные препараты можно назначать как монотерапию. Многие иммунотропные препараты прошли клинические исследования с позиций доказательной медицины (двойной слепой контроль с назначением плацебо пациентам контрольной группы): механические и химические бактериальные лизаты, интерфероны (ИФН), синтетические бактериальные лизаты, инозин пранобекс, лечебные моноклональные антитела и др.
Единой общепринятой классификации иммунотропных препаратов пока нет. Свои классификации предложили авторы: Хаитов Р.М., Пинегин Б.В. (1996); Ширинский В.С. (1997); Нестерова И.В., Сепиашвили Р.И. (2000); Нестерова И.В., Старченко А.А., Иванова С.А., Симбирцев А.С. (2002); Маркова Т.П. (2003) [1–4].
В таблице 1 представлена классификация иммунотропных препаратов с учетом их происхождения [1] и приведены наиболее известные средства. Ряд препаратов в настоящее время имеет историческое значение. В практике чаще используют бактериальные лизаты, препараты растительного происхождения, интерфероны и индукторы выработки интерферонов.

Среди иммунотропных препаратов растительного происхождения изучены лекарства, полученные из эхинацеи (Echinacea angustifolia и Echinacea purpurea), родиной которой является Северная Америка. Индейцы использовали эхинацею в лечении инфекционных заболеваний, для заживления ран, ускорения выздоровления больных. Растительные препараты более безопасны, но не надо забывать о возможности развития лекарственной непереносимости. Растительные препараты менее эффективны и требуют более длительного приема. Сочетание экстракта эхинацеи и витамина С повышает эффективность [5]. Изучены также иммунотропные свойства прополиса и, в меньшей степени, меда. Прополис усиливает фагоцитоз, стимулирует созревание лимфоцитов в тимусе. Есть данные, что мед также стимулирует фагоцитоз [6, 7].
С 1970-х гг. в клинической практике стали использовать бактериальные лизаты. Препараты были получены из бактерий, наиболее часто высеваемых из дыхательных путей при респираторных инфекциях. Некоторые представители данной группы (например, бактериальный липополисахарид) в настоящее время уже не применяются. Предполагалось создание специфических вакцин, но изучение свойств и механизма действия бактериальных лизатов подтверждало их иммунотропный эффект и указывало на отсутствие формирования стойкого протективного иммунитета против возбудителей, из которых были изготовлены лизаты. Более правильно называть эти лекарственные средства бактериальными иммуномодуляторами, их можно подразделить на препараты системного и местного действия. Большинство бактериальных лизатов получены химическим путем. Исключение составляет механический лизат, полученный методом механического воздействия на бактерии, что приводит к сохранению и повышению иммуногенности.
Клинический эффект бактериальных лизатов направлен прежде всего на снижение числа и тяжести респираторных инфекций. Механизм действия связан, с одной стороны, с выработкой специфического IgA и фиксацией на слизистых, а с другой стороны — с активацией иммунной системы (Т-, В-клетки, макрофаги, дендритные клетки). Гибель инфицированных клеток и патогенов усиливается после активации макрофагально-фагоцитарного звена, цитотоксических Т-, ЕК-клеток [8, 9].
При респираторной инфекции бактериальные антигены взаимодействуют с TLR-рецепторами на поверхности дендритных клеток, что приводит к их созреванию, активации и миграции в лимфатические узлы. Дендритные клетки регулируют дифференцировку Th0-лимфоцитов в Th1, Th2 или Т-регуляторные клетки. Дендритные клетки стимулируют Тh1-лимфоциты, синтезирующие ИФНγ при повышении уровня ИЛ-12 у больных ОРЗ. При низком уровне ИЛ-12 дендритные клетки стимулируют дифференцировку Th2-лимфоцитов, синтез ИЛ-2, ИЛ-4 и пролиферацию В-лимфоцитов. Образующиеся плазматические клетки синтезируют специфические IgA и s-IgA, обеспечивающие целостность слизистых и опсонизацию патогенов [10, 11].
Бактериальные лизаты можно назначать в острый период ОРЗ в сочетании с этиотропной терапией, для профилактики ОРЗ их можно использовать как монотерапию [1, 12–14, 8]. Приведенные данные показывают широкий спектр иммунологических взаимодействий, в которых могут участвовать иммунотропные препараты, включая межклеточные взаимодействия, синтез цитокинов, ИФН.
Адаптогены
В народной медицине можно найти рекомендации для больных по назначению женьшеня, элеутерококка, лимонника и других растительных препаратов, ускоряющих выздоровление после вирусных инфекций, уменьшающих астенизацию. Эти препараты относятся к адаптогенам, повышающим сопротивляемость организма к различным воздействиям (физическим, химическим, биологическим), но, к сожалению, механизмы их действия и влияние на иммунную систему изучены недостаточно.
Единственный хорошо изученный адаптоген — это синтетический препарат оксиэтиламмония метилфеноксиацетат (триэтаноламмониевая соль 2-метилфеноксиуксусной кислоты), выпускаемый отечественной компанией Solopharm под торговым названием Трекрезан ® . Данный препарат относится к фармакотерапевтической группе адаптогенов и обладает воздействием на иммунную систему. Препарат был создан в Иркутском институте органической химии СО РАН, зарегистрирован в 1994 г. и защищен авторскими свидетельствами и зарубежными патентами. В экспериментах in vitro показано, что Трекрезан ® повышает цитокиновую активность суммарной триптофанил-мРНК-синтетазы (ТРСазы) через стимуляцию синтеза специфической матричной РНК-синтетазы. Взаимодействуя с цитоплазматическими мембранами клеток, препарат стабилизирует их, изменяя ион-ионные и ион-дипольные взаимоотношения в липопротеиновых комплексах, что приводит к запуску каскада эндоплазматических процессов, усиливая синтез белков. Большое значение имеет усиление синтеза триптофана, ускорение синтеза иммуноглобулинов и других белков. Препарат малотоксичен, обладает также антиоксидантным, репаративным, противовоспалительным, антитоксическим, энергостабилизирующим (антиастеническим) эффектами [15–18].
Различия между иммунотропными препаратами и адаптогенами
Необходимо отметить определенные отличия в воздействии иммунотропных препаратов и адаптогенов на иммунную систему. На примере бактериальных лизатов мы видим их влияние на дендритные клетки, Т-, В-клетки, синтез цитокинов, синтез и фиксацию на слизистых IgA
[8, 12–14, 19, 20]. В доступной литературе нет данных о репаративных, антиоксидантных эффектах, воздействии баклизатов на воспаление, гемодинамику. Адаптогены обладают антиоксидантным, репаративным, противовоспалительным, антитоксическим, энергостабилизирующим (антиастеническим) эффектами [15–18, 21].
Краткий обзор доклинических исследований препарата Трекрезан ®
Воздействие препарата Трекрезан ® на иммунную систему изучено в доклинических исследованиях на различных видах животных. При пероральном введении препарата Трекрезан ® индюшатам и цыплятам в дозе 10–50 мг/кг в течение 28 дней повышались уровень γ-глобулина, бактерицидная активность сыворотки крови и фагоцитарная активность лейкоцитов. Влияние на адаптогенные и стрессопротекторные механизмы исследовали на крысах после создания стрессовых ситуаций (лишение воды в течение суток). У крыс, получавших препарат, были менее выражены повреждения структуры клеток печени, селезенки, быстрее восстанавливалась микроструктура надпочечников и капилляров [15]. У интактных мышей линии CBA и гибридов B6D2F1 соответственно высоко- и низкочувствительных к Т-зависимому антигену, при введении препарата Трекрезан ® в индуктивную фазу развития иммунного ответа отмечали повышение синтеза IgM АТ и снижение выраженности реакций гиперчувствительности замедленного типа [22]. Внутрибрюшинное введение препарата Трекрезан ® мышам в дозе 25 мг/кг уже через 6 ч приводило к повышению синтеза ИФНα, а затем ИФНγ (табл. 2). Различия были достоверны по сравнению с данными показателями у животных контрольных групп, которые получали плацебо (физиологический раствор) или полинуклеотид И:Ц (положительный контроль). Через 6 ч у мышей наблюдали повышение уровня ИФНα, а через 24 ч уровень ИФНα снижался, но увеличивался уровень ИФНγ, различия были достоверны по сравнению с данным показателем у мышей, получавших плацебо, и мышей, получавших полинуклеотид И:Ц (положительный контроль). У мышей, получавших полинуклеотид И:Ц, наблюдали только повышение синтеза ИФНα [17]. При моделировании на крысах бронхолегочного воспаления показано, что препарат Трекрезан ® в дозе 25 мг/кг уменьшал воспаление, что сопровождалось снижением уровня лактата, АДФ, АМФ и повышением уровня пирувата и АТФ в лимфоцитах крови и легочной ткани [23].

Клинический опыт применения препарата Трекрезан ®
При назначении препарата Трекрезан ® больным в острый период гепатита В на 15–16-й день в дозе 0,1 г 3 р./сут в течение 21 дня отмечена нормализация биохимических показателей в период ранней реконвалесценции по сравнению с данными показателями у пациентов контрольной группы. Отмечено повышение числа Т-киллеров, уровня ИФНα в сыворотке крови у 78,9% больных, снижался уровень ИЛ-1β, циркулирующих иммунных комплексов, антител к ДНК, вирусной нагрузки. Через 12 мес. у 89,5% больных, получавших исследуемый препарат, ДНК вируса гепатита не определялась, у 5,3% (2 человека) больных ДНК вируса определялась, был диагностирован хронический гепатит В. В контрольной группе хронический гепатит В диагностирован у 12,4% больных (проба на ДНК вируса была положительной) [22].
У больных туберкулезом при назначении препарата Трекрезан ® в комплексном лечении по 0,2 г 3 р./сут в течение 25–90 дней в зависимости от формы заболевания наблюдали улучшение самочувствия, ускорение рубцевания в области каверны, рассасывание инфильтратов легочной ткани. Контрольная группа из 30 человек была сходной по клиническим проявлениям туберкулеза. В ходе исследования у 33 больных с посттуберкулезным пиелонефритом, которые получали препарат Трекрезан ® в течение 25 дней, отмечено улучшение самочувствия, лабораторных показателей по сравнению с данными показателями у пациентов контрольной группы. При назначении 30 женщинам с туберкулезным аднекситом препарата Трекрезан ® в течение 45 дней отмечено улучшение самочувствия, уменьшение размеров инфильтратов, повышение уровня сывороточных IgG, IgM, IgA, количества Т-клеток (66,4±1,5%), уровня лизоцима (9,01±0,22 мкг/мл) у 22 больных. Положительная динамика показателей и клинических проявлений в контрольной группе отмечена только у 6 человек [22].
Антиастеническое действие препарата Трекрезан ® может быть использовано у больных с постинфекционной астенией при развитии тканевой гипоксии и метаболического ацидоза. Недостаток кислорода приводит к нарушению энергетического обмена клеток и накоплению продуктов ацидоза (молочной кислоты), что снова снижает способность к усвоению кислорода, усугубляет ацидоз и способствует формированию метаболического порочного круга, лежащего в основе астенического синдрома [21].
У больных с ишемической болезнью сердца и развитием хронической сердечной недостаточности назначение препарата Трекрезан ® в комплексе с нитратами улучшало показатели гемодинамики, состояния капилляров, снижало показатели ПОЛ. Известно, что гидроперекиси липидов ухудшают состояние мембран клеток, что приводит к нарушению регуляции мышечных сокращений [24].
Заключение
Разнообразие иммунотропных препаратов и адаптогенов ставит задачу изучения механизмов действия и определения показаний к их назначению. Препарат Трекрезан ® относится к адаптогенам и обладает иммуномодулирующим действием, что повышает его клиническую значимость. Препарат малотоксичен. Его действие изучено в ряде доклинических исследований на различных животных моделях, а также в клинических исследованиях с участием здоровых добровольцев, ликвидаторов аварии на Чернобыльской АЭС и пациентов с различной инфекционной патологией (вирусные гепатиты, туберкулез, герпес-вирусная инфекция, хронический трихомониаз). Показано антиастеническое действие препарата, которое может быть использовано в терапии больных с постинфекционной астенией. Необходимо проведение дальнейших исследований по применению препарата Трекрезан ® с позиций доказательной медицины, которые позволят уточнить механизмы действия препарата при различных иммунозависимых заболеваниях.
Только для зарегистрированных пользователей
Средства для повышения иммунитета
Вопрос иммунитета актуален сегодня, как никогда. Есть ли препараты для его усиления? Как правильно это сделать без вреда для здоровья?
Что влияет на иммунитет
Так как иммунитет — это комплекс реакций всего организма для защиты от внешних вторжений, на его работу влияет множество факторов. Сюда можно отнести:
Все эти факторы влияют на иммунитет в комплексе. Если, какое-то воздействие избыточно и организм не может с ним справиться в пределах нормальной реакции, могут возникать сбои, которые приводят в том числе и к снижению иммунитета. Например, короткий контролируемый стресс в виде закаливания, тренировки, некоторого периода голода простимулирует организм и поможет укрепить иммунитет.
Если стресс хронический, например, эмоциональный, это приводит к истощению нервной системы, разбалансировке гормонального фона и, естественно, отражается на иммунной системе. Так в исследованиях было показано, что после хронического стресса при контакте с вирусом, типа ОРВИ, у этих людей развивались выраженные симптомы, как слабость, выделения из носа. У другой группы, без воздействия стресса эти симптомы были минимальны или отсутствовали.
Значительная часть бактерий и вирусов поступает в организм через пищеварительную систему. Если нарушена работа ферментов, кислотность, микрофлора, повышена проницаемость кишечной стенки, есть воспалительные процессы, ослаблен местный иммунитет, тогда может снижаться защитная функция и чужеродные агенты могут попасть в кровь.
Гормональные препараты, вредные привычки, инфекции могут ослаблять иммунитет. Часто мы забываем о таком важном элементе здоровья, как сон. Недостаток сна и его нарушения, также могут снижать защитные силы организма.
Нарушения иммунитета
Изменения в работе иммунной системы можно разделить на 2 вида:
Во втором случае запускаются процессы воспаления, которые повреждают собственные ткани организма. Речь идет о таких проблемах, как:
Разберем более подробно ситуацию снижения иммунитета.
Низкий иммунитет
Как понять что иммунитет ослаблен и надо срочно что-то делать? Многие слышали такое понятие, как ЧБД — часто болеющие дети. Родители считают количество ОРВИ в год и если оно превышает 4 раза начинают волноваться. Но ВОЗ считает нормой у детей посещающих детский сад и младших школьников цифру 8, если это обычная простуда.
Насторожить как у детей, так и взрослых должны:
Проблемы с иммунитетом могут быть врожденного характера, связанные с генетическими особенностями, или приобретенного, то есть возникшие в процессе жизни.
Что делать
Кажется, что если иммунитет низкий, нужно срочно его повысить. Благо в аптеке можно найти множество иммуномодуляторов с обещанием сделать иммунитет сильнее. Прежде чем глотать таблетки, можно обратить внимание на факторы риска. Ведь без их устранения улучшения могут быть только временными. Это будет все равно что стучать молотком по пальцу, но каждый раз потом накладывать лечебную мазь. Может сначала стоит убрать молоток.
Выполнить все рекомендации мало кому удается, поэтому хочется прибегнуть к достижениям современной науки.
Препараты
Непосредственно к иммуномодуляторам можно отнести только те продукты, которые непосредственно модулируют, то есть напрямую действуют на какие-то звенья иммунитета. В идеале, они должны приводить его работу в норму. Все остальные как витамины, БАДы, адаптогены могут оказывать влияние на иммунитет, но называть их иммуномодуляторами не совсем корректно.
Иммуномодуляторы
Идеального иммуномодулятора, который бы при приеме приводил в норму все звенья иммунитета пока не существует. К настоящим иммуномодуляторам на сегодняшний день можно отнести:
Эти молекулы действуют на конкретные звенья иммунной цепи и их действие относительно изучено.
Лизаты
Витамины и микроэлементы
Витамин D обладает очень широким спектром действия на весь организм, а не только на состояние костей и мышц. Если рассматривать его влияние на иммунитет, то здесь он способствует снятию воспаления за счет блокирования взаимодействия между клетками иммунитета. При его дефиците растет риск аутоиммунных заболеваний (ревматоидный артрит, системная красная волчанка, сахарный диабет 1 типа). Витамин D обладает иммуномодулирующими свойствами и может повышать гуморальный и клеточный иммунитет. Существуют водо- и жирорастворимые формы холекальциферола. При нарушении работы пищеварения может нарушаться его усвояемость.

Витамин С оказывает стимулирующее действие на иммунную систему. Под его действием нейтрофилы увеличивают свою способность распознавать и уничтожать бактерии и вирусы. Аскорбиновая кислота нужна для синтеза эндогенных интерферонов и цитокинов. Комбинация витаминов А,С и цинка стимулирует выработку антител.
Цинк участвует в процессах влияющих на синтез Т-лимфоцитов, стимулирует фагоцитарную активность нейтрофилов. Запасов цинка в организме нет, он должен поступать с мясом, бобовыми, сырами.
Комбинированные препараты
Многие витамины и минералы обладают синергетическим эффектом. При недостатке одних, прием моно препарата может быть неэффективным. Для этого производители выпускают комплексные сбалансированные продукты:
БАДы
Обычно БАДы включают в себя различные вытяжки из трав с адаптогенным эффектом. Нередко их комбинируют с витаминами.
Интерфероны
Эта группа препаратов также очень распространена в России и на постсоветском пространстве. Западные коллеги не разделяют нашего оптимизма по использованию данной группы препаратов и применяют её в редких случаях при определенных заболеваниях. Но не у обычных людей с симптомами ОРВИ и тем более не для профилактики.
На нашем рынке представлены:
Вывод
Просто так принимать средства напрямую усиливающие иммунитет не следует. Это может спровоцировать аллергические и аутоиммунные реакции. Лучше заняться общим укреплением здоровья, правильным питанием, восполнением дефицита витаминов и микроэлементов. Если вы подозреваете серьезные проблемы с иммунитетом обратитесь к иммунологу, пройдите профосмотр.
Адаптогенными свойствами что это
Забайкальский край по природно-климатическим условиям относится к региону с экстремальными условиями жизни, что вызывает напряжение адаптационных механизмов у населения края. Одним из основных факторов риска развития заболеваний забайкальцев является экзогенная гипоксия. При гипоксии к основным повреждающим механизмам относятся активация свободно-радикального окисления, избыточная продукция активных форм кислорода, внутриклеточное накопление свободных радикалов, оказывающих повреждающее действие на целостность и функционирование мембран клеток организма, истощение антирадикальной защиты, обозначаемых как «оксидантный стресс» [4, 7]. Образованию свободных радикалов способствуют многие процессы, сопровождающие жизнедеятельность организма: стрессы, экзогенные и эндогенные интоксикации, влияние техногенных загрязнений окружающей среды и ионизирующего излучения, в том числе и повышение концентрации гомоцистеина.
Поэтому актуальной задачей современной медицинской науки является поиск биологически активных веществ с антиоксидантной и антигипоксической активностью. В данном аспекте наибольший интерес представляют растительные адаптогены, так как они легко включаются в биохимические процессы организма человека, оказывают многостороннее, мягкое, регулирующее и безопасное действие на его организм при длительном использовании.
Помимо вышеперечисленных эффектов, вещества, входящие в состав корня, проявляют Р-витаминную активность (дубильные вещества, флавоноиды); обладают спазмолитическим, болеутоляющим (сапонины, алкалоиды) действием, понижают кровяное давление, обладают антиаритмическим, успокаивающим, кардиотоническим, капилляроукрепляющим (сапонины, флавоноиды) действием, способствуют понижению отрицательного влияния на организм токсических химических соединений и радиоизлучений, выводят из организма соли тяжелых металлов, радионуклиды и другие токсины (дубильные вещества, флавоноиды) [1, 2, 3, 5, 6].
Важной особенностью травы астрагала является способность накапливать органический селен из почвы в количестве примерно в 5000 раз большем, чем это доступно другим растениям того же региона. В траве астрагала кроме селена содержится почти весь спектр необходимых человеку минералов и антиоксидантов (витамины А, Е, С; аминокислоты, биофлавоноиды, полисахариды, терпены и т.д.) [8].
Женьшень (Panax ginseng) используется Восточной медициной уже несколько тысячелетий. Произрастает в Приморье, Корее, Китае. Согласно современным представлениям [5, 6], гликозиды женьшеня имеют разные рецепторы-мишени как на плазматической мембране, так и внутри клетки. Взаимодействие с этими рецепторами приводит к регуляторному изменению метаболических процессов в различных органах и тканях. Гликозиды женьшеня в зависимости от структуры способны, подобно мембраноактивным комплексонам, взаимодействовать с компонентами мембран и, подобно гормонам, связываться и активировать внутриклеточные рецепторы стероидных гормонов, вызывая экспрессию специфических генов. В экспериментальных исследованиях полисахаридные фракции женьшеня повышают фагоцитарную активность макрофагов, продукцию эндогенного интерферона, а также показатели клеточного и гуморального иммунитета, вследствие чего повышается устойчивость животных к экспериментальной инфекции. Иммуномодулирующее действие препаратов женьшеня может быть также связано с индуцирующим воздействием полисахаридных фракций женьшеня на синтез эндогенного оксида азота. Помимо полисахаридной фракции определенную роль в иммуномодулирующем действии женьшеня играют гликозиды (гинсенозиды), обладающие преимущественно антиоксидантным действием. Возможно, именно с защитным действием гинсенозидов на мембраны лимфоцитов связан их иммуностимулирующий эффект.
Целью нашего исследования явилось изучение роли препаратов, полученных из корня молочая Фишера, астрагала и женьшеня в регуляции процессов перекисного окисления липидов и антирадикальной защиты при нормоксии, гиперкапнической нормобарической гипоксии и в условиях гипергомоцистеинемии.
Материалы и методы исследования
Экстракт и настойку из корня молочая Фишера получали из предварительно очищенного от смол сырья. Экстракт (ЭМФ) получали путем 4-этапного экстрагирования методом горячего хлороформно-спиртового извлечения (Патент РФ RU 2009102886, А, А61К36/00 «Способ получения биологически активного экстракта из корня молочая Палласа»). Настойку (НМФ) получали путем спиртового извлечения из растительного сырья без нагревания и удаления экстрагента согласно ГФ XI (1990 г.). Также в наших опытах мы использовали фармакопейные настойку женьшеня (НЖ) и настойку астрагала с женьшенем (НАЖ). Все настойки деалколизировали перед введением.
Исследования проводили на 110 белых лабораторных крысах средней массой 168,0 ± 20 г, которые были разделены на 11 групп по 10 в каждой, для оценки состояния активности процессов перекисного окисления липидов и антиоксидантной защиты в норме, в условиях гиперкапнической гипоксии и гипергомоцистеинемии.
Животные содержались в стандартных условиях вивария, оборудованного в соответствии с санитарными требованиями № 1045-73 от 06.04.73, получали стандартный корм и воду без ограничения. Эксперимент проводили на минимальном количестве животных в соответствии с требованиями «Международных рекомендаций по проведению биомедицинских исследований с использованием животных» принятыми Международным Советом Медицинских Научных Обществ (CIJVS) в 1985 г. По окончании эксперимента животных усыпляли передозировкой фторотанового наркоза.
Все опытные животные получали в течение 5 суток исследуемые препараты. Дозы экстракта и настойки молочая Фишера были определены в предварительных исследованиях на острую токсичность.
Гиперкапническую нормобарическую гипоксию моделировали методом Ковалева Г.В. (1990) в условиях гермокамеры [7].
Модель гипергомоцистеинемии формировали внутрибрюшинным введением гомоцистеина в дозе 0,001 мг на 1 мл ОЦК в течение 10 дней. Уровень гомоцистеина определяли методом ВЭЖХ.
В работе использованы следующие методы исследования:
1. ТБК-тест по методу Л.И. Андреевой с соавт. (1988).
2. Реакция хемилюминесценции по методу Ю.А. Владимирова, (1972). В работе использовали хемилюминометр BioOrbit 1251, диспенсер LKB 1291, аналогово-цифровой преобразователь фирмы Ampersand Ltd, программно-аппаратный комплекс МультиХром для Windows, версия 1.52k.
3. Показатель резервного времени жизни в условиях летальной гиперкапнической нормобарической гипоксии по методу Г.В. Ковалева (1990).
Статистическую обработку данных проводили методами непараметрической статистики с использованием критериев Вилкоксона и Манна-Уитни и Стьюдента (пакет программ Statistica 9.0).
Результаты исследования и их обсуждение
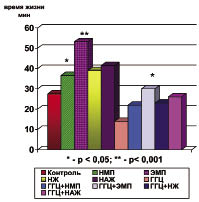
В ходе эксперимента получены следующие результаты. Уровень гомоцистеина у интактных животных составил в среднем 4,46 мкмоль/л. При моделировании ГГЦ к 10 суткам он достиг 39,1 ± 1,34 мкмоль/л.
В условиях ГГЦ процессы ПОЛ были еще более интенсивны. Так, по сравнению с контролем уровень ТБК-АП возрос на 167 % при снижении АОА на 92 %. На фоне ГГЦ ЭМФ и НАЖ также показали свою эффективность, снизив содержание ТБК-АП на 53 и 46 % соответственно при увеличении АОА на 63 и 48 % (р = 0,001). НМФ и НЖ в условиях ГГЦ не проявили антиоксидантной активности, снизив содержание ТБК-АП на 12 и 19 % соответственно (таблица).
Влияние адаптогенов на резервное время жизни крыс при летальной гипоксии и гипергомоцистеинемии
Влияние адаптогенов на содержание ТБК-АП в сыворотке экспериментальных крыс
на фоне гипоксии и гипергомоцистеинемии
Содержание ТБК-АП в сыворотке
(мкмоль/мг липидов)